CITA ESTE TRABAJO
Gutiérrez Martínez F, García Fuentes E, Olmedo Martín R, Fernández Castañer A, Rodríguez González F, VanDussen Martos JV et al. Efectividad a corto y largo plazo de risankizumab en enfermedad de Crohn: Resultados en práctica clínica real en dos centros de tercer nivel de Málaga. RAPD 2026;49(2):47-53. DOI: 10.37352/2026492.1
Introducción
Los inhibidores de la Interleuquina 23 (IL-23) constituyen una de las terapias avanzadas emergentes en el tratamiento de la enfermedad inflamatoria intestinal (EII) de aquellos pacientes con respuesta insuficiente, pérdida de respuesta o presencia de intolerancia al tratamiento convencional o biológico. Estos fármacos se unen a la subunidad p19 de la IL-23, inhibiendo de esta forma la señalización celular dependiente de esta IL y su consecuente liberación de citoquinas proinflamatorias[1].
Los inhibidores de la IL-23 aprobados para el tratamiento de la enfermedad de Crohn (EC) son guselkumab, mirikizumab y risankizumab.
Centrándonos en risankizumab, el estudio pivotal que sustenta su aprobación para la EC está compuesto por dos ensayos de inducción (ADVANCE y MOTIVATE) y uno de mantenimiento (FORTIFY). Estos estudios reportaron una tasa de remisión clínica del 45% y del 42% tras 12 semanas de tratamiento y del 52% tras 52 semanas[2],[3].
El objetivo de este estudio fue evaluar la efectividad de risankizumab en pacientes con EC.
Metodología
Diseño y población de estudio
Se realizó un estudio observacional, retrospectivo, multicéntrico que incluyó a pacientes diagnosticados de EC mayores de 18 años en seguimiento en el Hospital Virgen de la Victoria (HVV) y el Hospital Regional Universitario (HRU) de Málaga, que iniciaron tratamiento con risankizumab entre noviembre de 2023 y octubre de 2024. Se excluyeron pacientes con colitis ulcerosa o colitis no clasificada. La información se obtuvo mediante la revisión de las historias clínicas de los pacientes participantes, utilizando una base de datos anónima creada para tal fin.
El objetivo primario del estudio fue analizar las tasas de remisión y respuesta clínica a las 12, 26 y 52 semanas de iniciar tratamiento con risankizumab. Se definió respuesta clínica como una disminución ≥3 puntos en el índice de Harvey-Bradshaw (IHB), mientras que la remisión clínica se estableció como una puntuación ≤4 en el IHB.
La remisión biológica se evaluó mediante la determinación de calprotectina fecal (CPF) por inmunoensayo enzimático (ELISA), considerándose remisión biológica valores de CPF <250 μg/g.
La remisión clínica libre de corticoides se definió como una puntuación ≤4 en el índice de Harvey-Bradshaw (IHB) sin necesidad de iniciar tratamiento con corticoides (sistémicos o de acción tópica) durante el tratamiento con risankizumab. En aquellos pacientes que iniciaron risankizumab mientras se encontraban en tratamiento activo con corticoides, la remisión clínica libre de corticoides se definió como la capacidad de suspenderlos en un plazo inferior a 12 semanas.
Estudio estadístico
Las variables cualitativas se presentaron como valor absoluto y el porcentaje, mientras que las variables cuantitativas se mostraron como mediana y con el rango intercuartil (IQR).
Se realizaron comparaciones estadísticas de marcadores clínicos (IHB) y biomarcadores (CPF), empleando la prueba de Wilcoxon. Se consideró estadísticamente significativo un valor p ≤ 0.05. Las variables cualitativas se compararon mediante la prueba Chi cuadrado. La persistencia del fármaco se calculó mediante curvas de Kaplan–Meier. Para el análisis estadístico de los datos se utilizó IBM SPSS Statistics.
Resultados
Variables demográficas y clínicas
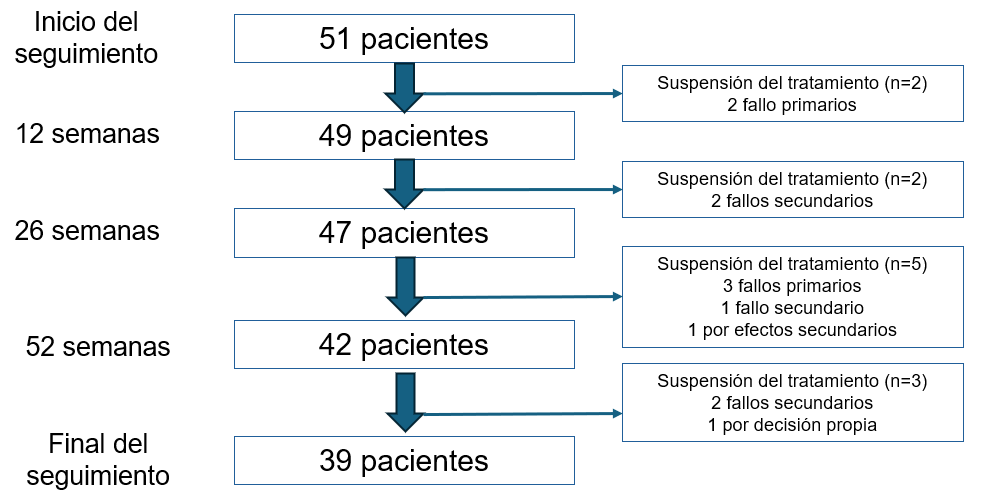
Se incluyó un total 51 pacientes en el estudio, 15 del HVV y 36 del HRU. La Tabla 1 recoge las características clínicas y demográficas, y la Figura 1, el flujo de pacientes.
Tabla 1
Variables demográficas y clínicas.
Análisis de remisión clínica
En la Tabla 2 se recogen la mediana de puntuación obtenida en el índice IHB a las 12, 26 y 52 semanas del inicio del tratamiento. La Figura 2 representa la tasa de remisión y respuesta clínica, tanto con tratamiento con corticoides concomitante como sin él.
Tabla 2
Puntuaciones en índices clínicos.
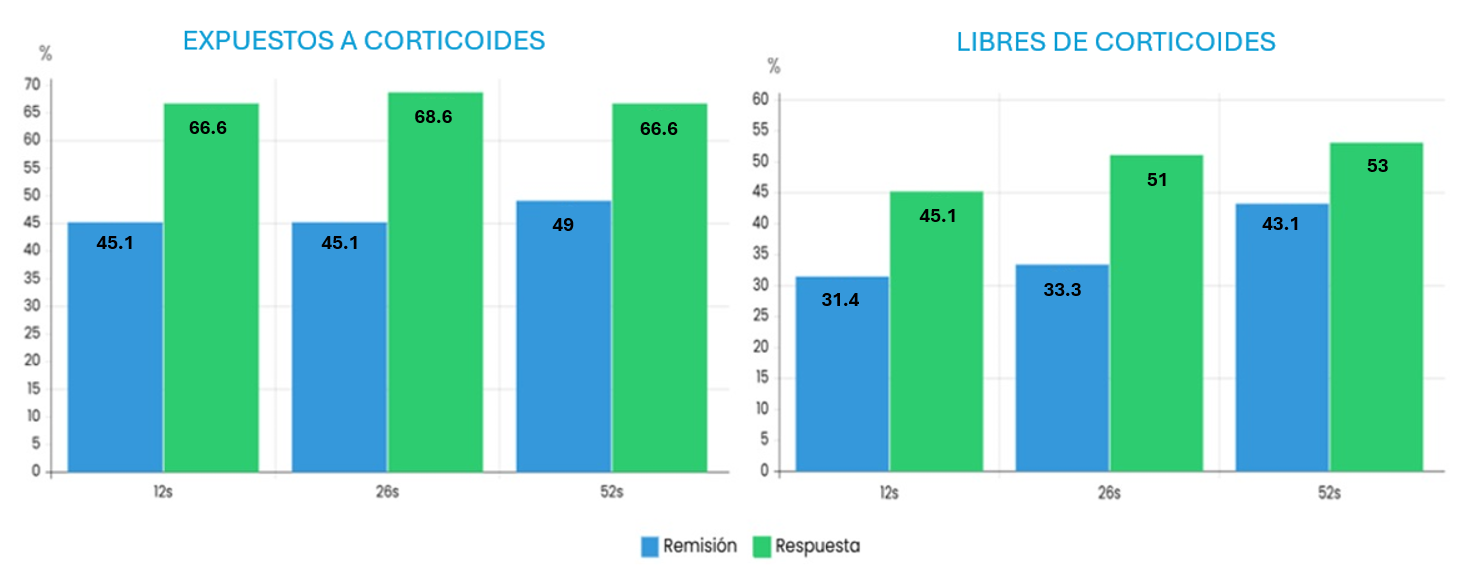
Figura 2
Remisión y respuesta clínica a corto, medio y largo plazo en pacientes expuestos. (A) y en pacientes libres de corticoides (B).
La mediana del IHB basal de los pacientes fue de 8 (IQR 6-12), con una disminución a 6 (IQR 4-9) en la semana 12 (p<0.001), a 5 (IQR 0-3) en la semana 26 (p<0.001) y a 4 (IQR 3-7) en la semana 52 (p<0.001).
De los 51 pacientes incluidos al inicio del seguimiento, a las 12 semanas hubo un 66.6% (34/51) que obtuvieron respuesta clínica y un 45.1% (23/51), alcanzaron la remisión. De los pacientes que alcanzaron la remisión, el 31.4% (16/51) lo hicieron libres de corticoides.
A las 26 semanas, hubo un 68.6% (35/51) que obtuvieron respuesta clínica. Alcanzaron la remisión el 45.1% de los pacientes (23/51), de los cuales, el 33.3% (17/51) lo hicieron libres de corticoides.
El 66.6% (34/51) respondieron tras 52 semanas de tratamiento. De estos pacientes, el 49% (25/51) obtuvieron la remisión clínica, y el 43.1% (22/51) sin necesidad de corticoterapia.
La pauta de mantenimiento con risankizumab se intensificó en 10 pacientes que habían presentado una respuesta incompleta. En todos los casos se acortó el intervalo de administración de 360 mg subcutáneo cada 8 semanas a 360 mg cada 6 semanas. La mediana para el inicio de la pauta intensificada fue de 9.5 meses (IQR 6-14). El 30% de los pacientes intensificados (3/10) experimentaron una respuesta clínica con este cambio.
Análisis de remisión biológica
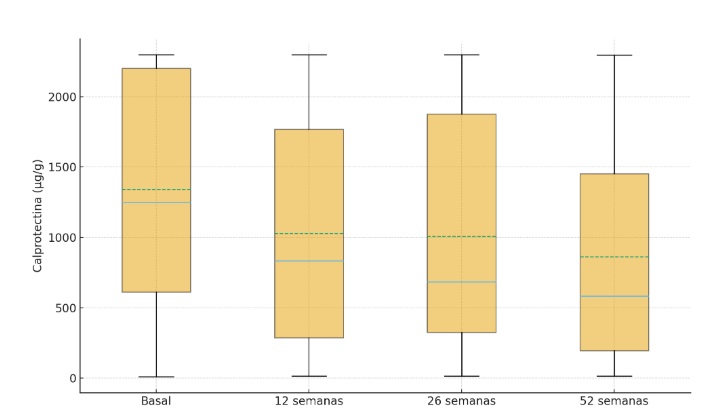
La remisión biológica, definida por una CPF<250, se obtuvo en 11 pacientes (21.56%) tanto a las 12 como a las 26 semanas (p<0.05), y en un total de 12 pacientes (23.52%) a las 52 semanas (p<0.001).
Persistencia del tratamiento
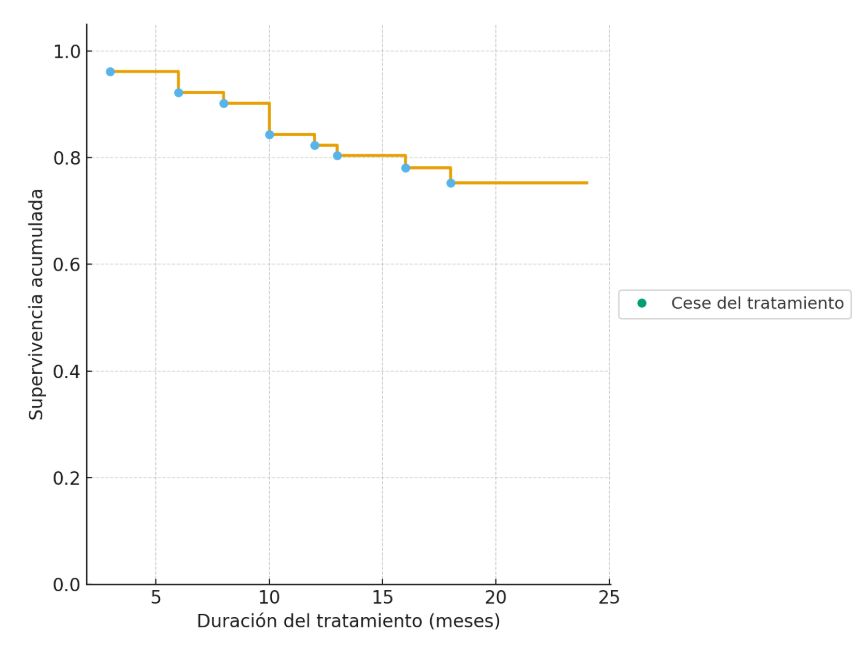
La curva de persistencia de risankizumab se representa en la Figura 4.
La mediana de duración de tratamiento fue de 18 meses (IQR 14-20), con una persistencia del tratamiento a los 12 meses del 84% y del 75% a los 24 meses. Un total de 12 pacientes (23.5%) suspendieron risankizumab a lo largo del seguimiento. Los motivos para la interrupción fueron: fallo primario en 5 pacientes (41.6%), fallo secundario en otros 5 (41.6%), efectos adversos en 1 (8.3%) y un caso de un paciente que se decidió suspender el tratamiento voluntariamente (8.3%). La mediana de tiempo hasta la retirada fue de 10 meses (IQR 6-13.5).
Seguridad del tratamiento
El 17.6% de los pacientes (9/51) reportaron eventos adversos durante el tratamiento con risankizumab, la mayoría de carácter leve (cefalea, rinitis, mareos…). Solo el 5.8% (3/51) experimentaron algún efecto adverso grave: (a) infección del tracto urinario, (b) neumonía y (c) una enfermedad neoplásica (adenocarcinoma de intestino delgado), siendo este último el único paciente del estudio que retiró el tratamiento de manera definitiva por un evento adverso, aunque este no puede atribuirse directamente al fármaco.
Discusión
Risankizumab es un fármaco recientemente incorporado al arsenal terapéutico de la EC, por lo que las referencias en la literatura al respecto son escasas. En este estudio se evaluó la efectividad y seguridad del tratamiento con risankizumab en pacientes con EC refractaria a otras terapias en la práctica clínica real en dos hospitales de tercer nivel de Málaga capital.
Las tasas de remisión clínica observadas en las semanas 12 y 52 fueron prácticamente idénticas a las descritas en los estudios pivotales (45% y 42% a las 12 semanas y 52% a las 52 semanas)[2],[3], y también concuerdan con los principales estudios en vida real publicados hasta la fecha, donde al igual que en nuestro estudio, se incluye una población altamente refractaria[4]-[8].
Nuestros resultados a medio y largo plazo muestran que risankizumab es efectivo para mantener la respuesta a lo largo del tiempo, con una tasa de persistencia del tratamiento al año del 84%, datos que coinciden con otros estudios realizados en vida real[9]-[11].
La normalización de la CPF se logró en aproximadamente 1 de cada 4 pacientes tras la inducción en nuestro estudio, hallazgos equivalentes a un análisis post-hoc del estudio pivotal de risankizumab[12].
Se observó un correcto perfil de seguridad, registrándose una tasa de eventos adversos graves inferior al 6%, cifra similar a la reportada en los estudios pivotales2,3 y los principales estudios en vida real[6],[7].
Las limitaciones del estudio fueron las derivadas de su naturaleza observacional retrospectiva, el pequeño tamaño muestral y la ausencia de evaluación endoscópica sistemática y de parámetros de imagen (ecografía o entero-RMN) para evaluar la respuesta al tratamiento.
En conclusión, risankizumab es un tratamiento efectivo para pacientes con EC refractaria a otros tratamientos avanzados en la práctica clínica real, con una buena tasa de persistencia del tratamiento a largo plazo y un perfil de seguridad adecuado.

 Descargar número completo
Descargar número completo Download full issue
Download full issue