CORRESPONDENCIA
Esperanza Pérez Rodríguez
Unidad Gestión Clínica Aparato Digestivo. Exploraciones Funcionales.
Hospital Universitario Reina Sofía
14004 Córdoba
Definiciones
Básicamente el estreñimiento se caracteriza por la presencia de heces escasas, secas o la presencia de esfuerzo o dificultad en la defecación.
El estreñimiento crónico funcional (en adelante ECF), comparte con el síndrome de intestino irritable tipo estreñimiento (SII-E) la ausencia en la mayoría de los casos de alteraciones morfológicas, metabólicas o neurológicas que los expliquen mediante métodos convencionales.
Por otra parte, el ECF puede deberse a tránsito lento, dificultad expulsiva o ambas situaciones.
El consenso de Roma IV[1] propone como criterios diagnósticos los siguientes, que coinciden básicamente con otras definiciones anteriores (Tabla 1).
Tabla 1
Criterios diagnósticos de Roma IV para el estreñimiento crónico funcional.
En cuanto al SII-E[2]-[4], su principal característica según el consenso de Roma IV sería la presencia de dolor abdominal recurrente relacionado con la defecación y con cambios en la frecuencia y/o consistencia de las deposiciones. Otras consideraciones previas como la mejoría con la deposición se han visto escasamente discriminadas en su diagnóstico. Tampoco lo son las molestias o distensión abdominal, que son con frecuencia síntomas que también pueden aparecer en el ECF, de forma que los pacientes presentan patrones que varían en el tiempo. En la práctica es muy difícil distinguir ambos procesos. Los trastornos funcionales intestinales aparecen así en un gran número de casos como un espectro contínuo de situaciones intermedias.
Además, estas definiciones no siempre coinciden con las percepciones de los pacientes[5]. La forma en que se denominan los síntomas tiene un gran influjo cultural. Como se constata por ejemplo en un estudio americano con 557 pacientes, los síntomas referidos como estreñimiento eran esfuerzo excesivo (79%), gases (74%), deposiciones duras (71%), molestias abdominales (57%), deposiciones infrecuentes (57%), distensión abdominal (57%) o sensación de evacuación incompleta (16%)[6].
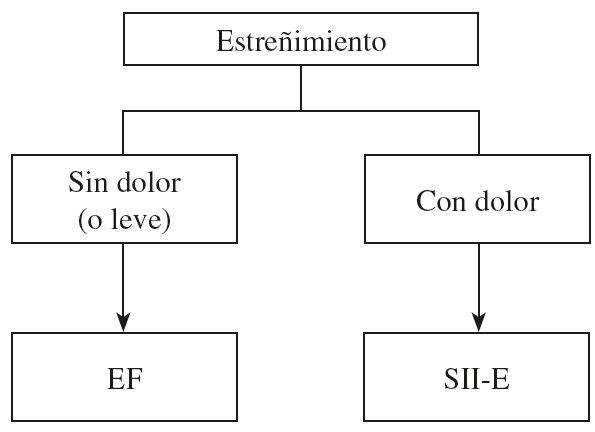
Por todo ello, a efectos prácticos, parece más razonable el abordar ambos trastornos conjuntamente, siendo la presencia o no de dolor el síntoma clave diferencial (Figura 1).
Fisiopatológicamente, esta diferencia podría estribar en que en el SII-E en muchos casos habría una hipersensibilidad visceral, mientras que es más frecuente en el ECF la hiposensibilidad rectal.
Epidemiología
Las estimaciones de la prevalencia del estreñimiento crónico varían mucho según los criterios para definirlo, tanto como entre un 2% y un 79% de la población, aunque la mayoría de los estudios la sitúan entre un 12-19% (con un promedio de 15%). Las tasas de prevalencia son menores si se usan los criterios de Roma que utilizando la percepción de los pacientes.
Es más frecuente en mujeres. El riesgo de padecerlo en este grupo de población fue entre 2,9 veces (autopercibido) y 4,6 (según los criterios de Roma II), mayor que en varones en un estudio español[5].
El estilo de vida sedentario, la obesidad, bajos niveles socioeconómicos y educativos, la historia familiar, la ansiedad y la depresión, y los abusos físicos y sexuales son otros factores que se han visto asociados un mayor riesgo de padecer estreñimiento[7],[8].
Se ha observado con más frecuencia asimismo cuando hay una baja ingesta de fibra dietética.
La edad también es un importante determinante de riesgo en esta patología, de forma que su prevalencia aumenta drásticamente con el envejecimiento. A partir de los 65 años más de 26% de hombres y 34% de mujeres se quejan de estreñimiento. En los hábitos dietéticos de estos grupos de población parece influir más la disminución de la ingesta calórica que de la fibra y líquidos[9].
En algunos estudios se estima que puede suponer hasta una de cada cuatro consultas de gastroenterología.
Manejo diagnóstico en los pacientes con estreñimiento funcional
El diagnóstico de los trastornos funcionales digestivos en general se basa en los síntomas, teniendo en cuenta los recursos sanitarios disponibles y el grado de incertidumbre que los pacientes y los médicos sean capaces de aceptar, y reservando la realización de estudios para aquellos casos en los que exista sospecha de alguna posible causa orgánica.
Es imprescindible una historia clínica cuidadosa investigando aspectos como los antecedentes familiares y personales. Entre los últimos son de gran importancia los antecedentes de paridad y quirúrgicos.
El estreñimiento crónico puede ser secundario en una gran proporción de pacientes a otras patologías (Tabla 2).
Tabla 2
Posibles causas secundarias de estreñimiento.
Es fundamental conocer las prescripciones de fármacos que pueden provocar este problema, siendo de especial importancia en los pacientes polimedicados y sobre todo aquellos tratados con opiáceos. La tabla 3 enumera algunos de los grupos de medicamentos más frecuentemente implicados.
Tabla 3
Fármacos frecuentes relacionados con estreñimiento.
La presencia de estreñimiento junto a determinados síntomas de alarma, como el sangrado rectal, pérdida de peso, anemia, una historia familiar de cáncer de colon o de enfermedad inflamatoria intestinal o el inicio agudo en edad mayor de 50 años obliga además a descartar patología orgánica, mediante la realización de colonoscopia.
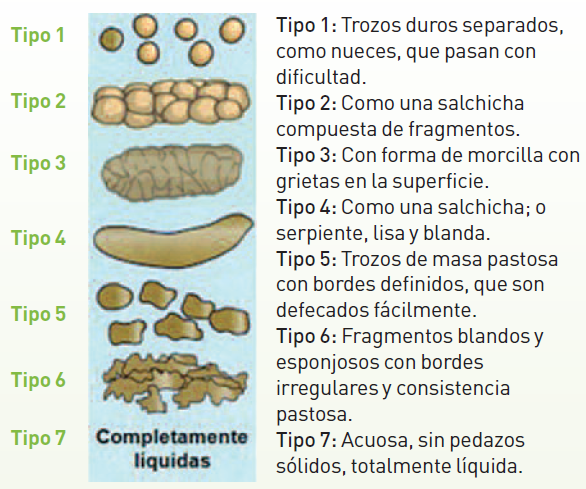
La historia actual debe recoger también el tiempo de evolución del estreñimiento, su forma de instauración (brusca o insidiosa) y circunstancias asociadas (viajes, cirugía, etc.) ritmo, síntomas acompañantes y factores modificadores, así como molestias que orienten hacia un problema distal, como el dolor, tenesmo, los esfuerzos prolongados o digitaciones, o por el contrario la ausencia de deseo defecatorio o presencia de heces muy secas, que sugieran un problema de inercia colónica. Para valorar la consistencia de las heces se suele utilizar la escala de Bristol (Figura 2). Igualmente ha de investigarse la presencia en las deposiciones de elementos patológicos.
Por otra parte la exploración física es fundamental para valorar la anatomía de la región anorectal, (cicatrices, fisuras, fístulas, abscesos, hemorroides, etc.). Durante el examen se puede comprobar la presencia del reflejo cutáneo perineal con la contracción del esfínter externo, cuya ausencia puede indicar patología del nervio sacro, examinar el esfuerzo de pujo, y el descenso fisiológico o patológico del periné.
El tacto rectal ofrece valiosa información sobre la presión basal y de esfuerzo del esfínter, la presencia y características de las heces en la ampolla rectal, la rectificación del ángulo rectoanal durante el esfuerzo defecatorio en respuesta al funcionalismo del músculo puborectal y su sensibilidad, la existencia de rectoceles, masas etc. Puede tener también valor la observación de la prensa abdominal mediante palpación bimanual.
Una vez orientada la sospecha diagnóstica hacia una patología funcional, y habiendo descartado el uso de fármacos imputables, iniciaremos un tratamiento escalonado, como se desarrollará más adelante.
Un gran número de pacientes responderán a un buen manejo terapéutico basado en una relación con el paciente adecuada, medidas higiénicas y tratamientos convencionales.
Sin embargo, cuando esto no ocurre, se hace conveniente evaluar la gravedad, ya sea mediante escalas individuales para los diferentes síntomas, o con cuestionarios de calidad de vida, para seleccionar los casos que precisarán estudios funcionales y tratamientos específicos.
Es muy útil en estas ocasiones instar a los pacientes a realizar un diario tanto de sus diferentes molestias como de las deposiciones para poder evaluar de forma objetiva la situación.
Un fracaso de esta estrategia nos obligará a realizar un estudio funcional, que clasificará adecuadamente el trastorno en ECF con tránsito normal (ETN), tránsito lento (ETL) o trastorno defecatorio distal (ETD), pudiendo asociarse estas situaciones.
El discernir el tipo de alteración fisiopatológica nos ayudará a realizar en adelante un tratamiento específico.
Son motivos para derivar para estudios, tanto en la evaluación inicial como en pacientes que ya han sido diagnosticados previamente de un trastorno funcional, la necesidad de descartar un trastorno orgánico por las causas antes mencionadas, un empeoramiento o modificación injustificado de los síntomas, y específicamente la realización de pruebas funcionales, si hay sospecha de una disfunción defecatoria que pueda beneficiarse de tratamiento específico, o la falta de respuesta a tratamiento.
Una causa para realizar más exámenes puede ser la actitud de algunos pacientes que por diversos motivos no aceptan ningún nivel de incertidumbre diagnóstica o tienen características (hipocondría, trastornos psicológicos, etc.) por las que demandan especialmente la realización de pruebas. En todos, pero más aún en este perfil individual es especialmente un desafío una buena comunicación clínica.
En cuanto a las exploraciones complementarias necesarias en los pacientes que cumplen criterios de Roma y no tienen motivos para sospechar patología orgánica, solo el hemograma se ha visto útil para descartar anemia o infección. La bioquímica, hormonas tiroideas, radiología y colonoscopia no se han visto discriminantes ni costo eficaces para el diagnóstico de estreñimiento funcional con respecto a la población normal que no padece esta patología por lo que se recomienda solicitarlas solo en caso de sospecha clínica de patología específica.
Estudio funcional en el ECF
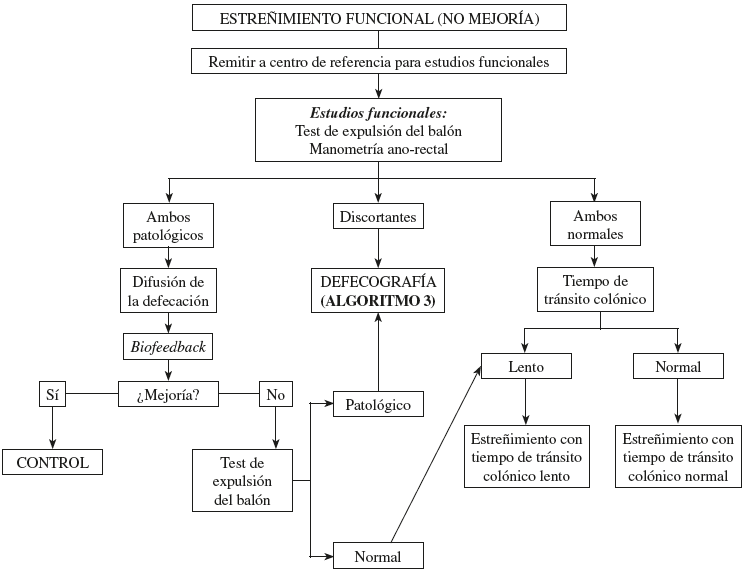
Una vez establecida la conveniencia de realizar estudios funcionales, teniendo en cuenta que el trastorno más prevalente es la disfunción defecatoria, y sobre todo si los datos de la historia clínica (dolor anal, maniobras digitales, esfuerzo o sensación de bloqueo, etc.) y de la exploración física (contracción del músculo puborectal con la maniobra defecatoria, etc.) así lo hacen sospechar, se solicitaría un test de expulsión del balón y manometría anorrectal, para continuar según el la figura 3 hasta llegar a establecer la causa del trastorno y comenzar tratamiento específico.
Estreñimiento funcional con tránsito normal
Con frecuencia estos pacientes tienen una percepción inadecuada de la existencia de estreñimiento. En la historia clínica hay a menudo antecedentes de distrés psicosocial. Algunos de ellos tienen asociadas alteraciones de la sensibilidad y función motora anorectal indistinguibles de los de tránsito lento, con relación con los síntomas poco clara. La diferencia con el SII-E suele ser la presencia de hiposensibilidad rectal, pero a menudo encontramos que pueden pasar de un diagnóstico a otro en el tiempo.
Estreñimiento funcional con tránsito lento
El tránsito lento puede deberse a disfunción de la actividad del músculo liso colónico, reflejos colocolónicos, neurotransmisores o actividad de las células marcapasos colónicas.
Este tipo de estreñimiento es relativamente común en mujeres jóvenes con movimientos intestinales infrecuentes (menos de una vez por semana). En las mujeres con un retraso mínimo en el tránsito de las heces en el colon, los factores culturales y dietéticos tienen gran influencia sobre la sintomatología. En estos pacientes, una dieta rica en fibra, que aumente el volumen de las heces, hace disminuir la duración del tránsito en el colon, consiguiéndose así un alivio en el estreñimiento y en la percepción subjetiva del mismo.
Cuando el tránsito en el colon es más lento, la mejoría que se consigue incrementando el contenido en fibra de la dieta es mucho menor e incluso puede empeorar otros síntomas asociados, y la respuesta al tratamiento con laxantes dista de ser óptima.
En estos pacientes se ha visto que hay menos contracciones de gran amplitud después de las comidas. Este tipo de ondas peristálticas son más comunes tras la ingesta de alimentos, siendo las responsables en gran medida del tránsito de las heces a través del colon. La inercia del colon se caracteriza además de por la falta de actividad motora después de las comidas, por la ausencia de respuesta al Bisacodilo (Dulcolaxo®), fármacos colinérgicos o medicamentos anticolinesterásicos (vg. Neostigmina).
Los estudios histopatológicos en los pacientes con lento tránsito en el colon han mostrado alteración en el número de neuronas del plexo mesentérico que liberan sustancia P (neurotransmisor excitador), VIP (péptido intestinal vasoactivo, neurotransmisor inhibidor en este caso), y NO (óxido nitroso). También se observa una disminución del número de células de Cajal, que se cree tienen una función reguladora de la motilidad intestinal.
Los síntomas que orientan hacia este trastorno son la infrecuencia defecatoria, el antecedente de instauración en la infancia, y la dependencia de los laxantes, pero únicamente la consistencia de las heces (muy duras, escala de Bristol <3) se ha objetivado que tiene un valor predictivo para el diagnóstico de TCL (sensibilidad 85%, especificidad 82%)[10].
Además del estudio radiológico de tiempo de tránsito colónico (TTC) existen otras pruebas útiles en el diagnóstico de este trastorno aunque menos difundidas, como la gammagrafía colónica tras ingesta de comida o de cápsula con Indio y la cápsula inalámbrica de motilidad (Smart Pill), o la manometría colónica, que suelen estar limitadas a centros especializados y usarse sobre todo en evaluación prequirúrgica para descartar trastornos asociados de motilidad gastrointestinal.
Estreñimiento con obstrucción defecatoria
Los trastornos en la fase expulsiva de la defecación pueden ser debidos a una serie de problemas orgánicos como los que se enumeran en la tabla 4.
Tabla 4
Posibles patologías causantes de la defecación obstructiva.
En ausencia de otras patologías, pueden existir problemas que deriven en alteración de las fuerzas propulsivas, o a defecación disinérgica por contracción inadecuada de la musculatura del suelo pélvico.
Estos son los criterios según el consenso de Roma IV para el diagnóstico de este tipo de trastornos funcionales (Tabla 5). Estos trastornos se estudiarán más a fondo en temas aparte.
Tabla 5
Criterios diagnósticos de Roma IV para el trastorno funcional de la defecación.
La contracción paradójica del músculo puborrectal es un trastorno funcional defecatorio al que se le supone una etiología multifactorial, posiblemente adquirida en su mayor parte, caracterizado por disfunción con alteración de la relajación del músculo puborectal durante el esfuerzo defecatorio que ocasiona bloqueo expulsivo. El tacto rectal en muchos casos puede tener una buena sensibilidad y especificidad para su diagnóstico. Hay que tener en cuenta que los estudios funcionales pueden dar sucesivamente datos discordantes; el test de expulsión de balón es patológico; manométricamente se define como una contracción inapropiada del suelo pélvico o relajación inferior al 20% de la basal. Sin embargo la manometría sola es insuficiente para su diagnóstico. El tratamiento más apropiado de este trastorno es el biofeedback.
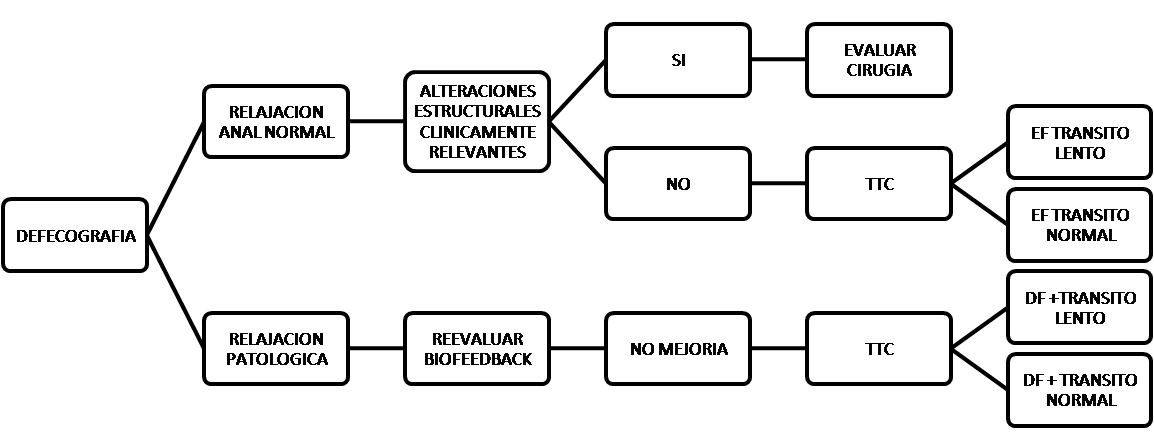
Cuando los estudios funcionales son discordantes, o tras un diagnóstico inicial de defecación disinérgica no hay una respuesta adecuada a tratamiento específico con biofeedback, y es necesario una evaluación más precisa para plantear otro tipo de tratamientos, la defecografía ya sea convencional con contraste o con RMI nos permite confirmar la presencia de una relajación inadecuada en la fase expulsiva, y apreciar alteraciones anatómicas de relevancia clínica. El siguiente algoritmo indica el manejo en esta situación y las opciones diagnósticas en función de los hallazgos en esta exploración (Figura 4).
Megacolon y megarrecto
Una pequeña proporción de pacientes estreñidos tienen megacolon o megarrecto, aunque la mayoría de las personas con recto o colon dilatados tienen trastornos defecatorios. Los hallazgos radiológicos no siempre se correlacionan con los manométricos.
El megacolon puede ser primario (Hirschsprung) o secundario (adquirido, por retención fecal crónica o por lesiones en la espina lumbosacra, mielomeningocele, etc), y se puede acompañar de clínica de impactación fecal y rebosamiento.
Los hallazgos manométricos en estos pacientes suelen ser una compliance aumentada, aumento de umbrales sensitivos, y menor grado de relajación del EAI con la distensión del balón. En algunos pacientes es posible revertir con tratamiento adecuado las anomalías sensoriales y motoras.
Manejo terapéutico del estreñimiento funcional
Un considerable número de pacientes con ECF responderán a simples modificaciones higiénico dietéticas. Es importante insistir en la no necesidad de tener deposiciones diarias, de forma que hasta tres deposiciones semanales pueden ser normales, y por tanto evitar la dependencia de los laxantes en casos innecesarios.
Entre las medidas aconsejables que parecen ayudar en el tratamiento del estreñimiento están la realización de ejercicio adecuado a la situación física personal, el cual parece mejorar también la distensión y flatulencia.
Se debe instar al los pacientes a buscar el momento adecuado para la defecación, evitando retrasarla en lo posible, y realizarla preferiblemente por la mañana y/o tras la ingesta en que la actividad motora colónica es máxima.
Asimismo, aunque sea una recomendación de baja evidencia, es conveniente evitar la deshidratación con una ingesta hídrica adecuada, (1,5-2 litros/día).
La alimentación debe ser regular y variada, rica en fibra soluble (más de 25-30 g), (ciruelas secas por ejemplo) evitando comidas grasas, copiosas, flatulentas o la fibra insoluble por la frecuencia con que producen distensión y malestar, y su especial intolerancia en los pacientes con tránsito lento. Algunos pacientes se benefician de ciertas restricciones concretas.
Las anteriores medidas en conjunto, aunque avaladas por distintos tipos de estudios, tienen un nivel de evidencia IV (grado C de recomendación).
Los suplementos de fibra, sobre todo soluble, pueden ser inicialmente aconsejables aunque no todos los pacientes la tolerarán. Es aconsejable comenzar con cantidades bajas (NE II, GR B).
Si estas medidas son insuficientes, los laxantes osmóticos (de ellos parece algo superior el polietilenglicol, NE I, GR A) pueden ser de utilidad. También la lactulosa (NE II, GR A), aunque puede aumentar otros síntomas asociados sobre todo en el SII-E.
Los laxantes estimulantes son el siguiente escalón terapéutico, con un perfil de seguridad algo inferior a los anteriores. Igualmente pueden empeorar síntomas asociados (picosulfato, Bisacodilo NE I, GR B).
Combinaciones de los anteriores también pueden usarse si la respuesta no es adecuada.
Otros fármacos pueden introducirse si ninguno de los anteriores ha sido eficaz.
Lubiprostona, derivado prostaglandínico, no está comercializada en Europa, aunque ha demostrado eficacia y seguridad en el estreñimiento.
Prucalopride, agonista selectivo de los receptores intestinales de la serotonina, está indicado en ficha técnica para el tratamiento del estreñimiento funcional refractario. Tiene un buen perfil de seguridad cardiaco, aunque hay que usarlo con precaución en insuficiencia renal y hepática graves. Mejora también en menor medida los síntomas de distensión o dolor pero no se ha comercializado en España para la indicación de SII-E. En ancianos hay que reducir la dosificación.
Linaclotide, agonista de la guanilato ciclasa, actúa tanto sobre la secreción hidroelectrolítica hacia la luz colónica como sobre los receptores del dolor, por lo que tiene un doble efecto sobre el estreñimiento y las molestias abdominales. Se ha comercializado como fármaco de primera elección en SII-E refractario a otros tratamientos. Tiene buen perfil de seguridad siendo la diarrea el efecto secundario más frecuente.
Los tres anteriores se han evaluado mediante estudios controlados (NE I, GR A). Ninguno de ellos se recomienda en el embarazo o lactancia.
La siguiente tabla (Tabla 6) recoge los fármacos más comúnmente empleados junto con su dosificación y efectos secundarios.
Tabla 6
Fármacos más comúnmente empleados en el ECF.
Otros tratamientos como los probióticos, antidepresivos, tratamientos psicológicos o acupuntura, no tienen un efecto suficientemente demostrado en el EF como para establecer claras recomendaciones.
Los distintos fármacos y sus combinaciones se pueden ensayar durante periodos de unas cuatro semanas, de forma que si ninguno de ellos obtiene respuesta satisfactoria, habría que reevaluar el cumplimiento, constatar que no exista una percepción inadecuada de la existencia de estreñimiento, considerar otros diagnósticos asociados como SII, o alteraciones psico-psiquiátricas subsidiarias de un tratamiento específico, investigar la toma de fármacos inadvertidos o la posibilidad cambios clínicos que orienten hacia la aparición de patología orgánica.
El estreñimiento inducido por opioides merece tratarse en tema independiente. Los fármacos PAMORA, (antagonistas de los receptores periféricos μ de los opioides) como la metilnaltrexona, alvimopan o naloxegol, revierten el efecto gastrointestinal de estos fármacos sin atravesar la barrera hematoencefálica y por tanto se utilizan con este fin.
Cuando el estreñimiento es debido a disfunción defecatoria, el biofeedback se ha visto más eficaz que los laxantes, los ejercicios de relajación muscular y los fármacos miorrelajantes, de ello la importancia del diagnóstico en su caso (ver temas correspondientes)[20]-[23].
Tratamiento en el estreñimiento crónico grave refractario
A pesar de todas las medidas referidas en apartados anteriores, algunos pacientes no consiguen un resultado adecuado. En ellos, tras un estudio protocolizado tal como se describió en el apartado anterior, se pueden considerar otras alternativas de tratamiento.
La estimulación del nervio tibial posterior (PTNS) comenzó usándose en otros problemas del suelo pélvico como la incontinencia urinaria y la vejiga hiperactiva, observándose beneficio en algunos pacientes sobre problemas gastrointestinales como la incontinencia y el estreñimiento. Su mecanismo preciso de acción es desconocido aunque parece actuar sobre neuroreceptores en vías aferentes pélvicas sobre mecanismos de control central[24],[25]. Es un tratamiento seguro, aunque requiere de sesiones repetidas y su efecto no siempre es duradero. Su efectividad, así como la mejor forma de realizarla están bajo evaluación.
La neuroestimulación de las raíces sacras S3 y S4 mediante electrodos implantados en principio temporalmente (cuatro semanas), y si hay respuesta de forma definitiva, ha mostrado eficacia para tratar el estreñimiento con tránsito lento en una revisión sistemática Cochrane (Thaha et al., 2015). Las evidencias sobre su utilidad están basadas en su mayoría solo en estudios no controlados frente a otros tratamientos, o retrospectivos, (Nivel de Evidencia IV), aunque existen dos trabajos que presentan un nivel IIb. Se ha podido demostrar adecuada sobre todo en el estreñimiento con inercia colónica, aunque también parece mejorar la sensibilidad rectal. Son necesarios más estudios para indicarla en la disfunción defecatoria, y también es necesario que los estudios que se realicen incluyan datos como la mejoría de los distintos síntomas por separado y medidas objetivas de la calidad de vida[26],[27].
Está contraindicada si se produce un embarazo y no está exenta de efectos secundarios.
Como última alternativa, en los pacientes con estreñimiento con calidad de vida muy deteriorada, está la cirugía, consistente en la realización de colectomía total. La preservación del ciego o del sigma se han visto asociadas a peores resultados. Solo estaría indicada en aquellos casos de estreñimiento crónico funcional grave, con patrón de inercia colónica, siempre que el síntoma que predomine no sea el dolor abdominal. Habría previamente que descartar seudoobstrucción o trastorno de motilidad generalizado mediante estudios manométricos y radiológicos, así como disfunción del suelo pélvico[28]-[30].
La colectomía se ha visto en revisiones de series de casos de estudios no controlados que puede mejorar hasta en 65% de los pacientes el tránsito intestinal[28]. No está exenta de mortalidad (0,2%) y morbilidad, así como de complicaciones tardías muy variables en su frecuencia.
Las resecciones segmentarias solo podrían ser útiles en algunos casos de megasigma o sigmoidoceles aislados o con volvulaciones recurrentes.
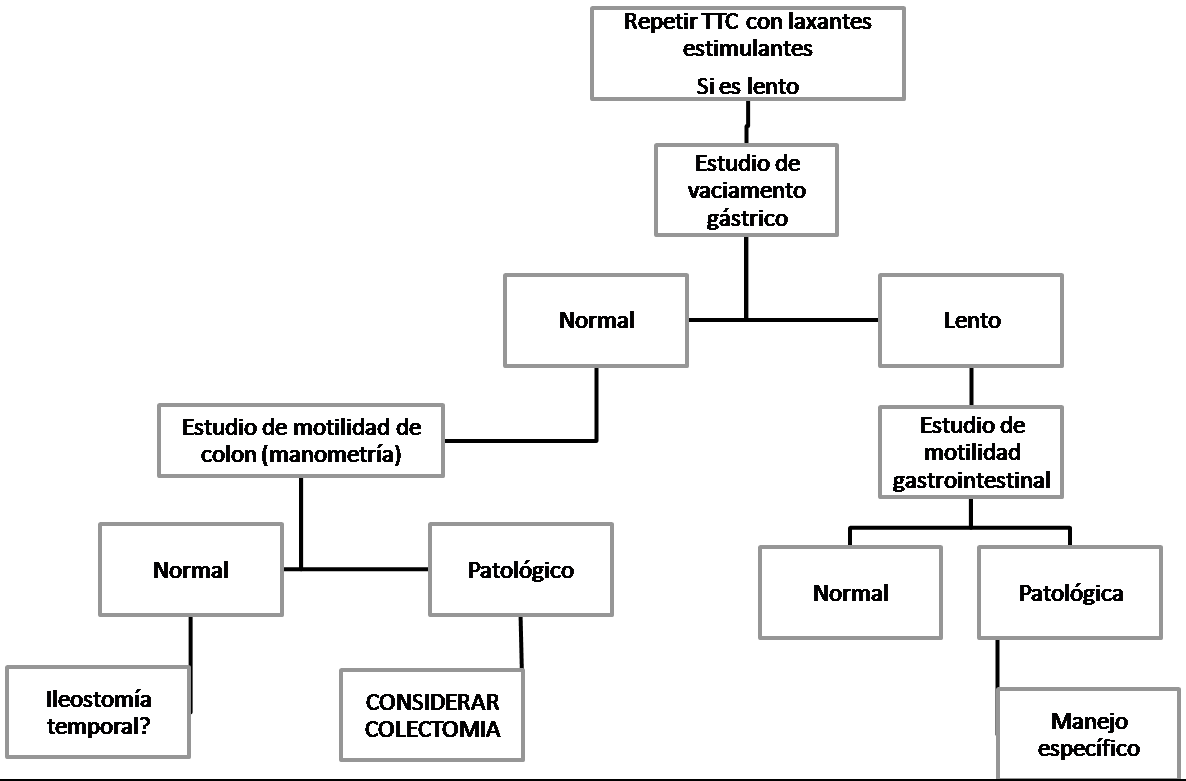
La figura 5 propone la secuencia diagnóstica en esta situación.
Por último, antes de considerarla se debe realizar una evaluación psicológica adecuada, y los pacientes en deben ser remitidos a centros especializados. Es recomendable documentar el tránsito lento en estudios repetidos.
Las alteraciones anatómicas distales que provocan defecación obstructiva (rectocele, intususcepción, etc.) también pueden ser subsidiarias de cirugía, y como hemos comentado se tratan en temas aparte.

 Descargar número completo
Descargar número completo Download full issue
Download full issue