CP-073. AGENESIA DORSAL DEL PANCREAS, UNA EXTRAÑA ENTIDAD; A PROPÓSITO DE UN CASO
Flores Moreno H, Tenorio González E, Palomino Luque P, Vera García P
Sección Aparato Digestivo. Hospital Comarcal de la Axarquía, Vélez-Málaga.
Palabras clave: agenesia, dorsal, pancreas.
Introducción
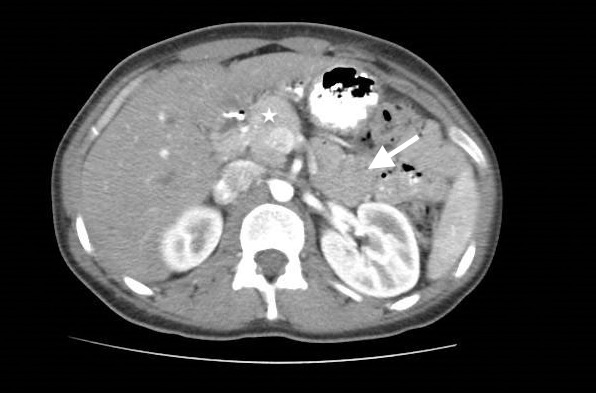
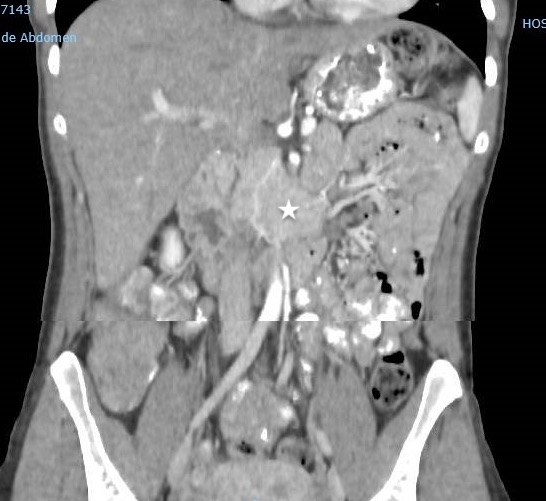
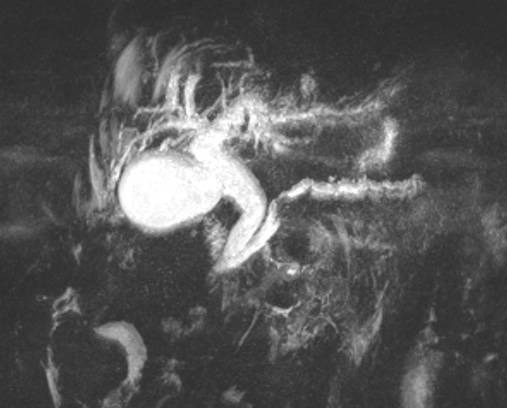
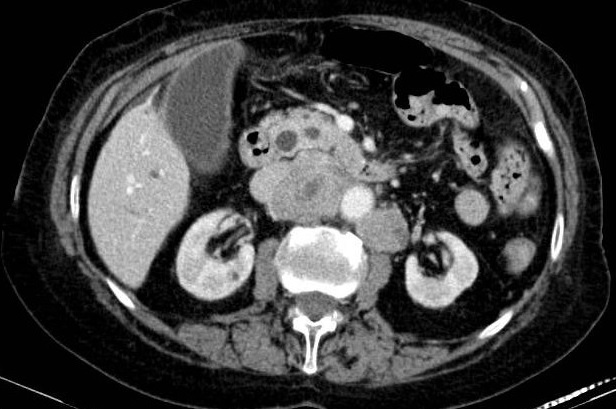
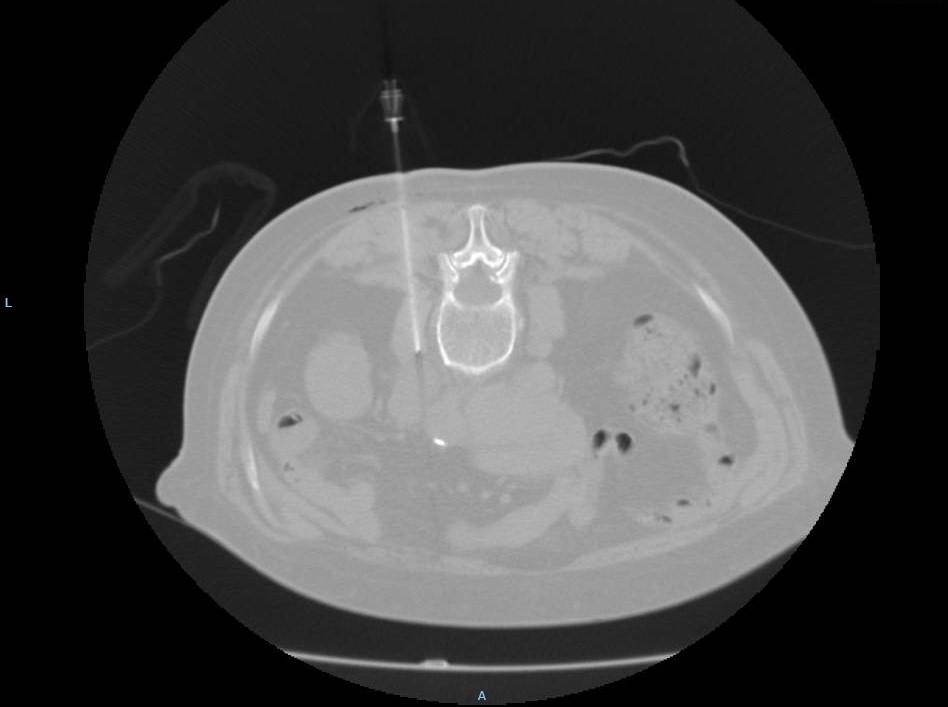
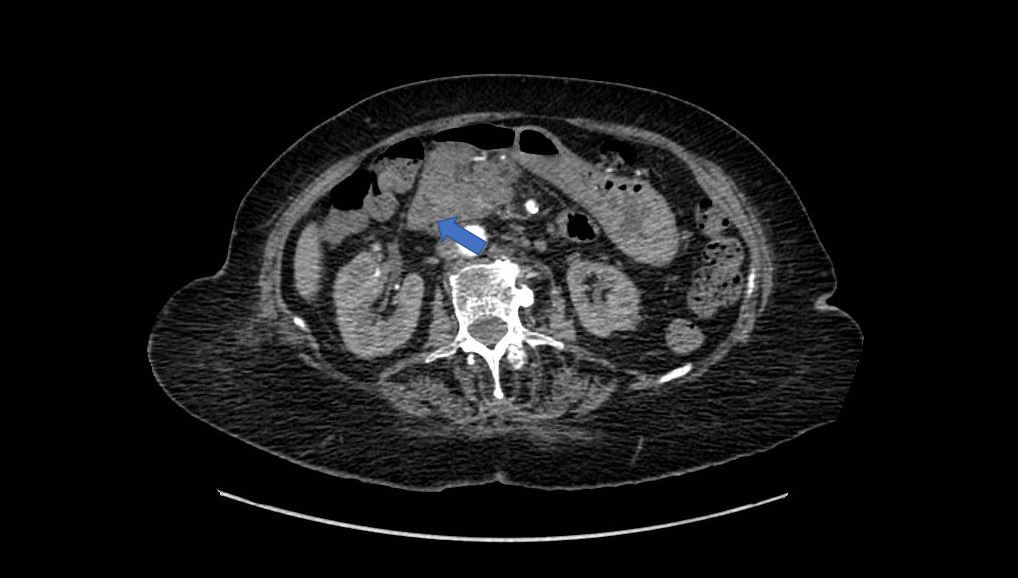
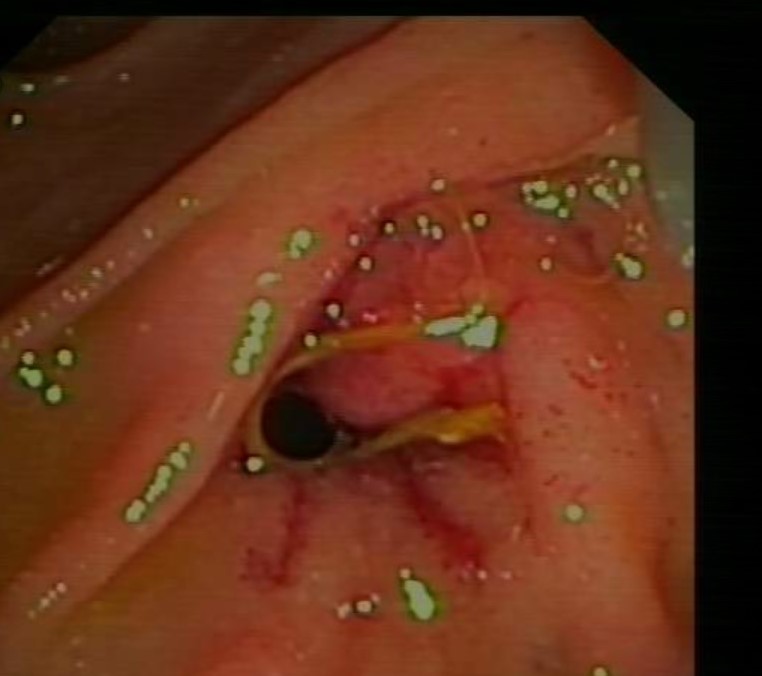
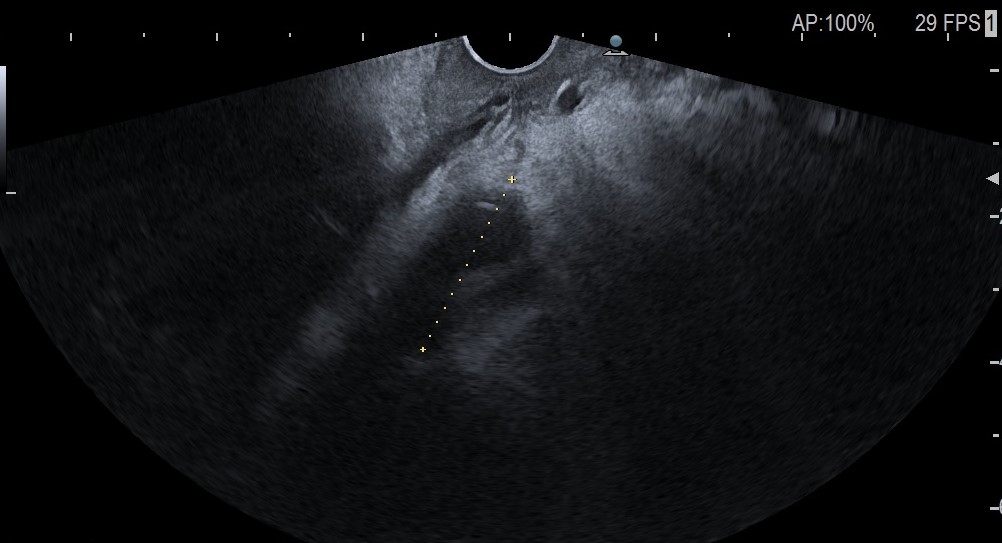
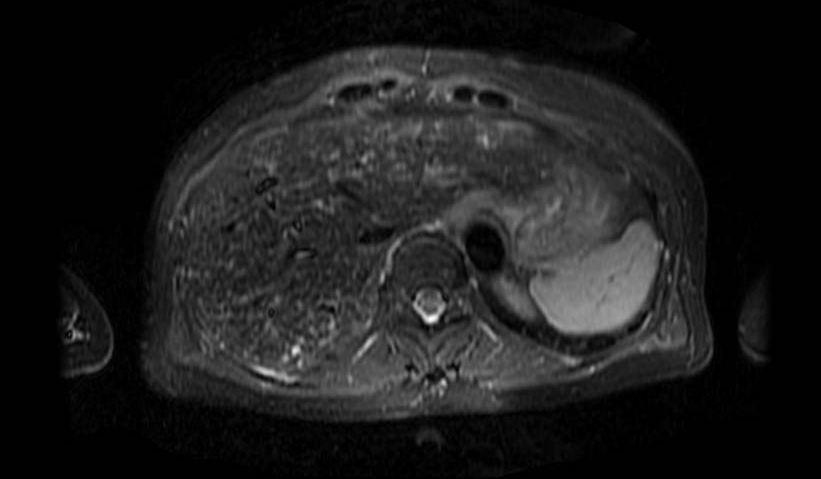
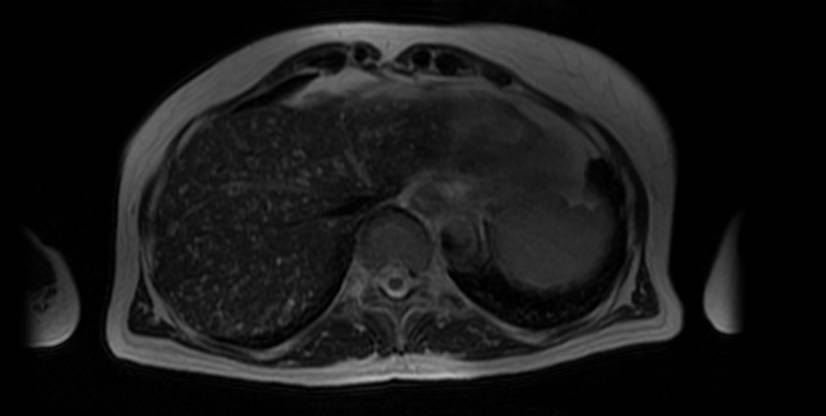
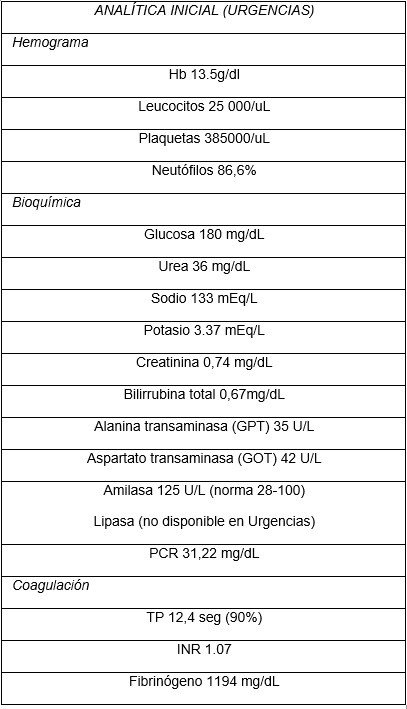
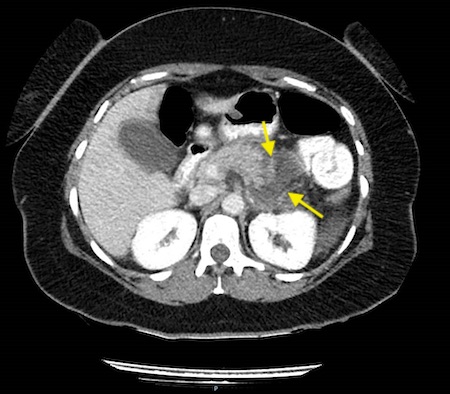
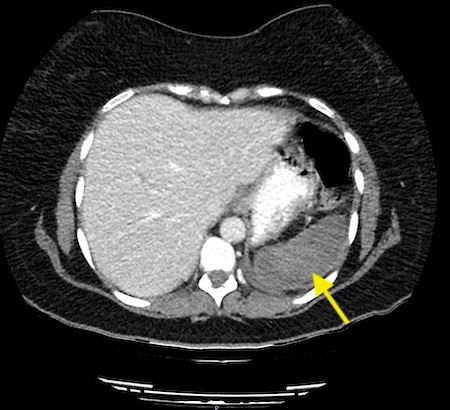
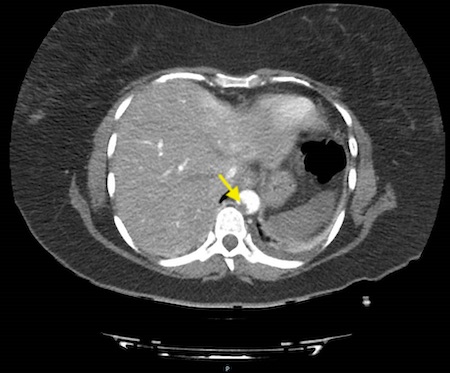
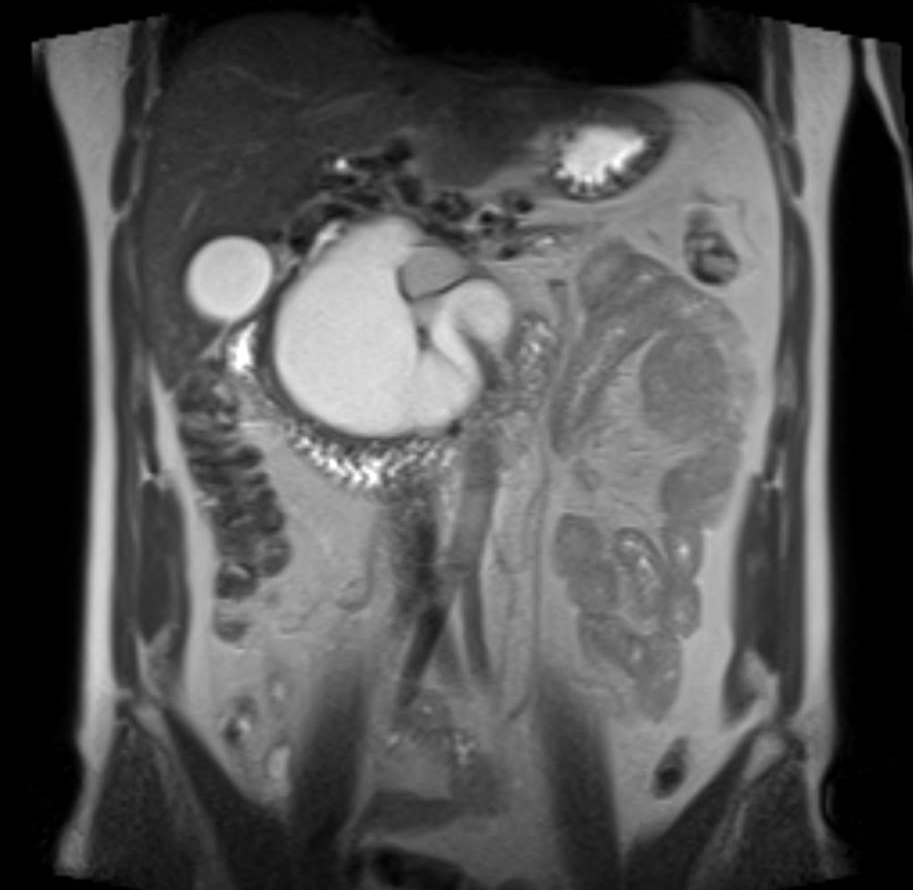
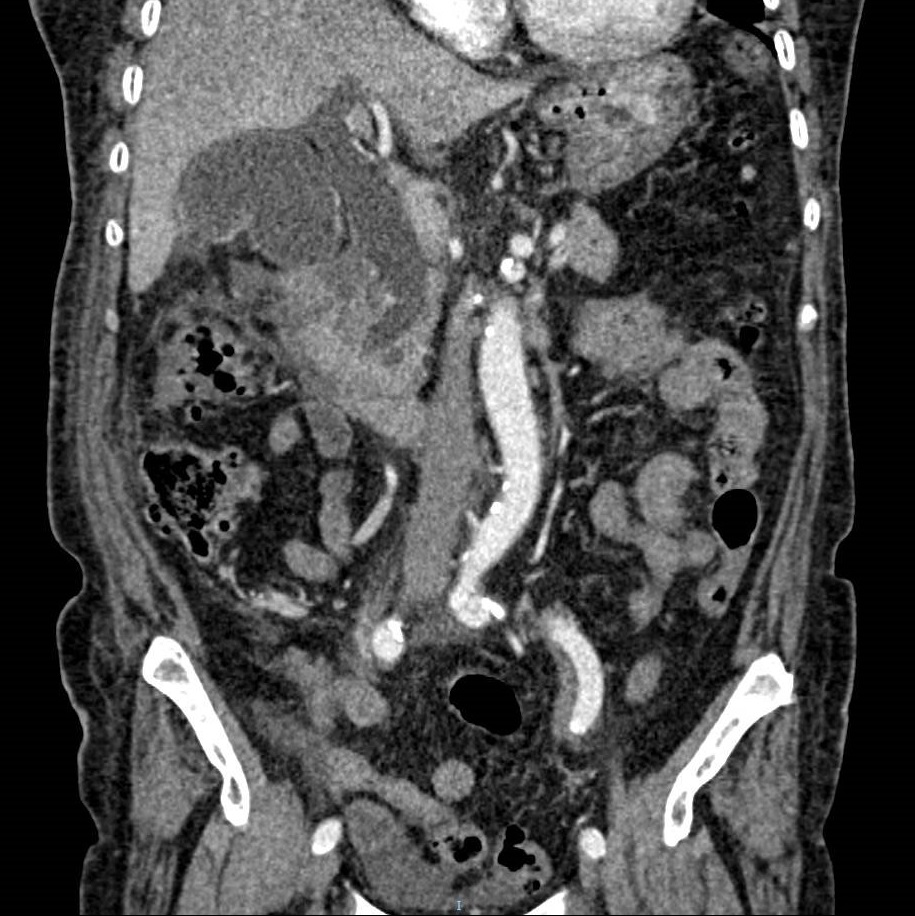
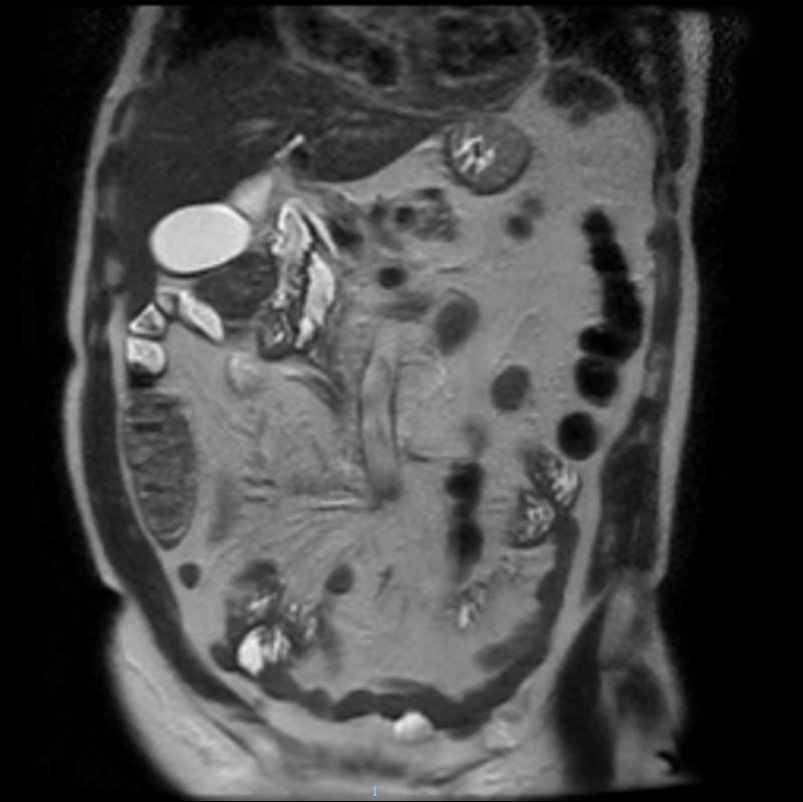
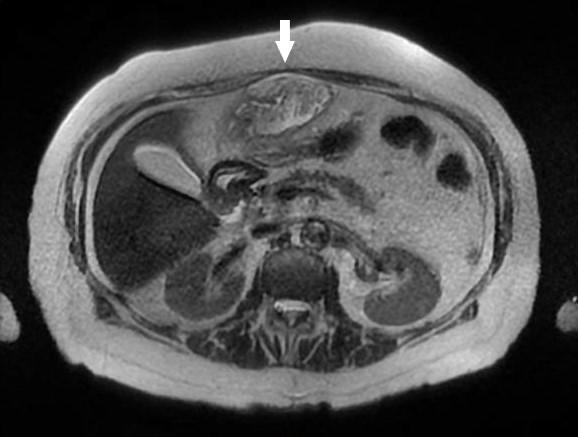
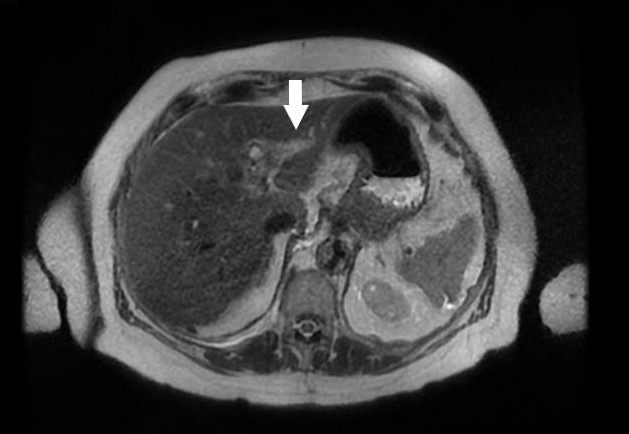
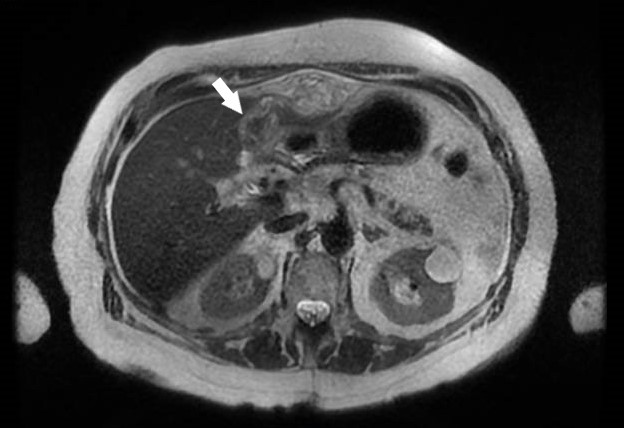
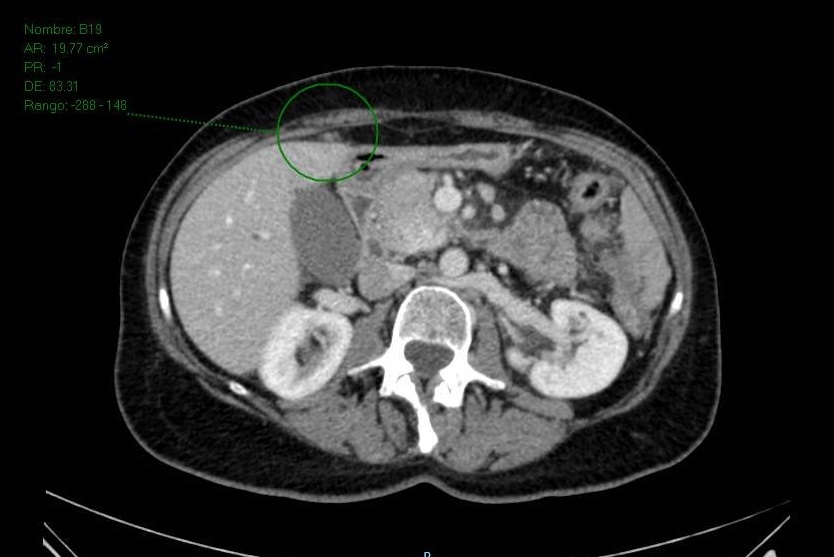
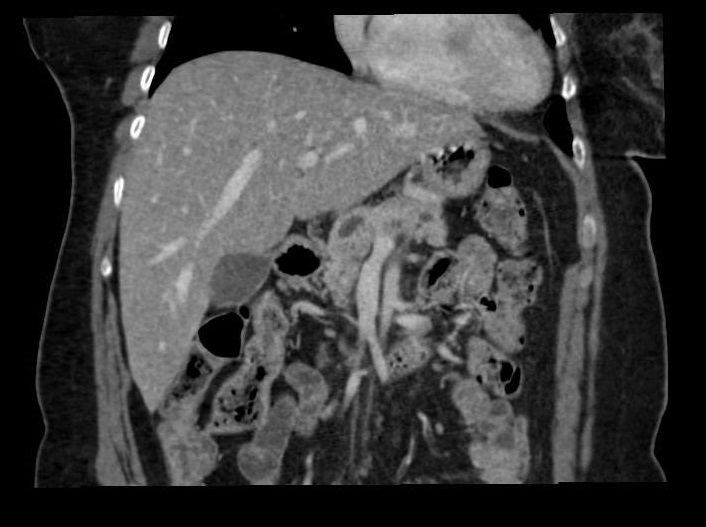
La agenesia del páncreas dorsal es una rara entidad que consiste en la ausencia de cuello, cuerpo y cola pancráticos. Esto es debido al doble origen embriológico del páncreas. El páncreas primitivo consta de un esbozo dorsal y otro ventral, que surgen de forma independiente para posteriormente fusionarse durante el desarrollo embriológico. La parte dorsal se origina a partir de un divertículo de la porción dorsal del duodeno, y de aquí derivan la porción craneal de la cabeza, el cuello, el cuerpo y la cola del páncreas. La parte ventral surge de un divertículo común junto con el colédoco, y a partir de este se forma la parte caudal de la cabeza y el proceso uncinado. A las 6 semanas, el esbozo ventral rota 270º para colocarse posteroinferiormente al esbozo dorsal y posteriormente fusionarse. La clínica puede estar ausente y presentarse como un hallazgo incidental, o bien detectado tras un estudio de dolor abdominal asociado o no a una pancreatitis aguda. La agenesia de páncreas dorsal también puede predisponer a desarrollar diabetes mellitus, ya que la mayoría de los islotes de Langerhans están en la cola y cuerpo. Existe mayor predisposición a desarrollar adenocarcinoma por la tendencia del páncreas residual a una respuesta compensadora. Nuestra actitud debe ser expectante y el tratamiento sintomático.
Caso Clínico
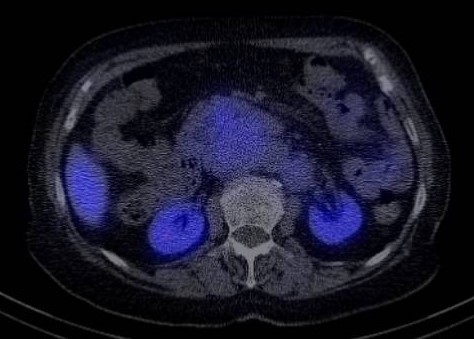
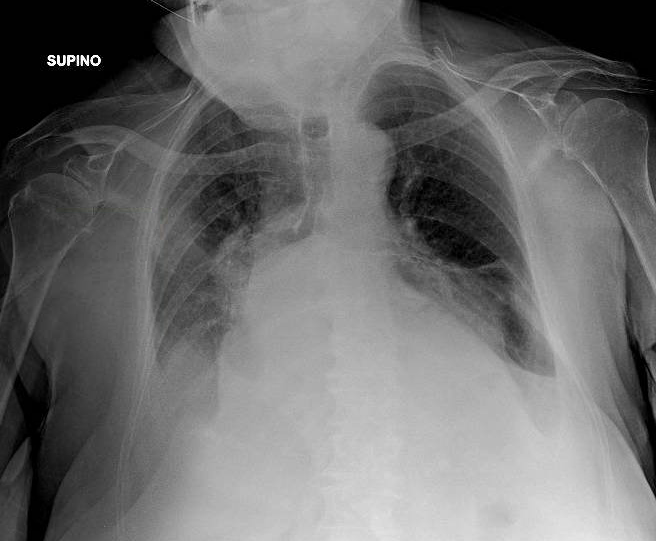
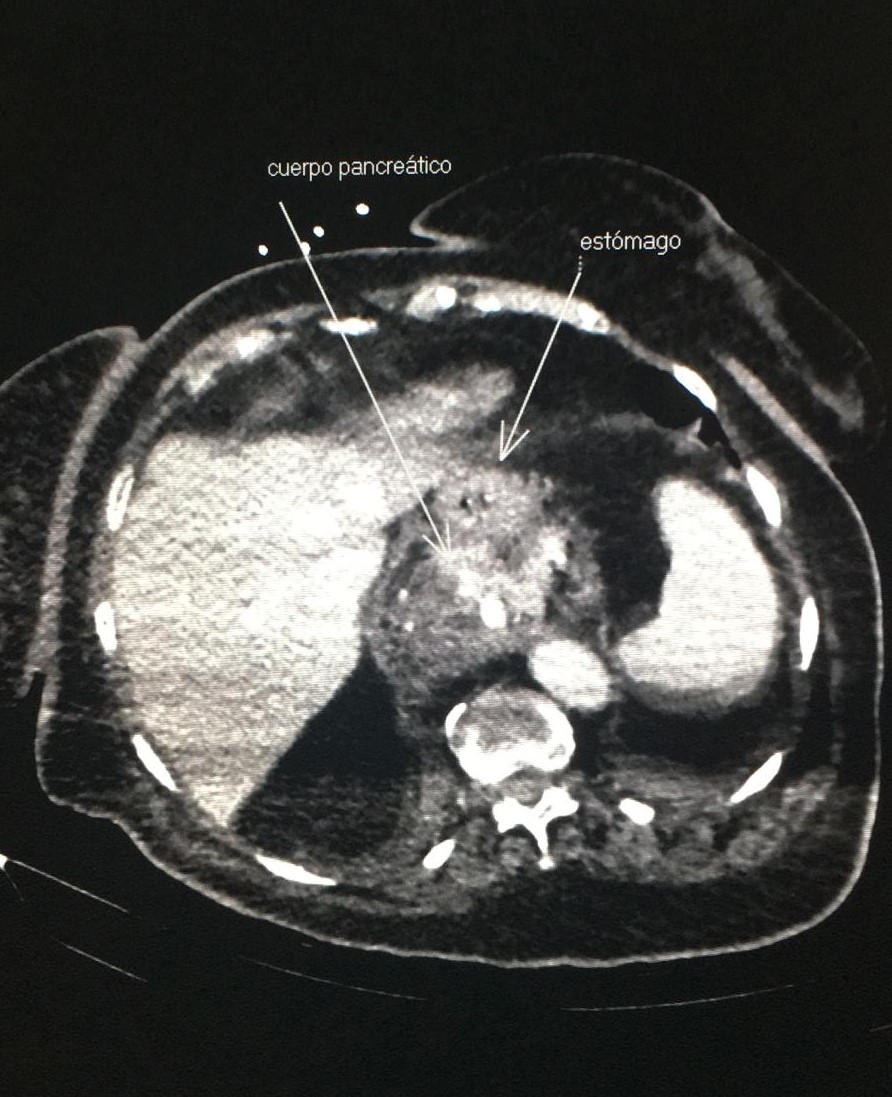
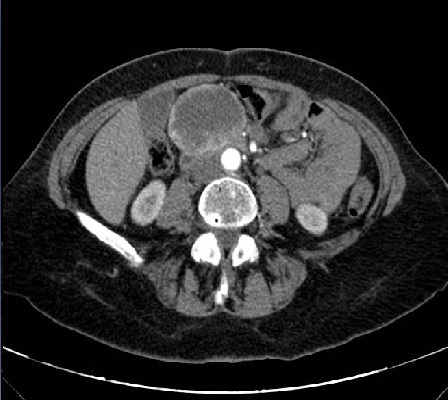
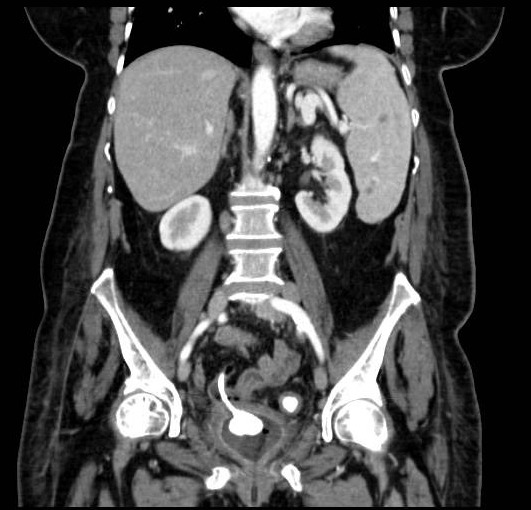
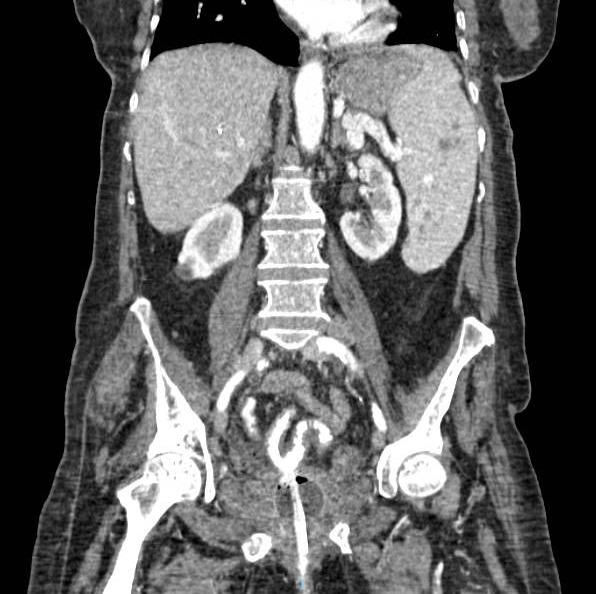
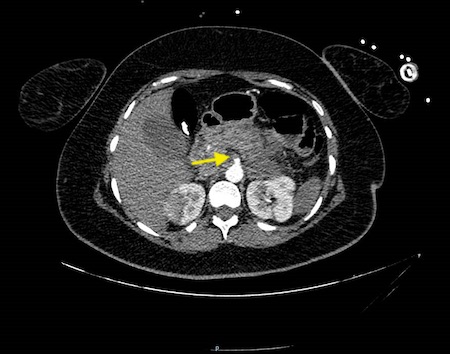
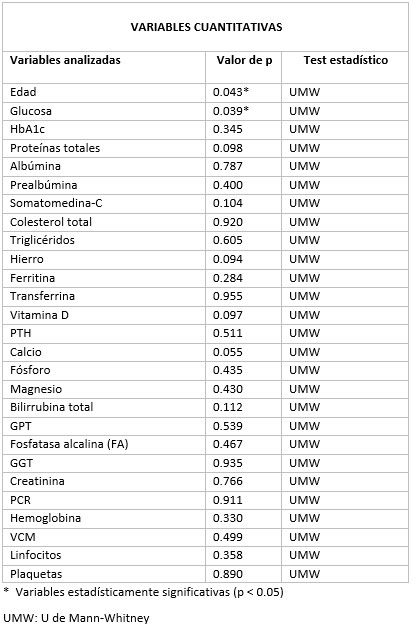
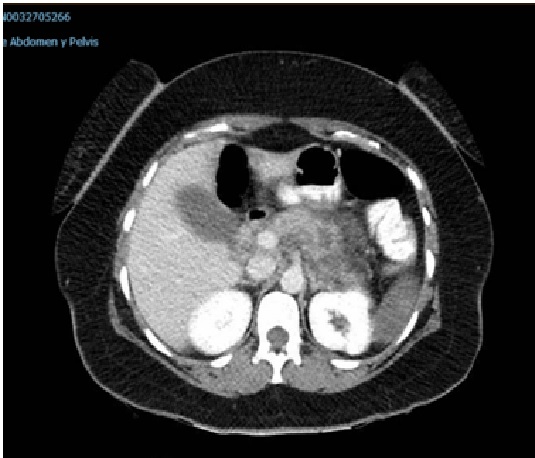
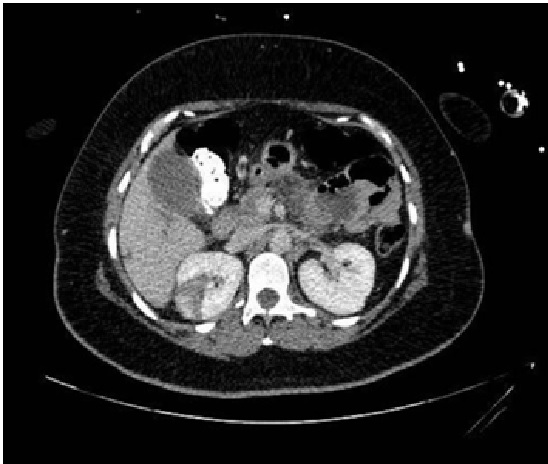
Paciente de 32 años que a raíz de un episodio de pancreatitis aguda leve es diagnosticada mediante pruebas de Figura de agenesia del páncreas dorsal. La paciente debuta con dolor abdominal epigástrico irradiado a espalda y aumento de lipasa y amilasa (> 3 LSN). En TAC de abdomen se observa ausencia de cuerpo y cola pancreáticos, estando en su lugar ocupado por asas intestinales (imágenes 1 y 2). Estos hallazgos son confirmados con colangio-RMN. Previamente al diagnóstico la paciente presenta molestias abdominales inespecíficas de forma ocasional. Tras el alta evoluciona favorablemente estando asintomática en consultas ambulatorias, sin presentar en el momento actual datos de pancreatitis crónica ni diabetes mellitus.
Paralelamente en estudio por parte de ginecología ha sido diagnosticada de malformación uterina, con útero unicorne incompleto. La agenesia dorsal del páncreas puede aparecer de forma aislada o asociada a otros síndromes heterotáxicos.
CP-074. CARCINOMA NEUROENDOCRINO METASTÁSICO DE ORIGEN INCIERTO
Vida Pérez L1, Fernández González R1, Martínez Rivas F2, Espejo Herrera JJ3, Carmona Asenjo ME4, Serrano Blanch R5
1UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba. 2Consulta Medicina Familiar y Comunitaria. Hospital Comarcal Infanta Margarita, Cabra. 3UGC Radiología Intervencionista. Complejo Hospitalario Regional Reina Sofía, Córdoba. 4UGC Medicina Nuclear. Complejo Hospitalario Regional Reina Sofía, Córdoba. 5UGC Oncología Médica. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: carcinoma neuroendocrino, adenopatías retroperitoneales, obstrucción biliar.
Introducción
Los tumores neuroendocrinos son infrecuentes. Aunque de manera habitual asientan en páncreas o tracto digestivo, pueden originarse en cualquier órgano. La mayoría son esporádicos aunque pueden aparecer en el contexto de síndromes hereditarios asociados a mutaciones germinales. Dentro de los gastroenteropancreáticos encontramos a los carcinomas pobremente diferenciados, de comportamiento agresivo y con frecuencia metastásicos.
Caso Clínico
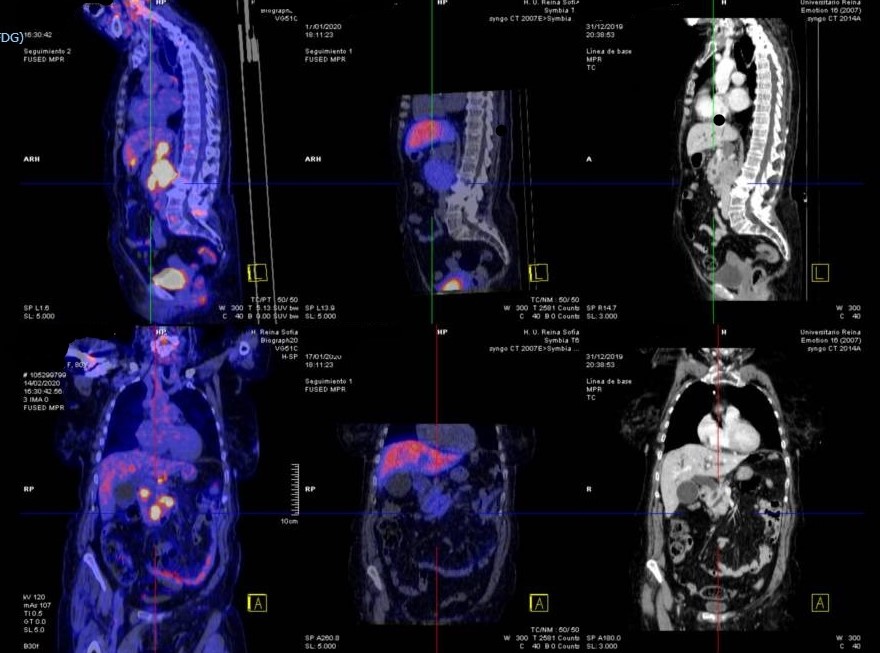
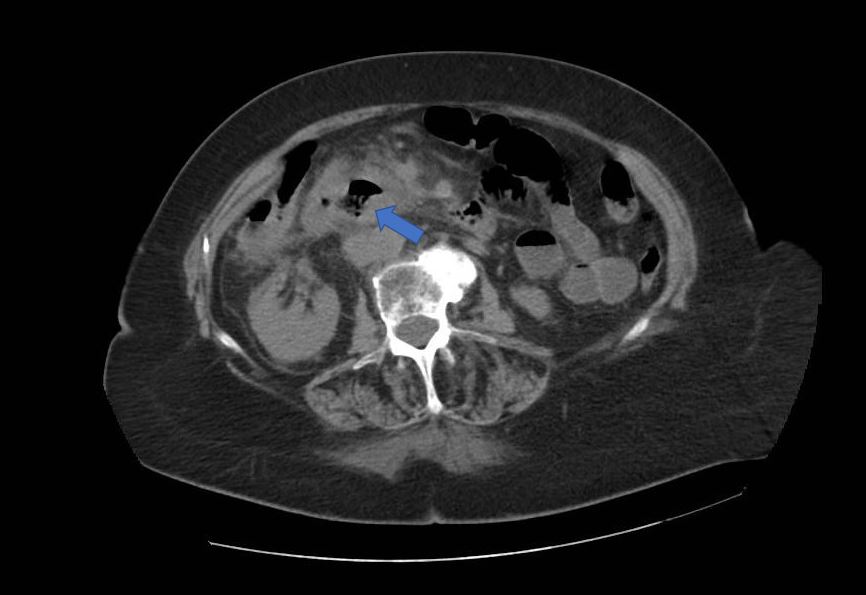
Paciente de 81 años que consulta por dolor abdominal en hipocondrio derecho. En la ecografía practicada al ingreso se apreció una masa de 50x30 mm que parecía depender de la cabeza del páncreas. Se completó estudio mediante colangio-resonancia que evidenció dilatación de la vesícula, de la vía biliar intrahepática y principal así como del conducto pancreático principal (Figura 1). El TC abdominal con contraste intravenoso evidenció una masa irregular y heterogénea posterior al proceso uncinado pancreático y en contacto con el mismo (Figura 2). No fue posible biopsia de la masa por ecoendoscopia pero sí por vía retroperitoneal bajo control tomográfico (Figura 3). Se completó estudio mediante resonancia hepática que objetivó dos lesiones focales de 14 y 9 mm en segmentos IVa y III compatibles con metástasis. La anatomía patológica fue compatible con carcinoma neuroendocrino pobremente diferenciado con inmunohistoquímica positiva a: CK AE1/AE3, CDX2 , Sinaptofisina , Cromogranina focal y alto índice proliferativo (60%). Se completó estudio mediante Gammagrafía y SPECT-TC de Receptores de Somatostatina (99mTc-Octreótido)(Figura 4) que mostró leve sobreexpresión de los mismos en las adenopatías (Krenning1). Finalmente se realizó PET/TC como estudio de tumor de origen desconocido que evidenció aumento focal del metabolismo glicídico en tercera porción duodenal (SUV máximo de 10,8) que podría corresponder a lesión primaria (Figura 5). La discordancia metabólica entre gammagrafía y PET sugiere comportamiento más agresivo y proliferativo. Ante los hallazgos la paciente fue remitida a Oncología donde se inició tratamiento con análogos de somatostatina (lanreótida) a la dosis inicial de 120 mg cada 28 días por vía subcutánea.
FIGURA 1
Colangio-resonancia. Dilatación de la vía biliar intra y extrahepática (colédoco de 14 mm) y aspecto arrosariado del conducto pancreático principal.
FIGURA 2
TC abdominopélvico. Masa sólida de 53x30 mm posterior al proceso uncinado del páncreas con cambios necrótico-quísticos y adenopatías circundantes.
FIGURA 3
Punción percutánea translumbar con aguja gruesa bajo control tomográfico de masa retroperitoneal adyacente a aorta abdominal.
Discusión
El caso presentado es una forma de presentación inusual de tumor neuroendocrino de probable localización intestinal con metástasis ganglionares en retroperitoneo que plantea el diagnóstico diferencial con otras patologías más prevalentes como los tumores biliopancreáticos. Son tumores raros y se asocian a mal pronóstico pues suelen diagnosticarse en estadios avanzados. En cuanto al tratamiento para tumores no resecables se incluyen los análogos de somatostatina, terapias biológicas, terapias dirigidas con radionúclidos, tratamientos locorregionales y quimioterapia en función de las características y síntomas del paciente.
CP-075. DIVERTICULITIS DUODENAL COMPLICADA CON PANCREATITIS EN PACIENTE DE EDAD AVANZADA
Del Pino Bellido P, Muñoz García-Borruel M, Aguilera Jaldo VI, Rodríguez Téllez M
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: divertículo duodenal, diverticulitis, pancreatitis.
Introducción
El duodeno es la segunda localización más frecuente de diverticulosis gastrointestinal (1-2%), después del colon (5-60%). Generalmente, los divertículos se localizan en la pared medial de la segunda porción duodenal, en la proximidad de la papila de Vater y la cabeza pancreática. Suele presentarse en la sexta o séptima década, siendo la mayoría de pacientes (90%) asintomáticos, o presentando síntomas inespecíficos (dolor abdominal, náuseas, vómitos…). Las complicaciones de los divertículos duodenales son raras e incluyen obstrucción intestinal, diverticulitis y sangrado gastrointestinal.
Caso Clínico
Paciente de 85 años, colecistectomizada en 2013, con colangitis secundaria a coledocolitiasis residual en 2015, resuelta mediante CPRE. Ingresa por dolor abdominal en epigastrio y fiebre. Analíticamente destaca leucocitosis (20290) con neutrofilia y PCR 78. En TC de abdomen urgente sin contraste (figura 1), se evidencia colección de 32 mm en cabeza pancreática, con líquido y gas en su interior y pared realzada, que provoca estenosis distal del colédoco con dilatación secundaria (15 mm). Se completa estudio con colangioRNM que describe que dicha lesión comunica con la luz duodenal y presenta características radiológicas compatibles con divertículo duodenal complicado con diverticulitis y absceso de 3cm, apreciando vía biliar extrahepática levemente dilatada, sin contenido en su interior.
Inicialmente se decide manejo conservador con antibioterapia (ceftriaxona y metronidazol) dada la edad y las comorbilidades de la paciente. A las dos semanas la paciente presenta cuadro clínico-analítico compatible con pancreatitis aguda y en controles por TC se aprecia evolución radiológica desfavorable, con leve aumento del tamaño del absceso y aparición de signos de pancreatitis aguda sin necrosis, con colecciones líquidas peripancreáticas. Se decide ecoendoscopia para drenaje del absceso (figuras 3 y 4) pero no es abordable por dicha técnica. Se replantea tratamiento quirúrgico que finalmente se desestima, por lo que se escala antibioterapia (meropenem) y tras dos semanas de tratamiento se comprueba la resolución del absceso, así como la mejoría clínica y radiológica de la pancreatitis (figura 2).
FIGURA 1
TC sin contraste: colección líquida medial con líquido y gas en su interior, con realce de su pared situada en la cabeza de páncreas.
FIGURA 2
TC con contraste al alta, donde se evidencia desaparición de colección líquida conocida, localizada en el surco pancreático duodenal.
Discusión
La diverticulitis duodenal es una patología infrecuente, aunque con complicaciones asociadas potencialmente severas. Al presentar una clínica inespecífica el diagnóstico es difícil y rara vez se sospecha inicialmente. Nuestra paciente presentó una clínica de dolor abdominal, fiebre y leucocitosis, con hallazgo de colección peripancreática en TC, estableciéndose el diagnóstico mediante colangio-RNM. Actualmente el tratamiento de elección es médico con antibioterapia de amplio espectro, en pacientes estables, dada la alta tasa de complicaciones asociadas con la cirugía como fuga duodenal, fístula y sepsis.
CP-076. EFECTO ADVERSO INFRECUENTE: PANCREATITIS AGUDA INDUCIDA POR RUCAPARIB
Amado Villanueva PP, Moreno Moraleda I, Lázaro Sáez M
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: inhibidor de la enzima poliadn ribosa polimerasa, pancreatitis aguda, efectos adversos de medicament.
Introducción
Determinar la etiología de la pancreatitis aguda es uno de los objetivos más importantes en el manejo de la enfermedad para prevenir la recurrencia y complicacaciones.
El rucaparib es un inhibidor de la enzima poliADN ribosa polimerasa (PARP1), dicha proteína es importante para la reparación del ADN donde está mutada en los procesos tumorales por lo que este fármaco se usa como agente quimioterápico.
Por motivos señalados presentamos el caso de un efecto adverso no documentado en un quimioterápico con pocos años de aprobación para este tipo de cáncer.
Caso Clínico
Paciente mujer de 66 años con antecedente de diagnóstico de adenocarcinoma seroso de alto grado IIIC en 2008 intervenido, metástasis de trompa 2011 intervenida, implante peritoneal 2015, que ha precisado tratamiento quimioterapico con carboplatino, cisplatino, trabectedina y en noviembre 2018 con rucaparib desde hace 3 meses. No refiere hábitos tóxicos.
Acude a urgencias por presentar dolor abdominal de 24 horas de evolución asociado a náuseas y vómitos a la ingesta de alimentos, tras no mejoría del dolor con analgésicos y posterior pruebas complementarias se objetiva una amilasa de 778 y lipasa de 2205 con leve elevación de las transaminasas y sin patrón colestásico por lo que se ingresa con diagnóstico de pancreatitis aguda.
En la prueba Figura se observó una vesícula alitiásica con paredes finas y en el páncreas cambios inflamatorios y edematosos con líquido peripancreático corroborando el diagnóstico inicial.
Discusión
Se realizó el estudio etiológico descartándose otras alternativas que pudieran justificar la enfermedad del paciente.
El Rucaparib como cualquier otro fármaco quimoterápico tiene variados efectos adversos, aunque produce sintomatología digestiva (dolor abdominal y distensión, náuseas, vómitos) no se ha documentado que la pancreatitis aguda sea uno de ellos por ello la importancia de este caso
CP-077. HAMARTOMATOSIS BILIAR MÚLTIPLE COMO HALLAZGO INCIDENTAL EN PRUEBA DE Figura
Barranco Castro D, Galván Fernández MD, Lorenzo González L, Benítez Rodríguez B, Caunedo Álvarez Á
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: hamartomatosis biliar múltiple, enfermedad de los complejos de von meyenburg.
Introducción
La hamartomatosis biliar múltiple (HBM) o enfermedad de los complejos de Von Meyenburg es una malformación congénita benigna secundaria a una falta de involución embrionaria de los conductos biliares. Esto da lugar a pequeñas lesiones hamartomatosas focales, constituidas por conductos biliares intrahepáticos dilatados, que no comunican con el árbol biliar, y se incluyen dentro de un estroma de colágeno denso.
Caso Clínico
Mujer de 74 años sin antecedentes patológicos de interés. Derivada a consultas de aparato digestivo por dolor intermitente a nivel de hipocondrio derecho irradiado a espalda, de unos 4 meses de evolución. No se acompaña de náuseas, vómitos, cambios en el hábito deposicional ni clínica constitucional. No ictericia, coluria ni acolia asociada. Exploración anodina.
Inicialmente se solicita analítica con perfil hepático y ecografía de abdomen para descartar patología hepatobiliopancreática. Los parámetros analíticos son normales y el informe ecográfico describe la existencia de colelitiasis y un hígado de tamaño normal y ecogenicidad heterogénea, aunque sin evidenciar claras lesiones focales. Con estos hallazgos y dada la persistencia del dolor, se solicita TAC de abdomen con contraste.
El informe radiológico describe a nivel del hígado la presencia de múltiples lesiones ocupantes de espacio hipodensas, de 2-3mm de tamaño, que podrían tratarse de múltiples quistes o estar en relación con hamartomas biliares en el contexto de la enfermedad de Von Meyenburg.
Para confirmar el diagnóstico se solicitó resonancia magnética de abdomen con contraste, visualizándose (imágenes 1 y 2) un hígado de tamaño normal con innumerables lesiones focales milimétricas a lo largo de todo su parénquima, hiperintensas en T2 e hipointensas en T1, que en el estudio dinámico con contraste no muestran realces significativos, aunque en fases tardías algunas presentan un pequeño halo periférico hipercaptante. Todos estos hallazgos, ratifican el diagnóstico de HBM.
Actualmente la paciente continua en seguimiento en nuestras consultas, pendiente de colecistectomía debido a colelitiasis sintomática.
Discusión
La HBM tiene una incidencia del 0,6-5,6%, siendo en la mayoría de los casos diagnosticada de forma incidental en estudios de Figura. La sintomatología se presenta de forma excepcional en relación con la presencia de múltiples lesiones junto a elevación de gamma-glutamiltransferasa. Generalmente es suficiente el manejo médico y seguimiento para evaluar evolución, reservándose la cirugía para sintomatología obstructiva o por compresión de estructuras.
CP-078. HERNIA PARAESOFÁGICA TIPO IV: UNA CAUSA INFRECUENTE DE PANCREATITIS AGUDA
Osorio Marruecos M, Ruiz Pagés MT, Listán Álvarez JC
UGC Aparato Digestivo. Hospital de Especialidades de Puerto Real, Puerto Real.
Palabras clave: hernia hiato, pancreatitis aguda.
Introducción
La hernia de hiato es una entidad que hace referencia al ascenso de elementos de la cavidad abdominal hacia la cavidad torácica a través del hiato diafragmático. Existen dos grupos: hernia por deslizamiento o tipo I que representa el porcentaje mayor y las hernias paraesofágicas (tipo II, III y IV).
La hernia paraesofágica tipo IV es un grupo minoritario. Se define como una herniación del estómago acompañado de otro órgano abdominal (colon, bazo, intestino delgado o páncreas).
Caso Clínico
Paciente mujer de 84 años, con antecedentes de demencia senil y sin consumo de tóxicos, que ingresa por episodio de dolor epigástrico irradiado en cinturón de horas de evolución. En control analítico destaca hiperamilasemia catalogándose el cuadro de pancreatitis aguda. Se realiza ecografía de abdomen y pruebas complementarias sin que se objetive causa posible de la inflamación pancreática. Ante persistencia de dolor y elevación de reactantes de fase aguda se decide realización de TC abdomen de control con evidencia de una gran hernia de hiato que engloba el estómago prácticamente por completo y el cuerpo del páncreas, con presencia de líquido libre peripancreático en el saco herniario, así como presencia de la arteria gástrica izquierda y la vena esplénica. (Figura 2). Ante dichos hallazgos se establece dicha hernia como causa del cuadro de pancreatitis aguda de la paciente.
Tras sueroterapia y medidas terapéuticas adecuadas la paciente presentó mejoría clínica y disminución de parámetros inflamatorios.
Durante su ingreso se mantuvo sin compromiso respiratorio ni clínica derivada de dicha ocupación torácica. Debido a la edad y morbilidad de la paciente se consensuó con paciente y familia la no intervención quirúrgica.
Discusión
La hernia transhiatal del páncreas es una entidad muy poco frecuente, reportándose hasta el momento muy pocos casos en la literatura. Constituye una entidad que rara vez se presenta como causa de pancreatitis aguda.
Entre las manifestaciones clínicas de las hernias paraesofágicas encontramos dolor epigástrico o subesternal, plenitud postpandrial o náuseas. El tratamiento idóneo cuando dan sintomatología se basa en la reparación quirúrgica.
CP-079. MASA PANCREÁTICA: NO SIEMPRE ES LO QUE PARECE
López González J1, Delgado Maroto A1, Cuello Entrena E2, Amado Villanueva PP1
1UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería. 2Servicio Anatomía Patológica. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: tumor gist, ecoendoscopia, paaf.
Introducción
El tumor estromal gastrointestinal (GIST) es el tumor mesenquimal más frecuente en el tracto digestivo. La mayoría de los GIST poseen una característica mutación con ganancia de función del gen c-KIT.
La localización más frecuente de estos tumores es la gástrica (50-70%), seguida de la yeyunal e ileal. El origen en duodeno es menos frecuente, representando únicamente un 5% de estos tumores.
Caso Clínico
Mujer de 64 años con antecedente personal de gastrectomía en y de roux que es derivada desde su médico de Atención Primaria por cuadro de anemia microcítica sin signos de sangrado digestivo, hiporexia y síndrome constitucional, con pérdida de unos 11 kilos en un año. A la exploración, destacaba a nivel abdominal una masa mesogástrica dolorosa a la palpación, sin otros datos de interés.
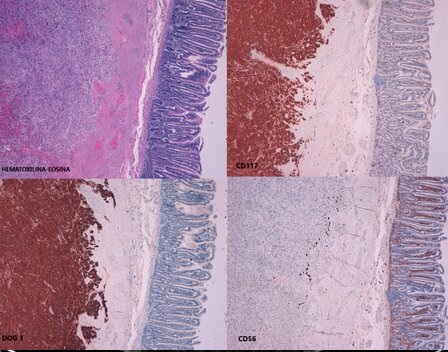
Durante su estancia en planta de hospitalización se realiza analítica sanguínea con Marcadores tumorales (alfafetoproteína, Ca 125, Ca 15.3 y Ca 19.9 normales), endoscopias digestivas alta y baja también normales y TAC toraco-abdominal, donde se objetiva masa de 5.8x4.4 cm a nivel del proceso unciado pancreático, heterogénea y con centro hipodenso (figura 1). Tras dichos hallazgos, ante la sospecha de neoplasia pancreática, se solicita Ecoendoscopia con Punción-aspiración con aguja fina, donde se observa masa pancreática compatible con tumor quístico mucinoso de unos 44 mm, con toma de biopsia. El análisis de la muestra obtenida determina la presencia de tumor del estroma Extra-gastrointestinal de origen pancreático, con positividad para CD34, c-KIT, DOG-1 y vimentina.
Tras estos resultados, se programa cirugía, donde se realiza resección de la tumoración, objetivándose en el acto intraoperatorio finalmente que el origen de la lesión es la tercera porción duodenal. El análisis de la pieza quirúrgica confirmó nuevamente el origen mesenquimal de la tumoración, confirmando el diagnóstico de tumor del estroma gastrointestinal de origen duodenal.
Discusión
Los tumores localizados en la cabeza de páncreas o en el mesenterio duodenal no siempre pueden ser completamente diagnosticados mediante pruebas de Figura, por lo que contar con la histología (obtenida con Ecoendoscopia) de estas lesiones puede cambiar de forma drástica el manejo quirúrgico de las mismas. Mientras que en las neoplasias de cabeza de páncreas se suele realizar resección radical con linfadenectomía asociada, en los tumores del estroma gastrointestinal de duodeno o páncreas basta en muchos casos con una resección simple del tumor, lo cual resalta la importancia de un certero diagnóstico anatomopatológico de estas lesiones.
CP-080. MIGRACIÓN DE ENDOPRÓTESIS BILIAR COMO CAUSA DE FÍSTULA ENTEROVESICAL
Jiménez-Riera G, Martínez-Baena D, Lorente-Herce JM, Parra-Membrives P
UGC Cirugía General y Digestiva. Complejo Hospitalario de Especialidades Virgen de Valme, Sevilla.
Palabras clave: endoprótesis biliar, migración, fístula enterovesical.
Introducción
El uso de prótesis biliares forma parte del tratamiento de múltiples enfermedades benignas y malignas biliopancreáticas. Aunque la mayoría de los stents migrados son expulsados sin provocar síntomas, en ocasiones puede provocar complicaciones. Las más frecuentes son las perforaciones duodenales debido a su angulación, pero existen casos de perforación en otras localizaciones donde el intestino está fijo de forma congénita o adquirida impidiendo su progresión (colon derecho, hernias, adherencias). Presentamos un caso de una fístula enterovesical causada por la migración de una endoprótesis biliar en una paciente con antecedente de enteritis y cistopatía rádica.
Caso Clínico
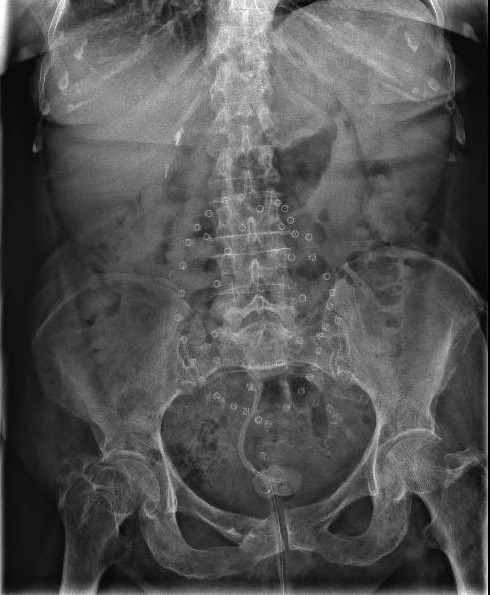
Mujer de 83 años, con antecedentes de histerectomía, doble anexectomía y braquiterapia por adenocarcinoma de endometrio, con cuadros de suboclusión por enteritis y cistopatía rádica, eventroplastia, colecistectomía, portadora de endoprótesis biliar tras una colangitis aguda por coledocolitiasis (no retirada por abandono del seguimiento) e infecciones urinarias de repetición. Consulta por fecaluria, síndrome miccional y dolor abdominal. Requiere sondaje por globo vesical, obteniéndose abundante material fecal. En la radiografía simple de abdomen (figura 1) se aprecia una Figura radiopaca alargada y otra redondeada en pelvis. La TAC con contraste intravenoso (figura 2) muestra en la vejiga una Figura redondeada de densidad calcio y una estructura tubular que se introduce en la vejiga desde un asa de íleon (prótesis transpapilar migrada). Tras administración de contraste a través de la sonda (figura 3) se observa llenado de íleon, sugiriendo una fístula enterovesical. Tras optimización nutricional se procede a la realización de una laparotomía exploradora, adhesiolisis y liberación de íleon terminal de cúpula vesical, retirada de prótesis y litiasis, ilecequectomía, anastomosis ileocólica y rafia vesical. El postoperatorio cursó sin incidencias de interés.
FIGURA 1
Se visualiza una Figura redondeada en pelvis, de densidad calcio, una Figura radiopaca alargada superpuesta a la anterior.
Discusión
Las migraciones de las prótesis biliares pueden ser proximales o distales. Las distales se producen hasta en un 6%. El riesgo de migración en mayor en casos de patología benigna. La mayoría son expulsadas a través del tubo digestivo sin complicaciones, pero pueden provocar perforaciones intestinales, generalmente en el duodeno, ciego, colon sigmoides, zonas fijas por adherencias o por hernias. La perforación libre es el cuadro más frecuentemente provocado, seguido de fístulas colovesicales o colovaginales, siendo la aparición de una fístula enterovesical con vesicolitiasis asociada un escenario extremadamente excepcional.
Es importante realizar un control de las prótesis biliares migradas y plantear su recuperación si no son expulsadas espontáneamente. Inicialmente por vía endoscópica y, en el caso de que este abordaje no sea posible, proponer una cirugía precoz para evitar futuras complicaciones.
CP-081. PANCREATITIS AGUDA ISQUÉMICA COMO DEBUT DE TROMBOSIS AÓRTICA PRIMARIA
Molina Villalba C, Vázquez Rodríguez JA, Gómez Torres KM, Gallego Rojo FJ
UGC Aparato Digestivo. Complejo Hospitalario de Poniente, Ejido, El.
Palabras clave: pancreatitis aguda, isquemia pancreática, trombosis aórtica.
Introducción
La isquemia pancreática es una causa rara de pancreatitis aguda, dado que es un órgano con un amplio aporte vascular.
Caso Clínico
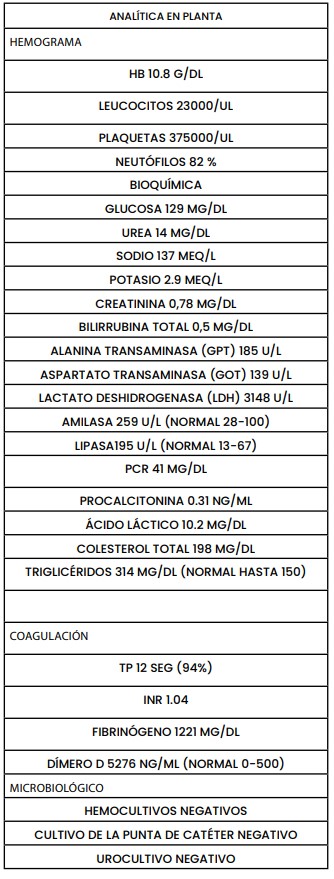
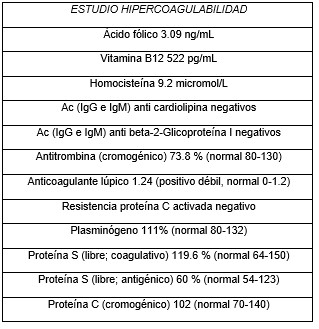
Mujer de 39 años con obesidad, hipertensión arterial y preeclampsia grave en el embarazo. Ingresó en digestivo por cuadro de 4 días de evolución de epigastralgia irradiada a hipocondrios y a espalda, asociando náuseas y vómitos al inicio del cuadro. A la exploración presentaba dolor abdominal generalizado, más intenso en epigastrio, sin peritonismo. Se realizaron analítica (tabla 1) y ecografía abdominal urgentes, observándose vesícula alitiásica y vía biliar normal. Dada la duda diagnóstica, se realizó TAC abdominal con contraste (figura 1-4) que informó de un defecto de captación a nivel del cuerpo de páncreas y edema de la grasa peripancreática sugerente de pancreatitis isquémica con necrosis < 20%, junto con amputación brusca del tronco celíaco sin visualizarse repleción en arteria hepática ni arteria esplénica. Además, hipodensidad difusa del bazo compatible con infarto esplénico completo, pequeños infartos subcapsulares hepáticos y trombo de 23 mm adherido a pared posterior de aorta torácica distal; confirmándose dichos hallazgos en angioTAC. Se remitió a cirugía vascular, con colocación de endoprótesis aórtica urgente y anticoagulación. En análisis posteriores (tabla 2) se descartaron infecciones, enfermedades autoinmunes, neoplasias y trombofilias (tabla 3). Se realizó estudio cardiológico sin objetivar patología y estudio genético de trombofilia sin alteraciones. Durante el ingreso, evolucionó favorablemente con manejo conservador del infarto esplénico y la necrosis pancreática, sin necesidad de abordaje quirúrgico del tronco celíaco.
Discusión
Los eventos vasculares abdominales suelen ser secundarios a patología infecciosa, neoplásica o patología inflamatoria como la pancreatitis aguda. En nuestro caso se descartaron otras causas de pancreatitis aguda (biliar, enólica, hipertrigliceridémica, famacológica, autoinmune) y la persistencia del trombo en aorta y en tronco celíaco confirmó el origen isquémico de esta.
La pancreatitis isquémica puede deberse a complicaciones de cirugía mayor (cardíaca, trasplante pancreático), quimioembolización de hepatocarcinoma, shock hemorrágico, eventos cardioembólicos (fibrilación auricular, endocarditis, aneurisma ventricular…), afectación ateroesclerótica de tronco celíaco y arteria mesentérica superior, así como a aneurismas, disección, lesiones traumáticas o estados de hipercoagulabilidad.
La trombosis aórtica primaria, descrita en casos aislados, consiste en la aparición de un trombo en aorta torácica descendente sin identificar patología sobre la misma, como es el caso que se presenta. El diagnóstico se realiza con TAC multicorte con contraste que permite además identificar complicaciones isquémicas.
La anticoagulación, la trombólisis y la cirugía con colocación de endoprótesis o trombectomía son opciones terapéuticas.
CP-082. PANCREATITIS AUTOINMUNE: EXPERIENCIA CLÍNICA EN NUESTRO CENTRO
Moreno Moraleda I, Diéguez Castillo C, Delgado Maroto A, Anguita Montes F
Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: enfermedades relacionadas igg4, pancreatitis autoinmune, inmunosupresores.
Introducción
La pancreatitis autoinmune (PAI) es una patología pancreática inmunomediada poco frecuente, que se asocia con otros trastornos de presunta etiología autoinmune, incluyendo la colangitis IgG4 y la enfermedad inflamatoria intestinal.
Material y métodos
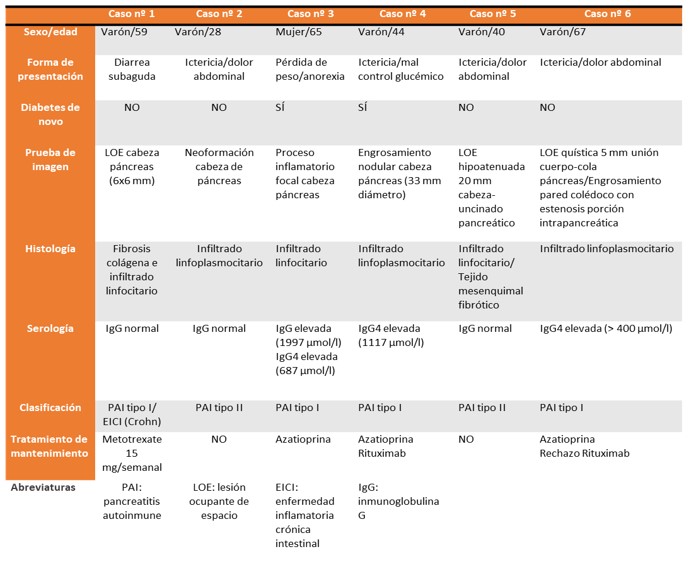
Revisión de carácter retrosprectivo en la que incluimos seis casos con diagnóstico de pancreatitis autoinmune en nuestro centro (C.H. Torrecárdenas), en un periodo comprendido entre enero de 2010 y diciembre de 2019 (tabla 1), obteniendo los datos de nuestra base informática Diraya Clínico.
Resultados
En nuestro hospital se han diagnosticado un total de 6 casos desde 2010 (tabla 2). La mayoría son varones (83%), con una edad media de 50.5 años. La forma de presentación varía en cada caso: ictericia y dolor abdominal es lo más frecuente (66%) y solo en dos casos (33%) se diagnosticó diabetes en su evolución.
En la mayoría de los casos se observó en las pruebas de Figura una LOE en cabeza de páncreas (83%) y solo en un caso (16%) se observó una LOE en unión cuerpo-cola de páncreas. En todos los casos en la histología se evidenció un infiltrado linfocitario (100%).
En cuanto a la serología, la mitad de los casos cursaron con inmunoglobulinas elevadas, siendo los tres casos diagnosticados como PAI tipo I. La otra mitad presentaron inmunoglobulinas normales: dos de ellos se diagnosticaron como PAI tipo II, y un caso se diagnosticó como PAI tipo I al presentar de forma simultánea dos enfermedades inmunomediadas (EII y PAI).
Los pacientes diagnosticados de PAI tipo II no han precisado tratamiento de mantenimiento (33%); al contrario de lo que sucede con los pacientes diagnosticados de PAI tipo I: tres casos han precisado inmunosupresores (metotrexato y azatioprina) y un caso ha precisado un anticuerpo monoclonal (rituximab).
Conclusiones
La pancreatitis autoinmune (PAI) es una forma especial de pancreatitis crónica que responde al tratamiento con glucocorticoides.
Clínicamente se manifiesta por dolor abdominal, con o sin ictericia, y pérdida de peso. Existe generalmente un aumento difuso o focal del páncreas y estenosis variable de la longitud del Wirsung en las pruebas de Figura.
Se distinguen dos tipos clínico-histológicos: el tipo I que se acompaña de elevación de inmunoglobulinas, especialmente IgG4; y el tipo II que afecta únicamente al páncreas y no se acompaña de alteraciones serológicas.
La resolución, parcial o total, de la lesión pancreática tras iniciar tratamiento con prednisona apoya el diagnóstico, aunque en muchas ocasiones es difícil distinguirla del cáncer de páncreas, formando parte de un complejo reto diagnóstico.
CP-083. PANCREATITIS CRÓNICA: ANÁLISIS DE LOS FACTORES IMPLICADOS EN LA PROGRESIÓN DE LA ENFERMEDAD
Dieguez Castillo C1, Jimenez Luna C2, Amado Villanueva PP1, Gonzalez-Ramirez AR3, Martín Ruiz JL4
1UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería. 2Grupo Investigación. Complejo Hospitalario de Granada, Granada. 3Departamento Investigación. Hospital San Cecilio, Granada. 4UGC Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: tabaco, alcohol, terapia sustitutiva con enzimas pancreaticas (tsep).
Introducción
Analizar la implicación de factores etiológicos (Tabaco y alcohol) y medidas terapéuticas (terapia sustitutiva con enzimas pancreáticas) en la progresión de la enfermedad.
Material y métodos
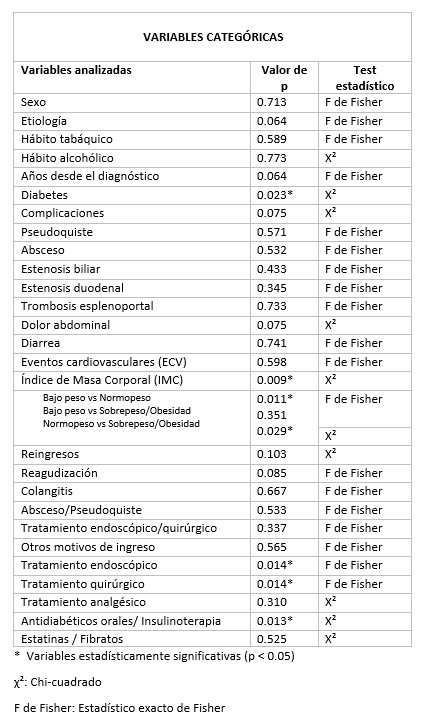
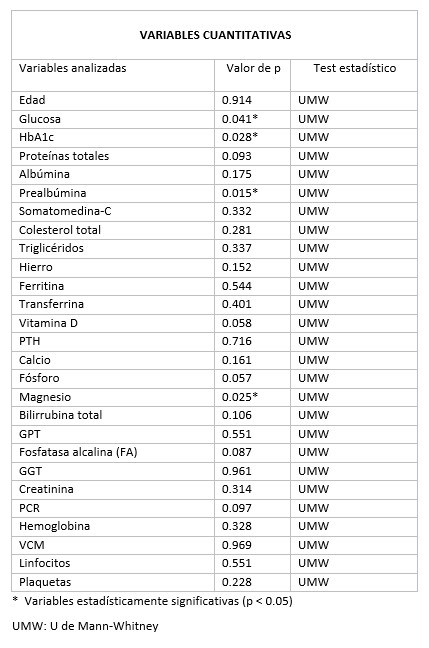
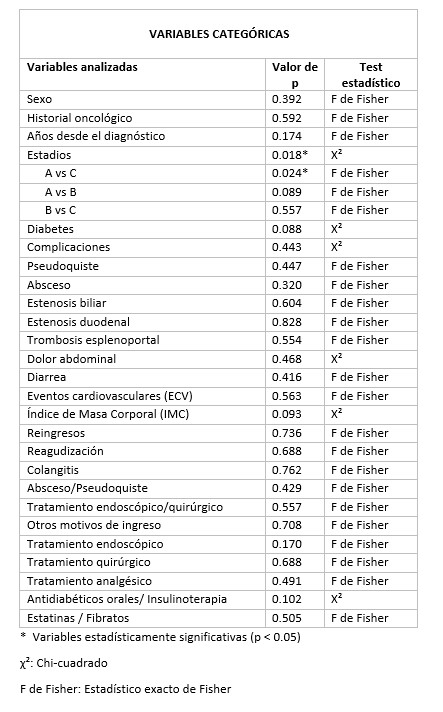
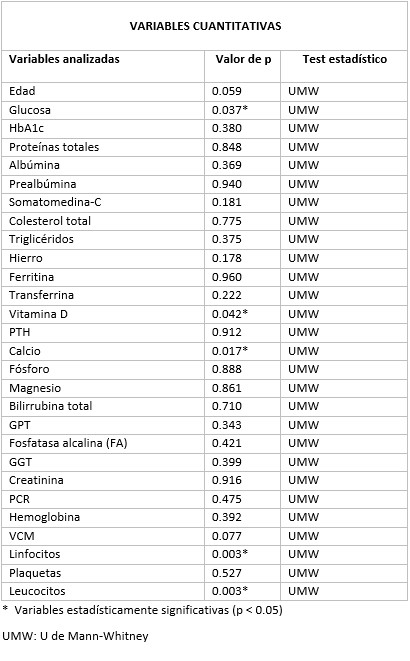
Se han reclutado 50 pacientes con diagnóstico de pancreatitis crónica y agrupado en función de las variables Tabaco, alcohol y TSEP. Posteriormente, se han analizado para ambos grupos distintas variables clínicas (ingresos hospitalarios, complicaciones, eventos cardiovasculares) y analíticos (parámetros nutricionales, reactantes de fase aguda, elastasa fecal) implicados en la progresión de la enfermedad (tablas 1-3)
Resultados
El grupo con TSEP muestra un mayor porcentaje de diabéticos, menor necesidad de tratamiento endoscópico y normalización del índice de masa corporal (table 1a), aunque con algunos parámetros nutricionales alterados (magnesio y prealbúmina) (table 1b). El grupo con consumo de Tabaco y alcohol muestra peor control glucémico (tablas 2b y 3b). El grupo de Tabaco muestra niveles bajos de calcio y vitamin D y aumento de reactantes de fase aguda (leucocitos y linfocitos) (table 2b). El grupo de alcohol presenta un rango de edad medio mayor, sin presentar una asociación con la dosis (table 3b).
Conclusiones
Se muestra una asociación positive en el desarrollo de insuficiencia pancreática tanto exocrine (IPE) como endocrina (DM). El TSEP disminuye la necesidad de tratamiento invasive y precisa de ajustes para mejorar aún más el perfil nutricional. El tabaco y alcohol parecen favorecer la progresión de PC, induciendo el tabaco un estado proinflamatorio. El Tabaco también altera el metabolismo del calcio lo que podría predisponer a osteoporosis.
CP-084. PANCREATITIS ISQUÉMICA SECUNDARIA A OCLUSIÓN VASCULAR MÚLTIPLE
Calvo Bernal MM, López González J, Lázaro Sáez M
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: pancreatitis aguda, isquemia pancreática, trombosis.
Introducción
La isquemia pancreática es una causa poco frecuente de pancreatitis aguda(PA). Su frecuencia se estima entre un 5-8%.
La PA isquémica es una enfermedad grave con una tasa de mortalidad cercana al 64% por lo que ha de incluirse en el diagnóstico diferencial para una corrección precoz de los factores precipitantes.
Presentamos el caso de una mujer joven que presentó una pancreatitis aguda en el contexto de una trombosis arterial.
Caso Clínico
Mujer de 39 años con antecedente de hipertensión arterial que acude a urgencias por dolor abdominal difuso de 4 días de evolución con náuseas y vómitos. No presenta fiebre ni otra sintomatología asociada.
En analítica destaca una elevación de reactantes de fase aguda (leucocitosis 23.4x103 y PCR 24 mg/dl) y LDH 500 mg/dl. Dada la persistencia de intenso dolor tras analgesia, se realiza TAC abdominal con hallazgos de trombosis aórtica, oclusión del tronco celiaco así como infarto esplénico y hepático y pancreatitis aguda con necrosis a nivel del cuerpo del 20%.
Se realiza intervención quirúrgica urgente con colocación de endoprótesis aórtica y se administra heparina en dosis terapéuticas.
Durante el postoperatorio, la paciente evoluciona lentamente, con episodios de dolor abdominal, picos de febrícula y vómitos ocasionales. Se realiza endoscopia alta que descarta lesiones isquémicas del tracto superior. En el TAC abdominal de control se objetiva estabilidad de la pancreatitis, con persistencia de necrosis sin colecciones asociadas. Los reactantes de fase aguda disminuyen progresivamente. Tras la mejoría clínica y tolerancia oral adecuada es dada de alta.
Discusión
La isquemia pancreática es una causa poco frecuente de pancreatitis aguda(PA). Su frecuencia se estima entre un 5-8%.
Puede aparecer de forma secundaria el contexto de una PA de otro origen o puede ser la etiología inicial de la pancreatitis. Esto ocurre con mayor probabilidad tras una cirugía abdominal, episodios de hipoperfusión u oclusión vascular o en relación con vasculitis.
Respecto al diagnóstico, la pancreatitis isquémica es difícil de reconocer, debido a su asociación con múltiples disfunciones orgánicas. Deben descartarse otras etiologías de pancreatitis. La TAC abdominal es la prueba de Figura de elección.
La clave del tratamiento es la restauración de la función circulatoria con fluidoterapia intensiva. Debe asociarse a heparina y corregir los trastornos de la coagulación. Los antibióticos están indicados dado que el riesgo de necrosis es extremadamente alto. La cirugía se reserva para pacientes con mala evolución o que tengan necrosis infectada.
CP-085. QUISTE LINFOEPITELIAL PANCREÁTICO COMO HALLAZGO INFRECUENTE
Romero Moreno S, de Vicente Ortega A, Arrollo Arguelles JM, Ayuso Carrasco CAB, Ojeda Hinojosa M
Servicio Aparato Digestivo. Complejo Hospitalario de Jaén, Jaén.
Palabras clave: quiste linfoepitelial pancreatico, quiste pancreático, lesión pancreática.
Introducción
El quiste linfoepitelial (LEC) pancreático es una lesión quística benigna sin potencial de malignización, localizada en el páncreas y representa un hallazgo infrecuente, suponiendo además un reto en el diagnóstico diferencial de otras lesiones quísticas pancreáticas. Casi el 90% de las lesiones quísticas pancreáticas corresponden a pseudoquistes tras una pancreatitis aguda, el resto de lesiones corresponden a verdaderos quistes o neoplasias quísticas. A continuación, presentamos un caso de LEC de páncreas.
Caso Clínico
Un varón de 44 años con presencia de dolor abdominal y saciedad precoz. Sin antecedentes personales de interés, hábitos tóxicos ni toma de medicación habitual. Se realiza ecografía abdominal que evidencia la presencia de lesión a nivel de epigastrio, sin poder asegurar la dependencia con el parénquima hepático de 12x12cm con cicatriz central. Analíticamente sin alteraciones significativas, salvo un CA 19.9 en 57.
Como parte de su estudio, se sometió a una endoscopia gastrointestinal superior, que confirmó una compresión extrínseca a nivel de la cara posterior antral.
Se completa estudio con una una resonancia magnética (RM) que informa de una Figura redondeada de 12,6 x 11.3 cm con realce de su interior y pequeñas calcificaciones a nivel de cabeza-cuerpo pancreática provocando desplazamiento de estructura vecinas (vesicular biliar, marco duodenal y curvatura menor gástrica) con dilatación leve de conducto de wirsung e importante circulación colateral venosa en hilio hepático y perigástrica (Figura 1). No había antecedentes de pancreatitis, insuficiencia pancreática o trauma.
Tras una pancreaticoduodenectomía se confirma el estudio histológico de LEC.
Discusión
Los LEC son extremadamente poco comunes, de tamaño variable distribuidas y que acontecen con mayor frecuencia al sexo masculino. Debido a su rareza, es una lesión mal caracterizada y su patogenia no se conoce completamente.
En la mayoría se presenta como un hallazgo incidental, y el resto de los pacientes se asocia con síntomas inespecíficos como náuseas, vómitos, diarrea, dolor abdominal, pérdida de peso y astenia.
Los LEC son lesiones benignas y no poseen potencial maligno, por lo que una identificación precisa de estas lesiones es importante para evitar intervenciones innecesarias. Actualmente, no existe un método de diagnóstico preoperatorio fiable, pudiéndose optar por la TC, RM o ecoendoscopia, con la ventaja de esta última técnica de la toma de biopsias.
La enucleación del quiste se puede considerar para lesiones no complicadas con un diagnóstico confirmado, pero la resección mediante pancreaticoduodenectomía o pancreatectomía distal, sigue siendo el tratamiento definitivo cuando no se puede descartar una malignidad.
CP-086. SÍNDROME DE LEMMEL: CAUSA INFRECUENTE DE PATOLOGÍA BILIOPANCREÁTICA
Díaz Alcázar MM, Ruiz Escolano E, García Robles A
UGC Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: síndrome de lemmel, divertículo duodenal periampular, ictericia obstructiva.
Introducción
El síndrome de Lemmel consiste en ictericia obstructiva por compresión mecánica por un divertículo duodenal periampular, en ausencia de coledocolitiasis o tumor. Los divertículos periampulares son pseudodivertículos de mucosa duodenal sin capa muscular formados en un radio de 2-3 centímetros desde la ampolla de Vater. Es raro que causen ictericia obstructiva, aunque la prevalencia de divertículos periampulares se estima en hasta el 22% según la sensibilidad del método diagnóstico.
Caso Clínico
Caso 1. Mujer de 79 años con hipertensión arterial y enfermedad renal crónica en hemodiálisis que consulta por epigastralgia. Analíticamente destaca elevación de bilirrubina y enzimas de colestasis y elevación moderada de enzimas pancreáticas (amilasa 606 U/L y lipasa 455 U/L). Ecografía abdominal objetiva dilatación de vía biliar intra y extrahepática por posible neoformación de papila o páncreas. Se completa estudio con tomografía computarizada abdominal con contraste confirmando la dilatación de vía biliar, divertículo duodenal parapapilar de 38x36 mm y pancreatitis aguda (Figura 1). Dada la mejoría clínica y analítica, y la situación basal de la paciente, se decide seguimiento.
Caso 2. Hombre de 80 años sin antecedes que consulta por dolor abdominal, fiebre e ictericia. Ecografía abdominal sin hallazgos. Se realiza colangiorresonancia magnética con diagnóstico de divertículo duodenal de 4 cm que desplaza colédoco y conducto pancreático (Figura 2). Buena respuesta clínica a antibioterapia. Se realiza CPRE con colocación de prótesis biliar plástica.
Discusión
Los divertículos duodenales periampulares habitualmente son asintomáticos y se diagnostican incidentalmente, pero en raras circunstancias pueden inflamarse y complicarse en hasta un 1-5% con diverticulitis, hemorragia, perforación, fistulización, ictericia obstructiva (síndrome de Lemmel), coledocolitiasis, pancreatitis aguda o crónica o colangitis.
Una de las teorías etiopatogénicas del síndrome de Lemmel es que la diverticulitis puede originar inflamación crónica de la ampolla y fibrosis de la papila. Otra teoría es que el divertículo causa disfunción del esfínter de Oddi. La tercera consiste en que puede haber compresión directa por contenido diverticular.
El diagnóstico del síndrome de Lemmel es un reto. Se debe tener en cuenta en individuos con un divertículo periampular. Los divertículos se pueden observar con pruebas de Figura, aunque el gold standard es la CPRE. El divertículo puede llenarse de contenido sólido o líquido, y confundirse en pruebas de Figura con lesiones en la zona de la cabeza pancreática como pseudoquistes, abscesos pancreáticos, neoplasias quísticas de páncreas o adenopatías. La CPRE con esfinterotomía y colocación de stent biliar es el tratamiento de elección en pacientes muy sintomáticos, habiendo demostrado disminución de la morbimortalidad. La alternativa es diverticulotomía quirúrgica.
CP-087. TROMBOSIS DEL LIGAMENTO FALCIFORME COMO COMPLICACIÓN DE UNA PANCREATITIS AGUDA
Torres Domínguez A1, Méndez Sánchez IM1, Lozano Calero CM2, Bisso Zein JK1, Jofré Peralta S1, Rivera Irigoin R1, García Gavilán MC1, Rosales Zábal JM1, Valdés Solís P2, Sánchez Cantos AM2
1Servicio Aparato Digestivo. Complejo Hospital Costa del Sol, Marbella. 2Servicio Radiodiagnóstico. Complejo Hospital Costa del Sol, Marbella.
Palabras clave: ligamento falciforme, pancreatitis aguda, trombosis.
Introducción
El ligamento falciforme es un vestigio de la vena umbilical fetal que se oblitera en los primeros meses de vida extrauterina. Su trombosis es un hallazgo muy infrecuente que se ha descrito principalmente como complicación secundaria a su canalización en cuidados intensivos neonatales, siendo rara en el contexto de una pancreatitis aguda.
Caso Clínico
Mujer de 89 años, hipertensa y asmática, con pancreatitis aguda de repetición sugestivos de origen biliar que ingresa en nuestro hospital por cuadro de epigastrialgia irradiada a ambos hipocondrios y náuseas. En analíticas se observa una hiperamilasemia (766 U/L) y elevación de la alanina aminotransferasa (422 U/L) y aspartato aminotransferasa (914 U/L), con bilirrubina normal. Esta vez el dolor es más intenso que en episodios previos y en epigastrio se palpa una zona nodular lisa dolorosa.
En la colangiopancreatografía y resonancia magnética abdominal, se observa una lesión inflamatoria entre la pared abdominal y el lóbulo hepático izquierdo que impresiona de necrosis grasa (Figura 1), identificándose en su espesor el ligamento falciforme engrosado y cambios inflamatorios compatibles con trombosis del mismo (Figura 2). También existe un aumento de señal de la rama portal izquierda sospechosa de trombosis que se descarta más tarde con ecografía-doppler. No se apreciaron colelitiasis ni coledocolitiasis. Estos hallazgos no estaban presentes en una resonancia magnética realizada hace un año durante el primer episodio de pancreatitis aguda.
La paciente evolucionó favorablemente con resolución del dolor y mejoría de los parámetros analíticos, no iniciándose anticoagulación por su situación basal.
FIGURA 1
Lesión de aspecto inflamatorio que se extiende desde el lóbulo hepático izquierdo y que ocupa la grasa properitoneal entre la pared abdominal y cara anterior gástrica compatible con necrosis grasa.
Discusión
La pancreatitis aguda asocia muchas complicaciones diversas, entre ellas las vasculares. El gran proceso inflamatorio puede irritar o comprimir los vasos del eje esplenoportal, aumentando el riesgo de trombosis(1,2). La necrosis grasa del tejido subcutáneo localizada en articulaciones también se ha descrito como complicación(1).
El ligamento falciforme une la pared abdominal con la cara anterior de hígado, dividiéndolo en ambos lóbulos hepáticos. Es un remanente de la vena umbilical fetal y se recanaliza en pacientes con hipertensión portal(3).
Son dos los casos publicados similares. Su hipótesis es que se genera una tromboflebitis del sistema venoso portal que se extiende al ligamento falciforme, provocando su recanalización espontánea y finalmente su trombosis. En estos casos existía trombosis de ramas portales(4, 5).
Respecto tratamiento anticoagulante no existe evidencia. En uno de los casos se inició heparina de bajo peso molecular y más tarde warfarina durante seis meses con resolución de la trombosis(4).
La trombosis del ligamento falciforme es una complicación infrecuente a tener en cuenta en pancreatitis aguda.
CP-088. TUMOR PANCREÁTICO: UN DIAGNÓSTICO POCO FRECUENTE
Palomino Luque P1, Berlanga Cañete S2, Pinto García I3
1Servicio Aparato Digestivo. Hospital Comarcal de la Axarquía, Vélez-Málaga. 2Servicio Aparato Digestivo. Hospital Comarcal de la Serranía, Ronda. 3UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: páncreas, ecoendoscopia, fnb.
Introducción
El adenocarcinoma ductal es la neoplasia pancreática más frecuente, representando el 85% de los tumores. Dentro de los menos frecuentes, las metástasis pancreáticas presentan una incidencia baja, en torno al 2-5%. Los tumores primarios que con mayor frecuencia metastatizan en páncreas son el carcinoma de riñón, pulmón y mama, y el melanoma.
Se describen tres casos de metástasis pancreáticas diagnosticadas mediante ecoendoscopia (EUS).
Caso Clínico
Caso 1: Mujer de 75 años con ictericia indolora y síndrome constitucional; presenta analítica con colestasis y Ca 19.9 normal, y TC con lesión quística en cabeza de páncreas sin atrofia del cuerpo, sugestivo de cistoadenoma seroso y carcinomatosis peritoneal (figura 1). Se realiza EUS con hallazgo de LOE hipoecogénica en cabeza pancreática con estudio citológico obtenido mediante aspiración con aguja fina (FNA) compatible con adenocarcinoma. Se decidió realizar biopsia percutánea de implante peritoneal siendo diagnóstica de carcinoma seroso. La biopsia con aguja fina (FNB) de una nueva EUS para estudio histológico se informó como tejido fibroadiposo con infiltración por carcinoma, compatible con metástasis de carcinoma seroso primario peritoneal.
Caso 2: Mujer de 61 años con antecedentes de leiomiosarcoma pleomórfico supracapsular intervenido en el año 2013, que presentó recaída local que requirió reintervención en 2017, con márgenes libres de enfermedad, y RT-adyuvante. En TC de control de 2018 se observó LOE en proceso uncinado con estenosis del conducto dorsal (figura 2). Se llevó a cabo FNA-EUS con resultado de células mesenquimales atípicas compatibles con sarcoma, decidiéndose finalmente realización de duodenopancreatectomía cefálica.
Caso 3: Mujer de 77 años con antecedentes de tabaquismo y de nefrectomía parcial izquierda en 2012 por carcinoma renal de células claras pT1a-NxMx. En TC de control de 2018 se apreciaron dos LOEs pancreáticas, planteándose el diagnóstico diferencial entre lesiones benignas y tumor neuroendocrino (TNE) por ausencia de captación en PET-TC. Se realizó FNA-EUS, que evidenció dos lesiones hipoecogénicas de márgenes bien definidos en cabeza de páncreas sugestivas de TNE con citología informada como grupo celular atípico sospechoso de neoplasia. En SPECT-TC posterior se halló depósito del trazador compatible con TNE. Se realizó FNB-EUS llegando al diagnóstico de metástasis de carcinoma renal de células claras.

 Descargar número completo
Descargar número completo Download full issue
Download full issue