CP-089. ADENOCARCINOMA GÁSTRICO QUE DEBUTA CON PERFORACIÓN EN PACIENTE CON SÍNDROME DE MUIR-TORRE
Arroyo Argüelles JM, de Vicente Ortega A, Romero Moreno S, Padilla Ávila F, Castillo Molina L
Servicio Aparato Digestivo. Complejo Hospitalario de Jaén, Jaén.
Palabras clave: síndrome de muir torre, perforación.
Introducción
El síndrome de Muir-Torre es una variante fenotípica del síndrome de Lynch, de herencia genética autosómica dominante.
Cursa con una predisposición al desarrollo de tumores de glándulas sebáceas y queratoacantomas, además del desarrollo de cáncer colorrectal y neoplasias extracolónicas (endometrio, intestino delgado, ovario, etc.), los cuales son propios del síndrome de Lynch.
En el 90% de los casos se producen mutaciones en los genes MLH1 y MSH2, dando lugar a una inestabilidad de microsatélites.
Caso Clínico
Se presenta el caso de un hombre de 61 años con antecedentes personales de Diabetes Mellitus tipo 2, hipertensión arterial y síndrome de Muir-Torre.
El paciente acude por dolor abdominal intenso en epigastrio de instauración súbita tras llevar tres días presentando vómitos de contenido alimenticio e intolerancia oral.
A la exploración física se encuentra con abdomen distendido y muy doloroso a la palpación. En la analítica presenta una leucocitosis con desviación izquierda y elevación de reactantes de fase aguda.
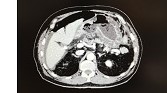
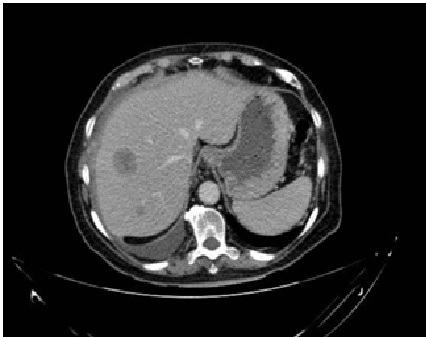
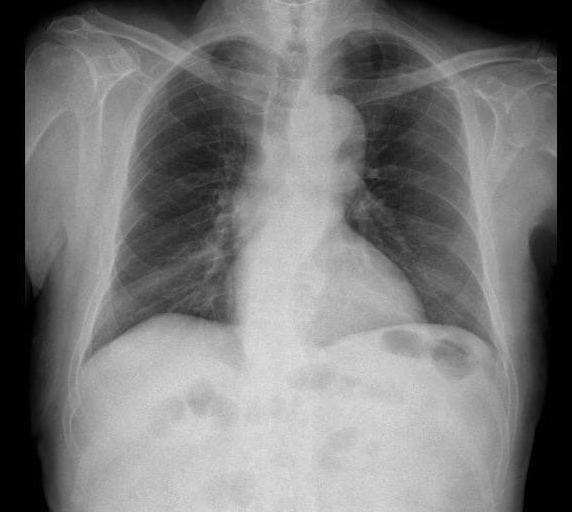
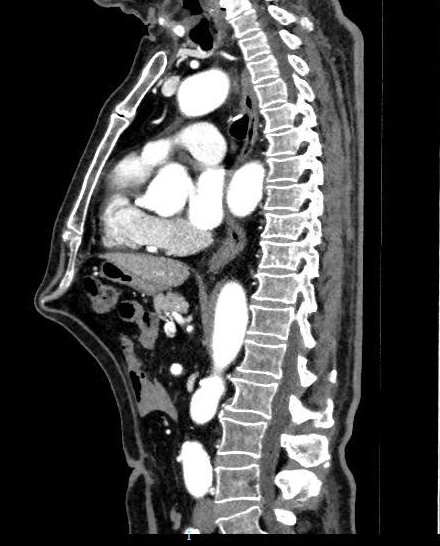
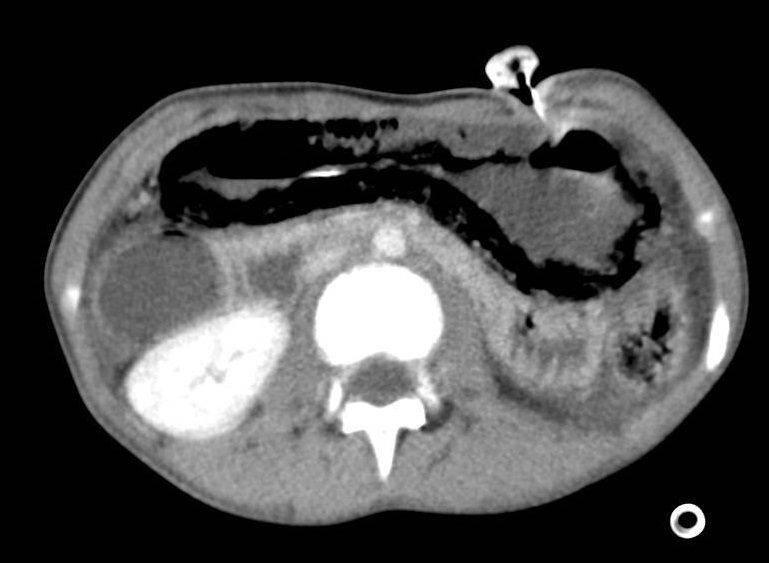
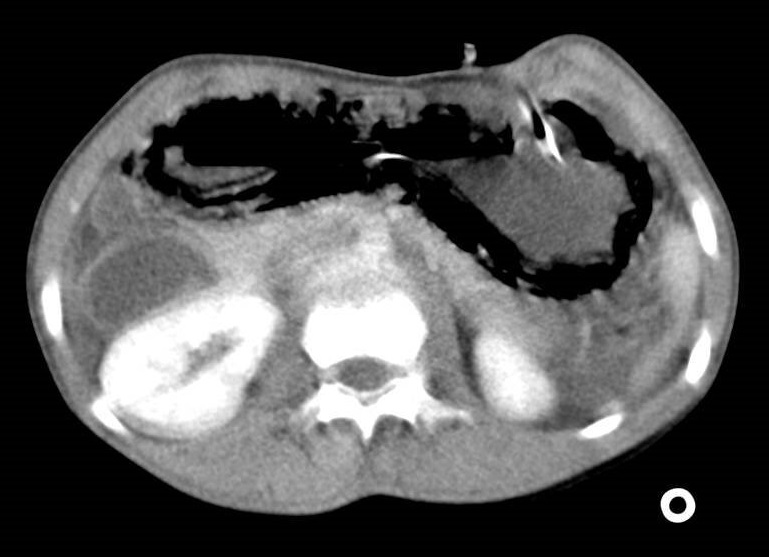
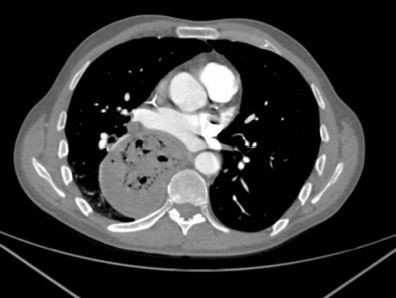
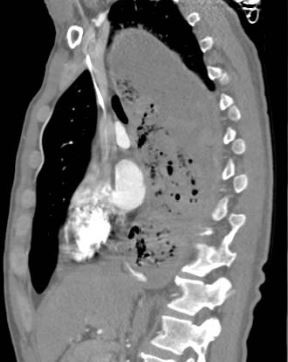
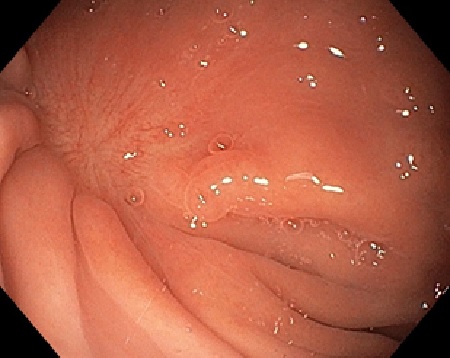
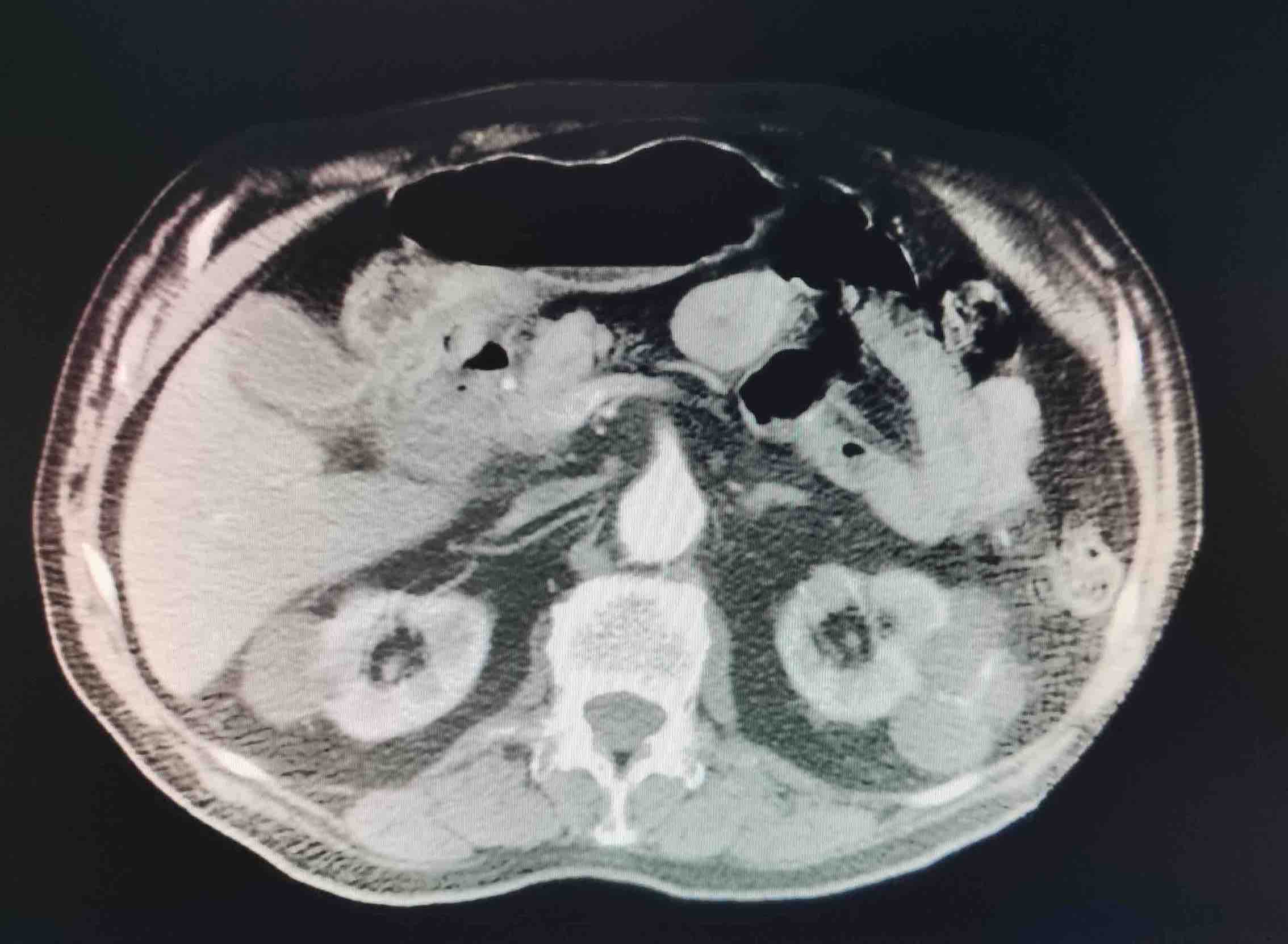
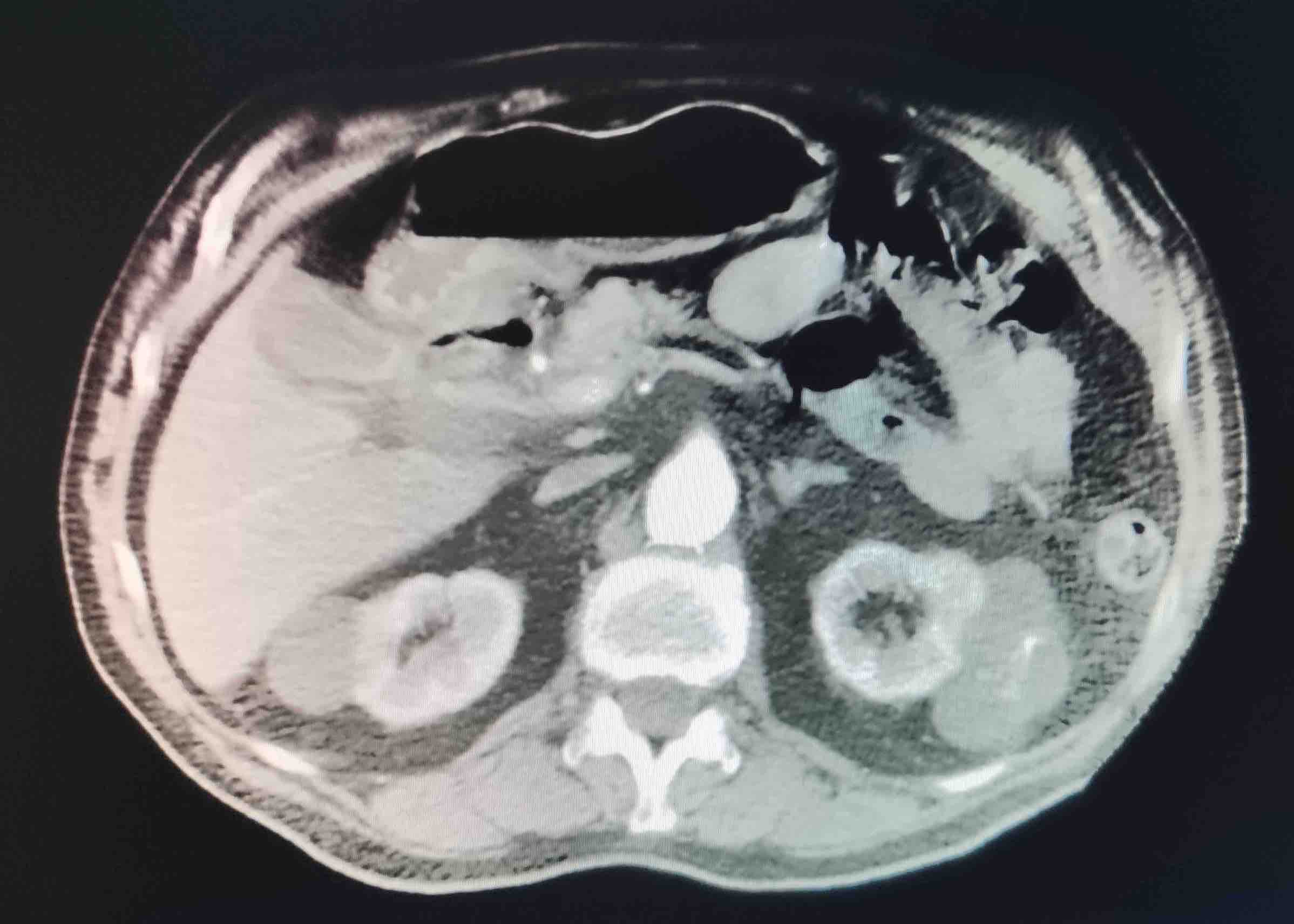
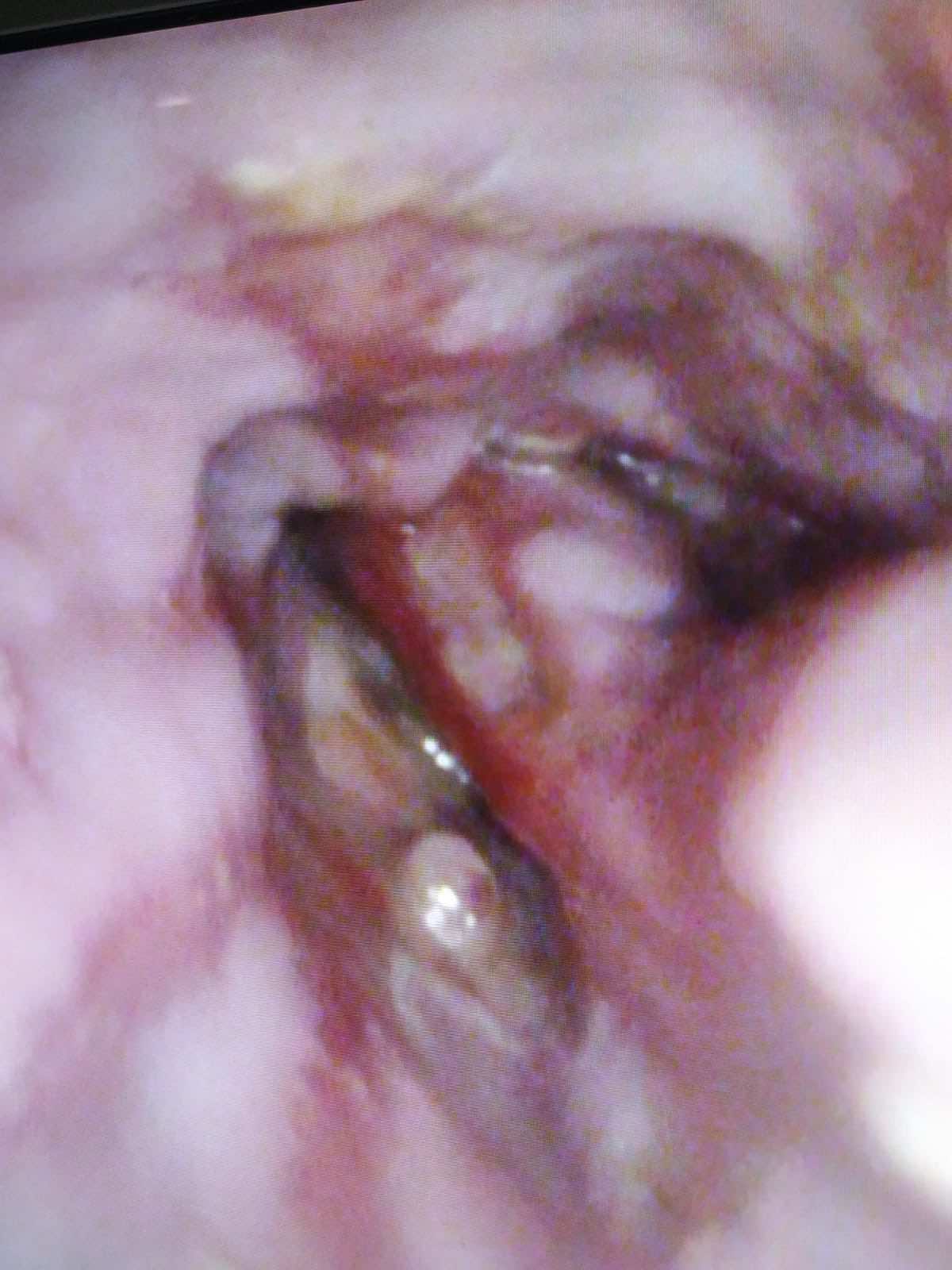
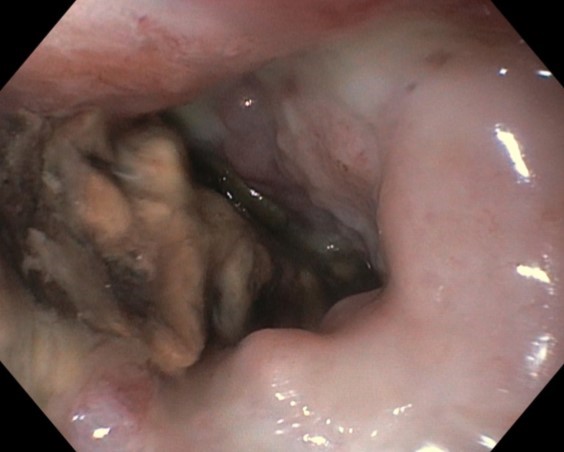
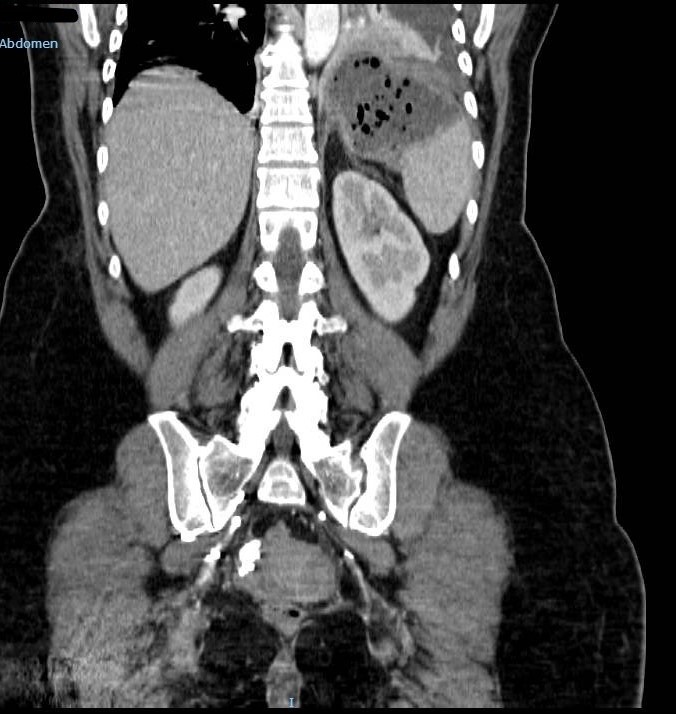
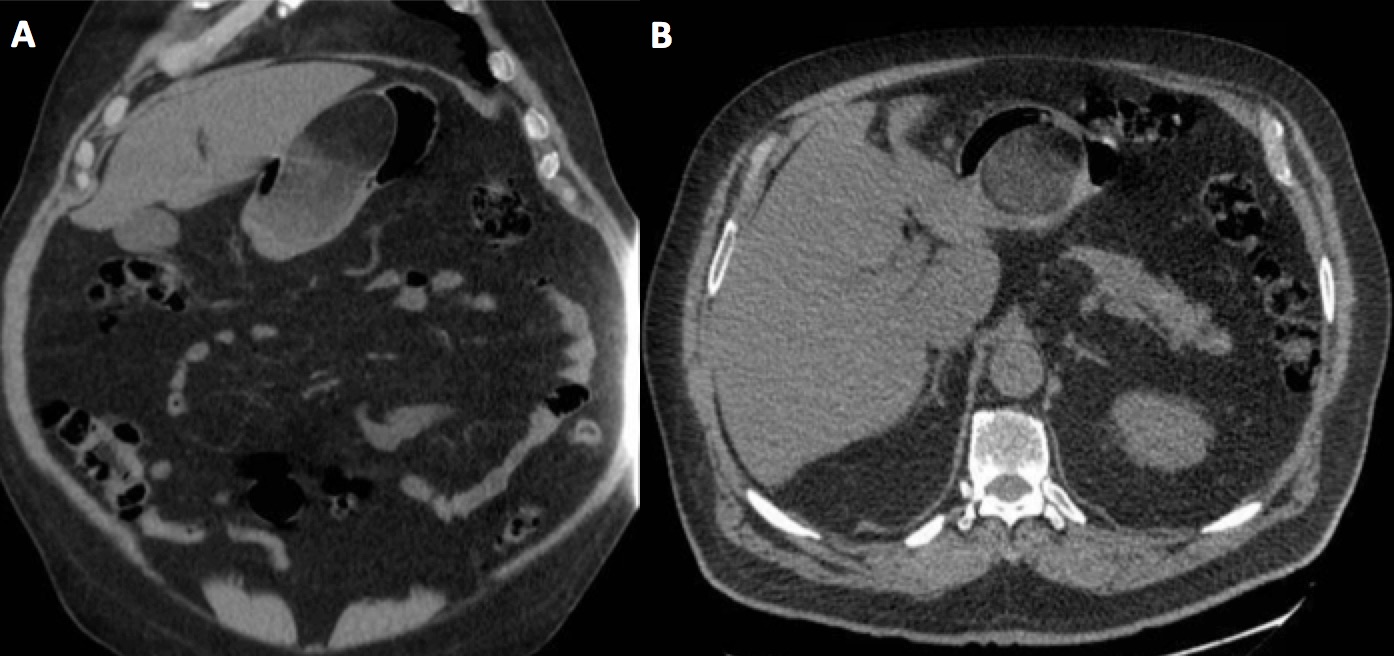
En el TC abdominal se observan hallazgos sugestivos de neoplasia gástrica difusa localmente avanzada con infiltración de la grasa en curvatura menor y diseminación ganglionar extensa, presentando perforación a nivel del antro gástrico (Figura 1) que condiciona un neumoperitoneo.
Ante el cuadro de perforación gástrica, se decide intervención quirúrgica urgente, realizándose una gastrectomía subtotal con anastomosis gastroyeyunal tipo Billroth II.
El resultado de Anatomía Patológica de la pieza quirúrgica informó de adenocarcinoma gástrico con invasión linfovascular perineural pT4N3b.
Discusión
El síndrome de Muir-Torre se caracteriza por la existencia de tumoraciones de la piel (adenomas sebáceos y queratoacantomas) y se debe sospechar ante un paciente con síndrome de Lynch que presenta este tipo de lesiones.
El adenoma sebáceo es el tumor más frecuente en este síndrome y habitualmente se localiza en la región facial del paciente, siendo de comportamiento benigno en la mayor parte de las ocasiones.
Hay que tener en cuenta que estos pacientes tienen una alta predisposición para el desarrollo de procesos neoplásicos por lo que ante un paciente ya diagnosticado de este síndrome que presente un cuadro abdominal hay que tener siempre en mente que puede tratarse de un proceso neoproliferativo en el tubo digestivo.
Al tratarse de una enfermedad con base genética, debe hacerse un rastreo de casos en los familiares del paciente afecto, ya que tienen más predisposición que la población general a padecer neoplasias de todo tipo.
CP-090. CARCINOMATOSIS MENÍNGEA DE ADENOCARCINOMA GÁSTRICO
Requena de Torre J, Ariza Fernández JL, Gómez Torres KM, Vázquez Rodríguez JA
UGC Aparato Digestivo. Complejo Hospitalario de Poniente, Ejido, El.
Palabras clave: carcinomatosis meníngea, adenocarcinoma gástrico, metástasis.
Introducción
En el momento del diagnóstico de cáncer gástrico, el 50 % de los casos se presenta con diseminación metastásica a distancia. La afectación meníngea es excepcional, con una confirmación diagnóstica difícil y un pobre pronóstico.
Caso Clínico
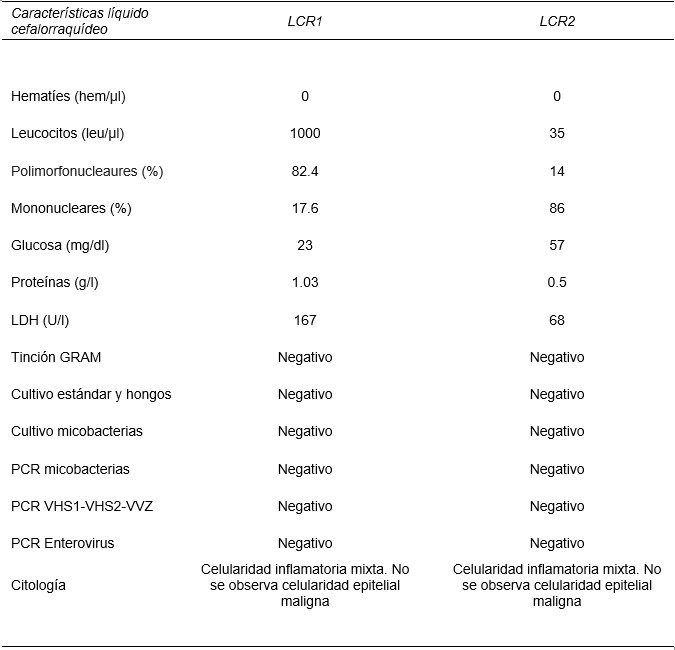
Mujer de 56 años que tras cuadro de cefalea de 2 meses de evolución sin otros síntomas neurológicos acompañantes y sin mejoría con analgésicos habituales y antiinflamatorios, acude a servicio de urgencias por hemorragia digestiva alta en forma de hematemesis y melenas con inestabilidad hemodinámica. En la gastroscopia urgente se evidencia úlcera gástrica Forrest IIb de aspecto maligno en incisura angular con histología compatible con adenocarcinoma pobremente diferenciado infiltrante. En el estudio de extensión con Tomografía toracoabdominopélvico se evidencia gran afectación metastásica adenopática de predominio mediastínico y abdominal. Una vez dada de alta de planta y antes de iniciar tratamiento quimioterápico vuelve a ingresar por cefalea intensa, vómitos, rigidez de nuca y signo de Regnik positivo. Un primer análisis del líquido cefalorraquídeo descarta la presencia microbiana aunque se pauta tratamiento antibiótico empírico al inicio del cuadro, sin mejoría. Desarrolla varias crisis convulsivas. En TC craneal y RM cerebral no se evidencian hallazgos patológicos y se decide un 2º análisis del LCR donde los hallazgos son compatibles con una carcinomatosis meníngea (Tabla 1) aunque no se evidencian células neoplásicas malignas en la muestra. La paciente empeora progresivamente falleciendo pocas semanas después del inicio del cuadro.
Discusión
La diseminación metastásica meníngea en el cáncer gástrico tiene una prevalencia menor del 1% con un pronóstico infausto que puede mejorar discretamente mediante la administración de quimioterapia sistémica e intratecal. Su diagnóstico en muchas ocasiones es dificultoso.
- Clínicamente puede manifestarse con diferentes síntomas neurológicos como cefalea, nauseas, vómitos, rigidez de nuca, convulsiones, afectación de pares craneales o nervios radiculares.
- En pruebas de Figura se puede demostrar una hipercaptación meníngea del contraste aunque puede resultar falsamente negativa hasta en el 30 % de las RM y el 50% en TC.
- El análisis del LCR se caracteriza por hiperproteinorraquia, hipoglucorraquia, ausencia de microorganismos y presencia de células malignas, aunque ésta última puede resultar negativa hasta el 50% de los casos. Nuevas técnicas inmunodiagnósticas y de biología molecular no han demostrado superioridad.
En el caso que nos ocupa el diagnóstico es altísimamente sugerente de carcinomatosis meníngea debido a la clínica y a los parámetros del LCR pero su evolución tan tórpida no permitió medidas terapéuticas específicas.
CP-091. CAUSA INESPERADA DE DISNEA EN PACIENTE LONGEVA
Requena de Torre J, Viñolo Ubiña C, Gómez Torres KM, Vázquez Rodríguez JA
UGC Aparato Digestivo. Complejo Hospitalario de Poniente, Ejido, El.
Palabras clave: hernia diafragmática, bochdalek.
Introducción
La hernia diafragmática congénita es un defecto de la formación y/o cierre del diafragma que permite el paso de parte o de la totalidad de las vísceras abdominales a la cavidad torácica, lo que produce dos consecuencias que van a marcar la evolución del recién nacido: hipoplasia pulmonar ipsilateral e hipertensión pulmonar. Presentamos el caso de paciente con diagnóstico inesperado al final de sus días.
Caso Clínico
Mujer de 83 años con antecedentes de cardiopatía isquémica, dislipemia, y obesidad. Acude a urgencias por cuadro de astenia, dolor en hemiabdomen izquierdo, pérdida de 10 Kg peso, disnea de pequeños a medianos esfuerzos y episodios paroxísticos de tos, sin cianosis, que refería como habitual y por los que nunca habia consultado.
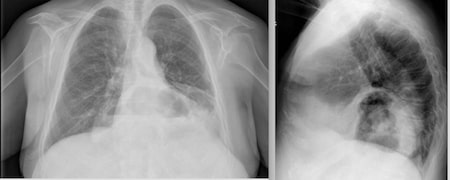
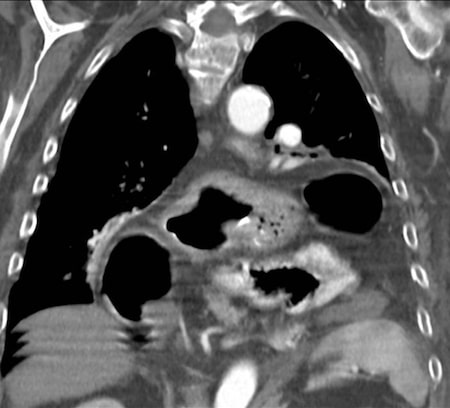
Analíticamente destaca hemoglobina 9,2 mg/dl y PCR 8,7 mg/dl. La radiografía de tórax ( Figura-1) sugiere Figura de hernia de hiato y la ecografía informa de engrosamiento a nivel de colon sigmoide. Se completa con colonoscopia que visualiza divertículos en sigma no complicados y estenosis en ángulo esplénico de origen compresivo de dificil maniobra e histología inespecifica. Se realiza body-TAC donde se objetiva (Figura-2) una voluminosa hernia de hiato diafragmático con presencia de estómago, asas de intestino delgado, cola de páncreas y ángulo esplénico de colon a nivel torácico.
Nuestra paciente mantenía molestias abdominales, lo que nos llevó al diagnóstico de sindrome diverticular; y la dificil maniobra endoscópica en ángulo esplénico,(que sugería estenosis) no nos orientó (hasta que realizamos el TAC) de que, en realidad, se trataba de la porción de colon intratorácico. Dadas las comorbilidades de la paciente no se planteó tratamiento quirúrgico. La paciente falleció por insuficiencia cardiaca congestiva.
Discusión
La hernia diafragmática de Bochdalek es un defecto congénito del cierre del trígono lumbocostal (forma pediátrica, generalmente más severa) o adquirido (forma del adulto, menos frecuente y menos severa). Su prevalencia es baja (en el adulto 0,17%) predominando en el sexo femenino (3:1). Se manifiesta frecuentemente como un distrés respiratorio grave del recién nacido y constituye una urgencia neonatal. Su diagnóstico en el adulto es excepcional y se han descrito pocos casos en la bibliografía. Estas hernias, localizadas entre las inserciones lumbocostales del diafragma, se descubren generalmente en la edad adulta de forma incidental o tras volverse sintomáticas, por compromiso intestinal o respiratorio.
El tratamiento definitivo es quirúrgico, pero debe individualizarse la indicación en función de la situación del paciente.
CP-092. CORIOCARCINOMA PRIMARIO GÁSTRICO: UN CASO INUSUAL
Calvo Bernal MM1, Hallouch Tatouh S1, Cuello Entrena E2
1UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería. 2UGC Anatomía Patológica. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: coriocarcinoma gástrico, neoplasia gástrica.
Introducción
El coriocarcinoma gástrico primario (CGP) es un tumor extremadamente raro, altamente invasivo y de rápida diseminación hematógena.
Presentamos el caso de una paciente de 69 años que presenta dolor abdominal, anemia y síndrome constitucional y es diagnosticada de coriocarcinoma gástrico primario.
Caso Clínico
Mujer de 69 años con antecedentes de hipertensión arterial y diabetes mellitus que acude a urgencias por presentar dolor abdominal epigástrico de 2 meses de evolución. Asocia síndrome constitucional con pérdida de 7 kg en último mes e hiporexia. En analítica destaca anemia normocítica (Hemoglobina 10 g/dl, Volumen corpuscular medio 83 fl), discreta elevación de reactantes de fase aguda (PCR 7) y CA 19.9 elevado.
Se realiza TAC toracoabdominal que objetiva engrosamiento de pared de antro gástrico, derrame pleural bilateral de origen metastásico, metástasis hepáticas y carcinomatosis peritoneal. No se objetivan lesiones en útero o anejos (Figura 1).
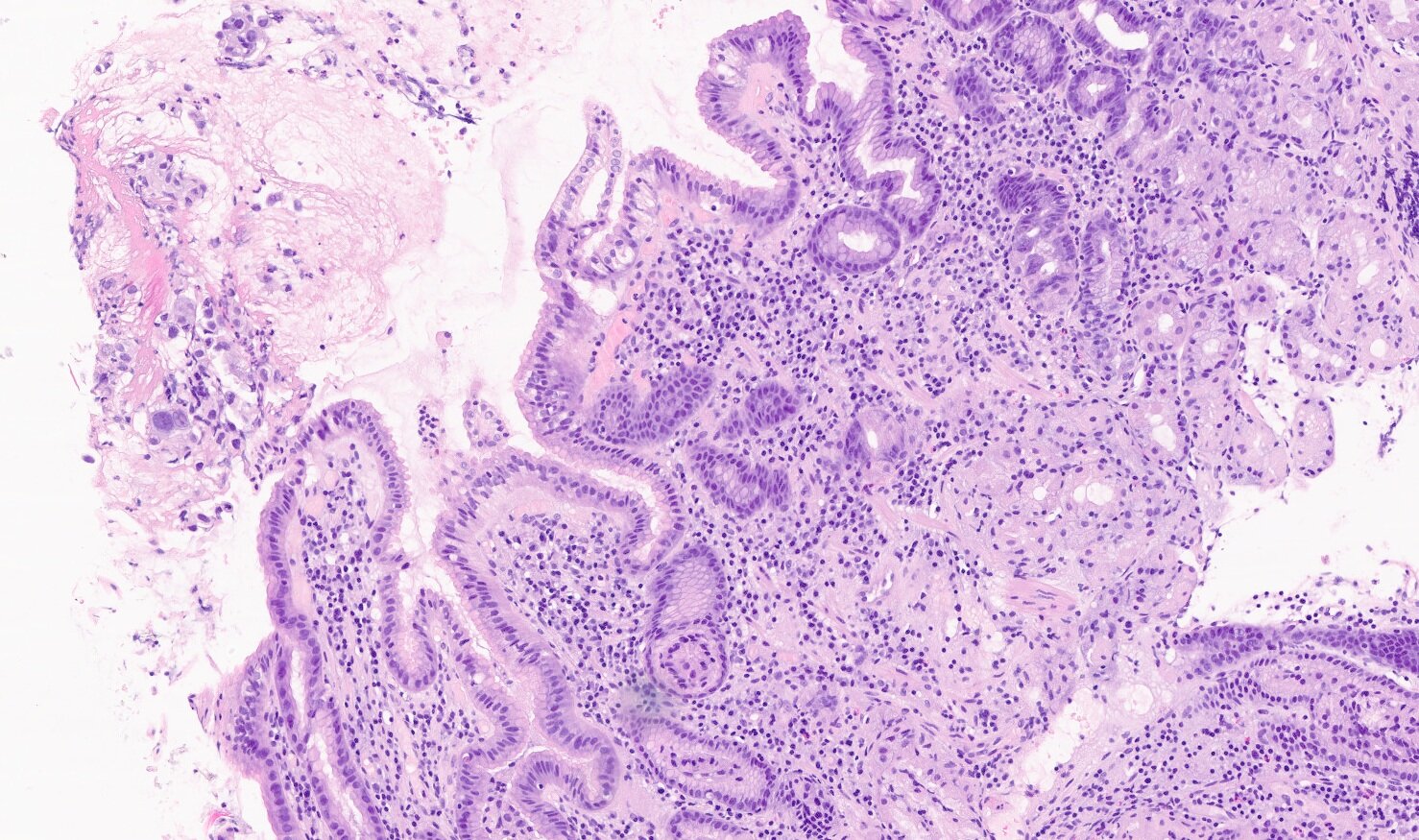
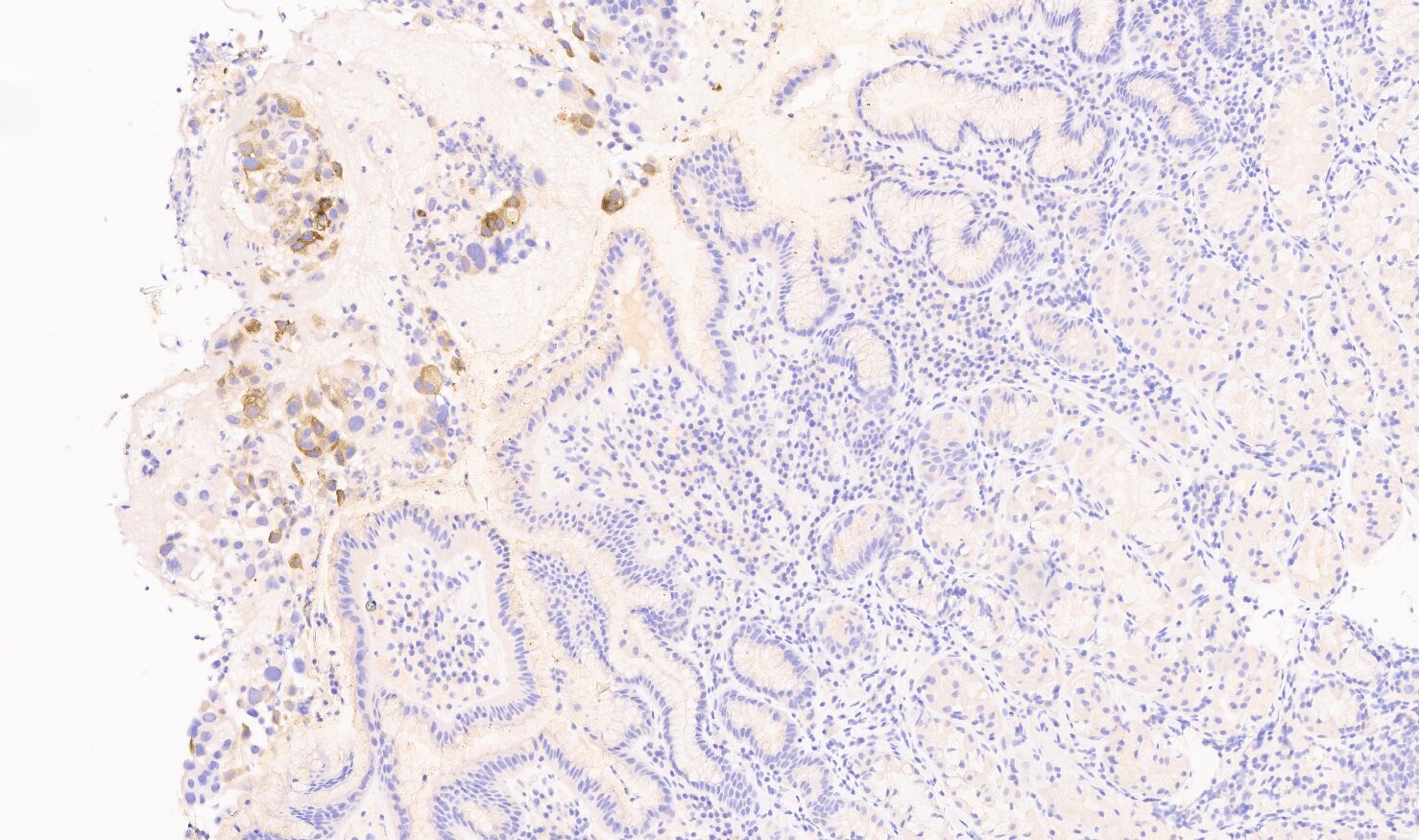
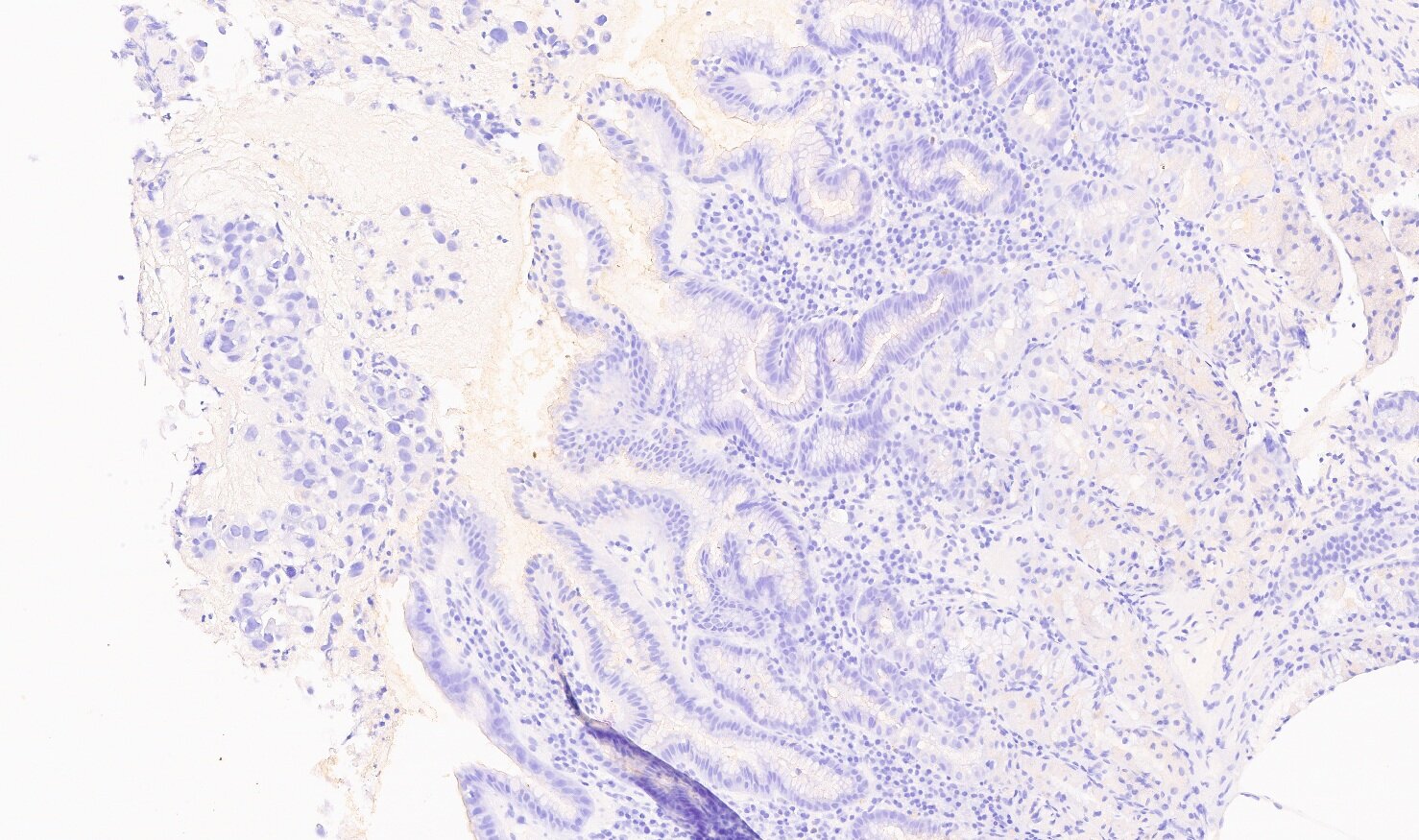
En la endoscopia digestiva alta se observa una lesión mamelonada de 3 cm en antro, ulcerada en su superficie . Se toman biopsias que son compatibles con adenocarcinoma invasivo y ulcerado pobremente diferenciado, objetivándose pleomorfismo celular con diferenciación citotrofoblástica y sincitiotrofoblástica. Se realiza estudio inmunohistoquímico positivo para β-HGC y CK7 y negativo para α-fetoproteína, lo que es altamente sugestivo coriocarcinoma gástrico(Figuras 2, 3 y 4). El nivel de β-HGC en suero estaba ligeramente elevado (65 mUI/ml, valor normal <5 mUI/ml).
FIGURA 1.
TAC abdominal: se aprecia engrosamiento de pared de antro gástrico, con retención de líquido en cámara gástrica. Podemos apreciar varias lesiones hepáticas sugerentes de metástasis.
FIGURA 2.
Anatomía patológica. Tinción con hematoxilina-eosina(x10): se aprecian cambios morfológicos focales con notable pleomorfismo y hábito seudosincitial de la celularidad neoplásica.
Discusión
El coriocarcinoma gástrico primario (CGP) es un tumor extremadamente raro. Habitualmente debutan en las gónadas aunque también puede afectar a órganos extragonadales. Dentro de estos, el coriocarcinoma gástrico primario alcanza una incidencia del 0,08%.
La mayor parte de los coriocarcinomas gástricos coexisten con adenocarcinomas. Es más frecuente en mujeres, con una edad media de presentación de 60 años. La localización más frecuente es el antro gástrico.
Las manifestaciones clínicas del PGC son dolor abdominal, y síndrome constitucional aunque también como puede debutar como hemorragia digestiva.
Histológicamente, existe una combinación de citotrofoblastos y sincitiotrofoblastos malignos. La inmunohistoquímica es positiva para β-HCG y la mayoría de los casos se acompañan de β-HCG sérica elevada.
El diagnóstico diferencial principal del PGC es un tumor trofoblástico metastásico con origen a nivel gonadal.
Esta neoplasia tiene un mal pronóstico por su alta capacidad para invadir y lograr una rápida diseminación metastásica. Las metástasis más frecuentes son linfáticas y hematógenas. Respecto al tratamiento, no está del todo establecido aunque la cirugía curativa con quimioterapia asociada es considerada de elección.
CP-093. DISFAGIA AORTICA POR ELONGACION DE LA AORTA TORÁCICA
García Gavilán MC, Torres Domínguez A, Rosales Zabal JM, Méndez Sánchez IM
Servicio Aparato Digestivo. Complejo Hospital Costa del Sol, Marbella.
Palabras clave: disfagia, disfagia aortica, elongación aortica.
Introducción
La disfagia es un síntoma frecuente en la vejez. Se ha descrito que el 7-10% de pacientes mayores de 50 años presenta disfagia. Su causa suele ser alguna alteración estructural o de la motilidad esofágica. La compresión extrínseca por estructuras vasculares es una causa menos frecuente de disfagia que se clasifica en disfagia lusoria y disfagia aortica (DA). Ésta última normalmente se produce por una dilatación aneurismática de la aorta ascendente, cambios ateroescleróticos o tortuosidad del trayecto de la aorta.
Caso Clínico
Varón de 78 años con antecedente de hipertensión arterial y diabetes tipo II, que durante el estudio de una lesión sólida renal por urología, comentó llevar meses con una disfagia progresiva a sólidos, junto con dificultad para la expulsión de gases y pérdida de peso de >10kg. Se le realizó una radiografía de tórax donde únicamente llamaba la atención una rectificación con desplazamiento central del cayado de la aorta (Figura 1) y una gastroscopia, donde se objetivó a nivel del tercio medio esofágico, una estenosis de la luz por compresión extrínseca, que no permitía la insuflación completa del esófago, aunque no impedía el paso del endoscopio a tramo distal, observándose una mucosa de aspecto normal. Se realizó una TC toraco abdominal con contraste, donde se observó una elongación marcada de la aorta, que era de calibre normal y que a nivel del tercio medio del esófago provocaba una compresión del mismo con una leve dilatación proximal, que era más evidente en los cortes sagitales (Figura 2). Presentaba múltiples calcificaciones en las arterias coronarias, aunque no a este nivel de la aorta. Por la edad y comorbilidad del paciente se consensuó con él seguir una actitud conservadora con dieta triturada y Levosulpirida 25mg con las comidas. Con estas medidas la clínica se controló y el paciente fue ganando peso de forma progresiva.
Discusión
La DA es más frecuentes en pacientes de edad avanzada, hipertensos, con miocardiopatía y osteopatía degenerativa. El esófago comienza en el lado derecho de la aorta torácica, va descendiendo y en su tercio medio-inferior cruza la aorta anteriormente, por lo que cualquier alteración del tamaño o trayecto de la aorta en este recorrido puede provocar la DA. En pacientes muy sintomáticos el tratamiento es una reconstrucción quirúrgica, aunque habitualmente los síntomas suelen ser leves-moderados y los pacientes de edad avanzada, con lo que se suelen tratar de forma conservadora con dieta triturada o líquida y procinéticos.
CP-094. GASTRITIS ENFISEMATOSA: ¿UNA COMPLICACIÓN DE LA GASTROSTOMÍA ENDOSCÓPICA?
Moreno Moraleda I, Hallouch Toutouh S, Calvo Bernal MM
Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: gastritis enfisematosa, gastrostomía endoscópica, enfisema gástrico.
Introducción
La presencia de aire en la pared gástrica es un hallazgo infrecuente que se presenta en situaciones con un pronóstico muy variable: enfisema gástrico, neumatosis gástrica y gastritis enfisematosa. Esta última es provocada por microorganismos que invaden la pared gástrica y producen gas intramural, asociándose en la mayoría de los casos con un daño previo de la mucosa gástrica, como ocurre en nuestro caso.
Caso Clínico
Varón de 14 años con parálisis cerebral tras encefalopatía hipóxica isquémica por convulsiones neonatales, con nutrición enteral a través de sonda de gastrostomía desde el diagnóstico. Acude a urgencias por vómitos persistentes, inicialmente de contenido bilioso. Tras 24 horas de su ingreso, el paciente presenta vómitos de material fecaloideo, decidiéndose realizar TC de abdomen urgente en el que se observa neumoperitoneo y neumatosis parietal de estómago.
Dada la situación clínica del paciente y los hallazgos radiológicos, se decide laparotomía exploradora urgente en la que se observa estómago enfisematoso, sin signos de neumoperitoneo, limitándose únicamente a realizar recambio de sonda de gastrostomía de forma intraoperatoria.
Tras la intervención se inicia tratamiento antibiótico intravenoso con metronidazol, amoxicilina-clavulánico y gentamicina hasta completar 10 días, empleándose hasta entonces nutrición por vía parenteral.
Tras una semana de tratamiento se decide cambio de nutrición parenteral a enteral, lográndose administrar fórmula polimérica vía gastrostomía y mantener la ingesta oral según dieta habitual. Ante la buena evolución clínica y la ausencia de complicaciones, se decide alta hospitalaria.
Discusión
La gastritis enfisematosa es una enfermedad infrecuente caracterizada por la presencia de aire dentro de la pared gástrica con signos de toxicidad sistémica.
Los factores predisponentes incluyen malignidad, ingestión cáustica, cirugía reciente, esteroides, inmunosupresores, quimioterapia, alcohol y AINEs. Generalmente se presenta con dolor abdominal, náuseas, vómitos, diarrea y, ocasionalmente, hematemesis y sepsis.
El método diagnóstico de elección es la tomografía computarizada. Varios estudios enfatizan la distinción entre gastritis enfisematosa y enfisema gástrico. El enfisema gástrico es una condición relativamente benigna en la que se observa gas en la pared del estómago generalmente secundario a un barotrauma, sin signos de infección o toxicidad sistémica. Este cuadro es muy distinto de la gastritis enfisematosa, que presenta una alta mortalidad si no se trata de forma precoz.
La antibioterapia mejora el pronóstico de estos pacientes, siendo cuestionado aún el papel de la exploración quirúrgica que por el momento ha aportado pocos beneficios en estos casos.
CP-095. HEMORRAGIA DIGESTIVA ALTA COMO COMPLICACIÓN ATÍPICA DE UNA ACHALASIA INTERVENIDA
Ocaña Ledesma A, Bravo Aranda AM, Martínez Burgos M, Jiménez Pérez M
UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: hemorragia digestiva alta, achalasia.
Introducción
La achalasia es una anomalía motora del esófago que se caracteriza por la pérdida de peristaltismo del cuerpo esofágico, así como, por la disfunción del esfínter esofágico inferior. La manifestación de una hemorragia digestiva alta como complicación de una achalasia tratada quirúrgicamente es muy infrecuente.
Caso Clínico
Varón de 54 años. Intervenido de achalasia a los 13 años. Refiere presión a nivel centrotorácico tras la cena, habiendo presentado vómito de contenido alimenticio y restos hemáticos. Asocia disfagia a líquidos y sólidos de años de evolución.
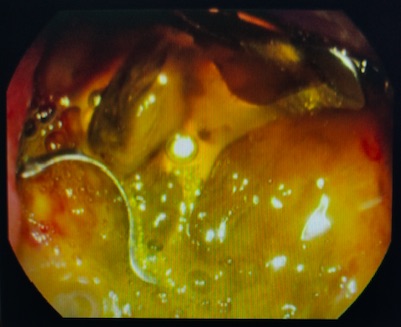
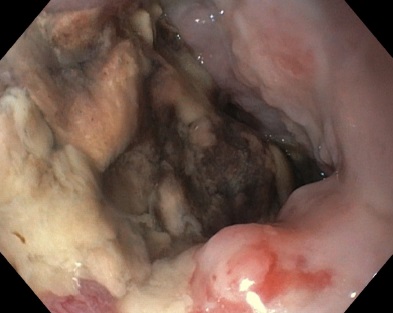
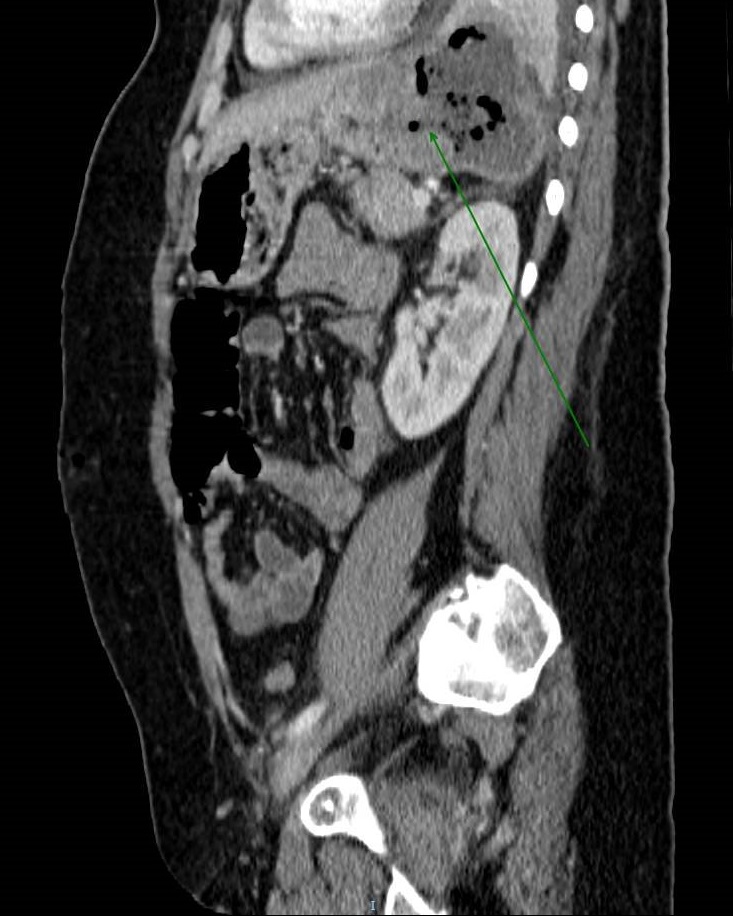
Pese a que inicialmente se pensó en una posible impactación esofágica, en la gastroscopia urgente se objetiva: megaesófago con úlceras esofágicas secundarias a retención crónica, gran coágulo que ocupa la totalidad de la luz esofágica secundaria a lesión sangrante en esófago distal no identificada. Dado episodio de inestabilidad hemodinámica, que requiere resucitación con hemoderivados y fluidoterapia, se decide realización de angio-TC urgente: esófago muy aumentado de calibre (megaesófago) con abundante contenido en su interior de carácter heterogéneo (figura 1 y figura 2). Se observa lámina hiperdensa en fase arterial que aumenta en fase portal a nivel de pared anterior y lateral derecha junto con estructura vascular hipertrófica de 8,5 x 8,5 mm, situada aproximadamente a 4 cm de hiato esofágico inferior, compatible con estructura vascular anómala hipertrófica con sangrado activo. Por lo que se procede a la realización de arteriografía y embolización con cianocrilato de vaso que nutre a segmento esofágico involucrado en el sangrado. Dada la masividad y la persistencia de la hemorragia, se decide esofagectomía parcial urgente mediante la técnica de Ivor-Lewis.
Tras la cirugía, se controló el sangrado, apreciándose en la pieza quirúrgica mucosa escamosa hiperplásica con inflamación crónica agudizada e inespecífica sin signos de malignidad.
Discusión
Una hemorragia digestiva alta (HDA) en el contexto de una achalasia es una complicación infrecuente, que puede estar en relación con una complicación de un tratamiento quirúrgico o endoscópico (dilatación neumática, inyección de toxina botulínica, miotomía endoscópica). No obstante, es posible una HDA no iatrogénica por la acción traumática de los alimentos retenidos, que causarían erosión de la mucosa esofágica; otro posible mecanismo sería una esofagitis de etiología infecciosa o medicamentosa; también la dilatación esofágica podría producir una dislaceración de sus paredes dando origen a una HDA; por último, existe un fenómeno por el cual la dilatación del esófago produciría una redistribución de la sangre procedente de la vena ácigos, dando lugar a varices esofágicas.
CP-096. HEMORRAGIA DIGESTIVA ALTA DE REPETICIÓN EN VARÓN DE 15 AÑOS
Ruiz Rodríguez AJ1, García Robles A1, Martín-Lagos Maldonado A1, Benavente Fernández A2, Selfa Muñoz A1
1Servicio Aparato Digestivo. Hospital San Cecilio, Granada. 2Servicio Medicina Interna. Hospital San Cecilio, Granada.
Palabras clave: hda de repetición.
Introducción
Las hemorragias digestivas en pacientes pediátricos son una entidad poco frecuente y suponen un reto diagnóstico-terapéutico.
Caso Clínico
Presentamos un varón de 14 años sin antecedentes que ingresa por dolor abdominal y vómitos en posos de café y toma de AINEs por cuadro catarral. La endoscopia digestiva alta (EDA) visualiza úlceras lineales milimétricas Forrest III en cuerpo. Tras 48 horas presenta hematemesis masiva, repitiéndose EDA observándose úlcera subcardial de dos centímetros con sangrado babeante y mucosa denudada, friable en cuerpo y fundus. Se colocan dos hemoclips e inyectamos adrenalina y etoxisclerol, controlándose la hemorragia. Nuevamente, a las 48 horas, presenta hematemesis, realizándose tercera EDA con sangrado babeante en la úlcera subcardial descrita previamente, sobre la que se colocan tres hemoclips y se aplica hemospray® periféricamente, ya que se observa una denudación difusa de parte superior del cuerpo, no susceptible de cierre mecánico. A continuación se implanta supraselectivamente microcoils en ramas de arteria gástrica derecha.
Durante el ingreso, es valorado por Enfermedades Infecciosas, por desarrollo de complicaciones infecciosas nosocomiales y, ante la atipicidad del cuadro, por Medicina Interna, en cuya exploración física aprecian hiperlaxitud generalizada que les lleva a realizar el Score de Beighton, resultando positivo 4 puntos (dorsiflexión pasiva del 5º dedo que sobrepasa los 90º de forma bilateral y aposición pasiva de los pulgares a la cara flexora del antebrazo de forma bilateral), junto a la presencia de hendidura palpebral antimongólica y cicatrices palpebrales, sospechando un trastorno del tejido conectivo, por lo que se solicita estudio genético cuyos resultados indican la presencia de la variante p.Arg1125GIn e n el gen de la FBN1 de forma heterocigota, siendo dicha mutación autosómica dominante, correspondiendo a un síndrome de Marfan.
FIGURA 1
Figura de endoscopia digestiva alta. Se aprecia el cuerpo gástrico con pliegues engrosados, morfología empedrada, parcheada, geográfica con aspecto denudado y sangrado espontáneo.
Discusión
Si bien en primera instancia cabe atribuir el sangrado a los AINEs, lo atípico de los hallazgos endoscópicos (mucosa denudada y friable), su evolución y los hallazgos físicos, permitieron establecer el diagnóstico diferencial con conectivopatías, confirmándose mediante estudio genético una mutación infrecuente del síndrome de Marfan. En ausencia de antecedentes familiares y manifestaciones clásicas esqueléticas-óculo-cardiovasculares, se requiere para su diagnóstico, un score sistémico positivo o la presencia de alguna mutación del gen de la FBN1, siendo la mutación p.Arg1125GIn de dicho gen la base del diagnóstico en nuestro caso. La HDA probablemente se debió a la alteración estructural y funcional del colágeno del tejido conectivo gástrico, disfuncional en esta enfermedad y fundamental en el soporte y protección del sistema vascular gástrico.
CP-097. HEMORRAGIA DIGESTIVA ALTA POR ULCERA DUODENAL SECUNDARIA A COLECISTITIS AGUDA COMPLICADA.
Angulo Mcgrath I1, Berlanga Cañete S2, Martinez Burgos M1
1 Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga. 2 Aparato Digestivo. Hospital Comarcal de la Serranía, Ronda.
Palabras clave: hda, ulcus duodenal, colecistitis aguda.
Introducción
La colecistitis aguda es la complicación más frecuente relacionada con la colelitiasis. Sin tratamiento los síntomas suelen desaparecer en unos 7-10 días. Sin embargo, dada su elevada frecuencia de complicaciones con elevada morbilidad suelen tratarse en el momento del diagnóstico mediante tratamiento quirúrgico definitivo (colecistectomía).
La fístula colecistoentérica se ha descrito como complicación hasta en un 2-3% de los casos, siendo la fístula colecistoduodenal la más frecuente de ellas. La etiopatogenia más frecuente es la necrosis vesicular hacia el lumen intestinal, consecuencia de la presión continua de las litiasis y la inflamación secundaria a la colecistitis aguda.
Caso Clínico
Varón de 84 años. Consulta en urgencias por dolor abdominal intenso. Analíticamente destaca PCR 98 y alteración de perfil hepático en analítica, sin embargo, la ecografía abdominal descarta colecistitis o dilatación de vía biliar. Acude nuevamente una semana después por persistencia del dolor, que se ha intensificado. A la exploración Muprhy positivo y persiste elevación de reactantes de fase aguda. Se realiza TC abdominal urgente, que describe vesícula biliar compatible con colecistitis aguda y engrosamiento de pared duodenal, sin poder descartar trayecto fistuloso (Figura 1 y 2).
Varias horas después el paciente presenta hematemesis franca con inestabilidad hemodinámica, realizándose en las siguientes horas dos endoscopias urgentes bajo monitorización por anestesista. En la primera de ellas no se consigue terapéutica eficaz, por no poderse acceder a segunda porción duodenal debido a gran coágulo en antro pilórico. En la segunda, se visualiza gran ulcera de unos 5 cm, con vaso visible y coágulo adherido en cara anterior de bulbo (Figura 3). Se realiza terapéutica con adrenalina, dos hemoclips y posicionamiento de Ovesco, sin complicaciones inmediatas.
El paciente presenta buena evolución posterior, sin nueva exteriorización. La colecistitis se maneja como evolucionada con tratamiento antibiótico. En EDA de control (Figura 4), se visualizan hemoclips y Ovesco normoposicionados con abundantes restos biliosos.
Discusión
Aunque epidemiológicamente las fístulas colecistoduodenales aparecen más frecuentemente relacionadas con una afectación crónica por colelitiasis, en nuestro caso presentamos una relacionada con un episodio agudo de colecistitis.
Destacar la potencial severidad de ésta complicación en una patología tan frecuente como es la colecistitis, haciéndose necesaria su sospecha y despistaje ante el diagnóstico de una colecistitis evolucionada.
CP-098. HEMORRAGIA DIGESTIVA MASIVA SECUNDARIA A DERMATOMIOSITIS.
Lorenzo González L, Jiménez García VA, Barranco Castro D, del Pino Bellido P, Rodríguez Téllez M
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: hemorragia digestiva, dermatomiositis.
Introducción
La dermatomiositis es una enfermedad autoinmune degenerativa de las fibras musculares y el tejido conectivo ocasionada por una microvasculopatía mediada por células CD4+ y linfocitos T, atrofia perifascicular y microinfartos musculares. Se trata de una enfermerdad poco frecuente que constituye un 20% de las miopatías inflamatorias del adulto y un porcentaje alto se asocia a carcinomas.
Caso Clínico
Paciente varón de 60 años con antecedentes personales de diabetes mellitus, hipertensión arterial y dislipemia, en reciente estudio por dermatología por cuadro compatible con dermatomiositis no neoplásica y en tratamiento con esteroides a dosis plenas. El paciente ingresa por una neumonía aguda adquirida en la comunidad y anemia en rango transfusional. Durante su ingreso en planta presenta hemorragia digestiva baja masiva con shock hipovolémico que tras realizar AngioTC urgente sin encontrar punto de sangrado, obliga a realizar hemicolectomía derecha ampliada (colonoscopia con colitis inespecífica reciente). Presenta evolución tórpida con persistencia de anemización a pesar de transfusiones, por lo que finalmente es necesario su ingreso en UCI donde se realiza gastroscopia con diagnostico de friabilidad esofágica y duodenopatía erosiva, sin signos de sangrado reciente. También se realiza colonoscopia, donde se aprecian restos hemáticos sin observar punto sangrante en recto-sigma. Para completar estudio se realiza cápsula endoscópica en la que se observa una panenteritis ulcerativa con restos hemáticos frescos, probablemente como manifestación de dermatomiositis.
Igualmente, se realizó estudio de coagulación encontrándose una disfunción plaquetaria achacable al tratamiento con esteroides.
El paciente presenta deterioro general rápido con persistencia de hemorragia digestiva siendo finalmente exitus. Se realiza autopsia clínica identificando causa de la muerte el shock séptico secundario a peritonitis aguda purulenta y hemorragia digestiva causada en comienzo por angiodisplasias intestinales añadiendo en la fase final coagulopatía propia de shock séptico.
Discusión
La dermatomiositis afecta principalmente a la piel y los músculos, pero otros órganos participan de forma variable. Pueden presentarse alteraciones cardiacas, cutáneas, anemia, polineuropatía y neumonía por aspiración. También pueden aparecer enfermedad por reflujo gastroesofágico si existe afectación esofágica. Además, en esta enfermedad puede aparecer vasculitis intestinal, pudiendo ocasionar ulceraciones, necrosis, perforación y hemorragia digestiva.
Nuestro paciente presentaba dichas complicaciones: vasculopatía intestinal con hemorragias graves que no conseguimos controlar ni con tratamiento esteroideo ni mediante cirugía.
Las miopatías son, por tanto, un grupo de enfermedades raras en las que debemos tener en cuenta posibles complicaciones gastrointestinales graves como las descritas en este caso.
CP-099. PAPEL DEL N-BUTIL-2-CIANOCRILATO EN EL TRATAMIENTO DE LA HEMORRAGIA DIGESTIVA ALTA DE ORIGEN VARICOSO. UNA SERIE DE CASOS
Olvera Muñoz R, Lara Romero C, Osorio Marruecos M, Otero López-Cubero S
Servicio Aparato Digestivo. Hospital de Especialidades de Puerto Real, Puerto Real.
Palabras clave: n-butil-2-cianocrilato, hemorragia digestiva alta de origen varicoso, cirrosis hepática.
Introducción
El tratamiento de elección en la hemorragia digestiva alta secundaria a varices esofagogástricas tipo 2 (VEG-2) y varices gástricas aisladas tipo 1 (VGA-1) de la clasificación de Sarín es la inyección endoscópica de sustancias adhesivas como el N-butil-2-cianocrilato.
El objetivo de esta serie de casos fue recoger la experiencia de nuestro centro acerca de este procedimiento, describiendo los resultados y complicaciones observadas.
Material y métodos
Se recogieron los datos de manera retrospectiva desde enero 2014 hasta enero 2020 del Hospital Universitario de Puerto Real (Cádiz) de pacientes cirróticos con episodio de hemorragia secundaria a rotura de VEG-2 o VGA-1 tratados mediante la inyección endoscópica de cianocrilato.
Se excluyeron pacientes <18 años y aquellos en los cuales se detecta otra posible causa de hemorragia.
Resultados
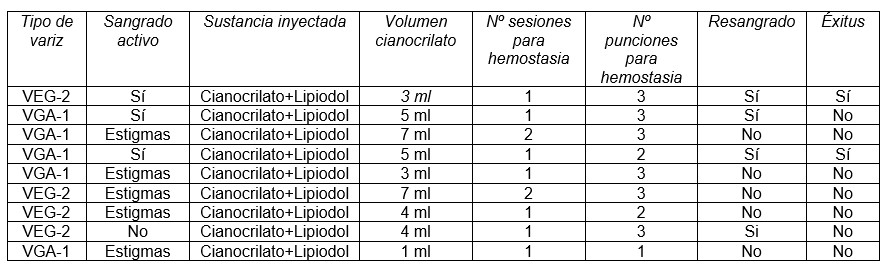
Se incluyeron un total de 9 pacientes con hemorragia por VEG-2 (4) y VGA-1 (5). En todos se diluye cianocrilato con lipiodol (proporción 1:1). La hemostasia se consigue en un primer abordaje endoscopio en 7 casos, requiriéndose segunda sesión en los 2 restantes. El volumen medio inyectado para la hemostasia fue de 4 ml [1-7], requiriendo entre 1 y 3 punciones en la variz. Se produce resangrado en 4 pacientes (3 por úlcera post-esclerosis), siendo en aquellos que se realizaron un mayor número de punciones; dos de ellos fallecieron como consecuencia del resangrado, uno respondió a tratamiento médico y en el último se coloca TIPS como terapia de rescate. No se objetiva ninguna complicación trombótica tras la técnica. Sólo 2 de los pacientes tenían historial de hemorragia previa de origen varicoso, habiendo sido tratados mediante ligadura con bandas. Únicamente 3 se encontraban bajo profilaxis con betabloqueantes. En el seguimiento ninguno de ellos recibe trasplante hepático. La etiología de la cirrosis hepática de base más frecuente fue la enólica (7), presentando los pacientes una puntuación media de B7-8 en la clasificación de Child-Pugh y de 11 en el índice de MELD. Uno de los pacientes fue diagnosticado de CHC durante el seguimiento.
Conclusiones
Aunque el número de pacientes sea limitado, el tratamiento con cianocrilato indicado en el sangrado y profilaxis secundaria de VEG-2 y VGA-1 resulta efectivo en más del 70% de los casos, con baja tasa de complicaciones asociadas al mismo aunque con una tasa de resangrado no desdeñable, por lo que se debe tener en cuenta la posibilidad de TIPS como tratamiento de rescate.
CP-100. PERFORACIÓN EN FUNDUS GÁSTRICO DE ORIGEN MALIGNO CONTENIDA POR COLECCIÓN INFRADIAFRAGMÁTICA CON EXTENSIÓN ENDOTORÁCICA
Díaz Alcázar MM, Martín-Lagos Maldonado A, García Robles A
UGC Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: linfoma gástrico, perforación gástrica, absceso infradiafragmático.
Introducción
La perforación gástrica es una complicación típica de úlceras pépticas, sin embargo raramente se asocia con tumores gástricos. Se han descrito pocos casos de perforación gástrica en contexto de linfoma primario gástrico.
Caso Clínico
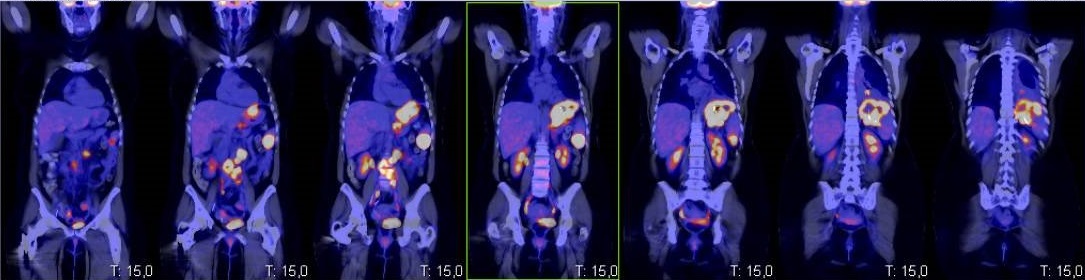
Mujer de 46 años que consulta por epigastralgia, hematemesis y melenas. Antecedente reciente de consumo de AINES por dolor costal. Se realiza esofagogastroduodenoscopia objetivando coágulo rojo en fundus, que se retira exponiendo úlcera de aspecto excavado rodeada por pliegues engrosados con sangrado babeante. Se trata con esclerosis y colocación de hemoclips. Se repite esofagogastroduodenoscopia varios días después con hallazgo de úlcera profunda que parece continuarse con una cavidad, con bordes sucios y fribrinados que impresiona de fístula o perforación (Fig 1). Dados los hallazgos se realiza tomografía computarizada toracoabdominal, encontrando perforación de la pared gástrica posterosuperior contenida por la formación de absceso infradiafragmático de 86x95x75mm, con burbujas de gas y signos de extensión endotorácica, ya que no se identifica plano de separación con el diafragma (Fig 2). Se realiza drenaje percutáneo de colección y colocación de catéter, con aislamiento de Pseudomonas aeruginosa. Estudio histológico de biopsias gástricas concluye linfoma B difuso de células grandes fenotipo no centrogerminal y subtipo inmunoblástico. Estudio de extensión con PET-TC objetiva afectación gástrica, ganglionar locorregional y retroperitoneal, esplénica y probablemente pulmonar (Fig 3). Se inicia quimioterapia con régimen CHOP.
FIGURA 1
Figura de endoscopia digestiva alta en que se observa cavidad con bordes sucios y fribrinados sugerente de perforación o fístula gástrica.
Discusión
El 40% de los linfomas no Hodgkin son extranodales, y fundamentalmente afectan al tracto gastrointestinal, aunque representan menos del 5% de las neoplasias a este nivel. El órgano más afectado, como en el caso presentado, es el estómago. La mayoría son linfoma T asociado a mucosas (MALT) y linfoma B difuso de células grandes (DLBCL). La clínica suele ser molestias dispépticas inespecíficas, siendo los síntomas B poco frecuentes, lo que retrasa el diagnóstico.
La perforación gástrica ocurre ocasionalmente en pacientes en tratamiento con quimioterapia. Sin embargo, la perforación espontánea es rara, y supone un factor de mal pronóstico además de tener elevada mortalidad. Se debe a que la necrosis tumoral alcanza la subserosa, independientemente de que haya úlcera concomitante. La perforación es más frecuente en tumores grandes ulcerados.
CP-101. PERFORACIÓN GÁSTRICA SECUNDARIA A LINFOMA B DIFUSO DE CÉLULAS GRANDES.
Ortiz Sánchez A, García Verdejo FJ, Vidal Vilchez B, Berdugo Hurtado F, Roa Colomo A
Servicio Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: perforación gástrica, h.pylori, linfoma .
Introducción
El linfoma gástrico primario es un tumor poco frecuente, representando el 5% del total de neoplasias gástricas primarias. El estómago es la localización más común de presentación extranodal de los linfomas no Hodgkin, siendo la perforación gástrica espontánea una complicación inusual en ausencia de quimioterapia previa.
Presentamos el caso de una perforación gástrica secundaria a linfoma B difuso de células grandes (LBDCG).
Caso Clínico
Mujer de 46 años con antecedentes de consumo crónico de AINEs y estudio de Antígeno de Helicobacter pylori en heces positivo, consulta por epigastralgia de semanas de evolución junto con tres episodios de hematemesis.
Se realiza endoscopia digestiva alta (EDA) observando gran coágulo en fundus gástrico, junto con pliegues engrosados y eritematosos a su alrededor.
Durante su estancia hospitalaria requiere realización de dos nuevas EDAs por recurrencia de sangrado digestivo, con colocación de clips de hemostasia y esclerosis con adrenalina.
Se realiza EDA de control para toma de biopsias con hallazgos de úlcera profunda subcardial (Figura 1), por lo que se realiza TC toracoabdominal con hallazgos de perforación de la pared gástrica posterosuperior contenida por la formación de absceso adyacente con signos de extensión endotorácica y adenopatías patológicas en hilio esplénico (Figura 2).
Se decide manejo conservador mediante drenaje percutáneo de colección subfrénica, y tras histología compatible con LBDCG y estadiaje mediante PET-TC, se inicia tratamiento con quimioterapia tipo CHOP-R previa a nueva valoración quirúrgica.
Discusión
La localización más frecuente de linfoma no Hodgkin extranodal es el estómago, presentándose en un 40% de los casos como tejido linfoide asociado a mucosas de bajo grado (MALT) y en un 60% como LBDCG de alto grado.
Ambos subtipos están relacionados con la infección por H. pylori, con escasas manifestaciones clínicas en estadios iniciales y una frecuencia de presentación con complicaciones como obstrucción o perforación extremadamente baja.
El tratamiento inicial de LBDCG depende de la extensión de la enfermedad, localización y presencia o ausencia de complicaciones. Hoy en día, la cirugía ha dejado de ser una piedra angular en el tratamiento de esta patología, reservándose para casos refractarios a primeras líneas de tratamiento o presencia de complicaciones.
Se ha demostrado un alta tasa de remisión tumoral mediante tratamiento erradicador de H.pylori exclusivo en estadios iniciales, manteniendo la quimioinmunoterapia con CHOP-R para casos refractarios o aquellos en estadios más avanzados, con una tasa de supervivencia global a 5 años entre el 50 y 70%.
CP-102. PÓLIPO FIBRINOIDE INFLAMATORIO SIMULANDO LESIÓN NEOPLÁSICA MALIGNA
Fernández Alvarez P1, Jimenez-García VA1, Rodríguez-Téllez M2, Caunedo Alvarez A1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla. 2UGC Endoscopia. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: pólipo fibrinoide inflamatorio, lesión submucosa gástrica.
Introducción
Los pólipos fibrinoides inflamatorios (PFI) son lesiones mesenquimales raras que afectan al tracto gastrointestinal, siendo la localización mas frecuente es antro gástrico.
Caso Clínico
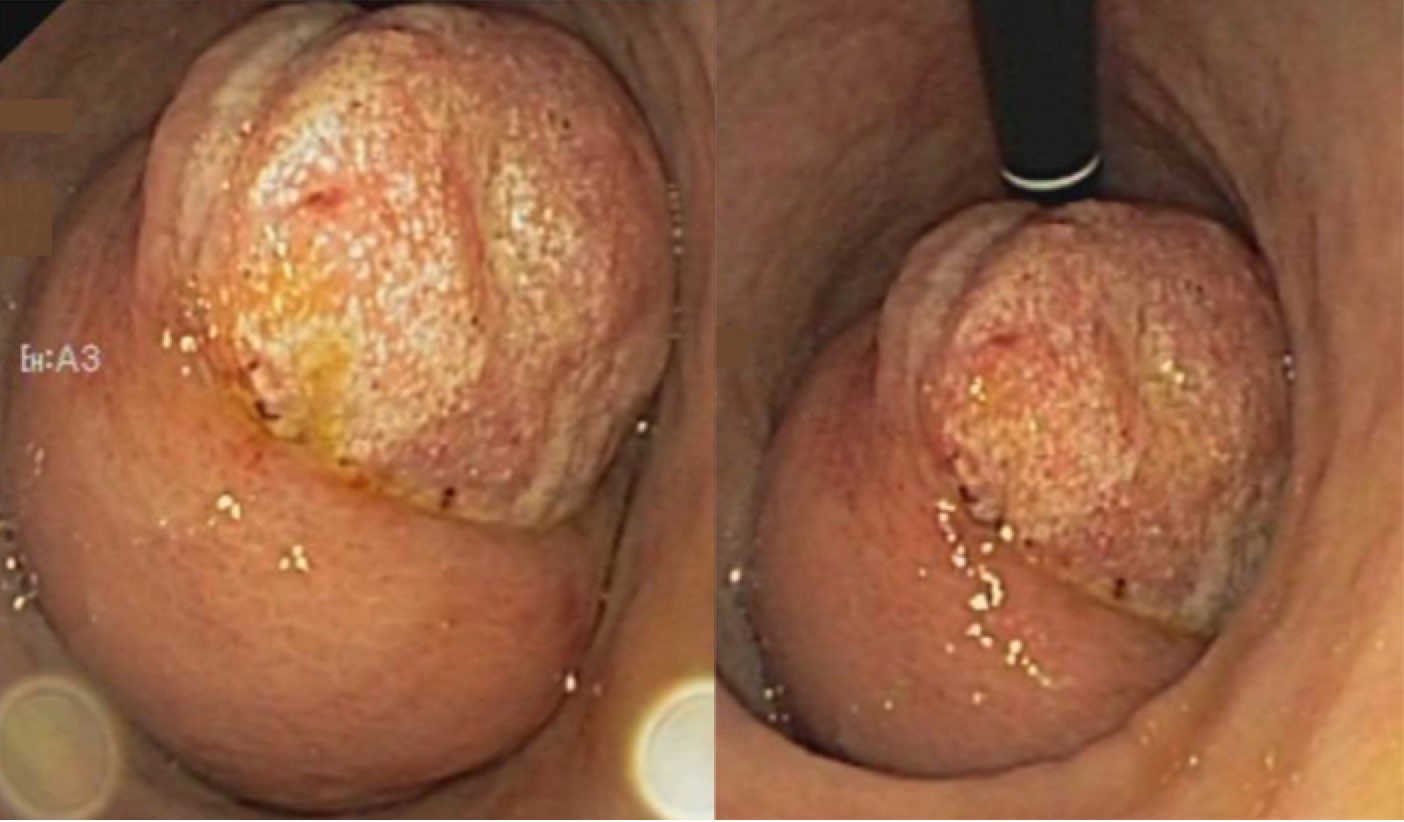
Mujer de 74 años sin antecentes conocidos que es derivada a nuestro hospital por presentar un cuadro de hemorragia digestiva alta exteriorizada en forma de melenas. Requirió transfusión de hemoderivados por cifras de hemoglobina en 7,2 g/dl, manteniendo estabilidad hemodinámica. Se realizó una gastroscopia de urgencia que mostró una gran formación pseudopediculada de aproximadamente 7 cm originada en la cara anterior del antro gástrico, justo distal a la incisura, respetándola. Presentaba un aspecto submucoso con superficie umbilicada, erosiones y fibrina en su porción distal (Fig.1). Durante el procedimiento se tomaron biopsias que no resultaron diagnósticas, pero no podían descartar la presencia de un liposarcoma gástrico. La tomografía computerizada realizada posteriormente mostró una protrusión intraluminal gástrica de densidad grasa sugestiva de lesión submucosa (Fig.2). Finalmente, se llevó a cabo un estudio ecoendoscópico para mejor definición de la lesión y estadíaje local que describió la presencia de una lesión hiperecogénica, vascularizada en su centro con bordes regulares y nacimiento en la 3ª capa, respetando la muscularis propia y sin presencia de adenomegalias (Fig.3). Ante estos hallazgos se decidió en “Comité quirúrgico” extirpación de la lesión realizando una gastrectomía parcial. Finalmente, el resultado histológico de la pieza quirúrgica informó de la benignidad de la lesión, reportando la presencia de lesión fibroinflamatoria gástrica esclerosante.
FIGURA 1
Imágenes endoscópicas de la lesión mostrando una gran formación submucosa. En retroversión se observa la porción distal que es umbilicada y presenta erosiones y lesiones fibrinadas sobre su superficie
Discusión
Los PFI fueron descritos por primera vez por Vanek en 1947. La serie mas amplia reportada, en una institución americana, describió únicamente 83 casos entre los años 1999 y 2012 .
Generalmente, constituyen lesiones benignas, de origen submucoso que se extienden hacia la mucosa siendo abordables por biopsias endoscópicas. Revisando la literatura, hemos encontrado dos casos de PFI invasivos con afectación de la capa muscular propia y extensión hacia la subserosa.
La etiología de las lesiones es controversial, existiendo varias hipótesis. Entre ellas, una respuesta descontrolada del huésped a una lesión local desconocida, una infección o una reacción alérgica. Se han descritos cambios morfológicos de los PFI tras erradicación del Helicobarter Pylori, lo cual apoyaría la teoría infecciosa.
El tratamiento podría ser endoscópico, siempre y cuando la muscularis propia no se encuentre afectada. En nuestro caso, nos planteamos la resección quirúrgica debido a la ausencia inicial de diagnóstico histológico de confirmación, las dimensiones de la lesión y el potencial riesgo invasivo, aunque infrecuente, descrito en la literatura.
CP-103. SÍNDROME ZOLLINGER-ELLISON
Solá Fernández A, Ruz Zafra P, Trigo Salado C
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla.
Palabras clave: tumor neuroendocrino, gastrinoma.
Introducción
El término síndrome de Zollinger-Ellison (SZE) se utiliza para describir un tumor neuroendocrino que secreta gastrina (gastrinoma), resultando en una hipergastrinemia que provoca invariablemente hipersecreción ácida.
Caso Clínico
Varón de 59 años, sano, que consulta por síndrome diarreico, epigastralgia severa y pérdida ponderal de 10 kg. Se realiza endoscopia digestiva alta (EDA) con hallazgo de amplia ulceración supracardial y numerosas úlceras superficiales de segunda porción duodenal de aspecto agudo y localización atípica. Se instaura tratamiento con inhibidor de la bomba de protones (IBP) a dosis doble. EDA de control con desaparición de las lesiones.
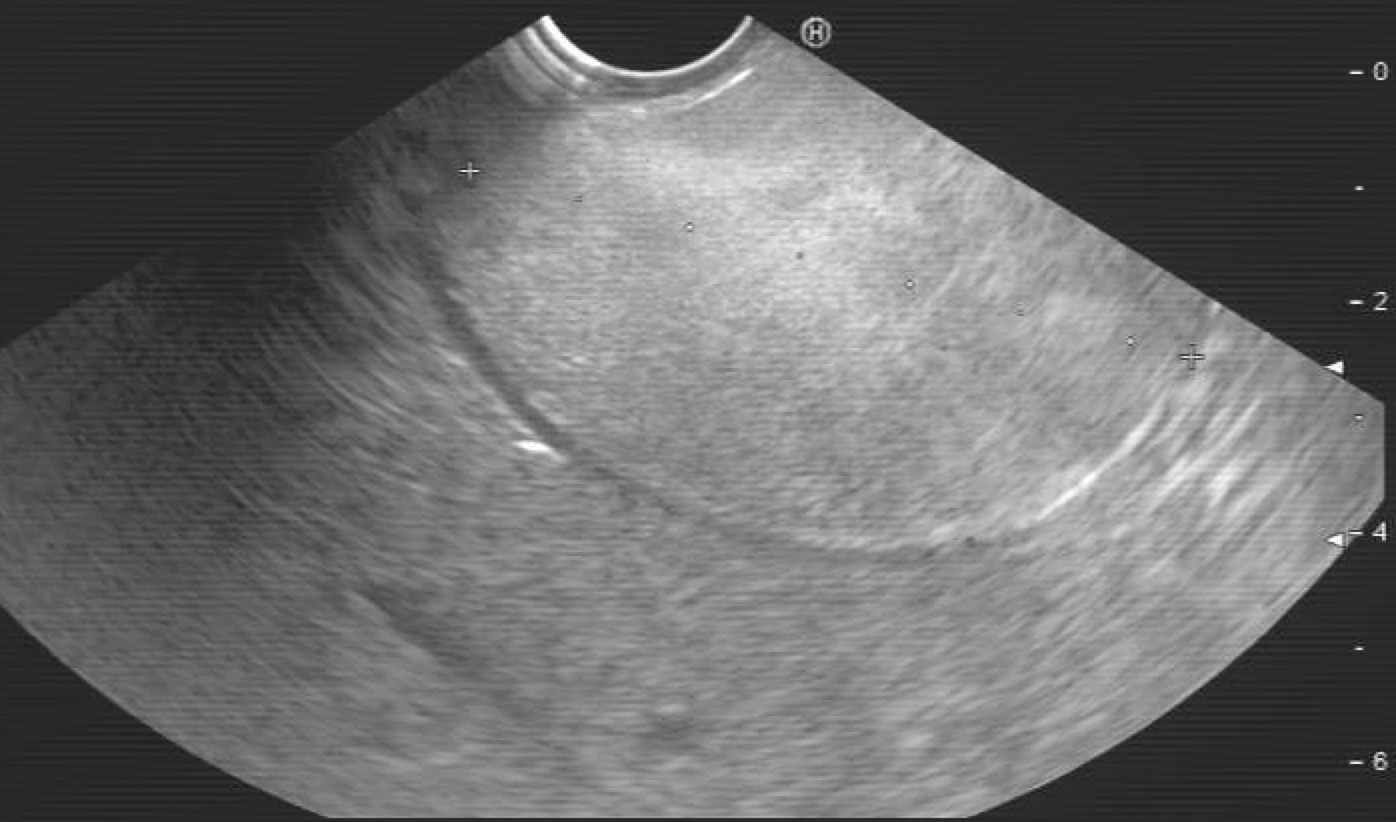
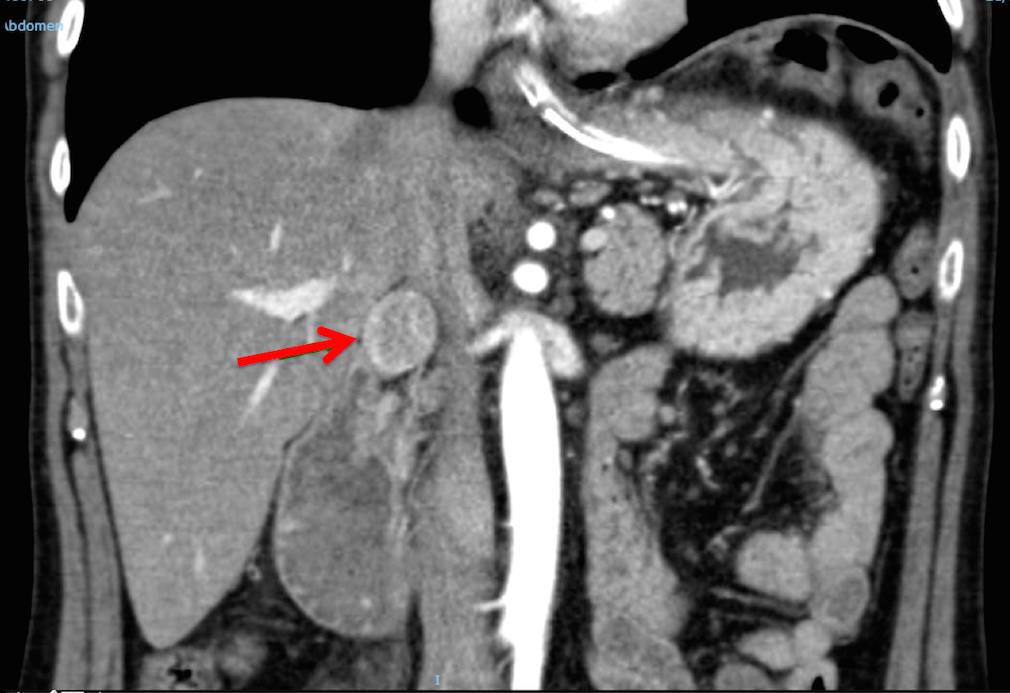
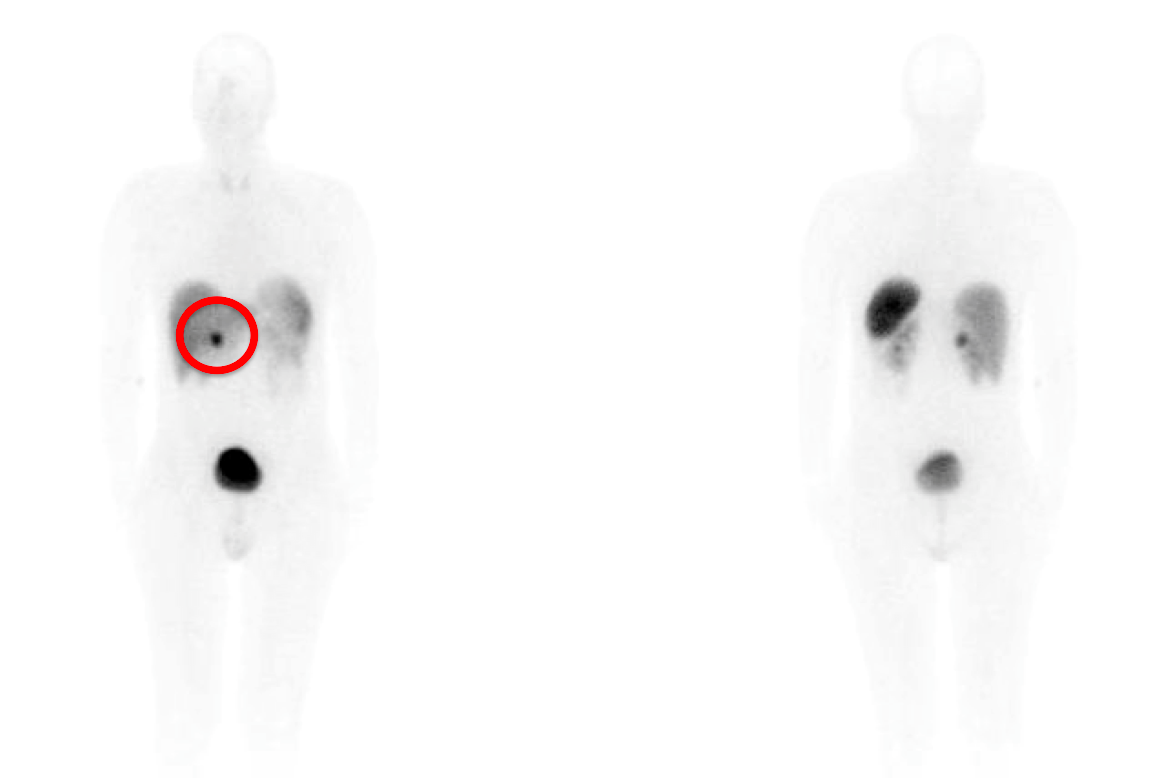
Dos meses más tarde, ingresa por epigastralgia y vómitos. Se realiza TC de abdomen en el que únicamente se objetiva nódulo hipervascular retroportal de 3 cm. A las 48 horas, episodio de melenas e hipotensión. Se realiza EDA con gran ulceración en segunda porción duodenal con sangrado activo y tratamiento subóptimo, que precisa embolización por radiología vascular. Ante la extensa y severa afectación ulcerosa y el hallazgo de nódulo abdominal peripancreático, se plantea la posibilidad de gastrinoma. Se confirma hipergastrinemia (gastrina 800 pg/ml), y cromogranina A elevada (717 ng/mL). Se solicita gammagrafía de receptores de somatostatina que confirma captación única por nódulo ya conocido, sin objetivarse otro foco local ni a distancia. Pendiente de intervención quirúrgica, aparición de dolor torácico severo de inicio abrupto. Se realiza TC que objetiva perforación de esófago distal secundaria a ulceración profunda, con extenso neumoperitoneo y neumomediastino. Dado estabilidad del paciente, se consensua manejo conservador con buena evolución clínica.
Tres semanas más tarde, se somete a intervención, con enucleación del tumor retroportal. Se confirma histológicamente tumor neuroendocrino bien diferenciado con inmunofenotipo compatible con gastrinoma.
Discusión
La incidencia anual de gastrinomas es de 0.5 a 2 por millón de población. La edad al diagnóstico oscila entre los 20 y 50 años, con mayor prevalencia en hombres. El síntoma inicial más frecuente es el dolor abdominal, seguido de la diarrea crónica. El 90-95 % de los pacientes desarrollan úlceras pépticas en el tracto gastrointestinal superior. Sólo el 10 % se presentan con sangrado y el 7 % con perforación.
La gammagrafía con análogos de somatostatina es el método que ha demostrado más sensibilidad en el diagnóstico de gastrinomas primarios y en la detección de sus metástasis. La cirugía es la opción curativa. De no ser posible, la terapia sistémica con análogos de la somatostatina puede retrasar el crecimiento del tumor y reducir los niveles de gastrina.

 Descargar número completo
Descargar número completo Download full issue
Download full issue