CO-06. EXPRESIÓN DE HEPATOQUINAS Y ADIPOQUINAS EN PACIENTES CON HEPATOCARCINOMA
Zamora Olaya JM1, Prieto De La Torre M1, Hermán-Sánchez N2, Amado Torres V1, De La Mata M1, D. Gahete M2, Rodríguez Perálvarez M1
1Departamento Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba. 2Laboratorio Investigación. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: hepatocarcinoma, hepatoquinas, adipoquinas.
Introducción
Analizar la expresión de una batería de hepatoquinas y adipoquinas como posibles biomarcadores de hepatocarcinoma.
Material y métodos
Estudio transversal en el que se comparó la expresión de 55 hepatoquinas y adipoquinas en tejido tumoral de pacientes con hepatocarcinoma en comparación con el tejido peritumoral adyacente al tumor. Como grupos control se utilizaron muestras de tejido hepático de pacientes cirróticos y de pacientes sanos sin hepatopatía. Se utilizó PCR cuantitativa para analizar la expresión de hepatoquinas y adipoquinas. Se construyó un panel de posibles biomarcadores mediante regresión logística multivariante para analizar la capacidad discriminativa entre tejido tumoral y peritumoral, y entre tejido sano y patológico.
Resultados
Se incluyeron 99 pacientes (78% hombres, edad media 59 ± 11,5 años). En los pacientes con hepatocarcinoma, la etiología de la enfermedad hepática más frecuente fue la etílica (47,2%), seguida del VHC (37,7%). Un 5,7% fueron tumores pobremente diferenciados. Se obtuvieron un total de 154 muestras de las cuales un 40.9% eran de tejido tumoral, el 30,3% de tejido peritumoral, un 25,4% provenían de pacientes cirróticos y un 3,4% de individuos sanos.
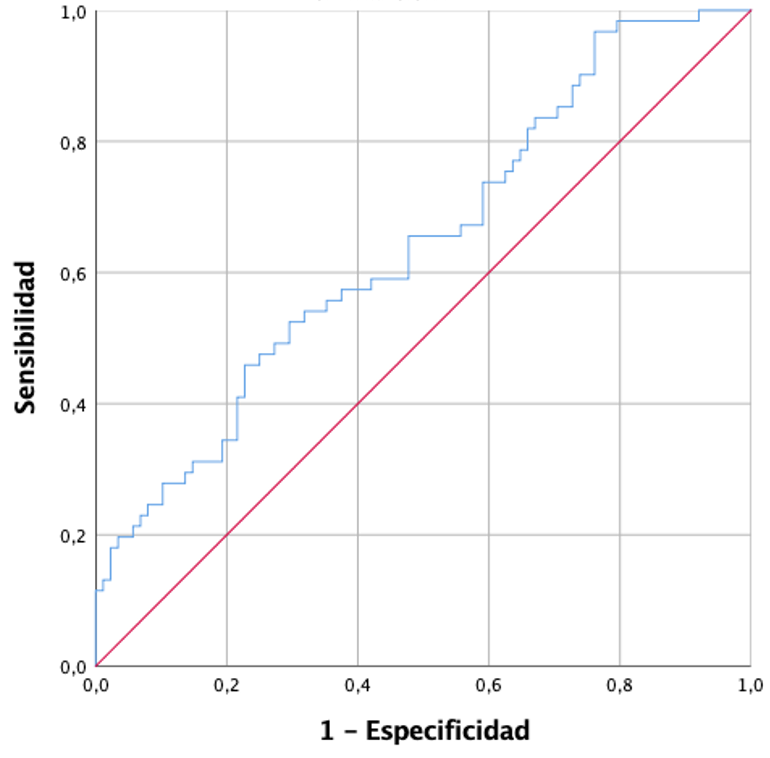
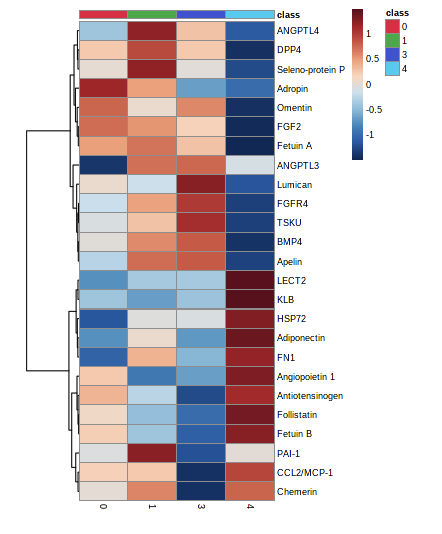
Al comparar las muestras de tejido tumoral con el resto de grupos, se obtuvieron tres moléculas en el análisis multivariante: CCL2/MCP-1 (OR 1,026, p=0,022), angiopoyetina 2 (OR 0,206, p=0,041) y fibronectina 1 (OR 1,006, p=0,008). El modelo obtuvo un área bajo la curva ROC de 0,64 para discriminar entre tejido tumoral y no tumoral.
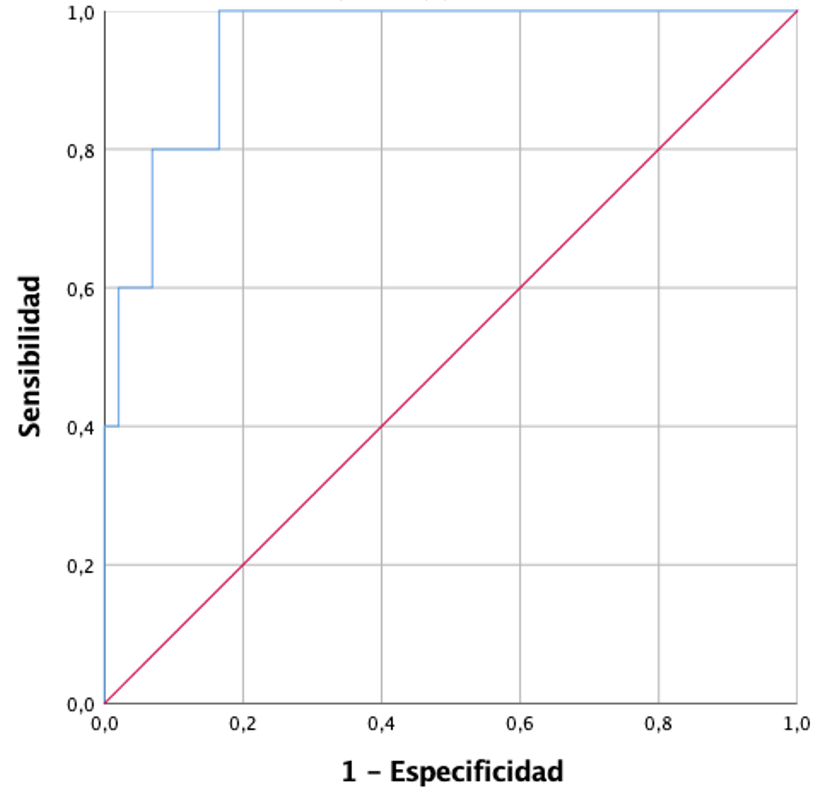
Al comparar las muestras de los individuos sanos con el resto de las muestras (tumoral, tejido adyacente y cirrosis), se obtuvo un modelo multivariante compuesto por 4 moléculas: proteína similar a la angiopoietina 1 (ANGPTL1) (OR=1,678, p=0,044), ANGPTL8 (OR=1,132, p=0,01), factor de crecimiento de fibroblastos 2 (OR=1,464, p=0,038) y dipeptidil peptidasa 4 (OR=1,031, p 0,058). El modelo obtuvo un área bajo la curva de 0,94 para discriminar entre tejido sano y patológico.
CO-07. ANÁLISIS DE RENTABILIDAD DEL TEST DE SANGRE OCULTA EN HECES EN PACIENTES ASINTOMÁTICOS FRENTE A COLONOSCOPIA EN PACIENTES SINTOMÁTICOS
Tejero Jurado R, Alejandre Altamirano RM, Pleguezuelo Navarro M, Serrano Ruiz FJ, Hervás Molina AJ
UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: cáncer colorrectal, test de sangre oculta en heces, cribado..
Introducción
Determinar la diferencia de incidencia de cáncer colorrectal (CCR) y sus lesiones precursoras, así como la diferencia de mortalidad por CCR en pacientes asintomáticos con resultado positivo de test de sangre oculta en heces (SOHi) frente a aquellos pacientes en que se ha realizado la colonoscopia por datos de alarma: anemia ferropénica, rectorragia o test de SOHi positivo indicado por síntomas.
Material y métodos
Estudio observacional, retrospectivo y unicéntrico, que incluyó un total de 2695 pacientes sometidos a colonoscopia tras SOHi positiva dentro del programa de cribado y colonoscopia indicada por síntomas (anemia ferropénica, rectorragia o SOHi positiva indicada fuera del programa de cribado) durante el año 2019 en el Hospital Universitario Reina Sofía, con un seguimiento posterior hasta el 31 de diciembre de 2021. Se recogieron variables demográficas de pacientes, relativas al procedimiento, hallazgos por endoscopia, características histológicas, diagnóstico de CCR, estadiaje, tratamiento, progresión o éxitus durante el seguimiento. Se analizó la relación entre la incidencia de CCR o sus lesiones precursoras, el estadío del mismo y la mortalidad en cada grupo.
Resultados
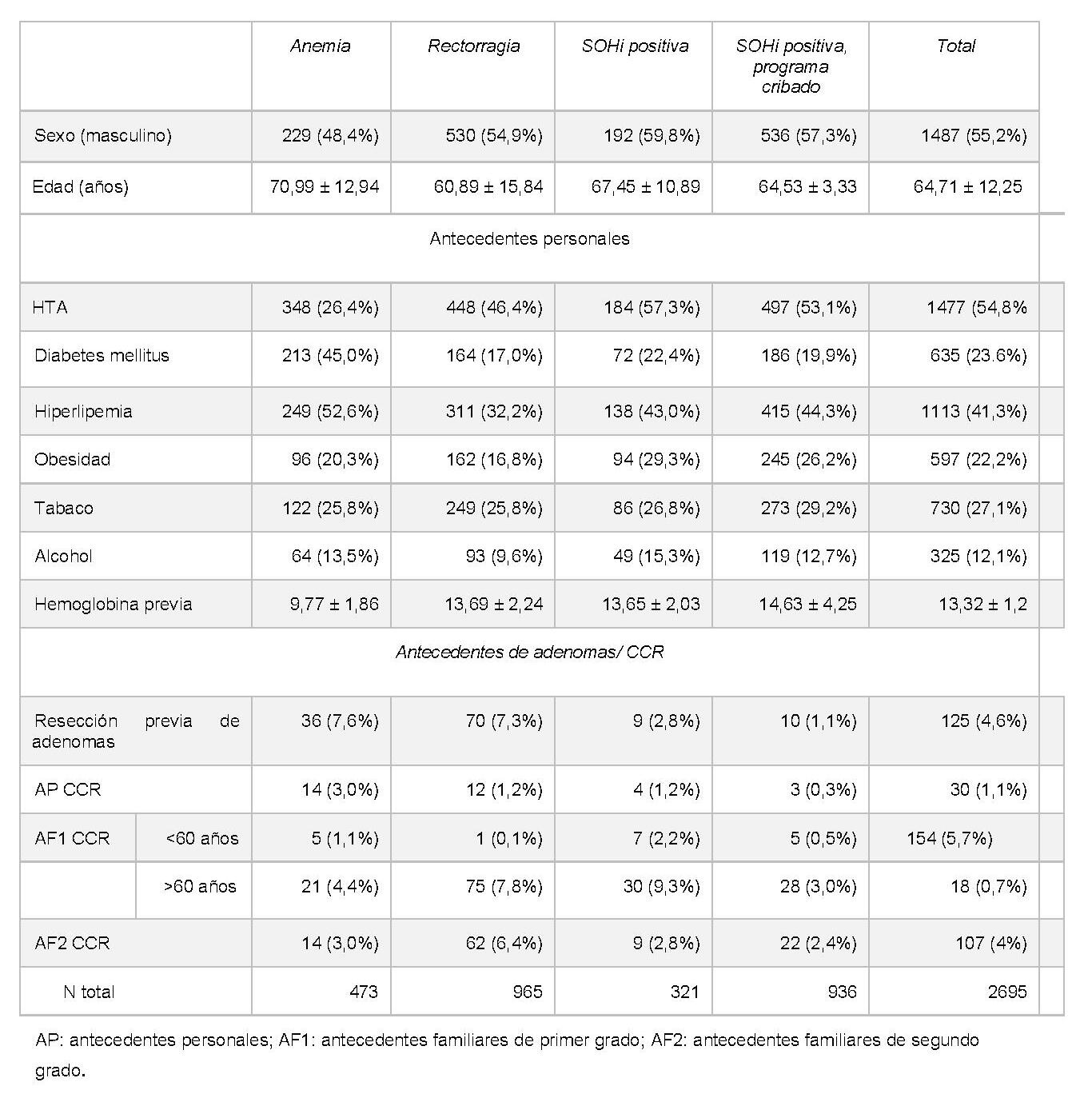
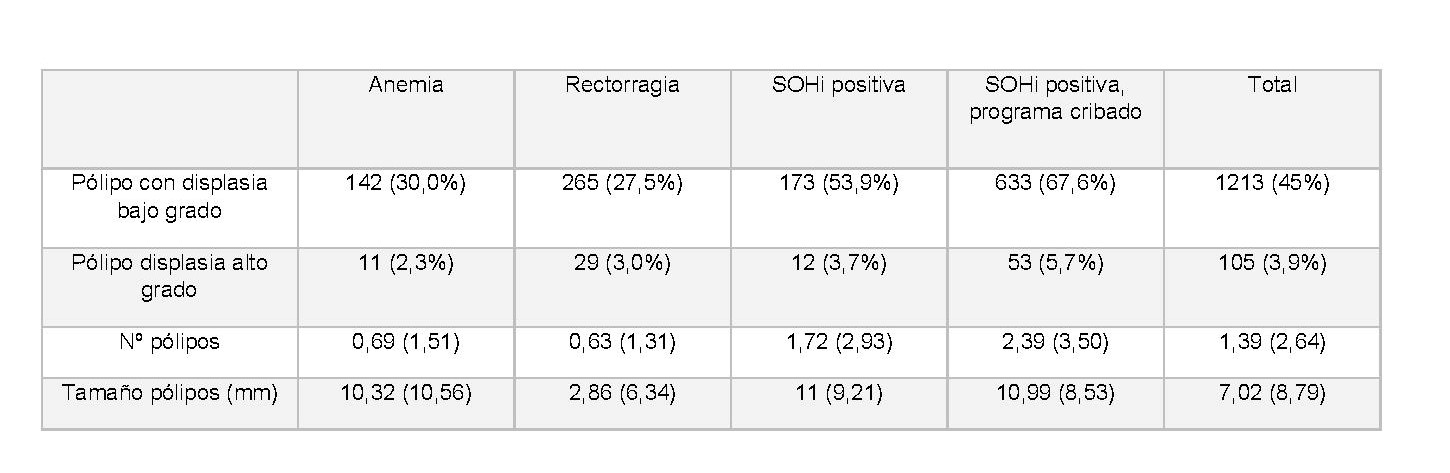
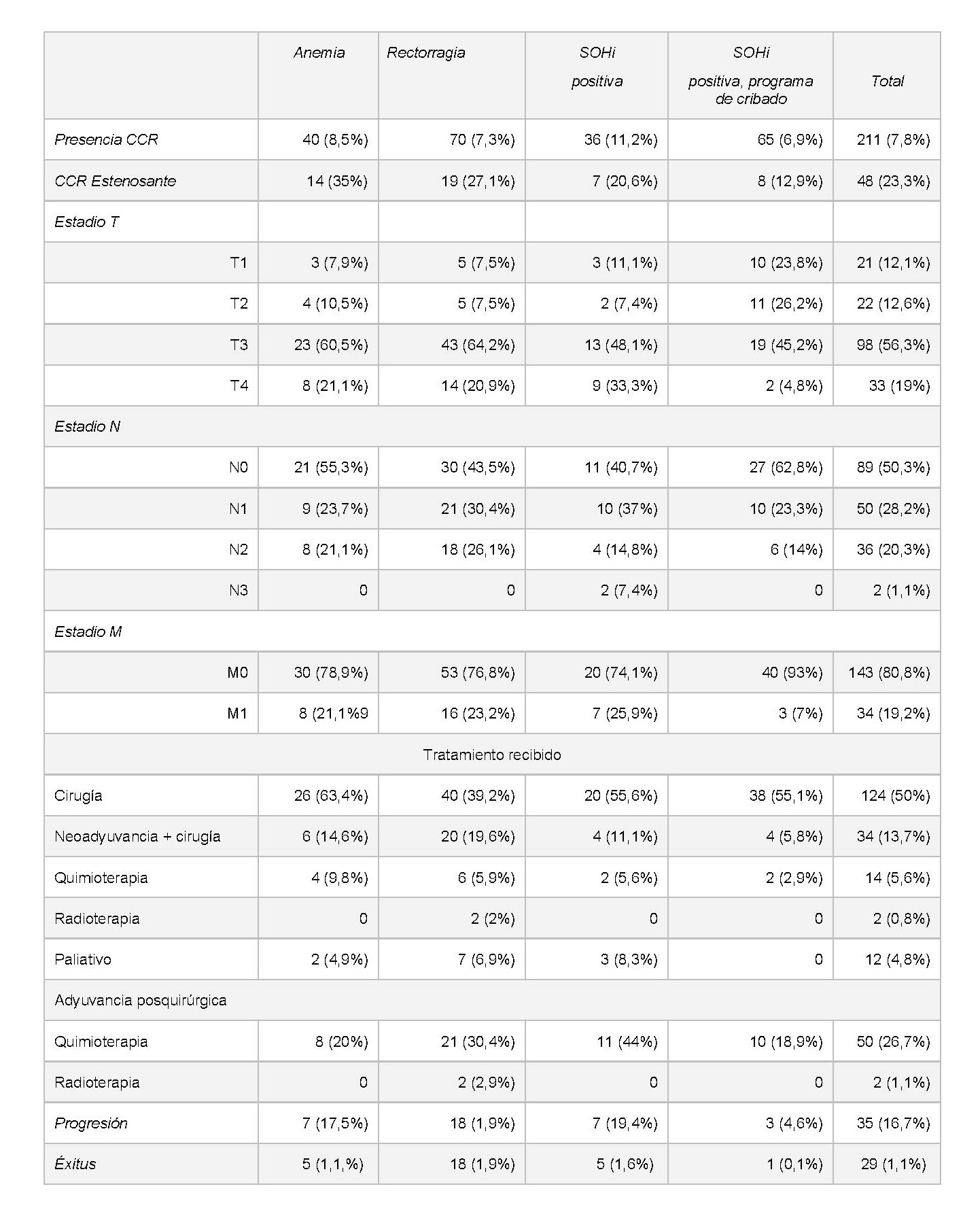
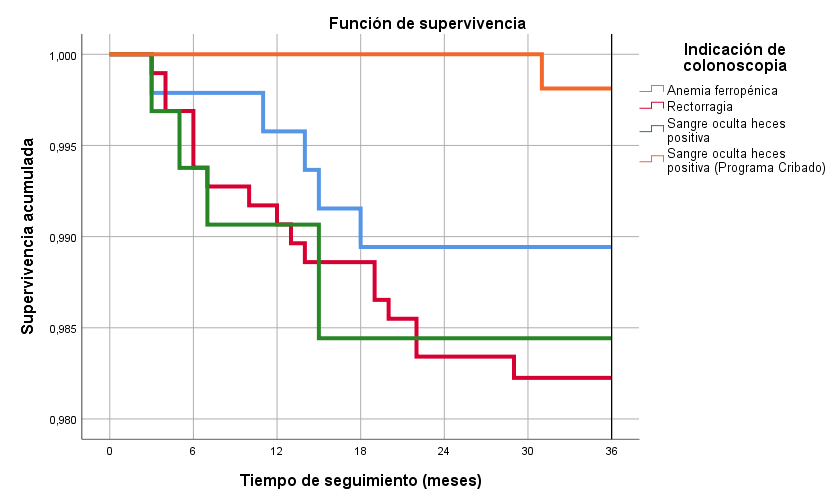
La indicación más frecuente de colonoscopia (35,8%%) fue rectorragia, seguida de SOHi positiva dentro de programa de cribado, anemia ferropénica y SOHi positiva fuera del programa de cribado (tabla 1). La colonoscopia realizada dentro del programa de cribado poblacional se asoció a un aumento de detección de lesiones precursoras de CCR (tabla 2, X2=296,43; p< 0,001), así como a un estadio más precoz en caso de diagnóstico de CCR (tabla 3, X2=21,03; p=0,019), siendo factor protector de mortalidad; al encontrarse menor tasa de enfermedad metastásica (X2=5,476; p= 0,019) y mortalidad (X2=12,656; p<0,001). El resultado positivo del test de SOHi realizado fuera del programa de cribado poblacional se asoció a un aumento de incidencia de CCR (X2=5,79; p= 0,016). La indicación por signos de alarma detectó una mayor tasa de CCR en estadio IV, con el consiguiente peor pronóstico (figura 1).
Tabla 1.
Características basales de los pacientes según la indicación de realización de colonoscopia.
CO-08. COMPARACIÓN DE ESTRATEGIAS DE CRIBADO EN UNA COHORTE DE FAMILIARES DE PRIMER GRADO DE PACIENTES CON CÁNCER COLORRECTAL
Puente Gutiérrez JJ1, Fernández Suárez A2, Marín Moreno MA1, Domínguez Jiménez JL1, López Lario B1, Chicano Gallardo M3, Gonzalez Cosano VM3, Diaz Iglesias JM4
1Servicio Aparato Digestivo. Hospital Alto Guadalquivir, Andújar. 2Servicio Análisis Clínico. Hospital Alto Guadalquivir, Andújar. 3Servicio Aparato Digestivo. Hospital de Montilla, Montilla. 4Servicio Anatomía Patológica. Hospital Alto Guadalquivir, Andújar.
Palabras clave: cáncer colorrectal, cribado, familiar.
Introducción
Hay pocas evidencias sobre resultados tras la aplicación de las guías de práctica clínica (GPC) de cribado en familiares de primer grado (FPG) de pacientes con cáncer colorrectal (CCR) sin síndromes hereditarios, que recomiendan colonoscopia en los casos de mayor riesgo y cribado poblacional en el resto.
Evaluar la eficacia diagnóstica de las principales GPC para detectar neoplasia avanzada (NA). Estimar el consumo de recursos que conllevan. Evaluar el impacto del descenso en los umbrales de edad y hemoglobina fecal (HbF).
Material y métodos
Estudio transversal sobre una cohorte prospectiva de FPG en la que se realizó colonoscopia y test de sangre oculta en heces (TSOH, umbral HbF=20g/g). La variable principal fue la presencia de NA (cáncer/adenoma/pólipo serrado ≥10mm o displasia alto grado o ≥5 adenomas). Se compararon los hallazgos tras aplicar las recomendaciones American College Gastroenterology-2021 (ACG), British Society Gastroenterology-2020 (BSG), European Society Gastrointestinal Endoscopy-2019 (ESGE) y Asociación Española Gastroenterología-2018 (AEG), (tabla 1). Se calculó sensibilidad, valor predictivo negativo/positivo (VPN/VPP), número de colonoscopias realizadas y coste (€/NA detectada).
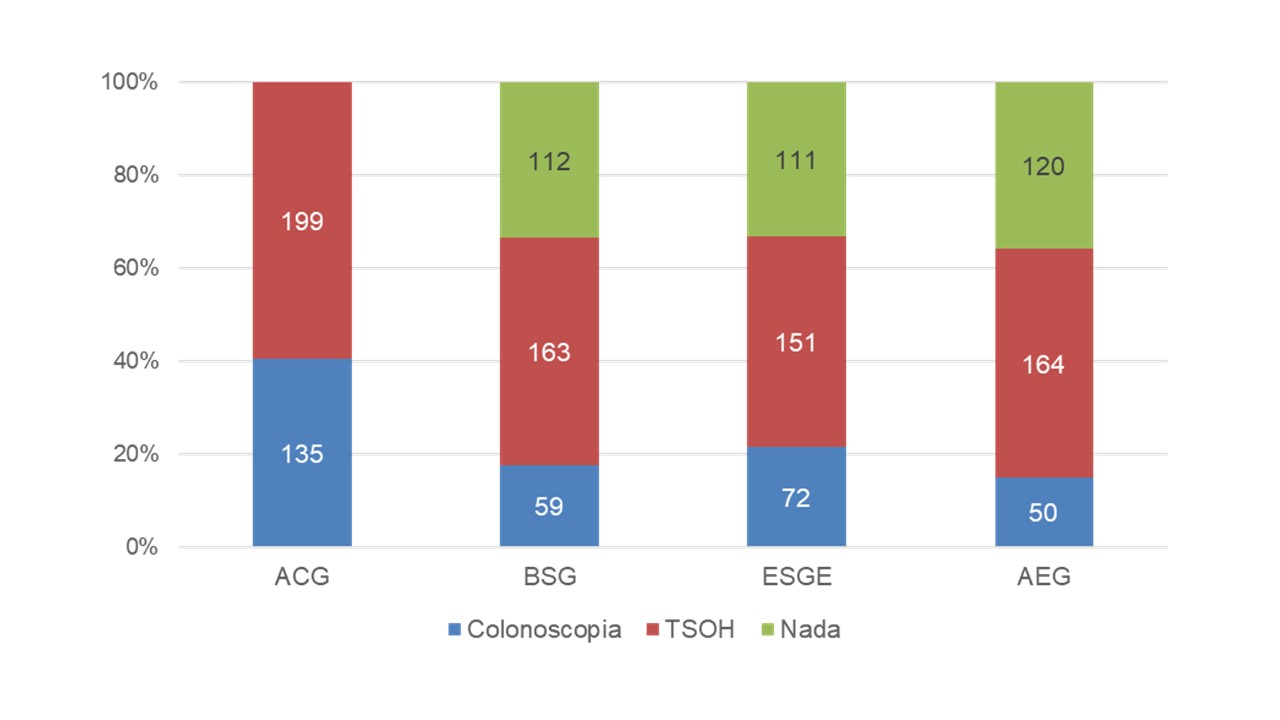
Figura 1
Distribución de pruebas de cribado asignadas (colonoscopia, TSOH, nada †) tras aplicar las recomendaciones de las guías. † Indicación de no cribado por estar por debajo de la edad de inicio del cribado poblacional (50 años).
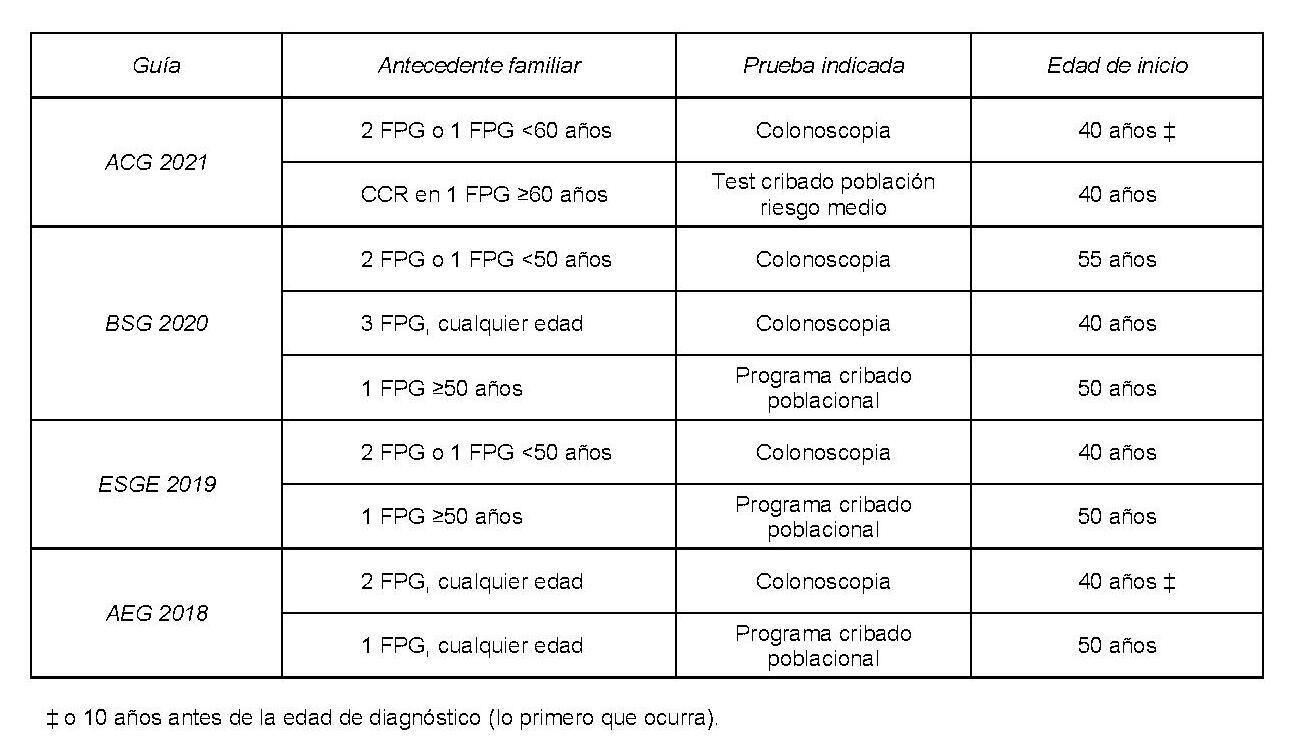
Tabla 1
Resumen de recomendaciones de cribado en caso de antecedente familiar de CCR (excluidos los síndromes hereditarios).
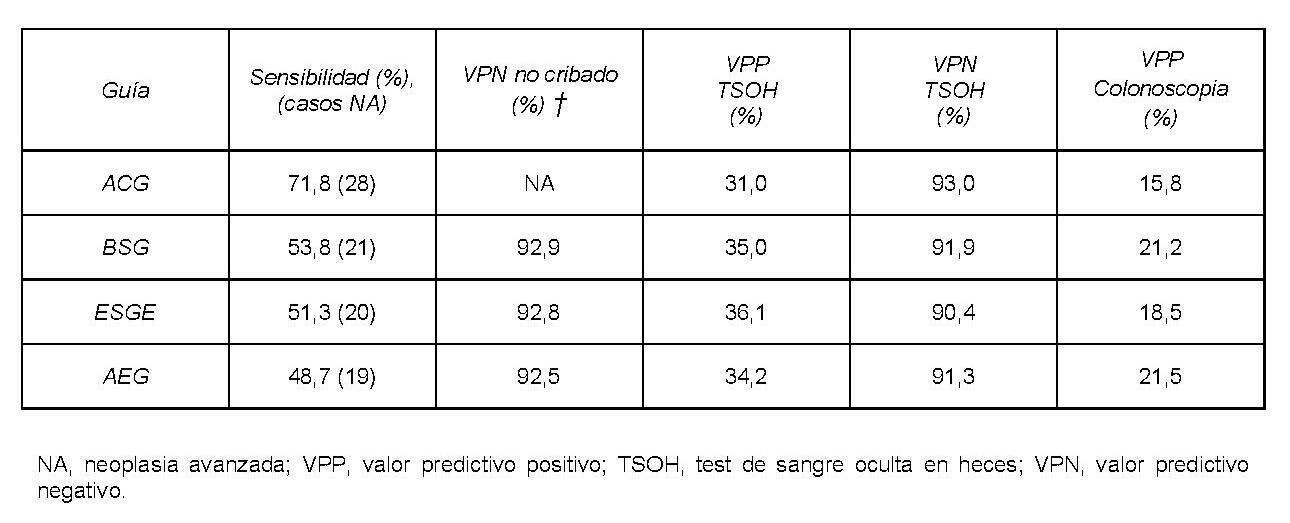
Tabla 2
Sensibilidad, VPP/VPN del TSOH (umbral HbF 20µg/g heces), VPP de la colonoscopia, y VPN de la no aplicación de medidas de cribado (†), (n=334; NA=39). † por estar por debajo de la edad de inicio del cribado poblacional (50 años).
Resultados
Se incluyeron 334 individuos (194 mujeres) con edad promedio 52,6 (rango 32-75); 72 (21,5%) tenían ≥2 FPG con CCR o uno <50 años. La colonoscopia detectó NA en 39 (11,7%): 4 adenocarcinomas, 8 displasia alto grado y 27 adenomas ≥10mm.
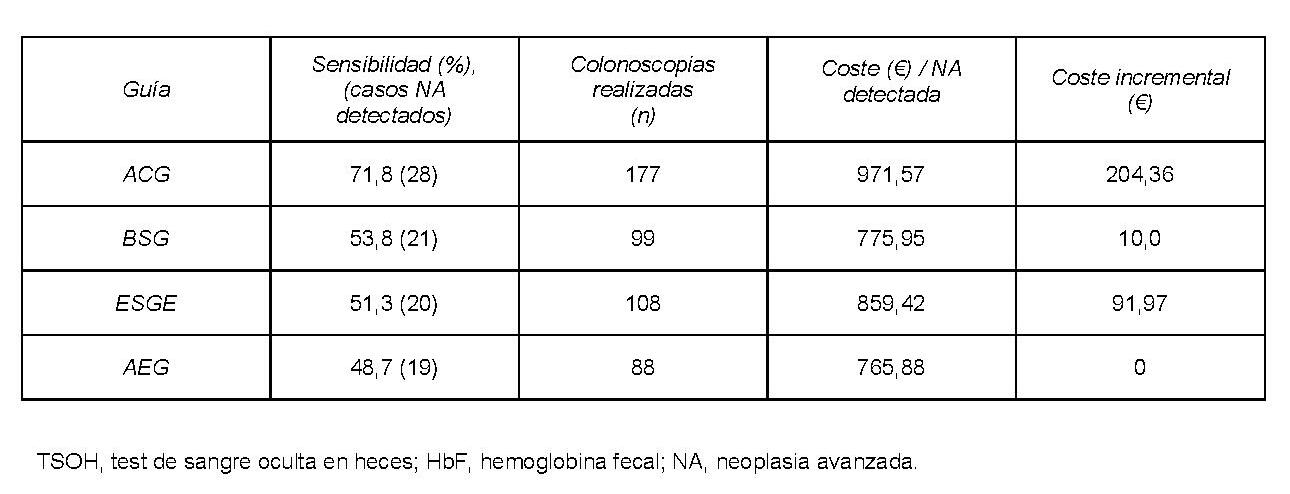
La distribución de pruebas diagnósticas según la GPC utilizada se detalla en la figura 1. La estrategia ACG fue la más sensible (71,8%, p=0.002), por encima de las europeas (48.7%-53,8%) (tabla 2). El VPN de la no indicación de cribado fue 92,5-92,9% y el del TSOH 90,4-93,05%. La guía ACG implicó realizar más colonoscopias que en el resto (ACG, 177; BSG, 99; ESGE, 108; AEG, 88), a un coste 971,57€/NA, 204,36€ más que la estrategia más barata (AEG) (tabla 3).
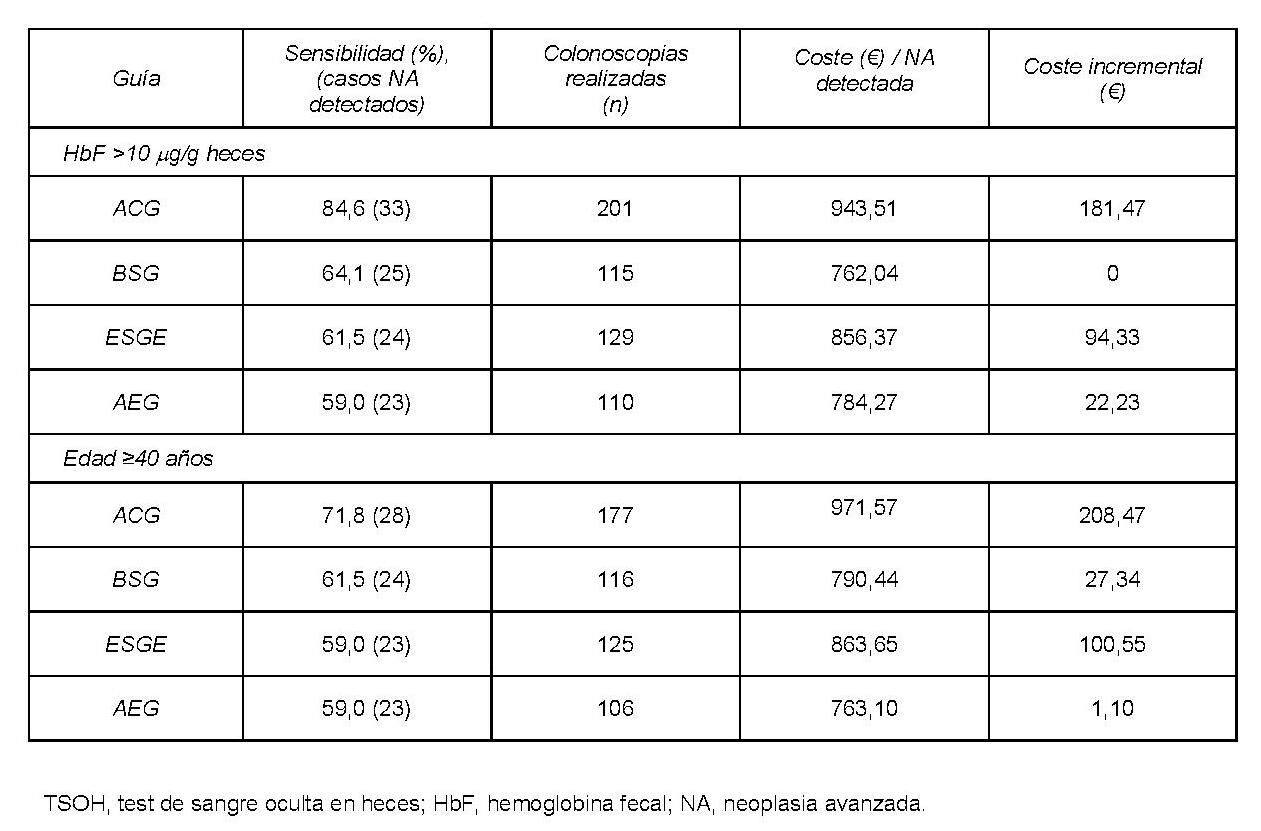
Un menor umbral de HbF (10g/g) aumentó la sensibilidad (ACG, 84,6%; BSC, 64,1%; ESGE, 61,5%; AEG, 59,0%) y el número de colonoscopias realizadas, aunque a un coste similar. La disminución de la edad de inicio de cribado con TSOH a 40 años obtuvo resultados similares (tabla 4).
Conclusiones
Las guías europeas apenas alcanzaron una sensibilidad del 50%. La GPC más sensible fue la ACG, dado un mayor uso de la colonoscopia y la ausencia de población no cribada, pero a un coste mayor; aun así, no superó el 72%. La reducción del umbral de HbF o de la edad de inicio del cribado pueden ser estrategias válidas para mejorar la sensibilidad a un coste aceptable.
CO-09. EFECTIVIDAD Y SEGURIDAD DE USTEKINUMAB EN ENFERMEDAD DE CROHN EN PACIENTES BIONAIVE: UN ESTUDIO MULTICÉNTRICO
VALDES DELGADO T1, ARGÜELLES ARIAS F1, IBORRA M2, HERRERA DE GUISÉ C3, FUENTES VALENZUELA E4, MELCARNE L5, MARTIN RODRIGUEZ MM6, KOLLE CASSO L7, DE CASTRO PARGA L8, PONFERRADA DIAZ A9, VICENTE LIDON R10, MANCEÑIDO MARCOS N11, VELAYOS JIMENEZ B12, LAZARO SAEZ M13, LOPEZ CAUCE B14, MESONERO GISMERO F15, GILABERT ALVAREZ P16, OLMEDO MARTIN R17
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla. 2UGC Aparato Digestivo. Hospital Universitari I Politècnic la Fe, Valencia. 3UGC Aparato Digestivo. Hospital Universitari Vall D'hebron, Barcelona. 4UGC Aparato Digestivo. Hospital Universitario Rio Hortega, Valladolid. 5UGC Aparato Digestivo. Hospital de Sabadell, Sabadell. 6UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada. 7UGC Aparato Digestivo. Hospital General de la Palma, Breña Alta. 8UGC Aparato Digestivo. Complexo Hospitalario Universitario de Vigo, Vigo. 9UGC Aparato Digestivo. Hospital Universitario Infanta Leonor, Madrid. 10UGC Aparato Digestivo. Hospital Universitario Miguel Servet, Zaragoza. 11UGC Aparato Digestivo. Hospital Universitario Infanta Sofía, San Sebastián de los Reyes. 12UGC Aparato Digestivo. Hospital Clínico Universitario de Valladolid, Valladolid. 13UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería. 14UGC Aparato Digestivo. Complejo Hospitalario Gregorio Marañón, Madrid. 15UGC Aparato Digestivo. Hospital Ramón y Cajal, Madrid. 16UGC Aparato Digestivo. Hospital de Viladecans, Viladecans. 17UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: ustekinumab, bionaive, efectividad y seguridad, .
Introducción
Evaluar efectividad y seguridad de ustekinumab en pacientes con enfermedad de Crohn (EC) sin exposición previa a tratamiento biológico.
Material y métodos
Estudio observacional, retrospectivo y multicéntrico nacional constituido por pacientes con EC activa moderada-grave en los que se han empleado ustekinumab como primer biológico.
Se analizó la respuesta y remisión tanto clínica como biológica libre de esteroides a las semanas 16, 24, 52 y 72.
Se definió remisión clínica como índice de Harvey-Bradshaw (IHB)<4 y remisión biológica combinada como calprotectina fecal (CF) <250 mg/g y proteína C reactiva (PCR)<5 mg/L.
Además, se evaluó la persistencia del tratamiento y la aparición de efectos adversos.
Resultados
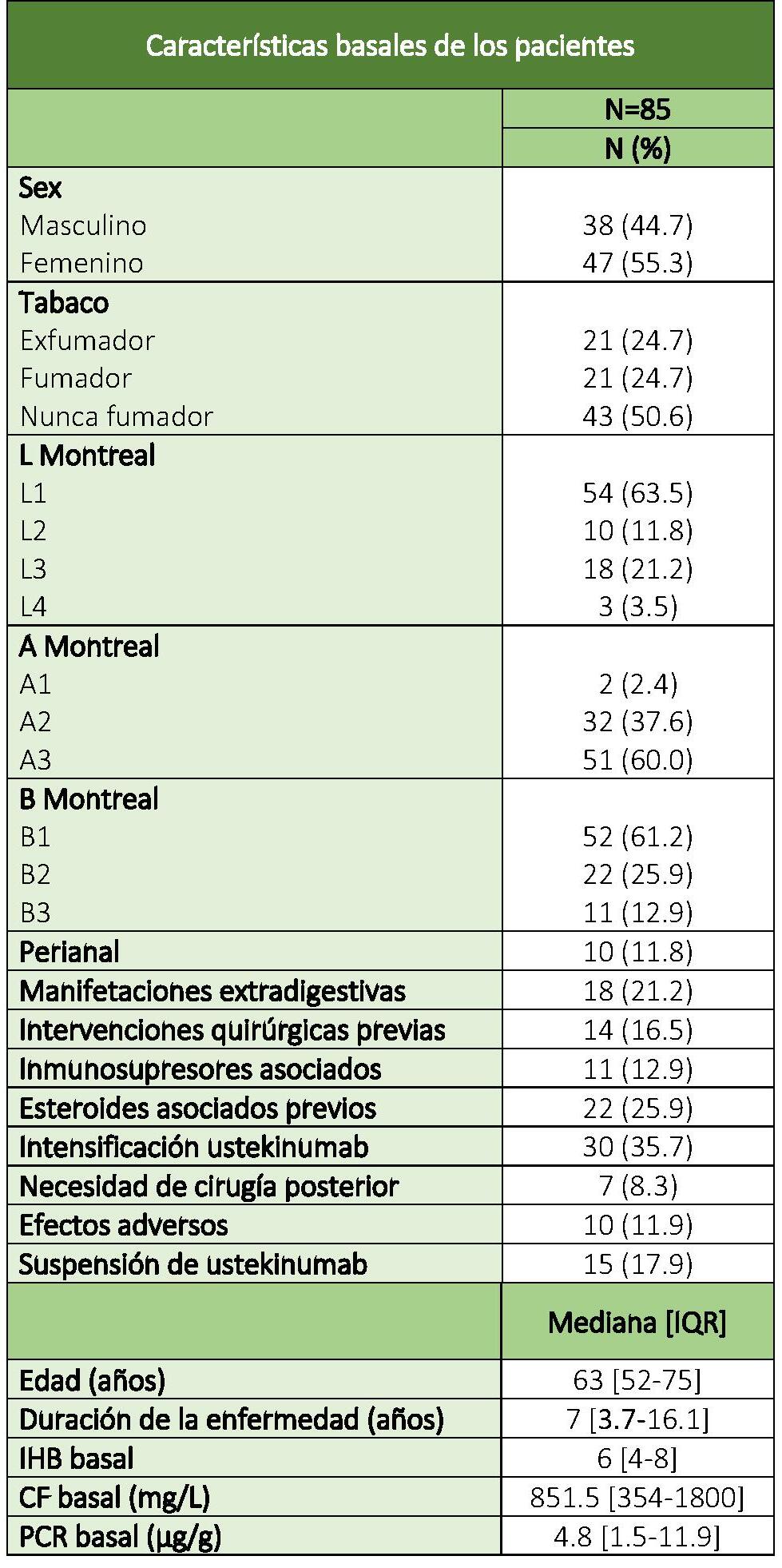
Se incluyeron 85 pacientes. 55.3% (47/85) eran mujeres con edad media de 61±17.5 años. La media de años de evolución de la enfermedad fue de 10±10 años. 61.2% (52/85) presentaban patrón inflamatorio, 63.5% (54/85) localización ileal y 11.8% (10/85) afectación perianal. 21.8% (18/85) presentaban manifestaciones extradigestivas, la más frecuente osteoarticulares. 12.9% (11/85) tenían inmunosupresores asociados y 25.9% (22/85) estaban previamente con esteroides, de los cuales 90.9% (20/22) lo interrumpieron por remisión libre de esteroides (tabla 1).
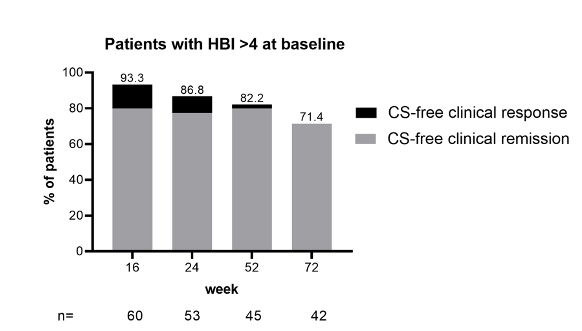
La proporción de pacientes en remisión o respuesta clínica libre de corticosteroides a las semanas 16, 24, 52 y 72 fue 93,3% (56/60), 86,8% (46/53), 82,2% (37/45) y 71,4% (30/42 ) respectivamente (Figura 1).
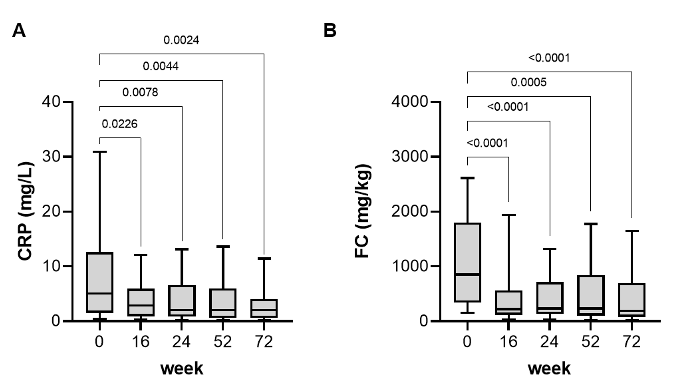
La mediana de la concentración de PCR en las semanas 0, 16, 24, 52 y 72 fue de 5,1 mg/L [IQR 1,5–12,6], 2,9 mg/L [IQR 0,9–5,9], 2,0 mg/L [IQR 0,86–6,6], 2,0 mg/L [IQR 0,7–6,0] y 2,0 mg/L [IQR 0,6–4,0], respectivamente (Figura 2A). La mediana del nivel de FC en las semanas 0, 16, 24, 52 y 72 fue de 851,5 mg/kg [IQR 341,3–1800,0], 223 mg/kg [IQR 115,5–565,0], 231 mg/kg [IQR 139,0–714,5], 233,5 mg/kg [IQR 103,5–841,3] y 191,5 mg/kg [IQR 83,25–698,2], respectivamente (Figura 2B).
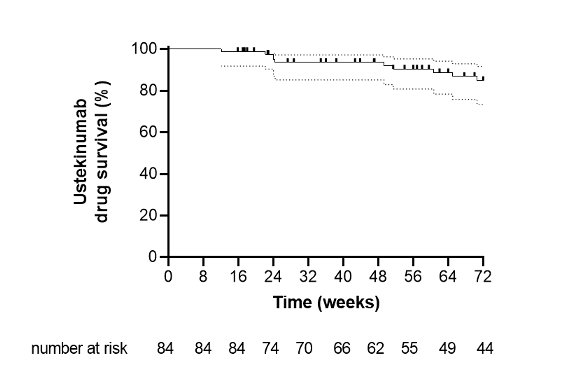
La probabilidad acumulada de permanecer en tratamiento con ustekinumab al final del seguimiento (semana 72) fue del 84,8% (IC 95%: 73,3-91,6) (Figura 3). Unicamente se observaron 4 efectos adversos que conllevó a la suspensión del fármaco.
CO-10. INFLUENCIA DE LOS INHIBIDORES DE LA BOMBA DE PROTONES EN EL “ACUTE-ON-CHRONIC LIVER FAILURE”: ANÁLISIS PRELIMINAR DEL ESTUDIO MULTICÉNTRICO ANDALUZ
García Gavilán MC1, Guerrero Misas M2, García García A3, Casado Martin M4, Castillo Molina L5, Sánchez Torrijos Y6, Sendra C7, Rosales Zábal JM1
1Servicio Aparato Digestivo. Complejo Hospital Costa del Sol, Marbella. 2Servicio Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba. 3Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Virgen de la Victoria, Málaga. 4Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería. 5Servicio Aparato Digestivo. Complejo Hospitalario de Jaén, Jaén. 6Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 7Servicio Aparato Digestivo. Hospital Comarcal Infanta Elena, Huelva.
Palabras clave: inhibidores de la bomba de protones, ibp, aclf.
Introducción
Analizar la posible asociación entre la toma crónica de inhibidores de la bomba de protones (IBP) y el desarrollo de un “Acute-on-chronic liver failure” (ACLF).
Material y métodos
Estudio de cohortes multicéntrico andaluz de 7 hospitales, donde se incluyen todos los pacientes que ingresan con ACLF y se clasifican como grupo expuesto o no expuesto, según la toma crónica de IBP. Se excluyeron aquellos con diagnóstico previo de hepatocarcinoma, inmunosupresión, cirugía del tracto digestivo y toma de IBP<3 meses. Al ingreso se valora el consumo crónico de IBP y tipo de IBP, el consumo de Norfloxacino, Rifaximina, Lactulosa, estatinas y antiagregación. Se determinó el score CLIF-C-OF y CLIF-C-ACLF al ingreso, CLIF-C-ACLF a los 3 días y 7 días, CHILD, MELD-Na y tipo de descompensación. Posteriormente se registran los ingresos en la unidad de cuidados críticos (UCI), los nuevos ingresos por ACLF y la mortalidad a los 28 días, 3 meses y 6 meses del episodio. Además, se recogieron variables analíticas de función hepática, renal y hematológica.
Resultados
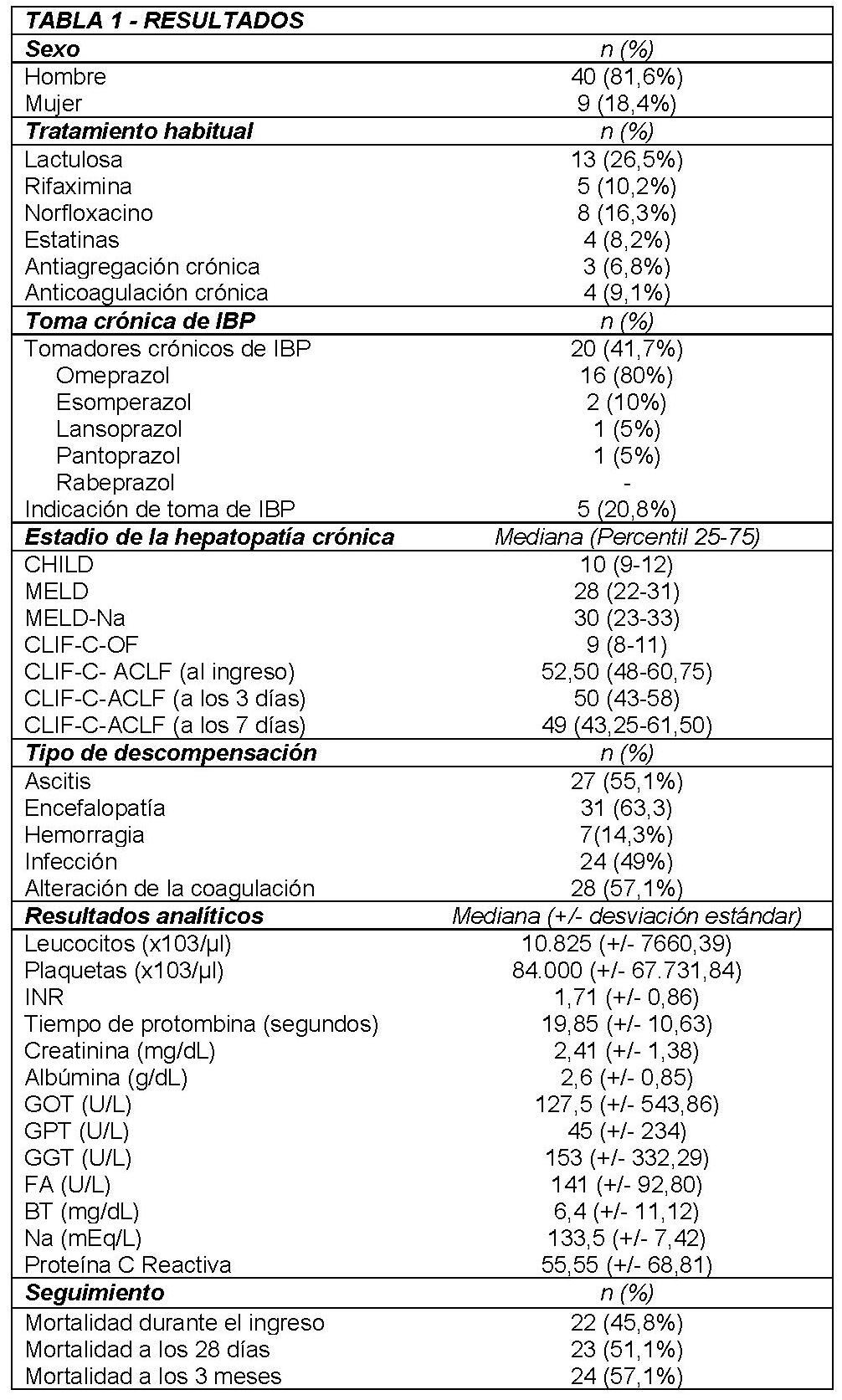
Se incluyeron 49 pacientes (mediana de edad de 59 años), 20 consumidores crónicos de IBP, 28 no consumidores. El 26,5% tomadores crónicos de Lactulosa, 10,2% Rifaximina, 16,3% Norfloxacino, 8,6% estatinas y 6,1% con antiagregación crónica. Al ingreso con una mediana de CLIF-C-OF de 1, CLIF-C-ACLF de 52,50, CHILD de 10 y Meld-Na de 30. El tipo de descompensación más frecuente fue la encefalopatía hepática, seguida de la coagulopatía y la descompensación hidrópica (63,3%, 57,1% y 55,1% respectivamente). En el 49% de los casos en presencia de una infección, siendo las más frecuentes, la infección respiratoria en el 20% y peritonitis bacteriana espontánea en el 18%. El 45,8% fallece durante el ingreso y solo el 14,3% de los casos ingresó en UCI (tabla 1). Al analizar nuestra muestra, el grupo tomador crónico de IBP fue similar al grupo no tomador, no encontrándose inicialmente relación con la gravedad del ACLF (p=0,85 para el CLIF-C-OF y p0,49 para el CLIF-C-ACLF) ni con la mortalidad durante el ingreso (p=1,00), a los 28 días (p=0,89) ni a los 3 meses (p=1,00). Encontramos una relación estadísticamente significativa con los niveles más elevados de creatinina (p=0,027) y los niveles más bajos de albúmina (p=0,04), aunque sin clara repercusión clínica.

 Descargar número completo
Descargar número completo Download full issue
Download full issue