CP-049. PRESENTACIÓN ATÍPICA EN EL PACIENTE CIRRÓTICO: ASCITIS QUILOSA. A PROPÓSITO DE UN CASO.
Hernani Alvarez JA, García Martínez A, Campos Gonzaba L, León Sanjuan G
Servicio Aparato Digestivo. Hospital de Especialidades de Jerez de la Frontera, Jerez de la Frontera.
Palabras clave: : ascitis quilosa (qa); líquido ascítico (la); hipertensión portal (htp); cirrosis hepática; soporte.
Introducción
La ascitis quilosa (AQ) es una entidad inusual en la cirrosis hepática, con una incidencia entre el 0,5-1%, siendo ésta su segunda causa más frecuente. El mecanismo fisiopatológico está asociado a un aumento del flujo linfático (compuesto fundamentalmente por quilomicrones provenientes del metabolismo de triglicéridos de cadena larga (LCT) y a la disrupción del sistema linfático secundaria a la hipertensión portal (HTP).
Caso clínico
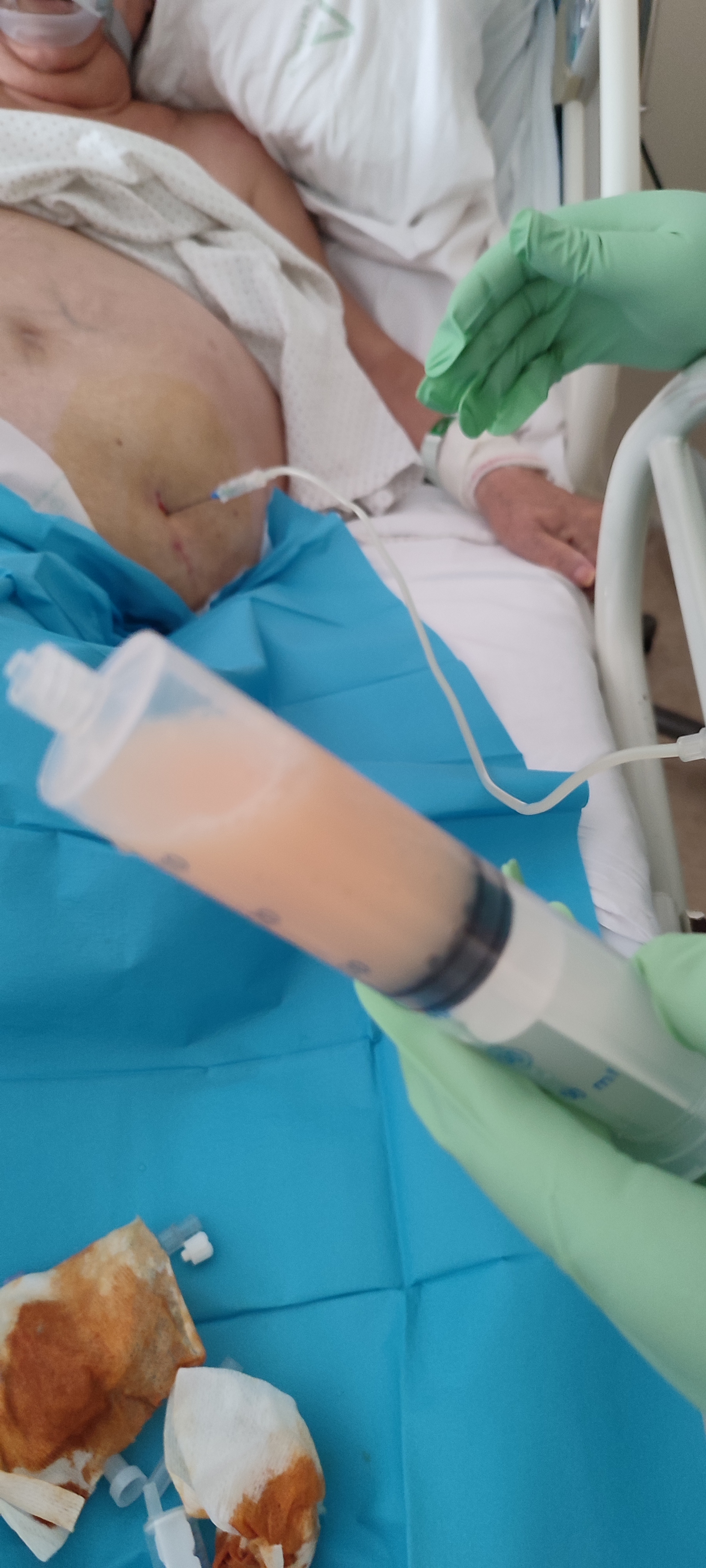
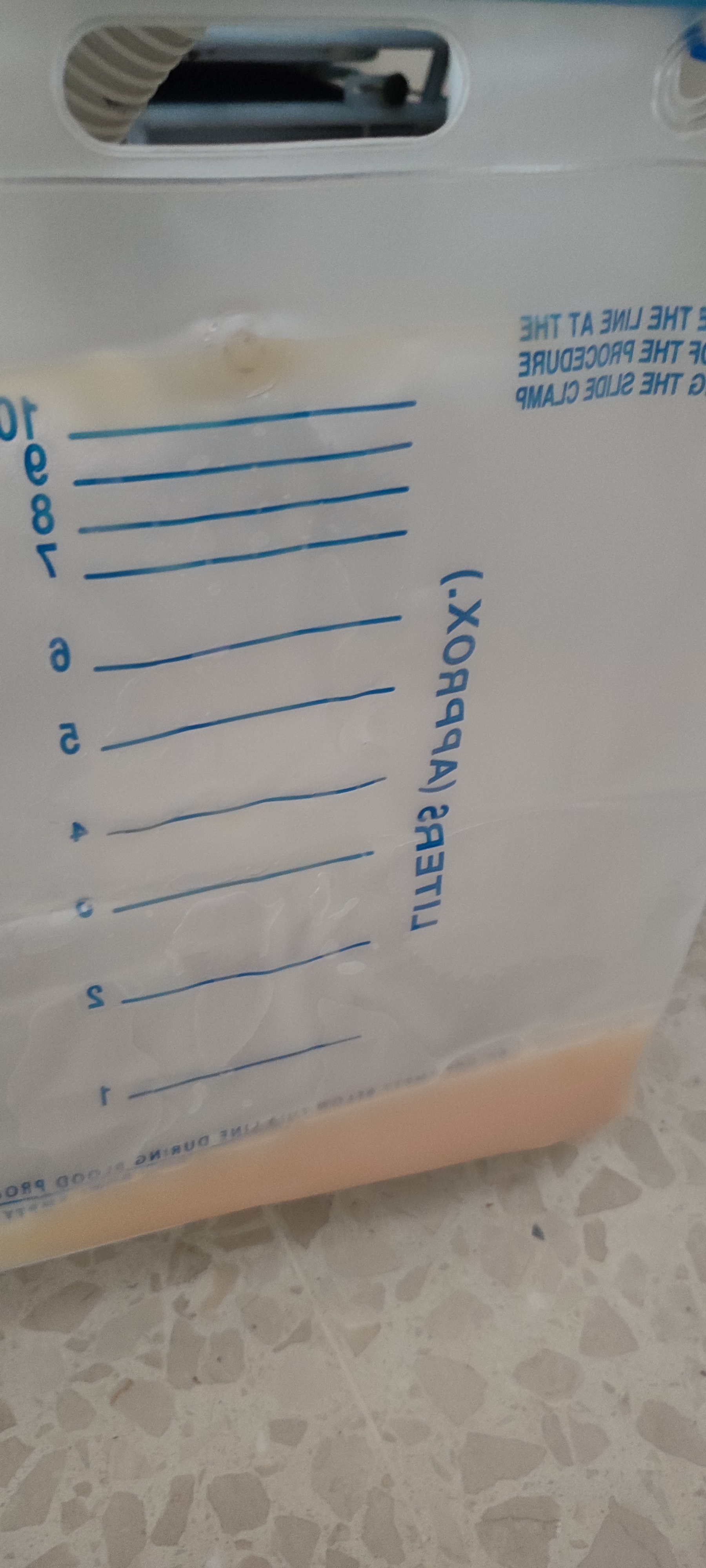
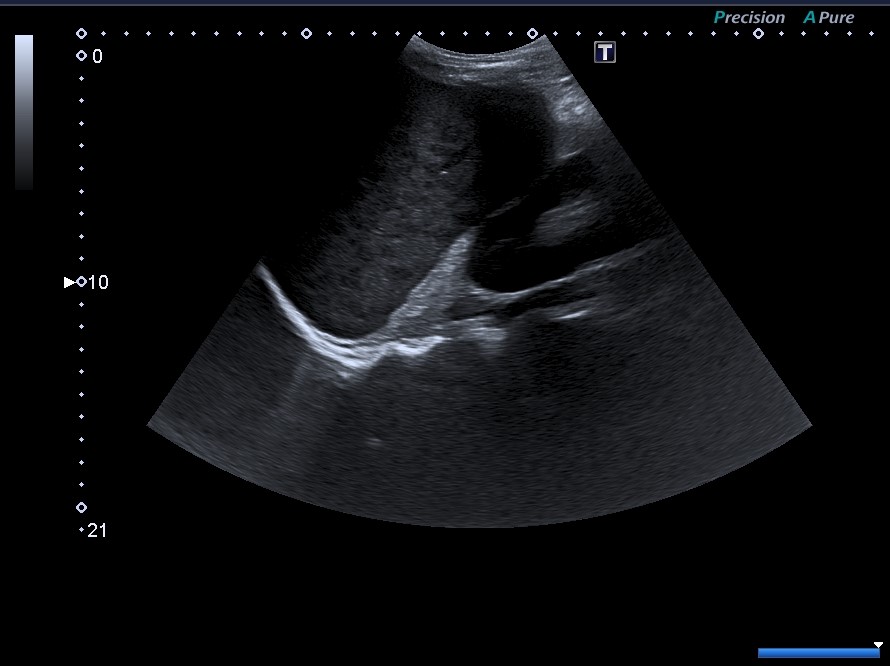
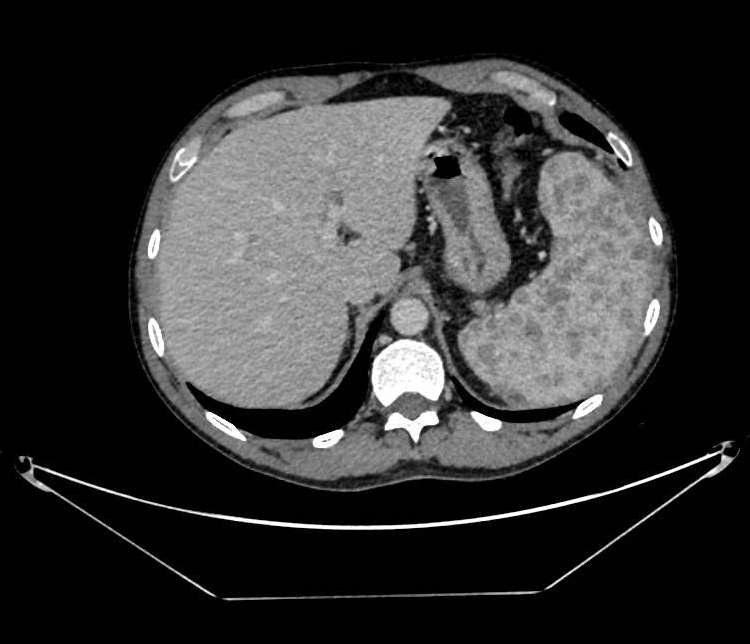
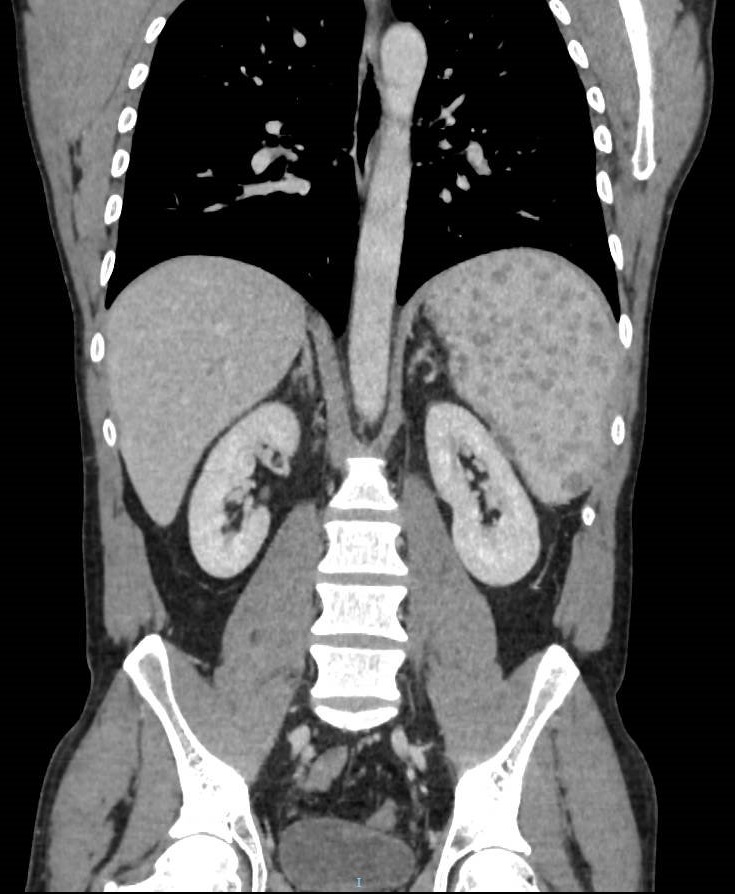
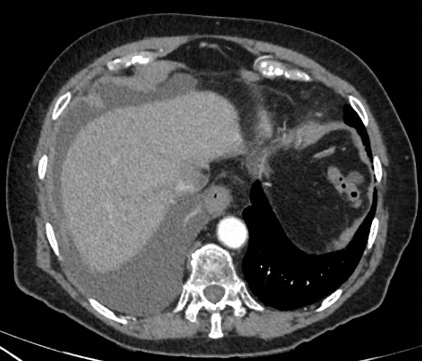
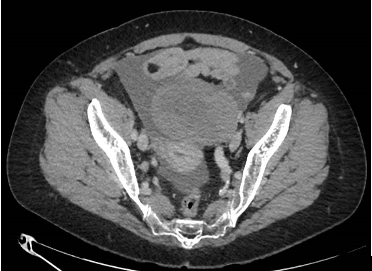
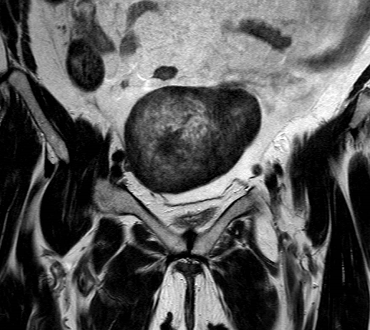
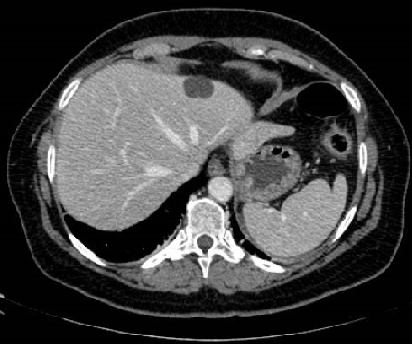
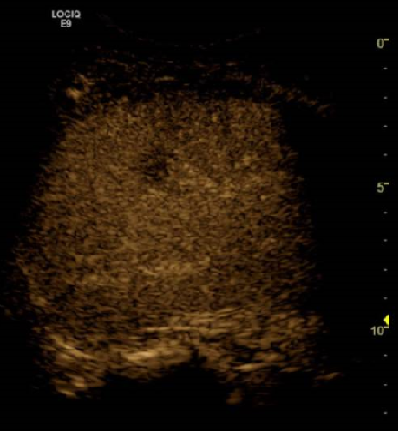
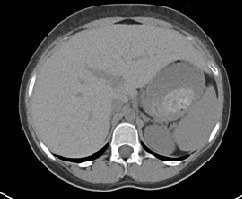
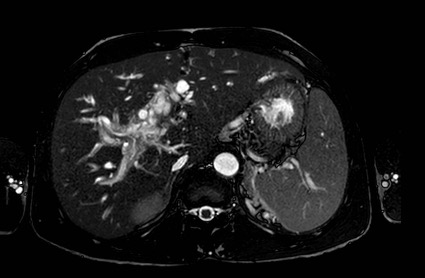
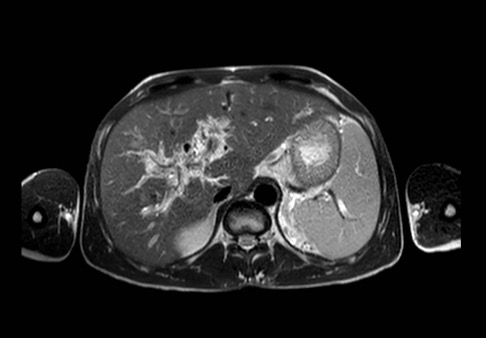
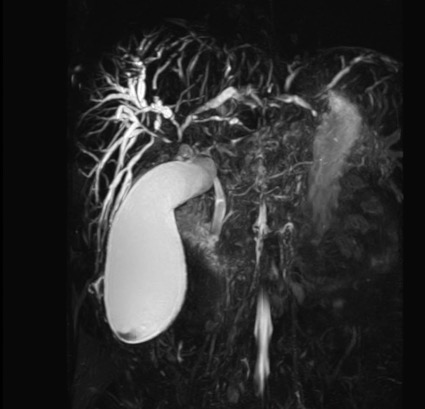
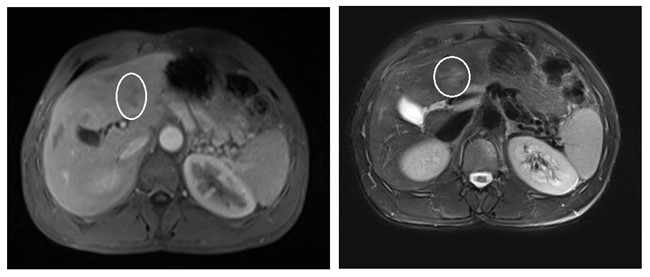
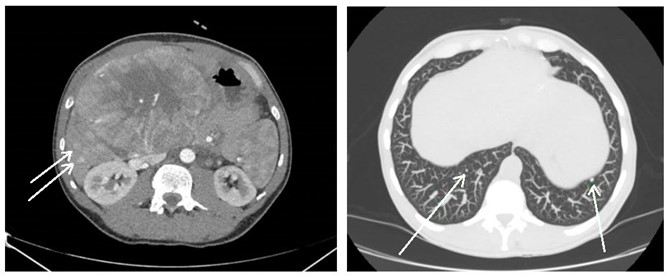
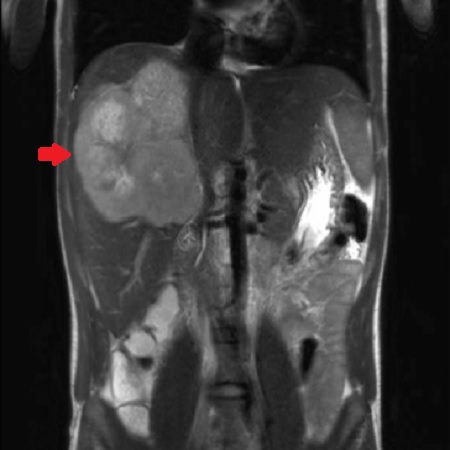
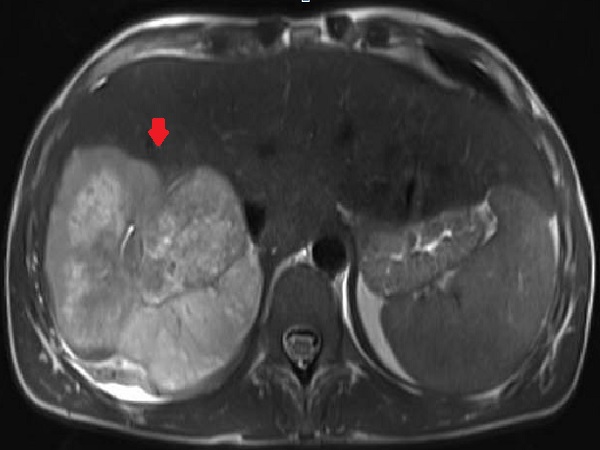
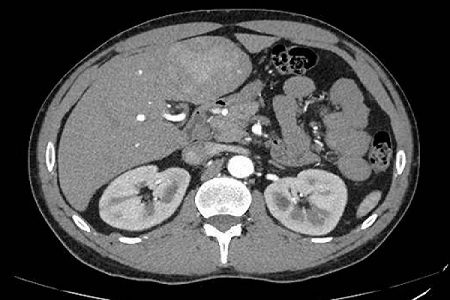
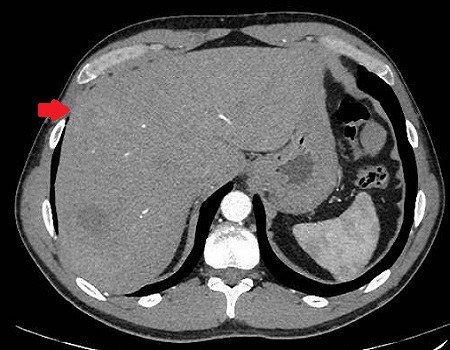
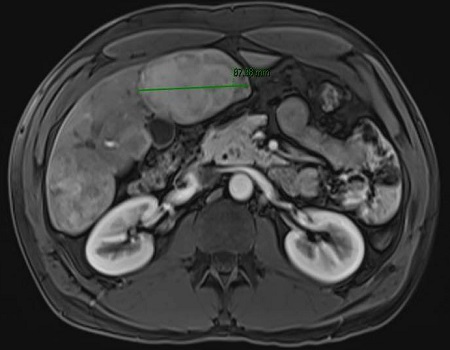
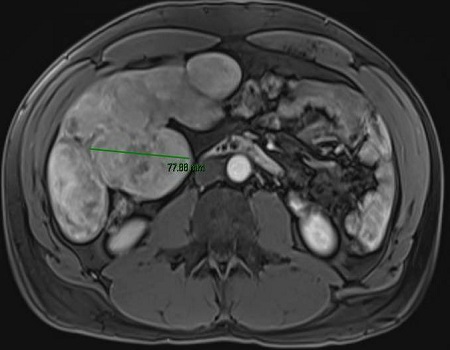
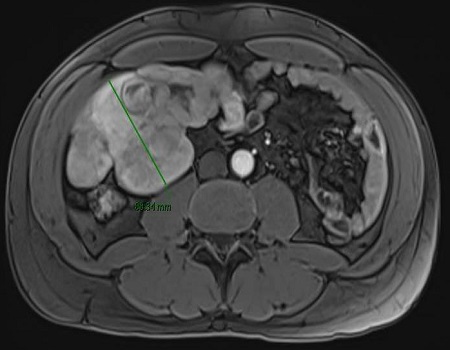
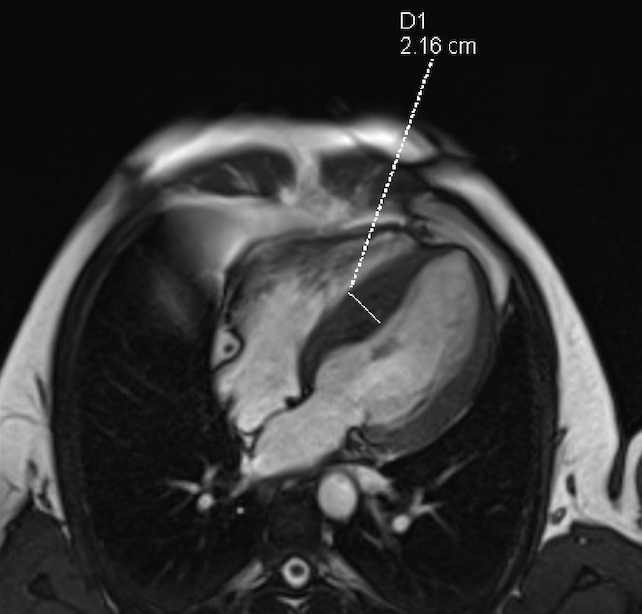
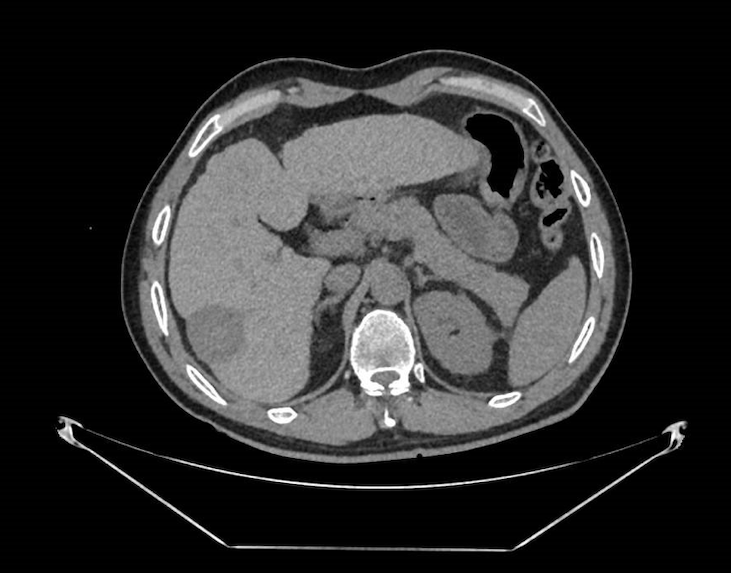
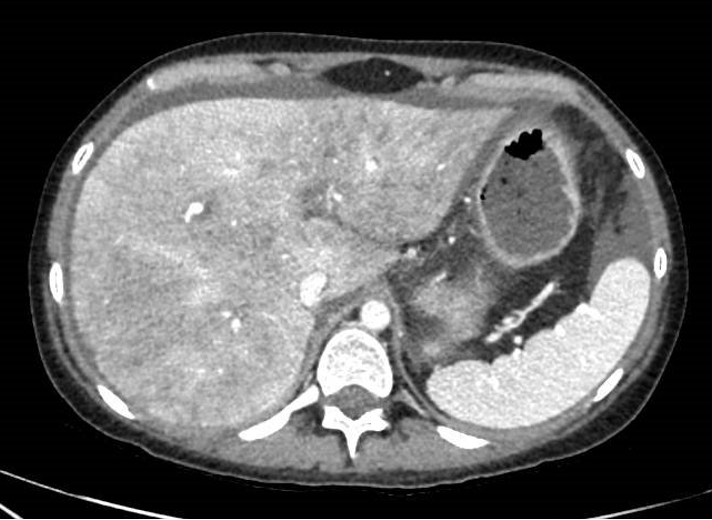
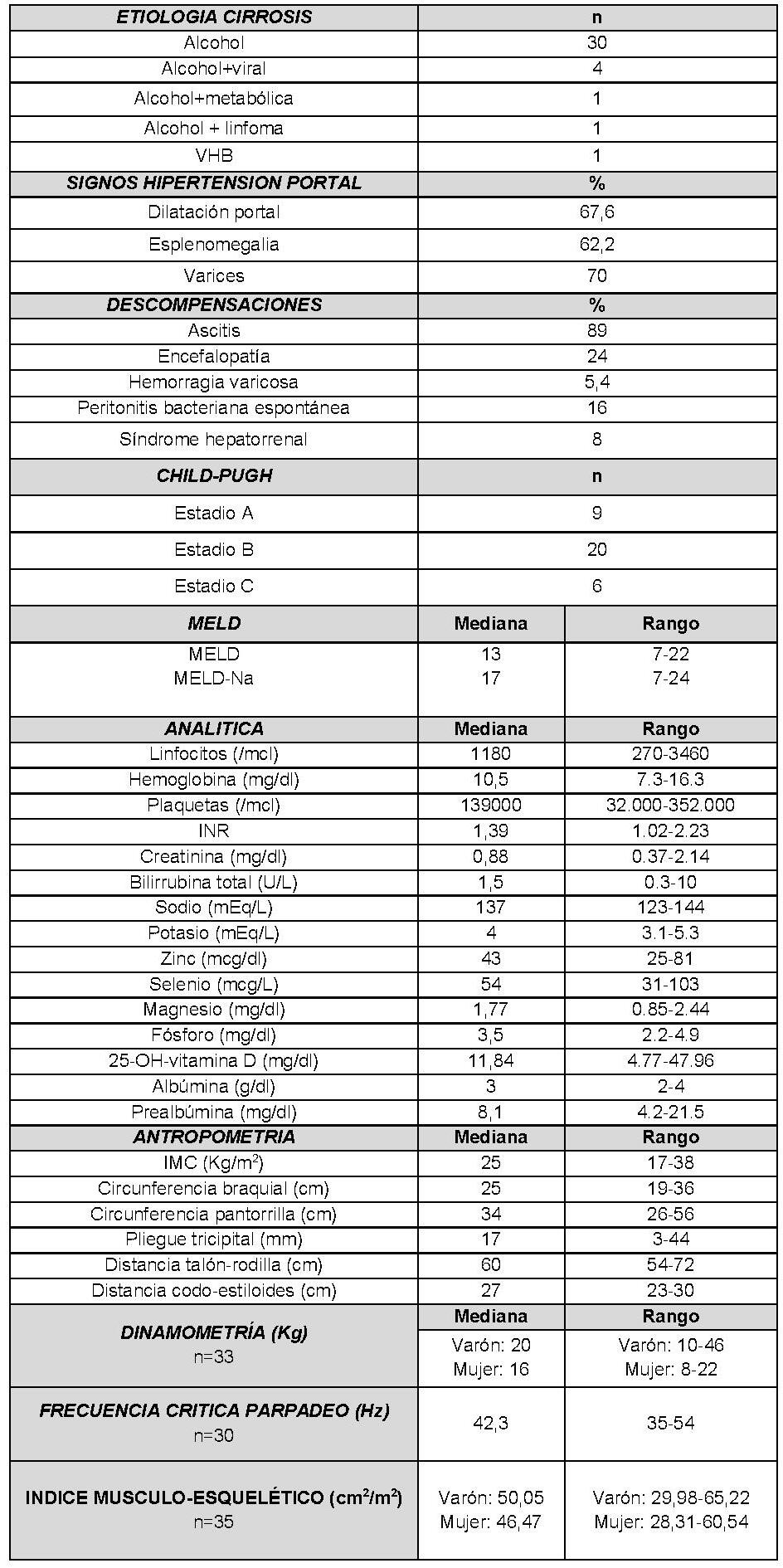
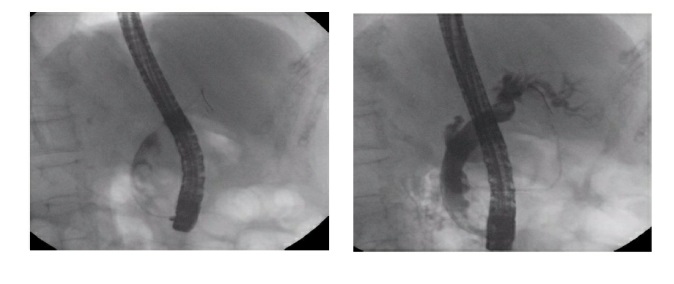
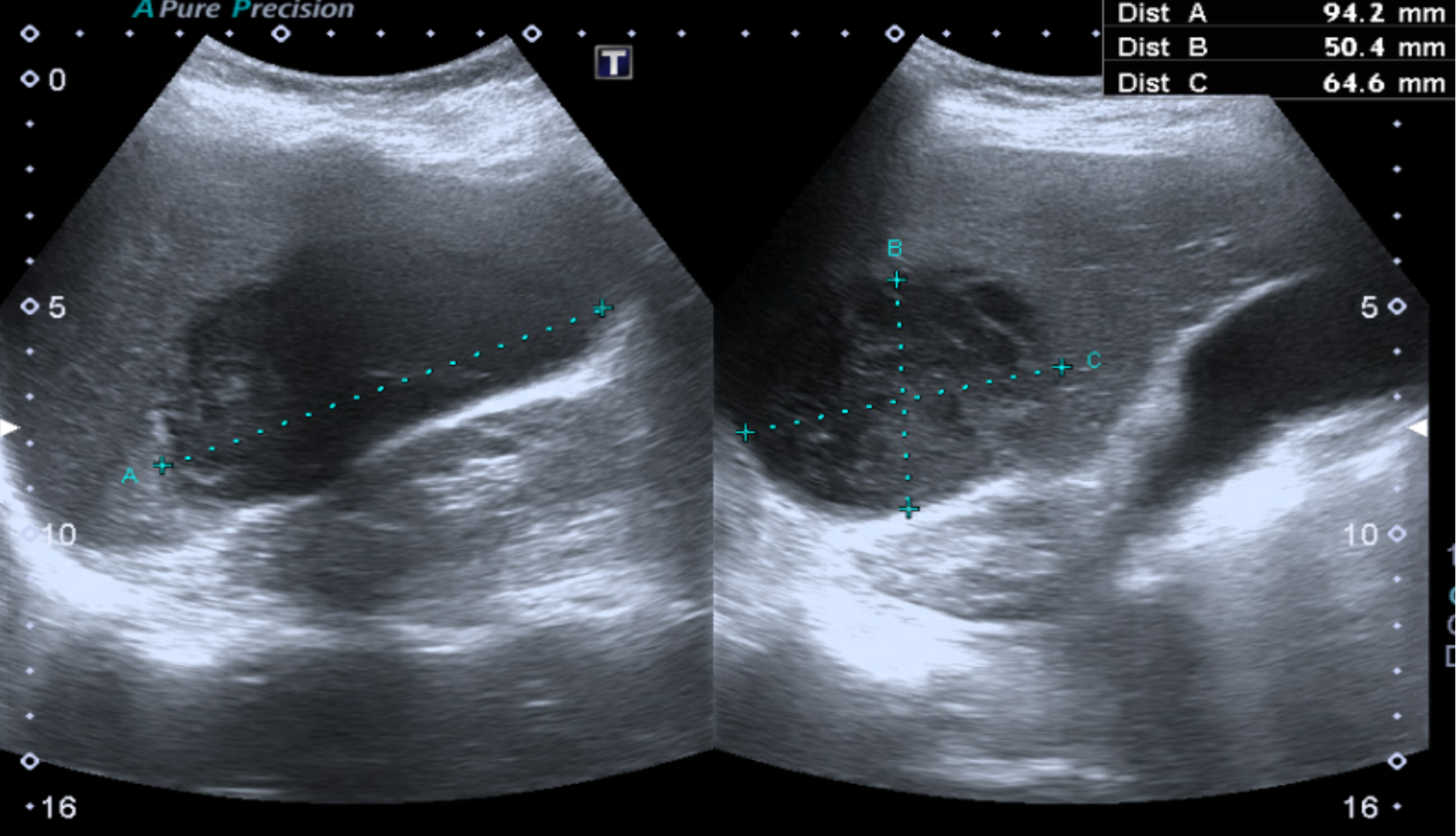
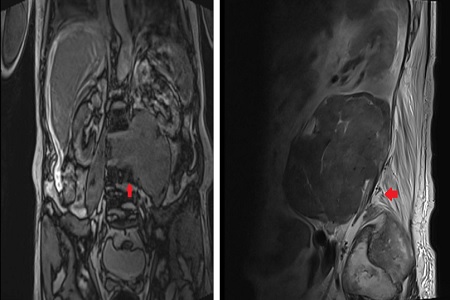
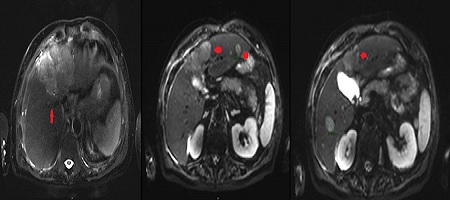
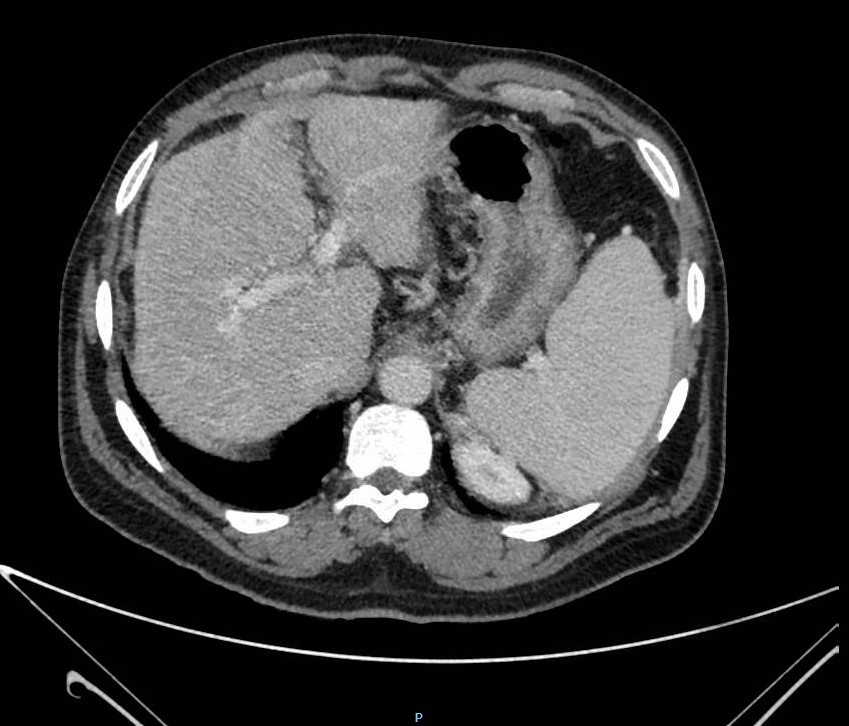
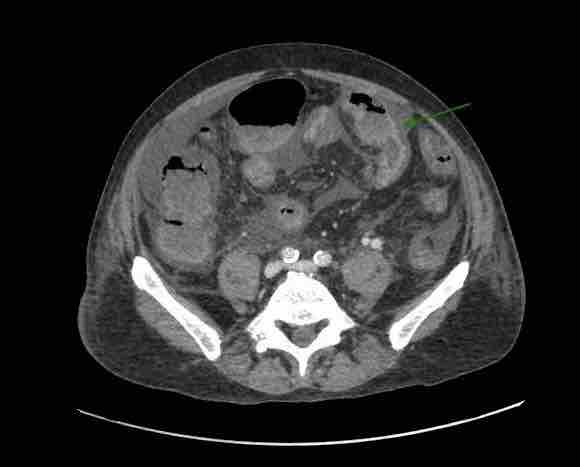
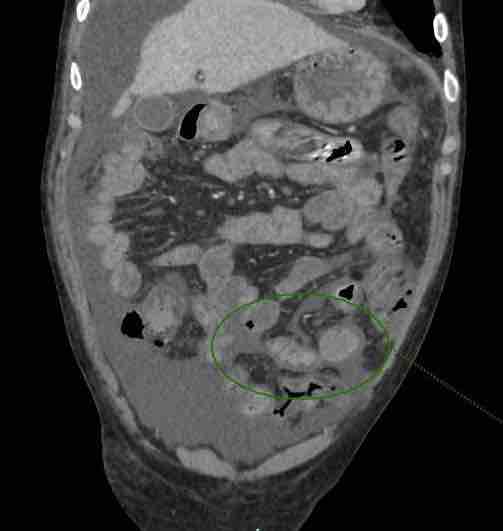
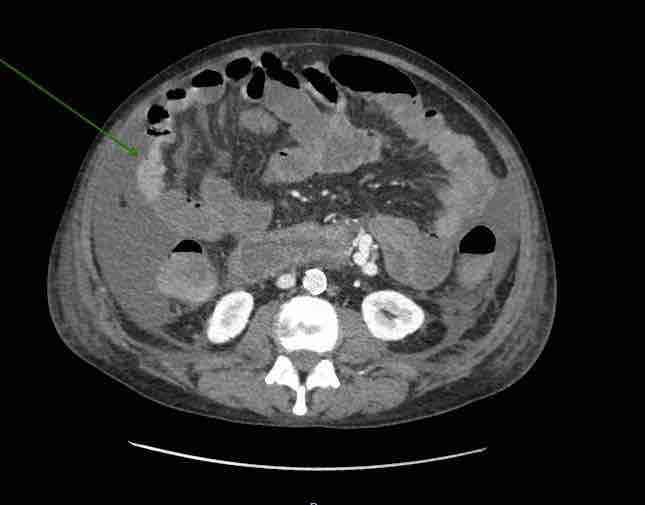
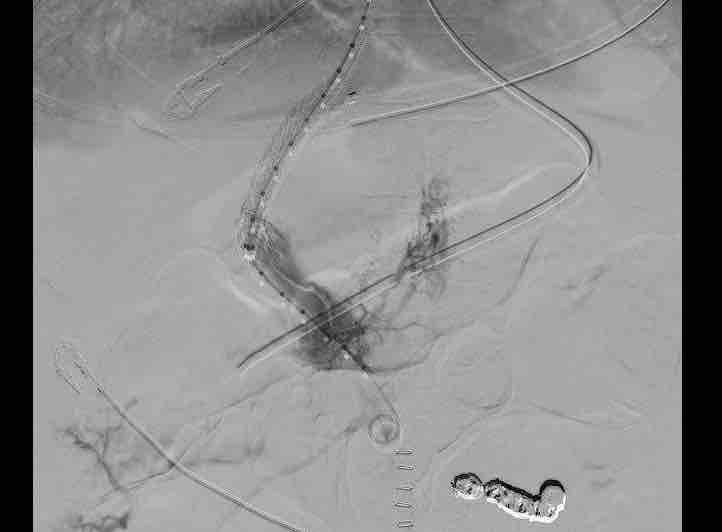
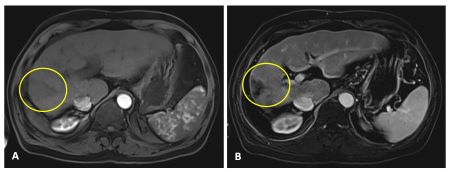
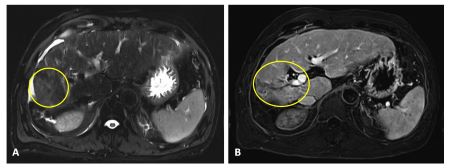
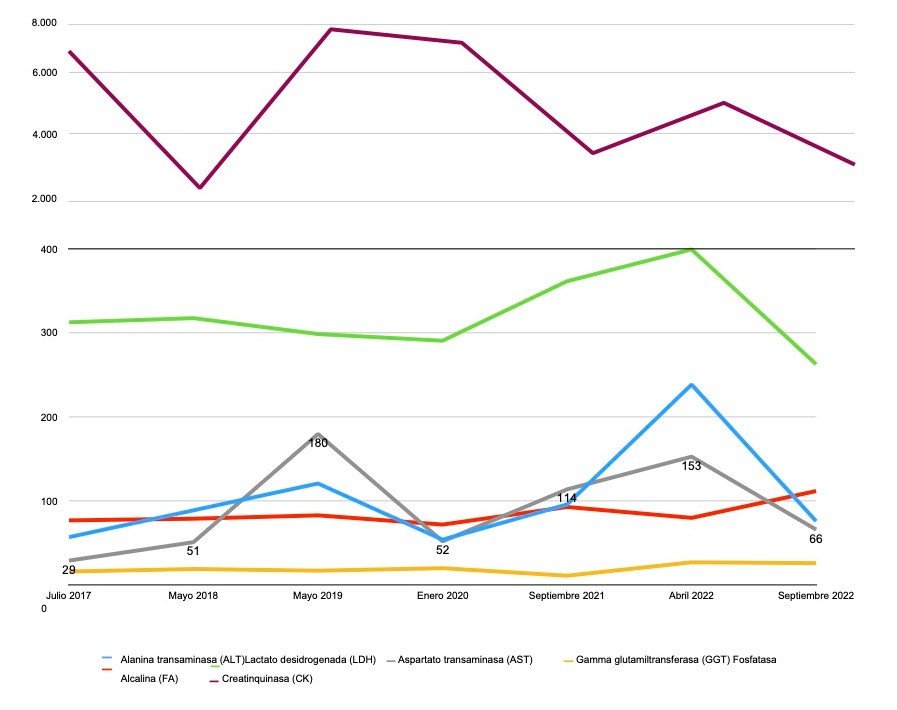
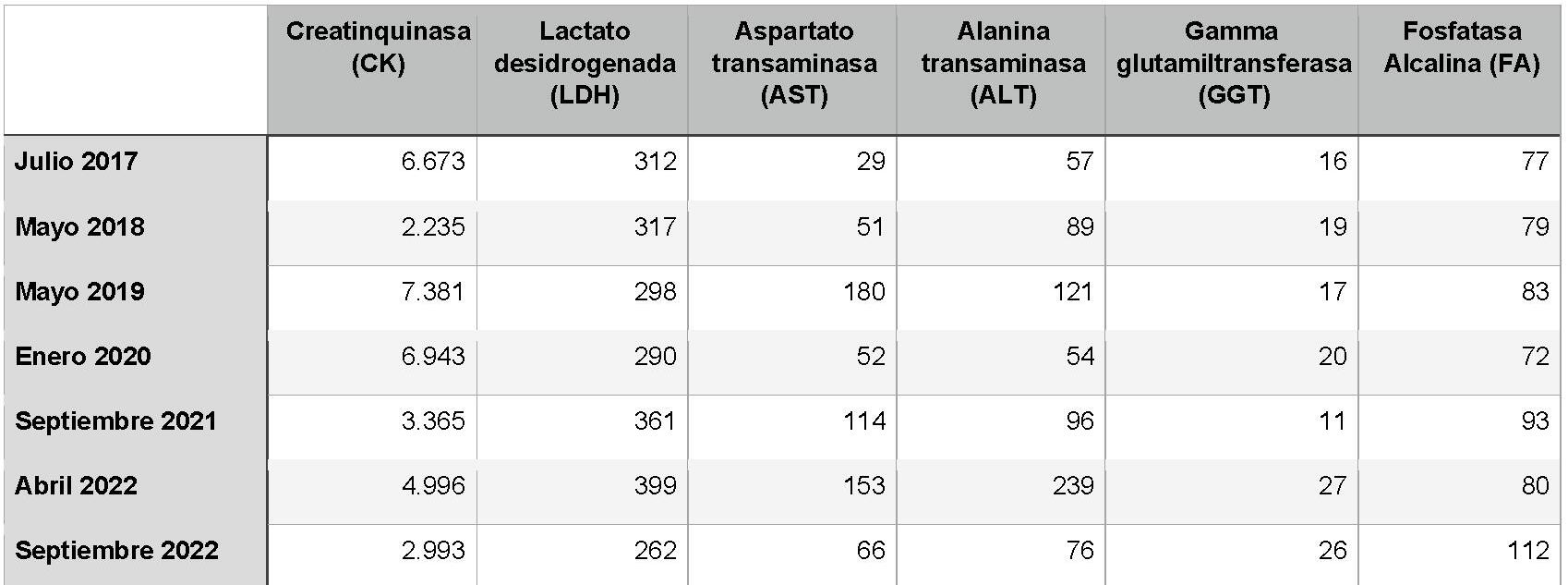
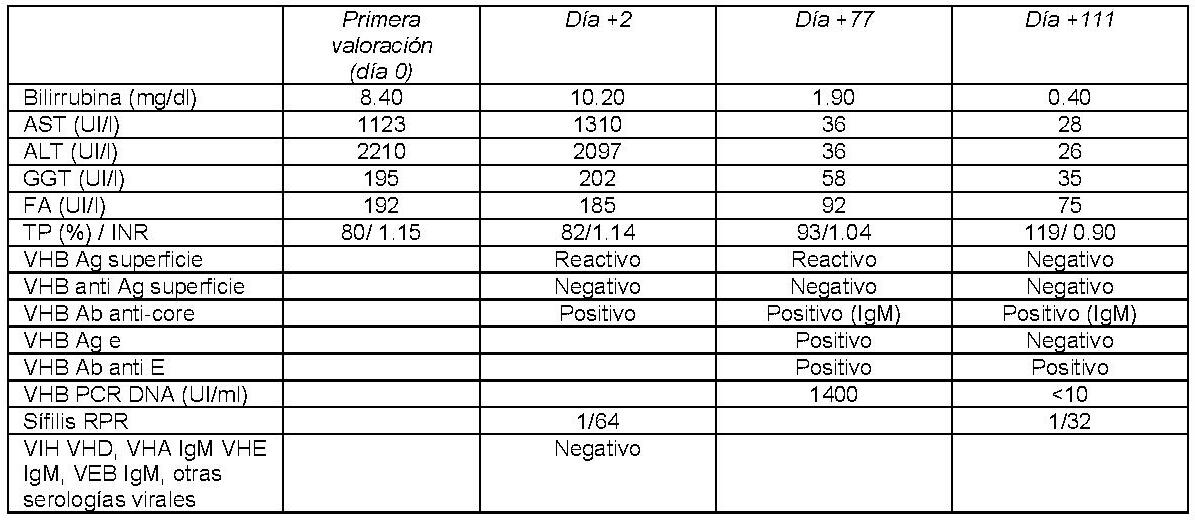
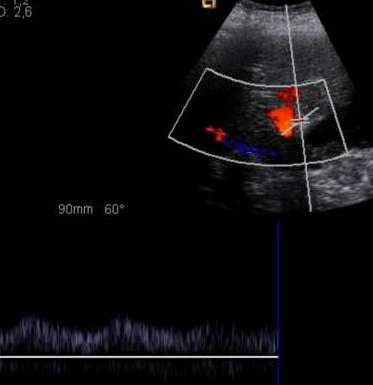
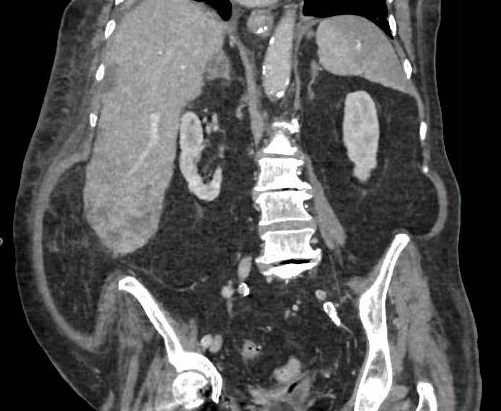
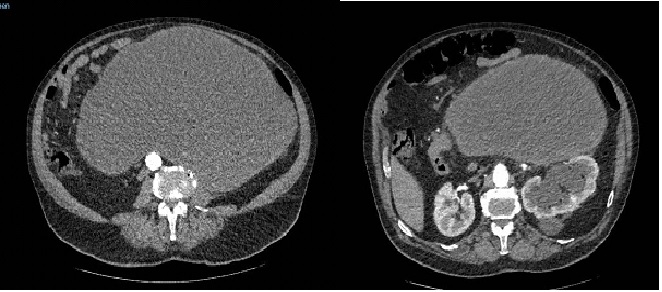
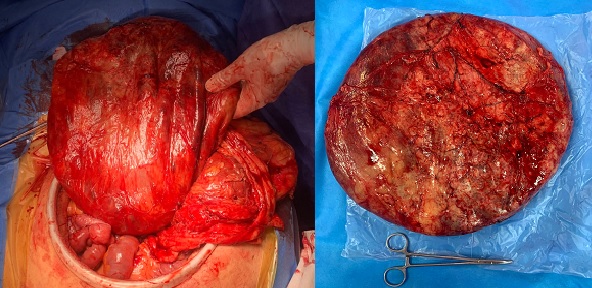
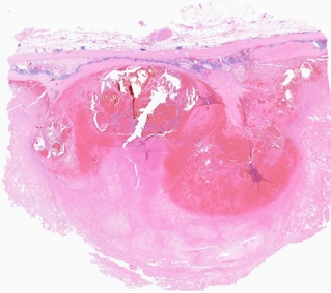
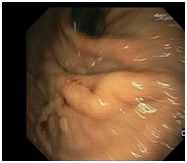
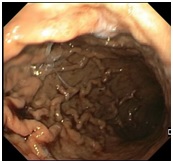
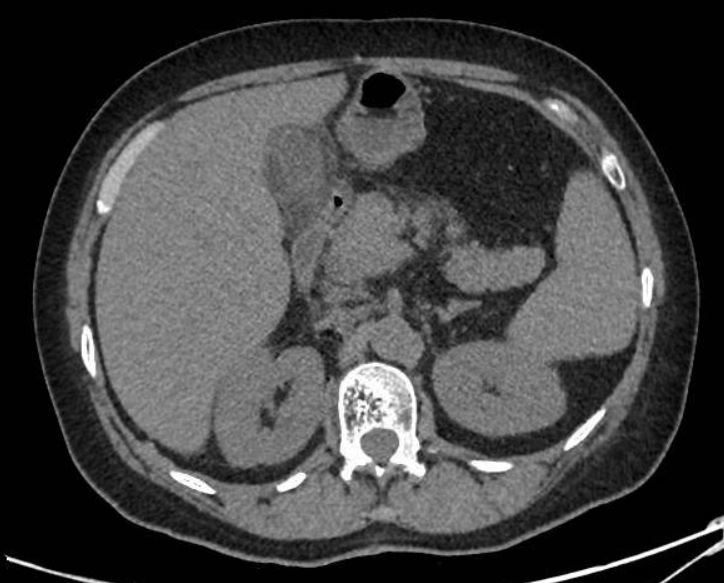
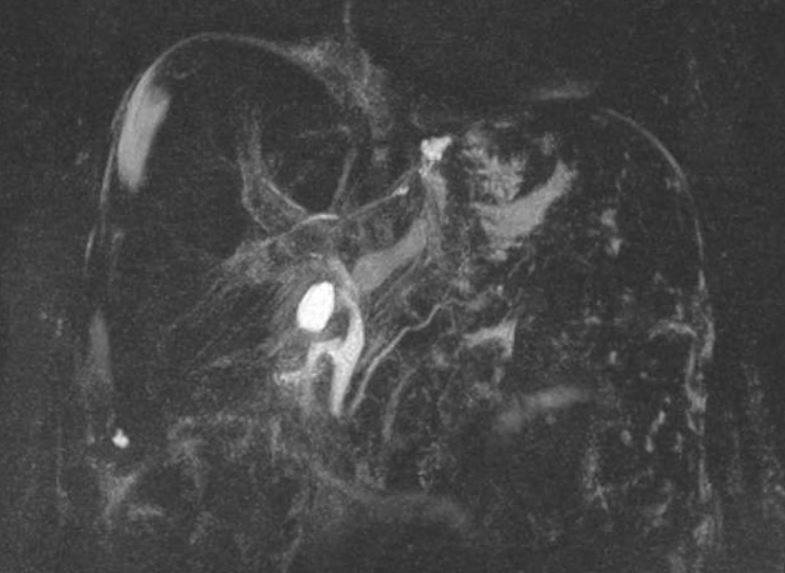
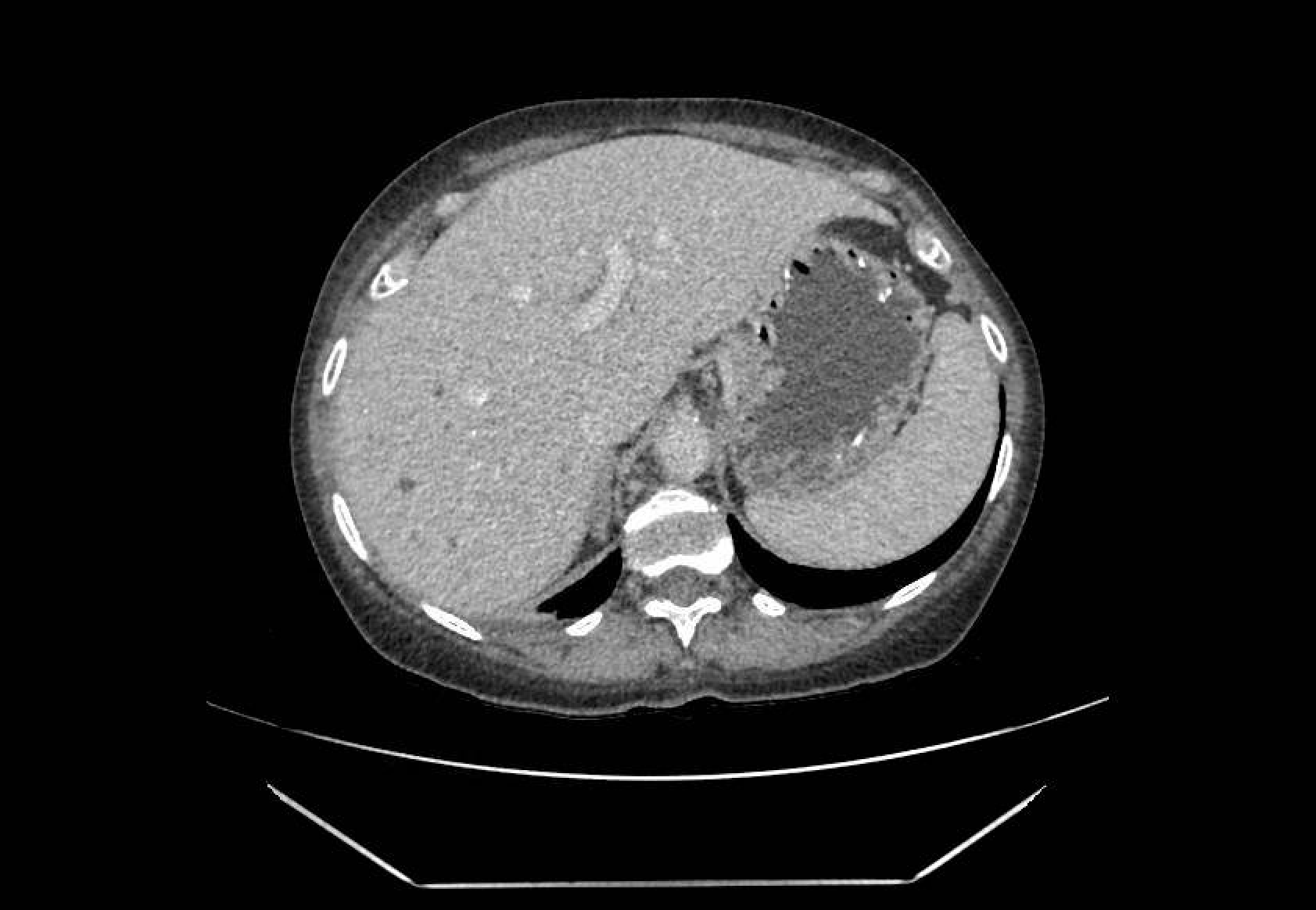
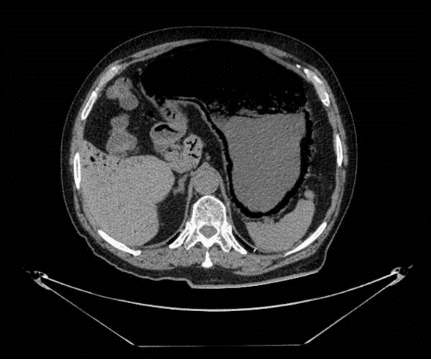
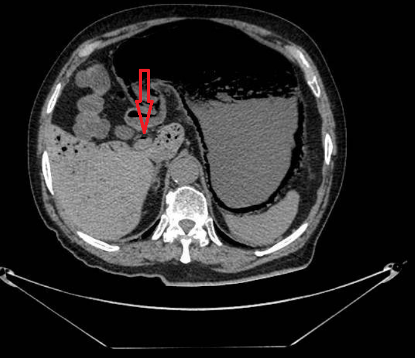
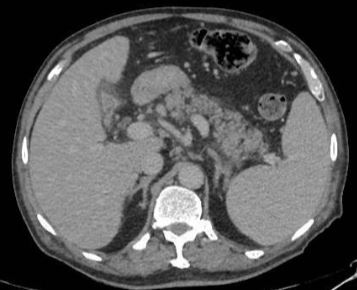
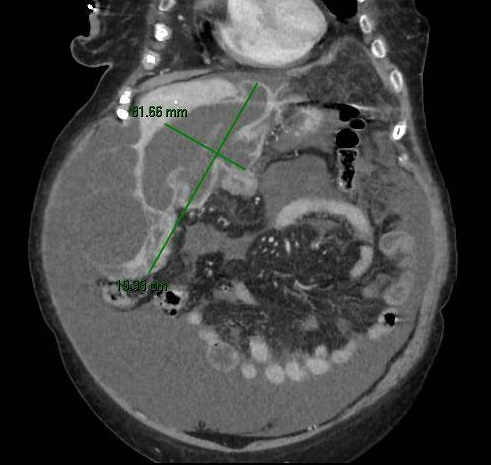
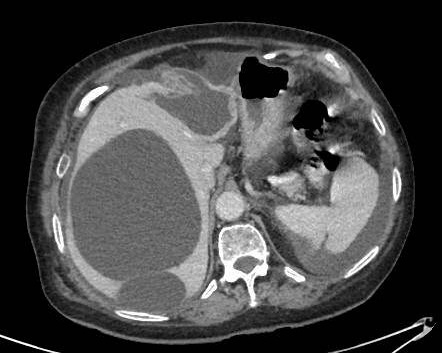
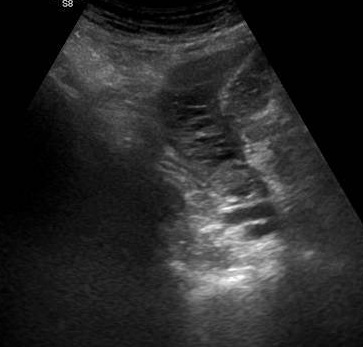
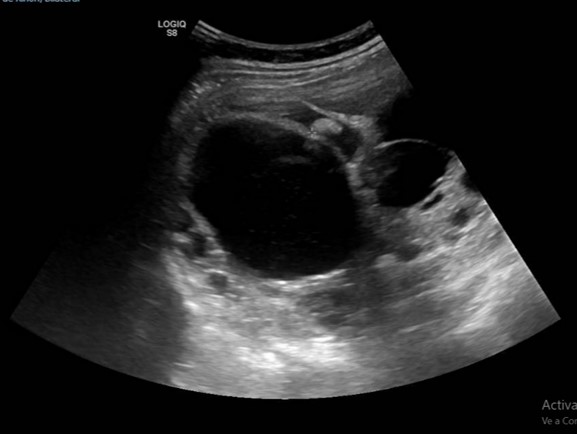
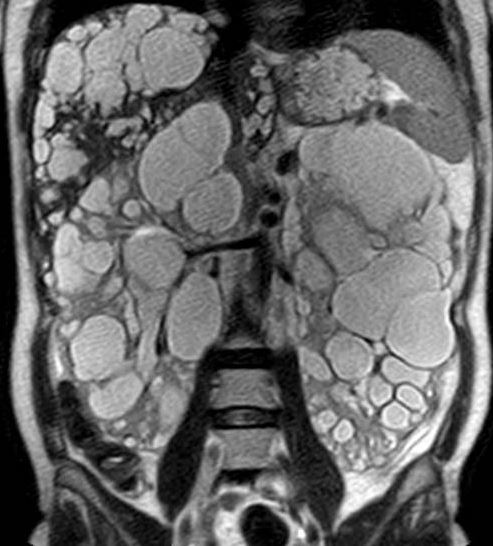
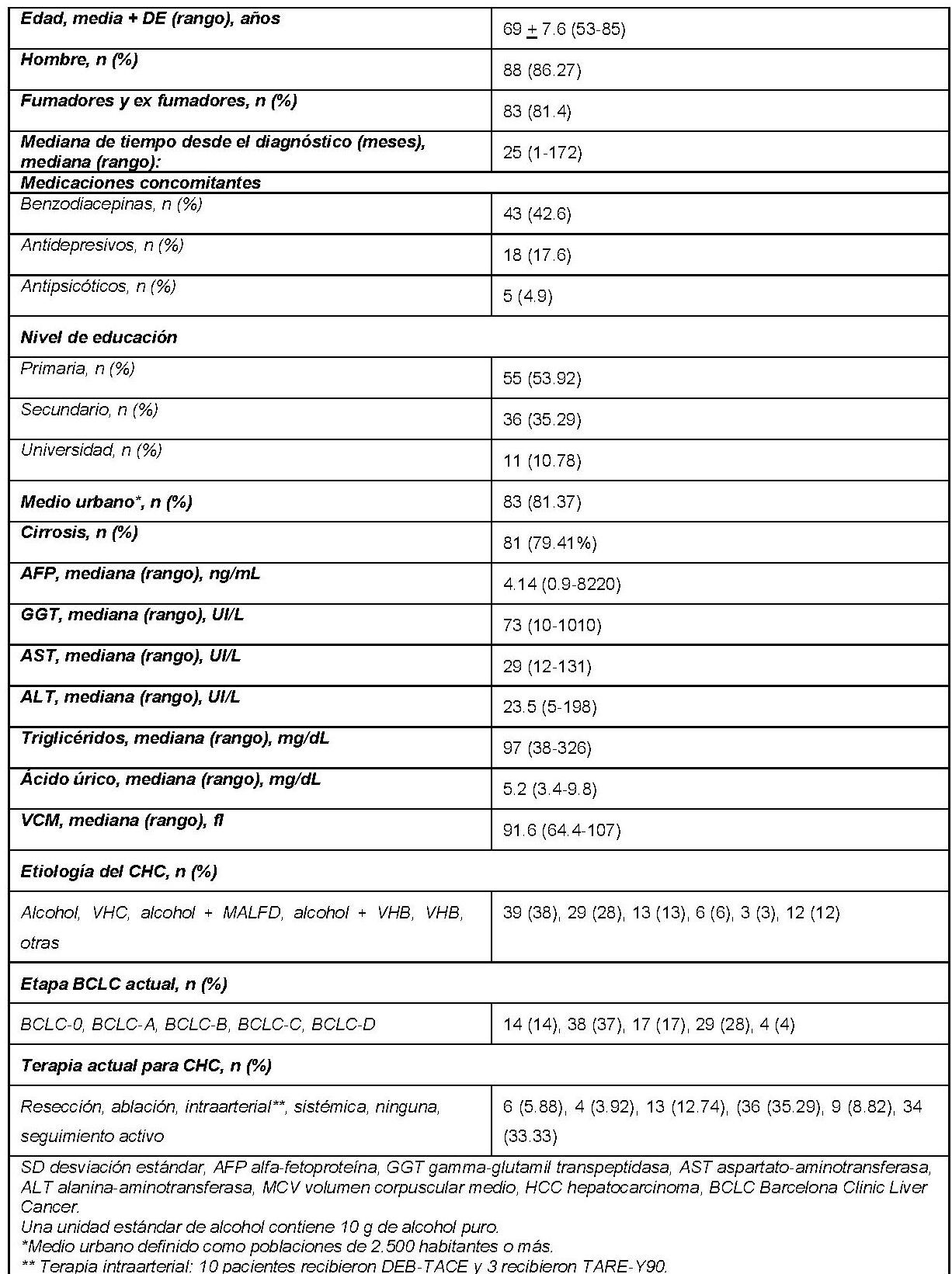
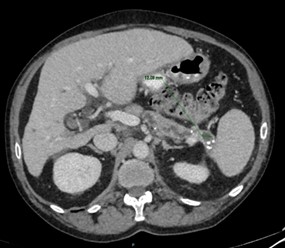
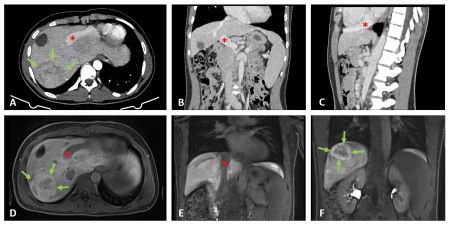
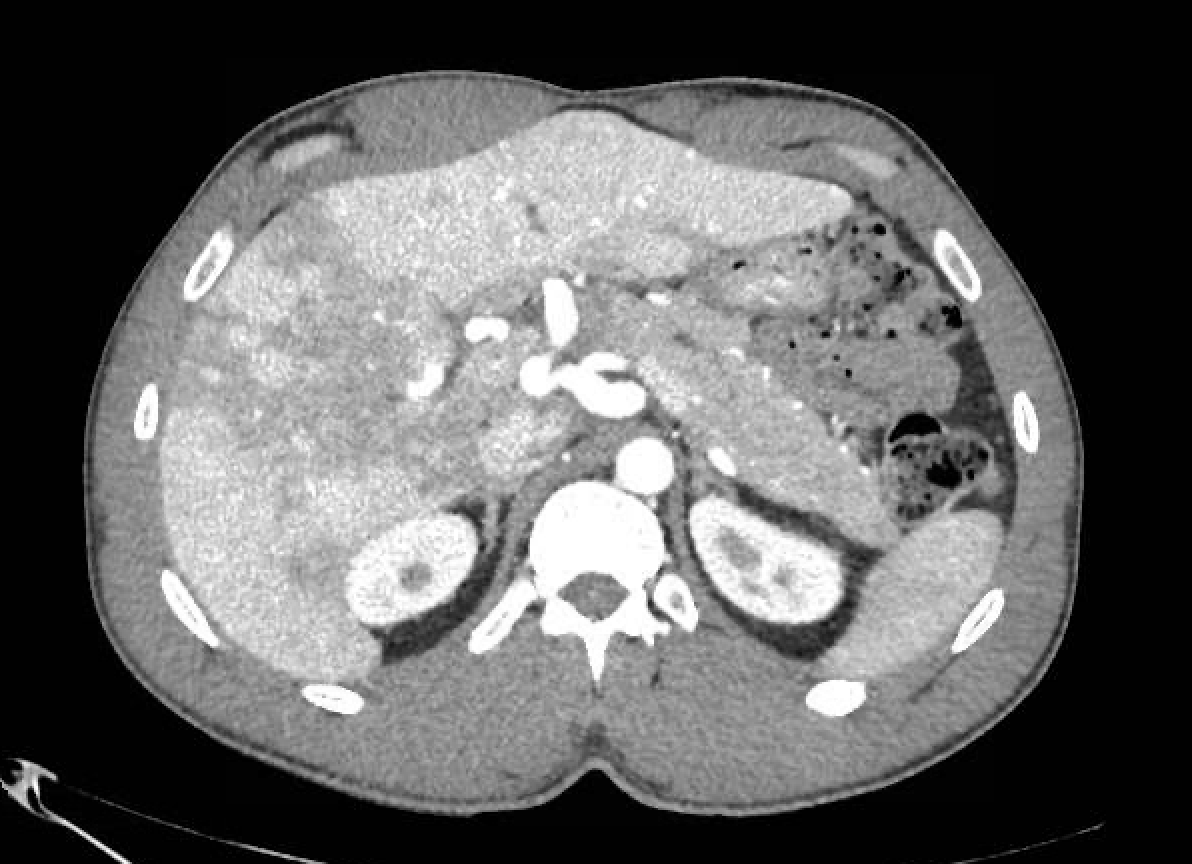
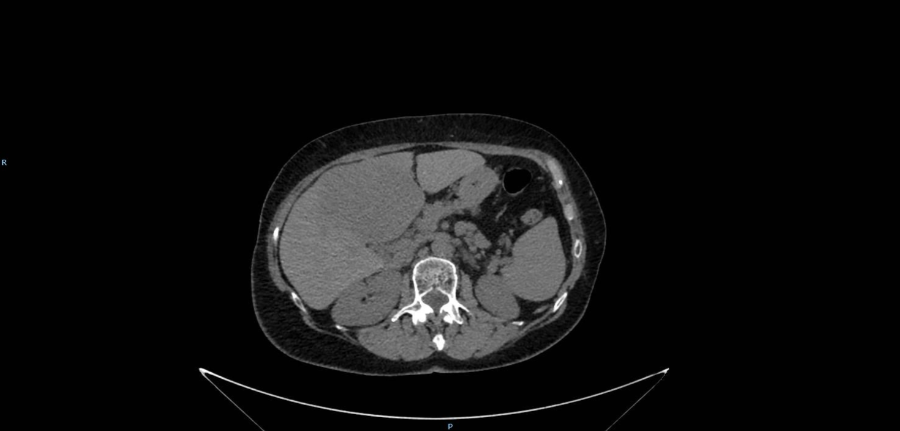
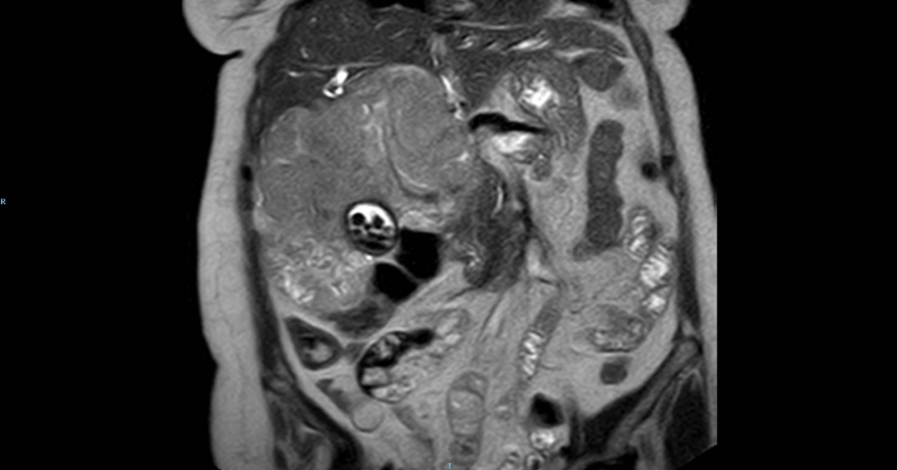
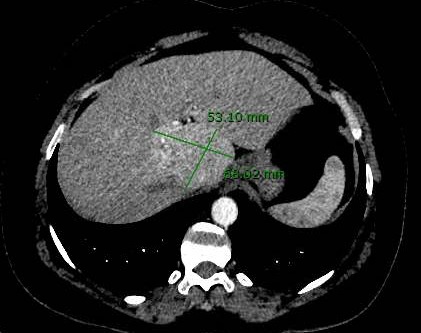
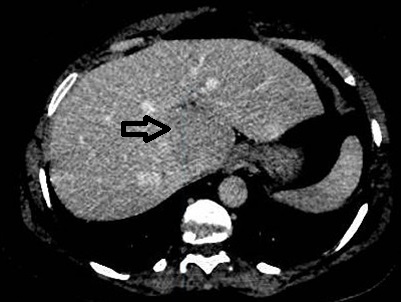
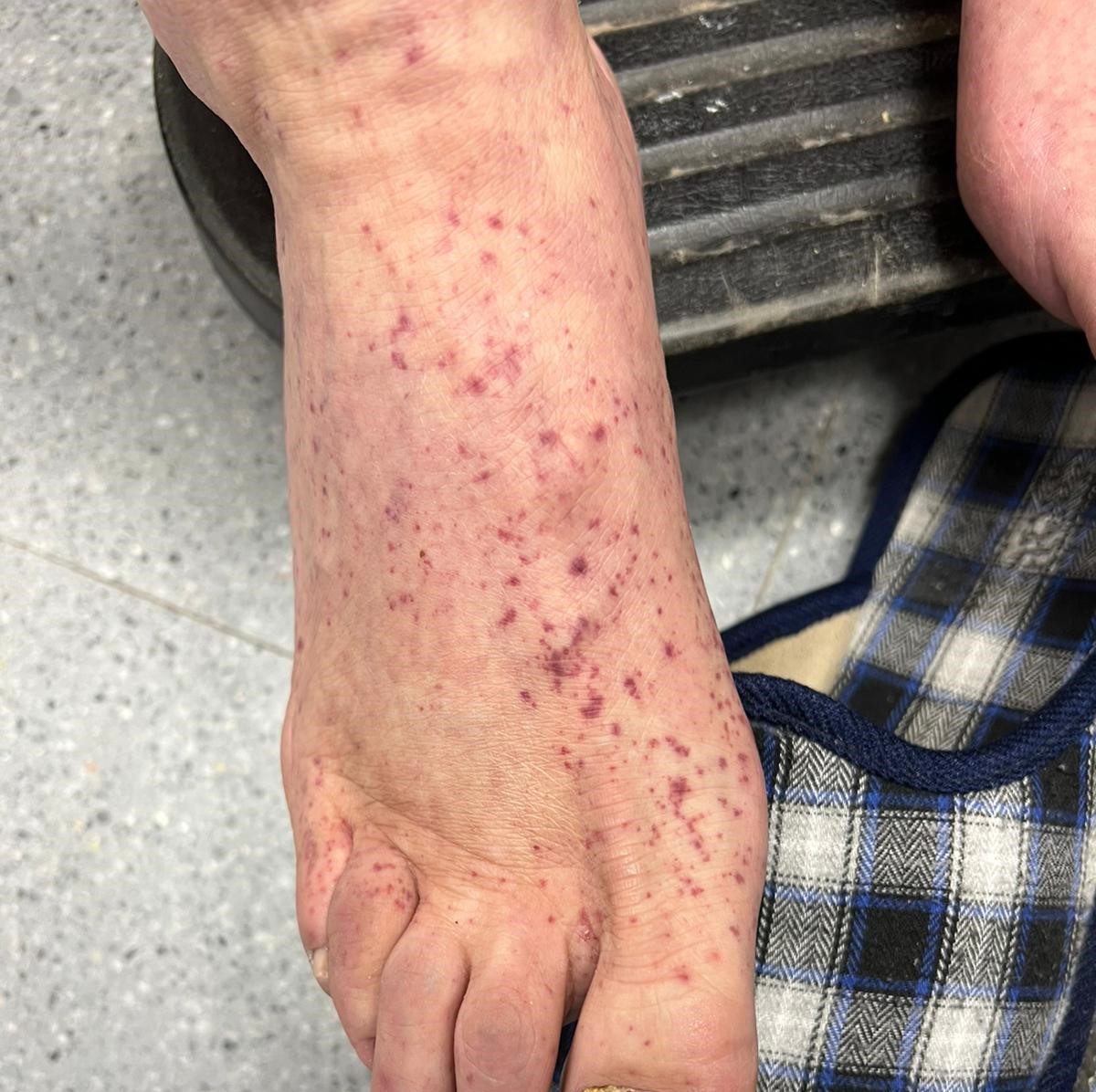
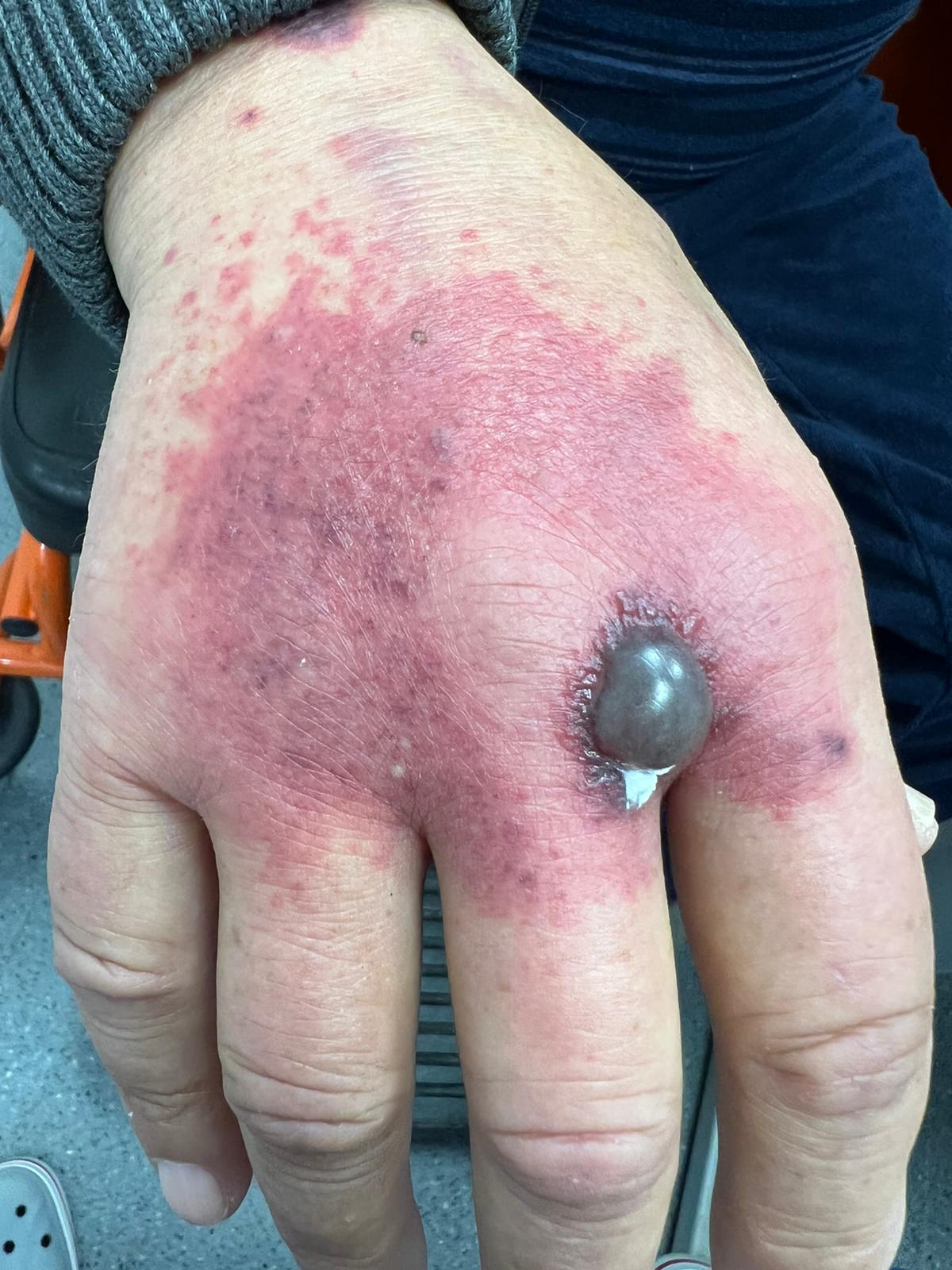
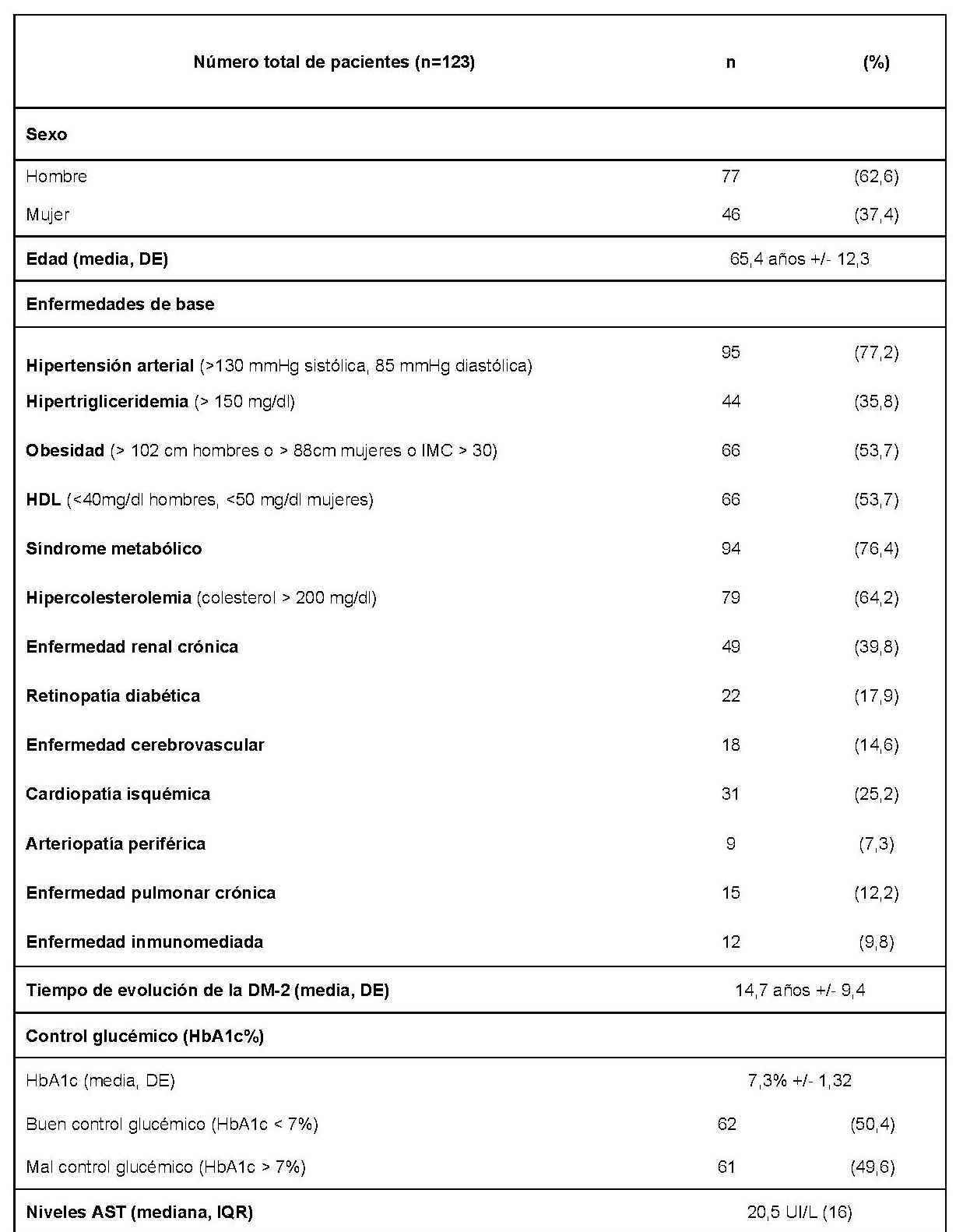
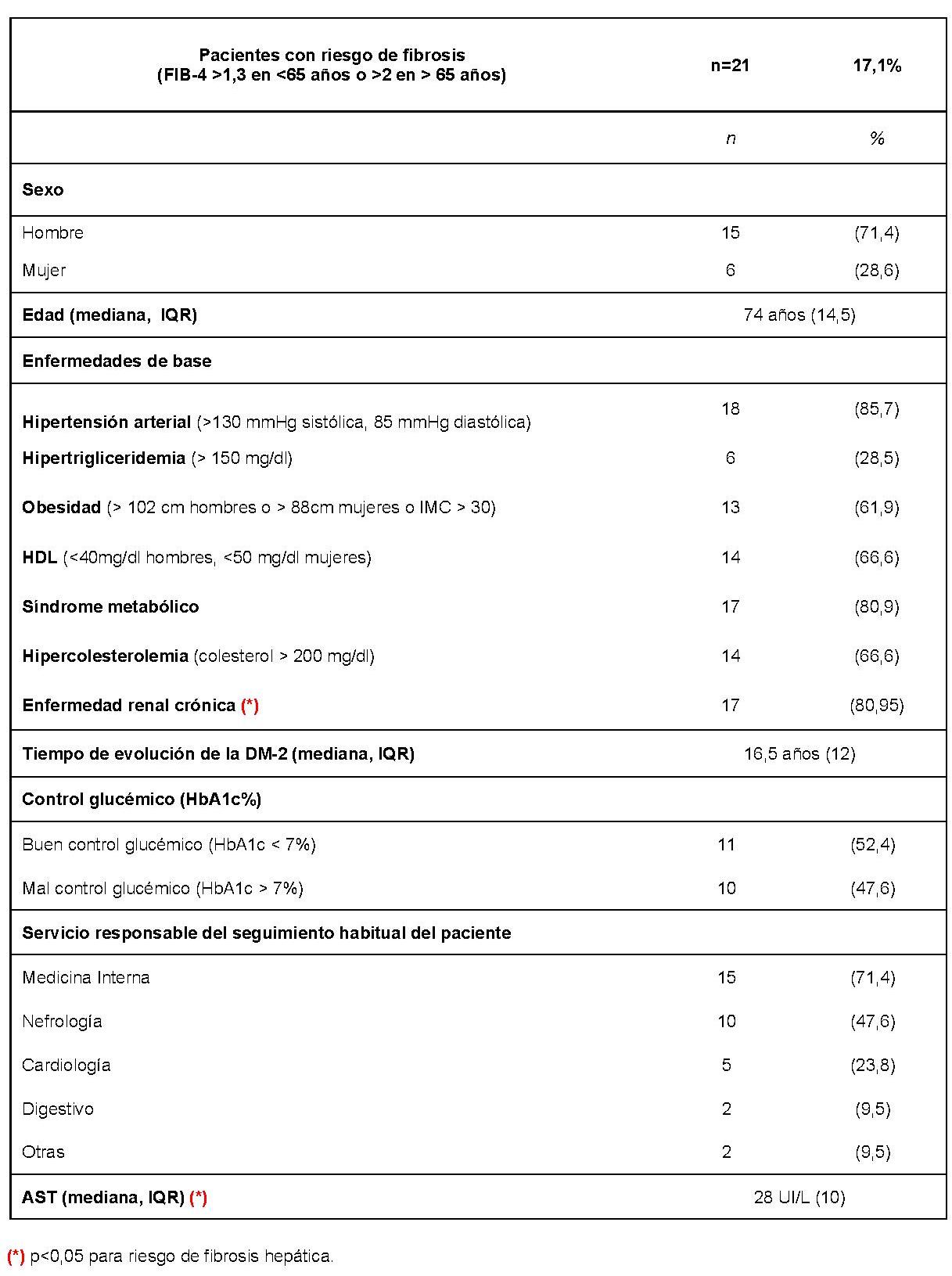
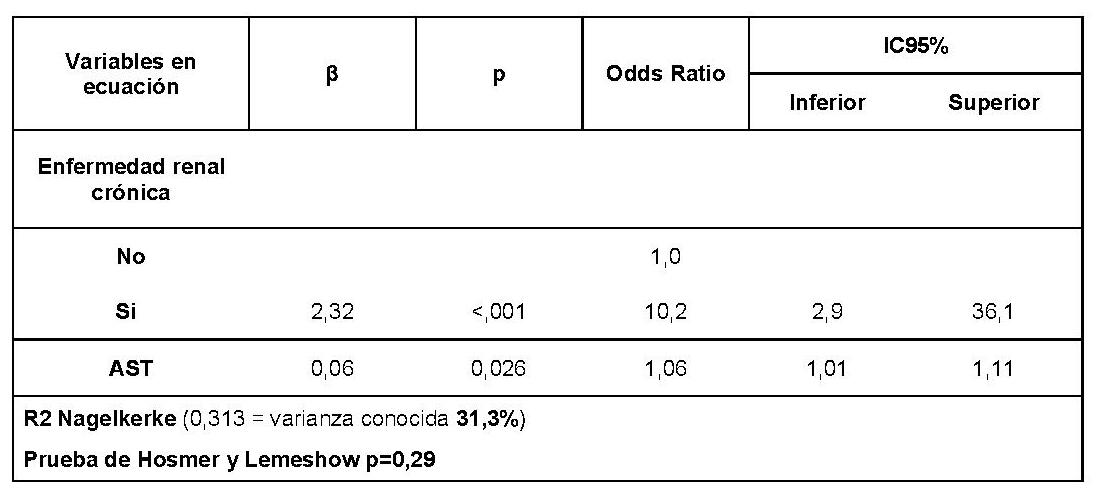
Presentamos a un varón de 60 años con antecedentes de cirrosis hepática y ascitis refractaria que ingresa por descompensación hidrópica, insuficiencia renal aguda AKIN III, encefalopatía hepática y desnutrición. Durante el ingreso se realizó un tratamiento multimodal mediante paracentesis evacuadora restrictiva con salida de LA quiloso (Imagen 1 y 2), cuyas características se reflejan en la tabla 1, con reposición de albúmina, así como fluidoterapia. Además, precisó del uso de terlipresina dada la falta de mejoría de la insuficiencia renal. Por otro lado, se insistió en la ingesta oral como pilar del tratamiento, precisando de soporte nutricional con Hepatotenex® diario a través de sonda nasogástrica. Tras mejoría de la función renal y de la semiología ascítica se decidió alta e inclusión en el programa de trasplante hepático.
Discusión
En el caso expuesto, el detonante de la AQ es la presencia de HTP. El incremento de presión del flujo sanguíneo hepático se traduce en un aumento de producción de líquido linfático y un aumento de presión que puede comprometer los canales endoteliales linfáticos con la consiguiente liberación de quilomicrones al abdomen, que almacenan Triglicéridos de cadena larga (TCL), derivados de grasa dietética. El diagnóstico se confirma tras obtener una concentración de TG mayor de 200 mg/dl en el líquido ascítico (LA).
El tratamiento de la AQ se basa en un enfoque multimodal centrado en el soporte nutricional con TG de cadena media (MCT), los cuales se reabsorben directamente por la circulación portal sin ser almacenados en forma de quilo (3); y fármacos que contribuyan a reducir el flujo linfático y el gradinte de HTP.
En nuestro caso, nos basamos en un SNE con Hepatotenex® (figura 2), fórmula rica en MCT y aminoácidos ramificados que constituye una dieta equilibrada en pacientes con Insuficiencia Hepática Crónica. La combinación de diuréticos, terlipresina, paracentesis y albúmina mejoró la semiología ascítica.
Es bien conocido que la AQ es rica en inmunoglobulinas y nutrientes, lo que predispone a un estado de inmunodeficiencia y desnutrición en el paciente hospitalizado. Por ello destacamos como conclusión la importancia de la nutrición en el paciente cirrótico.
CP-050. A PROPÓSITO DE UN CASO: HEPATOTOXICIDAD POR ESTANOZOLOL, UN TIPO DE ESTEROIDE ANABOLIZANTE
Angulo Domínguez G1, Carrión Rísquez A1, Avilés Recio M1, Serrano Romero M1, Navas García N2
1Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Virgen de Valme, Sevilla. 2Servicio Anatomía Patológica. Complejo Hospitalario de Especialidades Virgen de Valme, Sevilla.
Palabras clave: anabolizante, estanozolol, colestasis.
Introducción
Los esteroides anabolizantes son derivados sintéticos de la testosterona y, entre otros efectos, producen aumento de la masa muscular, motivo por el cual se suelen usar por deportistas. Entre sus efectos secundarios destaca la hepatotoxicidad, que puede ir desde una elevación asintomática de enzimas hepáticas hasta un fallo hepático fulminante. El patrón de lesión puede variar de necrosis hepatocelular, colestasis, peliosis hepática, hígado graso o tumores y depende del tipo de anabolizante.
Caso clínico
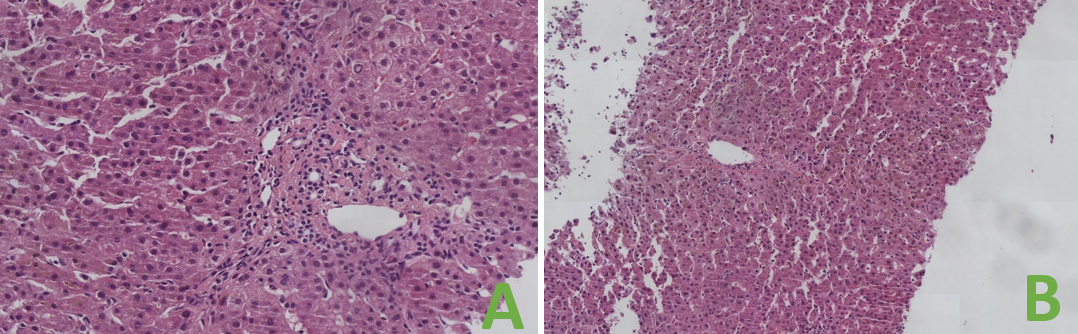
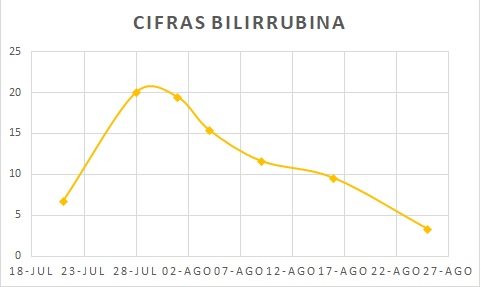
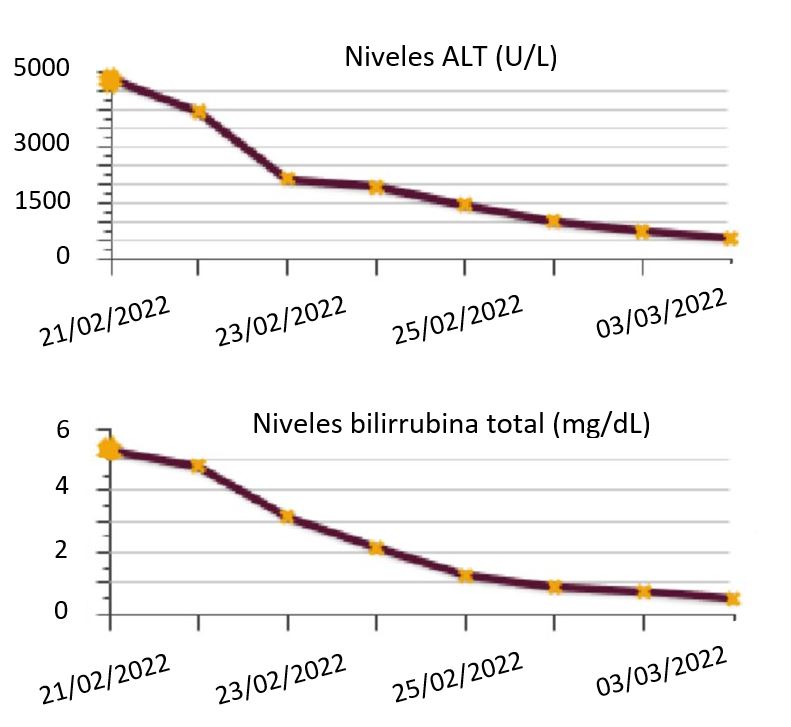
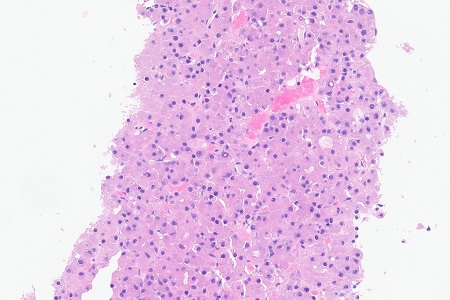
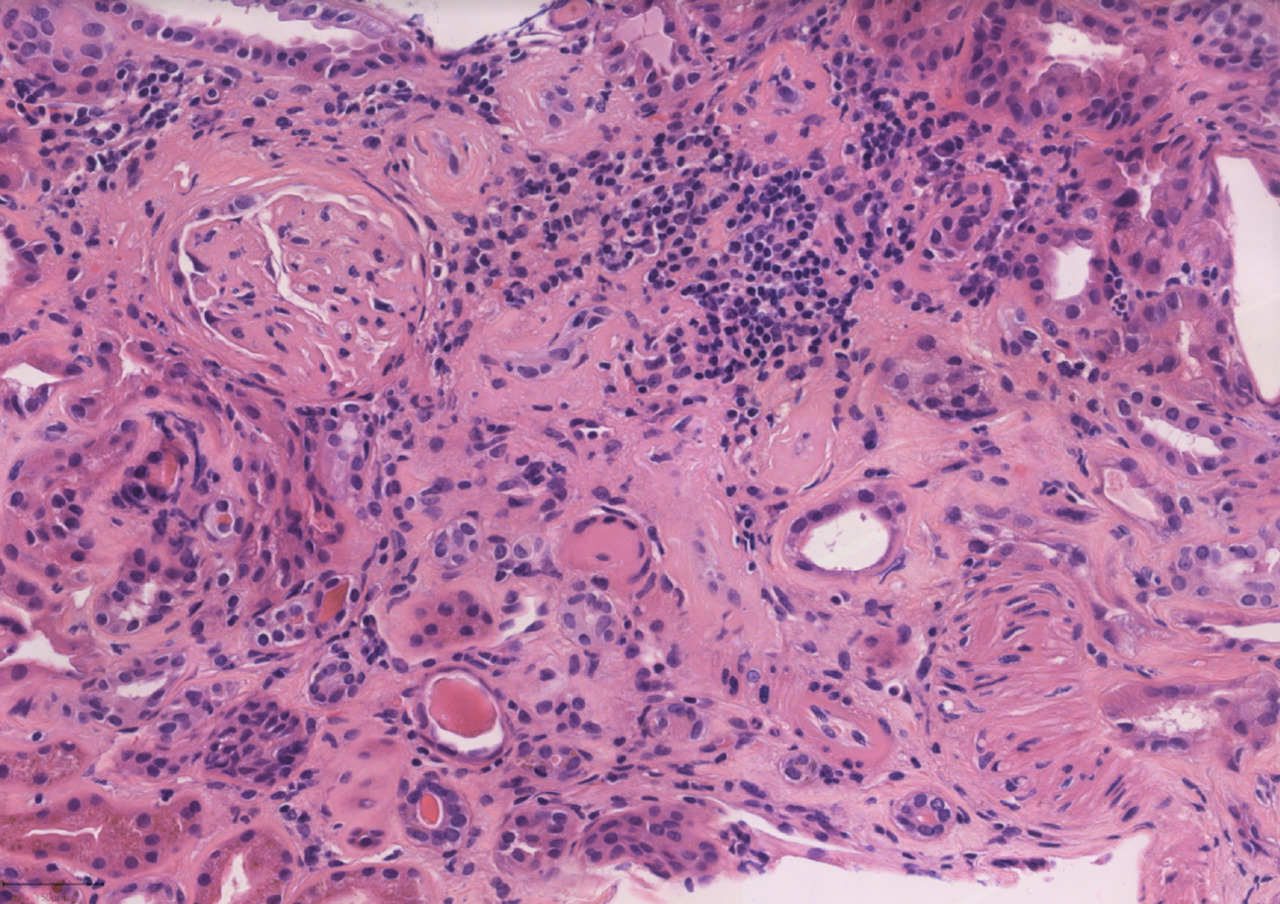
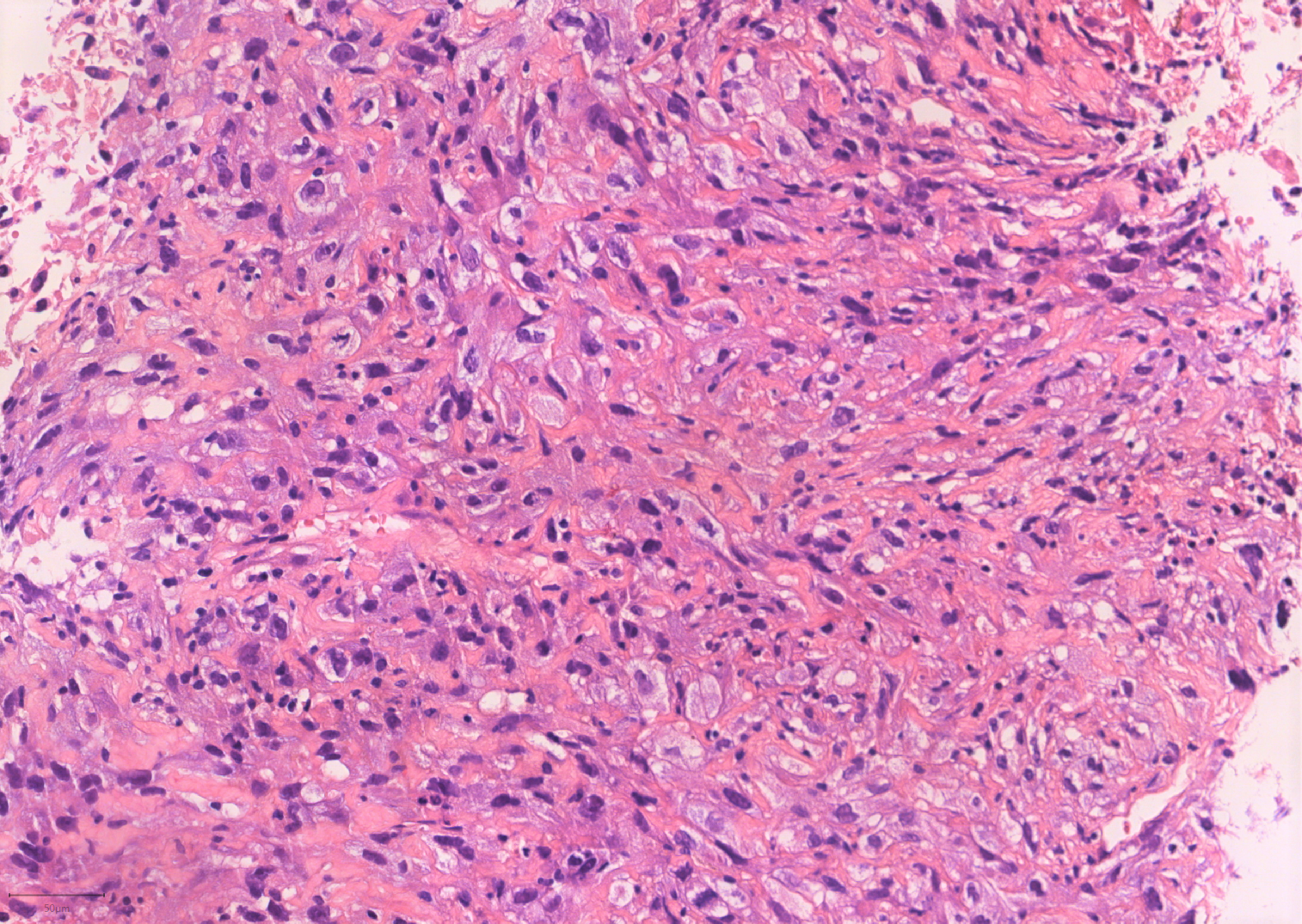
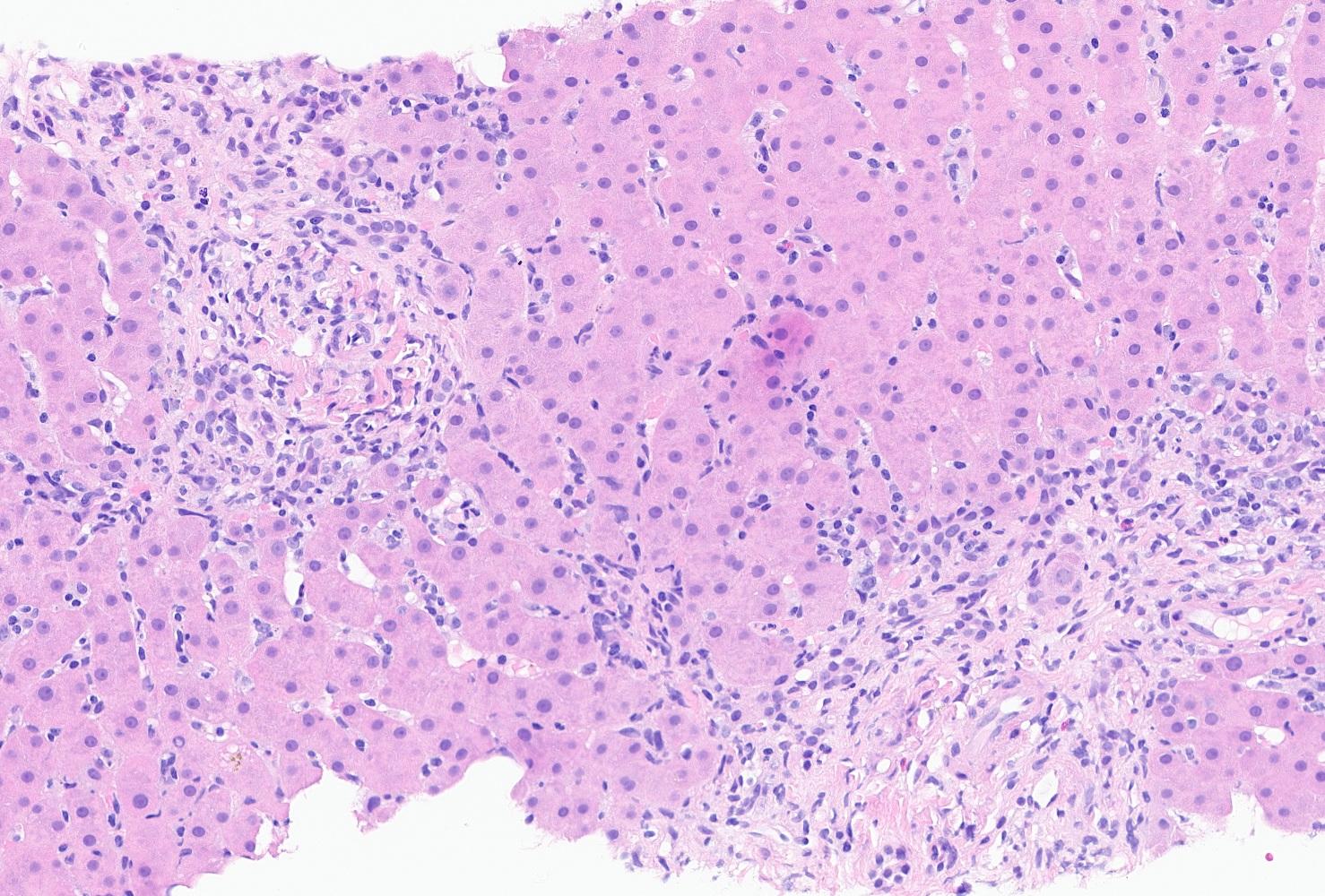
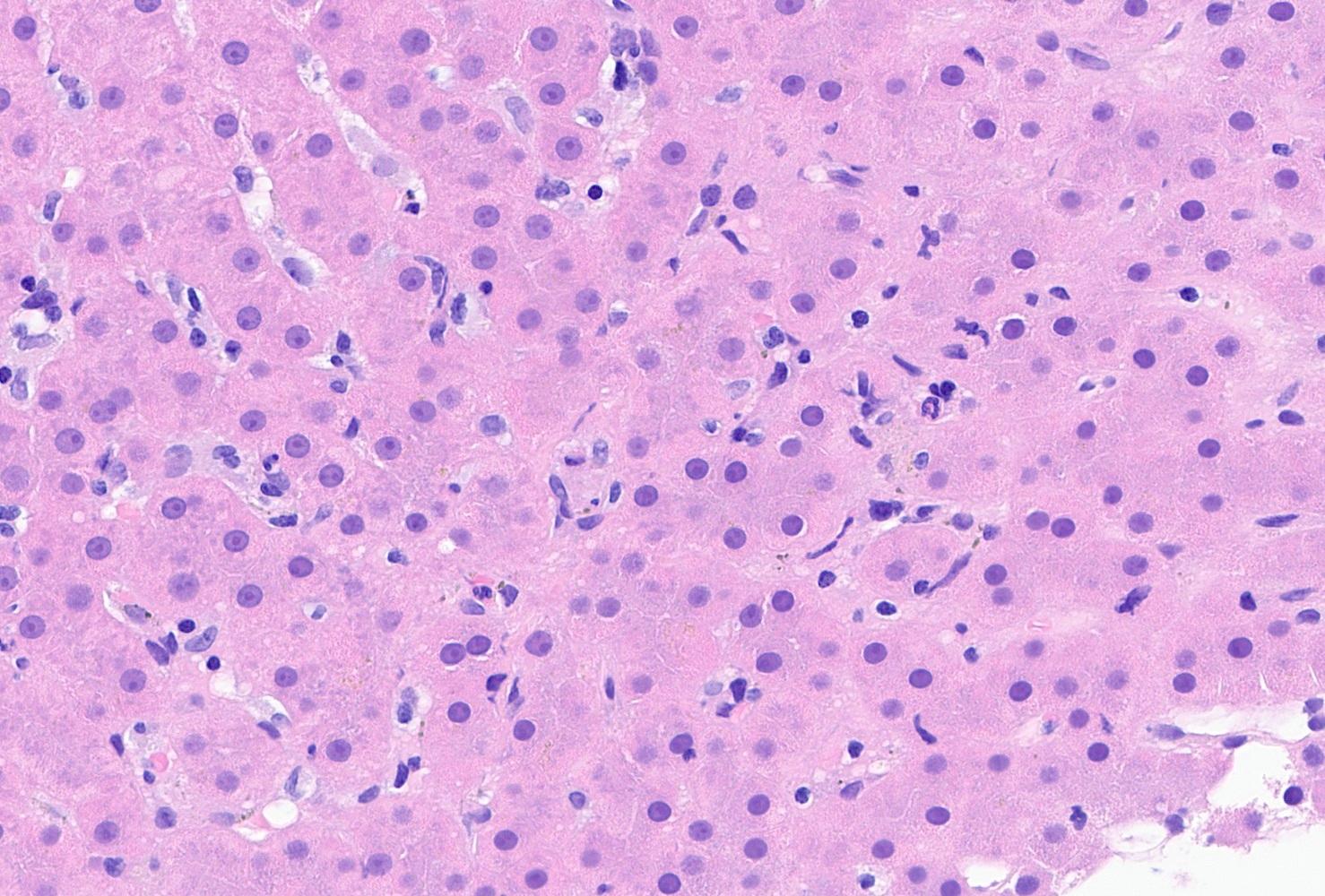
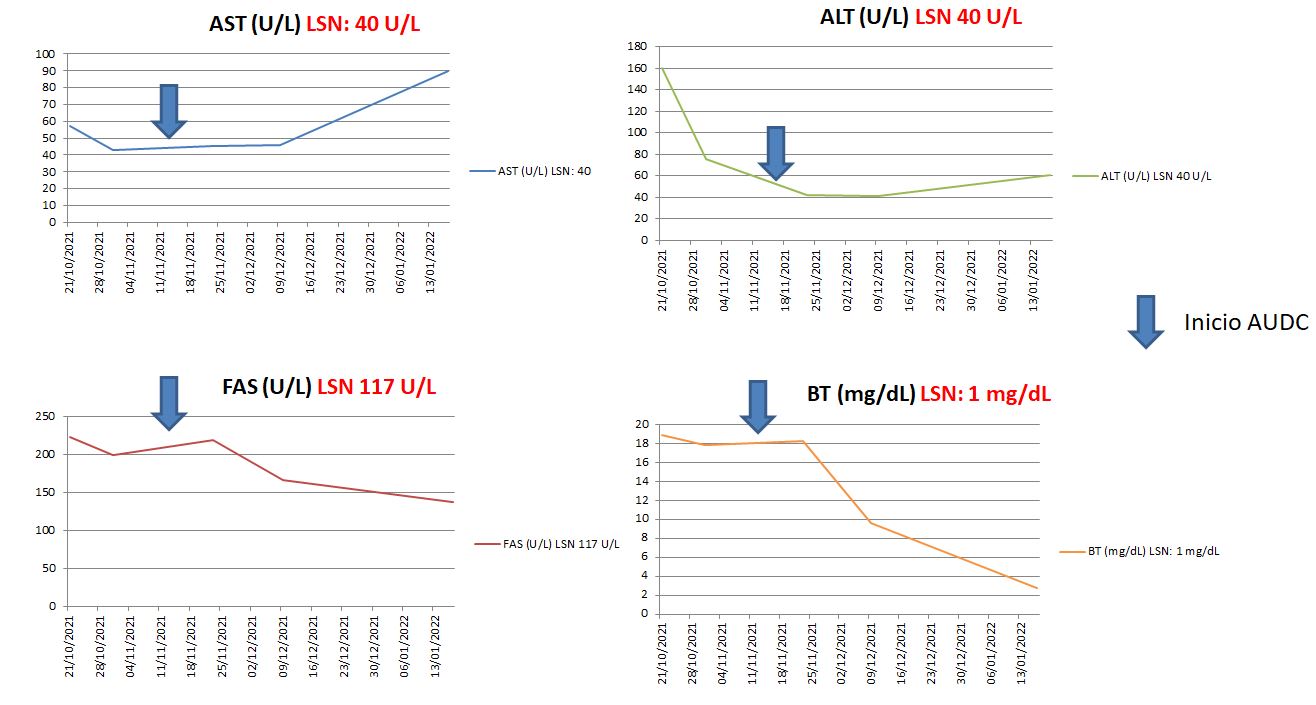
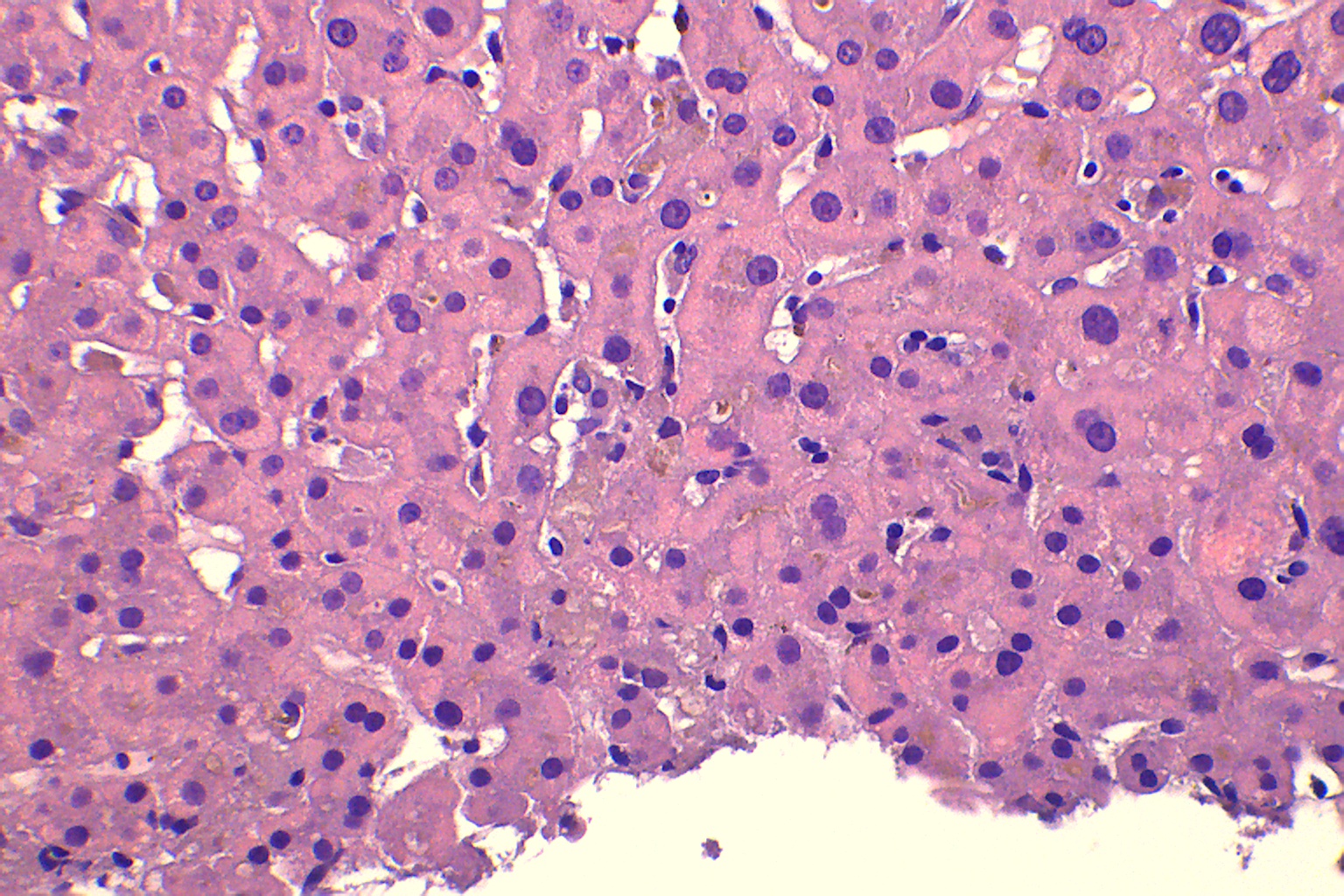
Varón de 43 años que ingresa por dolor en hipocondrio derecho e ictericia progresiva de dos semanas de evolución, con bilirrubina total de 6,74mg/dl. Reconoce consumo de 40mg diarios de estanozolol desde hace dos meses. Durante el ingreso, mantiene elevación marcada de bilirrubina a expensas de directa (pico máximo 20 mg/dl) con resto de perfil hepático prácticamente normal (mínima elevación de FA, ALT y AST). Pruebas de imagen y analíticas sin hallazgos, salvo colelitiasis. Se realiza biopsia hepática, siendo el hallazgo más relevante una colestasis canalicular extensa (Imagen 1). Se dio el alta con diagnóstico de toxicidad hepática por anabolizantes, con bilirrubina 11,65 mg/dl (directa 10,61 mg/dl). Un mes después de suspender consumo, asintomático y con bilirrubina 3,26 mg/dl (directa 2,35 mg/dl).
Figura 1
Tinción de hematoxilina-eosina con aumento 20XB (A) y 10X (B). Infiltrado inflamatorio leve de naturaleza linfohistiocitaria con extensión lobulillar, con ocasional necrosis hepatocitaria. Ductos biliares sin evidencia de daño ductal. Colestasis canalicular extensa y citoplasmática en menor medida.
Discusión
Estamos presenciando un aumento de lesión hepática asociada al consumo de anabolizantes, probablemente por el fácil acceso a estos productos y la creencia de que son seguros para mejorar la imagen corporal. De hecho, la mayoría de los casos los estamos observando en mujeres jóvenes, aunque en nuestro caso se presente en un varón de edad media. También es frecuente la recaída en el consumo a pesar de haber presentado algún efecto secundario.
El daño hepático por anabolizantes suele causar un patrón de citolisis, con aumento de ALT, AST y LDH, y se asocia a barro biliar. Aunque la colestasis es poco frecuente cuando se administran por vía parenteral, los compuestos alquilados en la posición 17-alfa-hidroxi (como el estanozolol), que se pueden administrar por vía oral debido a su mayor resistencia frente al efecto de primer paso hepático, pueden causar una forma muy característica de colestasis aguda. Las manifestaciones clínicas características son nauseas, astenia, ictericia y coluria, con bilirrubina y FA elevadas, pero sin elevaciones significativas de AST, ALT y GGT. Tales características son indicativas de colestasis con mínima inflamación hepática o del conducto biliar. La biopsia no es necesaria para el diagnóstico. La resolución se produce generalmente tras la interrupción de los anabolizantes.
CP-051. AFECTACIÓN ESPLÉNICA EN TUBERCULOSIS MILIAR
Martín Marcuartu P, Frutos Muñoz L, Rebertos Costela E, Carrillo Ortega G
UGC Aparato Digestivo. Complejo Hospitalario de Jaén, Jaén.
Palabras clave: tbcmiliar, esplenomegalia, hipertransaminasemia.
Introducción
La afectación esplénica por tuberculosis es poco frecuente entre las afectaciones extrapulmonares de esta enfermedad. Se da con mayor prevalencia en la tuberculosis miliar, en la que se afectan en mayor número los órganos más vascularizados, siendo el bazo es el tercer órgano más comprometido tras el pulmón y el hígado. Es más rara la infección aislada del bazo. Se da con mayor frecuencia en pacientes inmunodeprimidos, aunque también puede darse en inmunocompetentes.
La afectación extrapulmonar de la tuberculosis es producida por la diseminación hematógena y linfática del Mycobacterium tuberculosis a otros órganos.
La clínica puede ser inespecífica, como fiebre de origen desconocido, astenia y otros síntomas según los órganos implicados. Esto, unido a la dificultad de la detección del bacilo a través de las pruebas complementarias convencionales, dificulta su diagnóstico definitivo.
El tratamiento es similar a la tuberculosis pulmonar, con regímenes de antibioterapia durante 6 meses en total por lo general.
Caso clínico
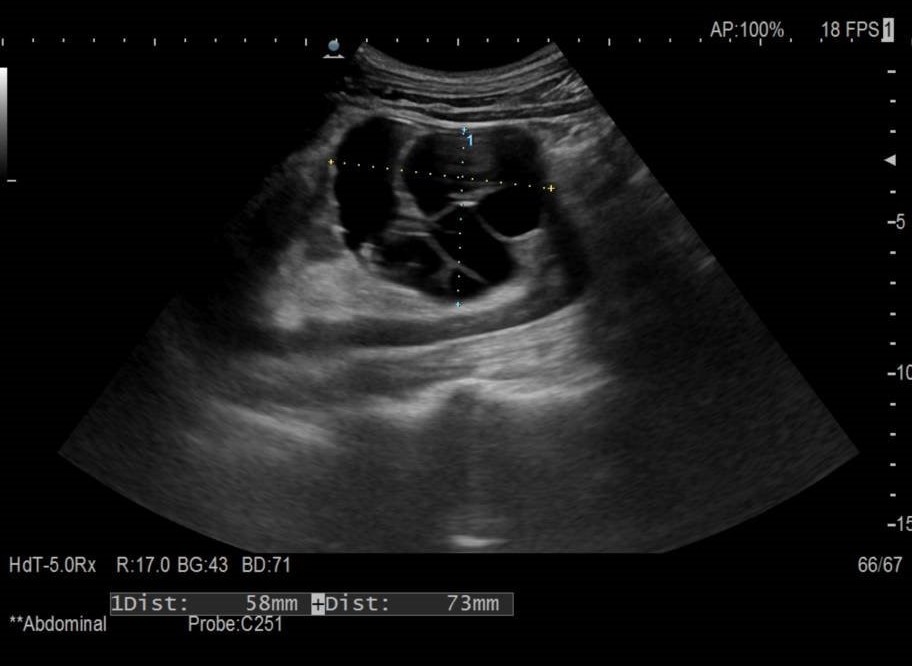
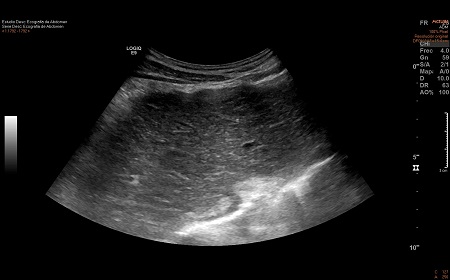
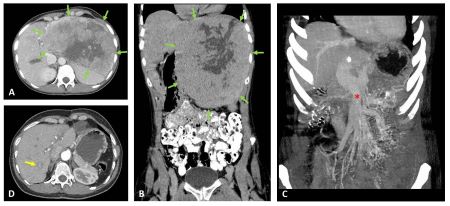
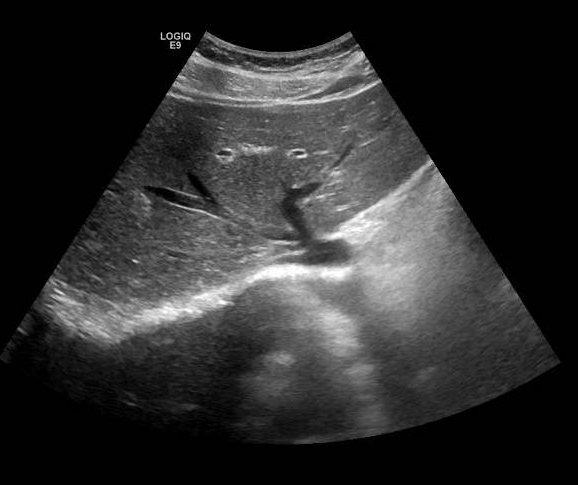
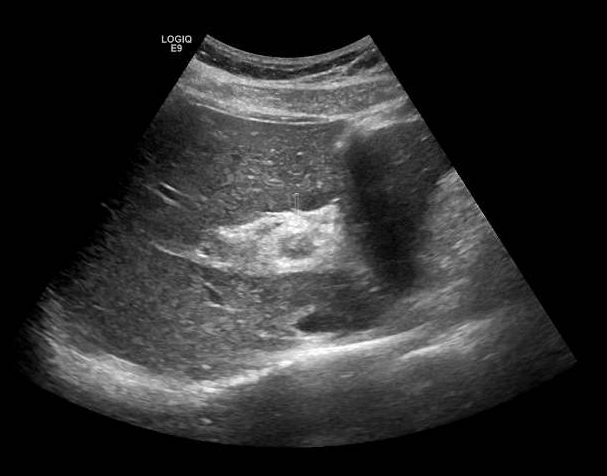
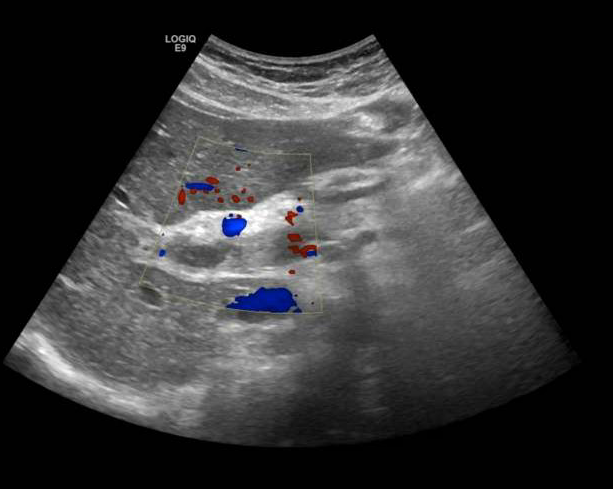
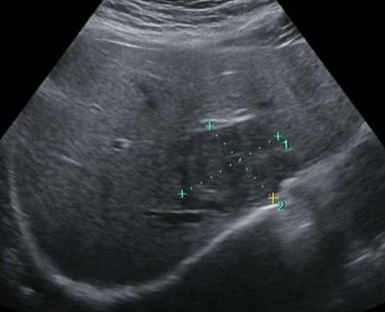
Varón de 41 años con antecedente de psoriasis en tratamiento con Adalimumab y sin alergias medicamentosas conocidas, que es remitido desde Dermatología por hipertransaminasemia con elevación de GGT. En ecografía realizada (Figura 1) se observa esteatosis hepática leve, esplenomegalia y posible afectación granulomatosa esplénica.
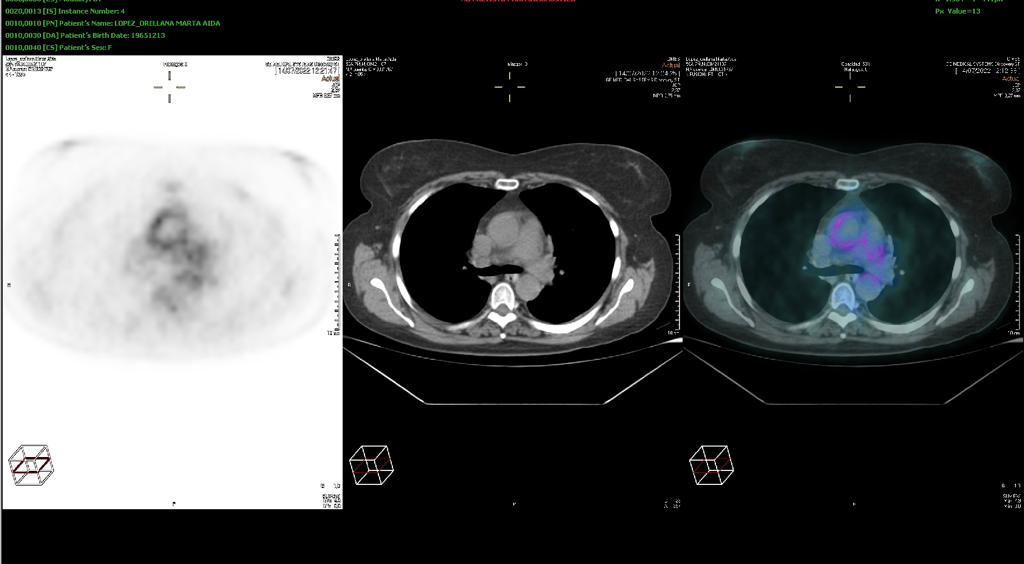
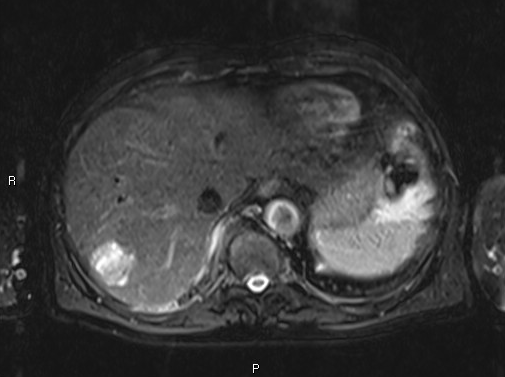
Meses después inicia cuadro febril con positividad para SARS-Cov2 con síntomas compatibles de ageusia y anosmia, persistiendo la fiebre pese al tratamiento hospitalario, con negatividad para baciloscopia, Mantoux, VIH y resto de serologías infecciosas. En TC toracoabdominal (Figuras 2 y 3) se observa patrón micronodular pulmonar bilateral con ganglios hiliares bilaterales y lesiones hipodensas esplénicas. Posteriormente se obtiene positividad en el cultivo de esputo y de aspirado de médula ósea para M. tuberculosis, concluyendo con diagnóstico de tuberculosis miliar con afectación medular, hepática, esplénica y pulmonar.
Figura 1. Ecografía bazo
Figuroa 1. Se observan lesiones hipoecogénicas con bordes bien definidos e irregulares que ocupan todo el parénquima esplénico.
Discusión
La baja prevalencia de afectación esplénica en una tuberculosis unido a la frecuente negatividad de las pruebas convencionales para el diagnóstico de la tuberculosis miliar, resulta en que la afectación del bazo sea habitualmente un hallazgo incidental, ya sea como hallazgo casual en una prueba de imagen en el estudio de fiebre de origen desconocido o en el contexto del estudio por la expresión clínica o analítica de la afectación de otros órganos, como es en este caso clínico la elevación de transaminasas por afectación hepática.
CP-052. AFECTACIÓN HEPATOPANCREÁTICA EN EL CONTEXTO DE UNA ENFERMEDAD SISTÉMICA
Tendero Peinado C, Lecuona Muñoz M, Rodríguez Gómez V, Redondo Cerezo E, Martín Rodríguez MDM, Valverde López F
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: timoma, autoinmunidad, afectación digestiva.
Introducción
La pancreatitis aguda es una inflamación aguda del páncreas, secundaria en dos tercios de los casos a litiasis vesiculares o a consumo excesivo de alcohol. Otras causas son hipercalcemia, hipertrigliceridemia, pancreatitis de origen autoinmune...
Por otro lado, el timo establece la tolerancia inmunológica central, que madura y diferencia los linfocitos T. Ante la existencia de un timoma, se genera un crecimiento desregulado y una selección aberrante de células T y como consecuencia, distintas complicaciones autoinmunitarias.
Caso clínico
Paciente mujer de 49 años con antecedentes de diabetes mellitus de reciente aparición y miastenia gravis seropositiva secundaria a timoma pendiente de intervención quirúrgica.
Es ingresada a cargo Digestivo por dolor abdominal epigástrico irradiado en cinturón junto con vómitos y amilasa y lipasa >3 veces el límite superior de la normalidad. Asimismo, la paciente presenta colestasis disociada (GGT 1047, FA 303).
En ecografía abdominal se evidencia colelitiasis y edema periglandular, con parénquima pancreático y vía biliar sin alteraciones.
Se realizan analíticas sucesivas de control, no descendiendo la colestasis a pesar de la mejoría clínica de la paciente por lo que se solicita ecoendoscopia, con engrosamiento de la cabeza pancreática de origen incierto (a descartar pancreatitis autoninmune), así como engrosamiento de colédoco.
Tras timectomía, es ingresada a cargo de Neurología para completar estudio, refiriendo en el período intercurrente aparición de pápulas y placas eritemato-escamosas, diarrea, y presentando persistencia de colestasis en analítica.
Se solicita estudio de autonimunidad, que resulta positivo (ANA, anticentrómero A, anti-LKM, Anti-ribosomales, anti-nucleosoma), y TAC de control donde se sospecha persistencia de timoma.
Se realiza además biopsia de lesiones cutáneas siendo diagnosticada de Autoinmunidad Multiorgánica Asociada a Timoma (AMOAT).
Discusión
La AMOAT es una entidad heterogénea y poco frecuente, con histología y clínica similar a la enfermedad injerto contra huésped (EICH). En ella, la activación de respuestas inmunes humorales y celulares provocan afectación a distintos niveles o restringidas a un solo órgano. Los órganos más frecuentemente afectados son la piel, el tubo digestivo y el hígado, con sintomatología frecuente como la diarrea crónica, erupción cutánea y anomalías de enzimas de colestasis, todo ello presente en nuestra paciente.
El tratamiento de primera línea para este síndrome se basa en la corticoterapia con el objetivo de frenar al sistema inmune.
Además de la afectación hepática por dicho síndrome, la pancreatitis aguda de nuestra paciente, probablemente sea consecuencia de la desregulación del sistema inmune en relación con la enfermedad de base de esta.
CP-053. ALTERACIÓN HEPÁTICA EN EL SENO DE UN TUMOR RENAL: SÍNDROME DE STAUFFER
Gil Ayuso J, Cózar Delgado E, López Ocaña A, Andrade Bellido R, García Cortés M
Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Virgen de la Victoria, Málaga.
Palabras clave: ictericia, tumor renal, síndrome de stauffer.
Introducción
Existen diversos síndromes paraneoplásicos que se pueden dar en el contexto de un proceso tumoral en los que el aparato digestivo puede verse involucrado. Supone un reto para el gastroenterólogo conocerlos y detectarlos de forma temprana de manera que podamos tener un impacto en el diagnóstico precoz de estos tumores.
Caso clínico
Presentamos el caso de un varón de 43 años, sin antecedentes de interés salvo bebedor de 2-3 cervezas diarias y celiaquía de años de evolución. Acude a Urgencias por ictericia, coluria y pérdida de peso de 14 días de evolución, sin dolor abdominal asociado ni datos de encefalopatía hepática. No refirió factores epidemiológicos que pudieran justificar daño hepático.
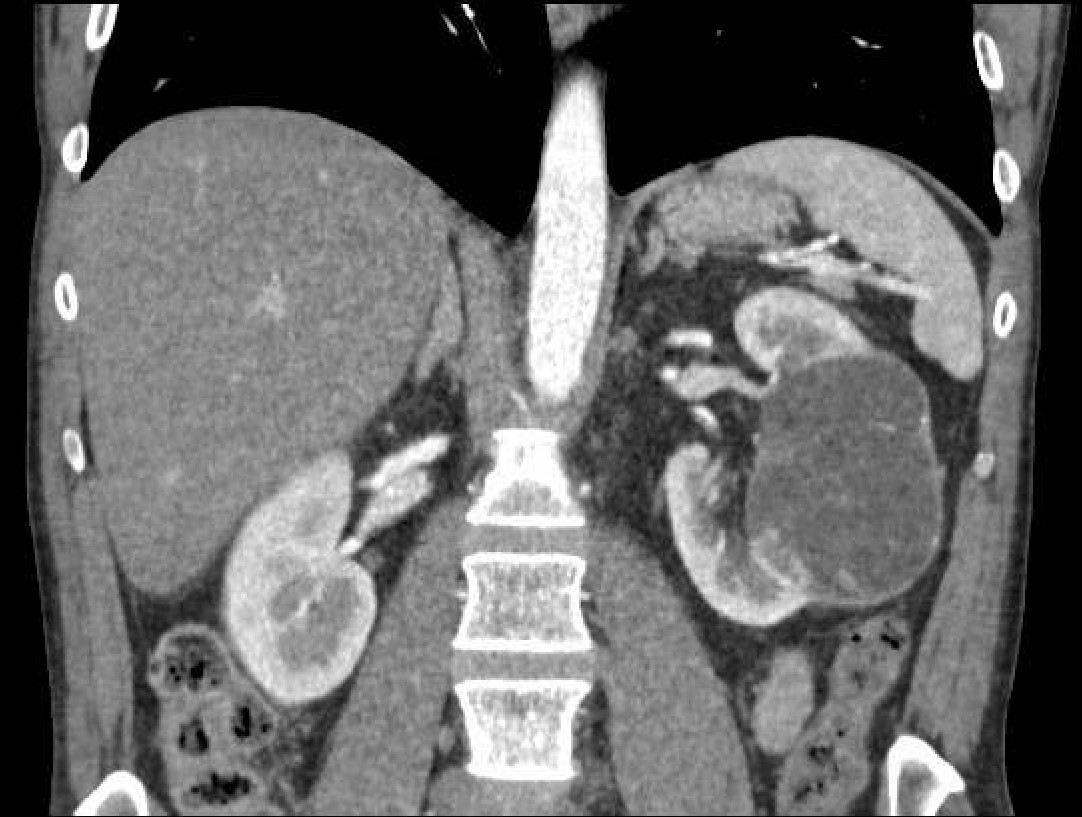
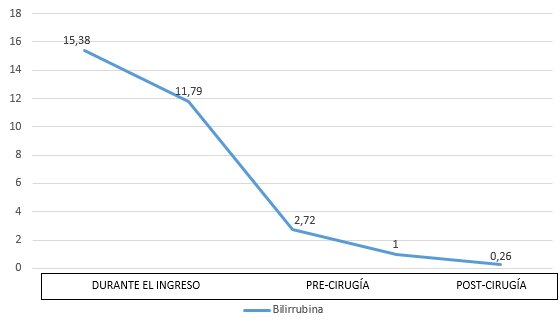
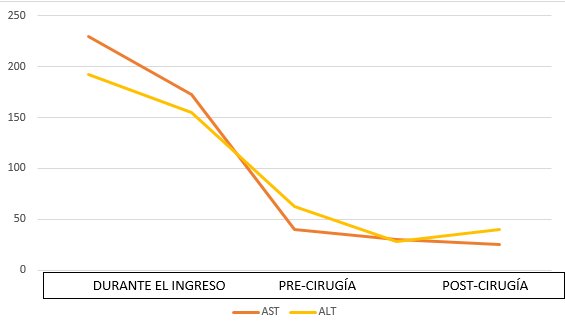
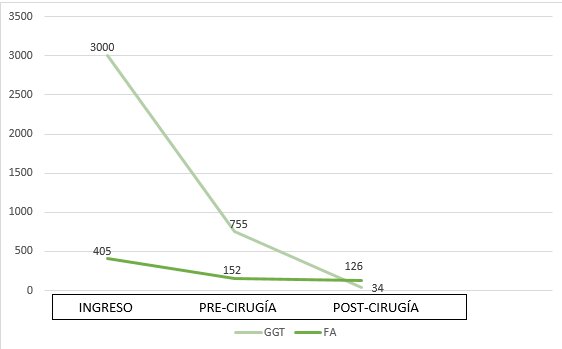
Analíticamente destacaba hipertransaminasemia leve con colestasis importante e hiperbilirrubinemia de 15,38 mg/dL a expensas de la fracción directa. Se realizó una ecografía de abdomen que reveló moderada esteatosis hepática, sin colelitiasis ni dilatación de la vía biliar. Sin embargo, destacaba una masa quística renal de unos 75mm de diámetro con múltiples septos y un polo sólido, obligando a descartar neoformación.
En el ingreso se llevó a cabo un estudio hepático que resultó negativo, incluyendo serología de virus hepatotropos y autoinmunidad. Tras consultar con Urología, se solicitó un TC focal renal que clasificó la lesión en Bosniak tipo IV altamente sospechosa de malignidad, observando un hígado de aspecto normal con áreas focales de depósito graso.
El paciente fue intervenido por parte de Urología, realizándose una nefrectomía radical laparoscópica, cuya histología reveló un carcinoma renal de células claras.
Posteriormente, acudió a consulta de Hepatología, donde el Fibroscan demostró ausencia de fibrosis significativa hepática (5,1Kpa) y objetivándose una normalización progresiva de los parámetros hepáticos tras la intervención.
Todo el cuadro nos hace pensar en un probable síndrome paraneoplásico manifestado como un daño hepático secundario a la liberación de toxinas por el tumor renal, conocido como síndrome de Stauffer; viéndose posiblemente potenciado por la ingesta de alcohol concomitante. Sin embargo, hubiese sido necesaria una biopsia hepática que descartase otras causas de daño hepático.
Discusión
Este caso nos hace reflexionar acerca de la importancia de las posibles manifestaciones sistémicas que pueden llegar a producirse en el contexto de un proceso tumoral. El síndrome de Staufffer se manifiesta como una colestasis intrahepática con ictericia y pérdida de peso asociada, tal y como sucedió en nuestro paciente. Si bien no es frecuente, tiene notable repercusión en el diagnóstico precoz y pronóstico a corto y medio plazo del paciente.
CP-054. ANALISIS DEL MANEJO CLÍNICO DE LA HAMARTOMATOSIS BILIAR: EXPERIENCIA EN NUESTRO CENTRO.
Valdivia Krag C, Orti Cuerva M, Órtiz Chimbo DS, Rodríguez Perálvarez M
UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: hamartomatosis biliar, complejos de von meyenburg, enfermedad quística hepática. .
Introducción
Describir las características epidemiológicas, motivos de consulta, estudios diagnósticos planteados y seguimiento realizado de la hamartomatosis biliar (HB) en un centro de tercer nivel.
Material y métodos
Realizamos un estudio observacional de carácter retrospectivo de los pacientes que se realizaron una ecografía abdominal dentro de la UGC de Aparato Digestivo del Hospital Universitario Reina Sofía de Córdoba. Se revisaron los registros desde enero 2014 hasta octubre 2022 (9 años) y con diagnóstico confirmado en pruebas de imagen de HB.
Figura 1
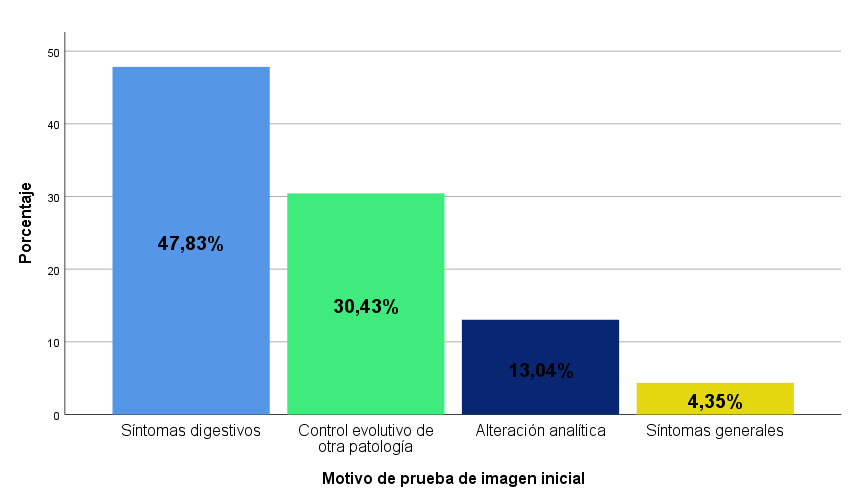
Diagrama de barras. Indicaciones que motivaron las pruebas diagnósticas en las que se sospechó la hamartomatosis biliar.
Resultados
Se incluyeron un total de 23 pacientes. El 69,6% eran mujeres, con una edad media de 58,1±24,7 años. El motivo principal de solicitud de valoración por parte de Aparato Digestivo fue un hallazgo en una prueba de imagen compatible con HB (70,8%), la cual se había solicitado por diversas indicaciones (Fig.1).
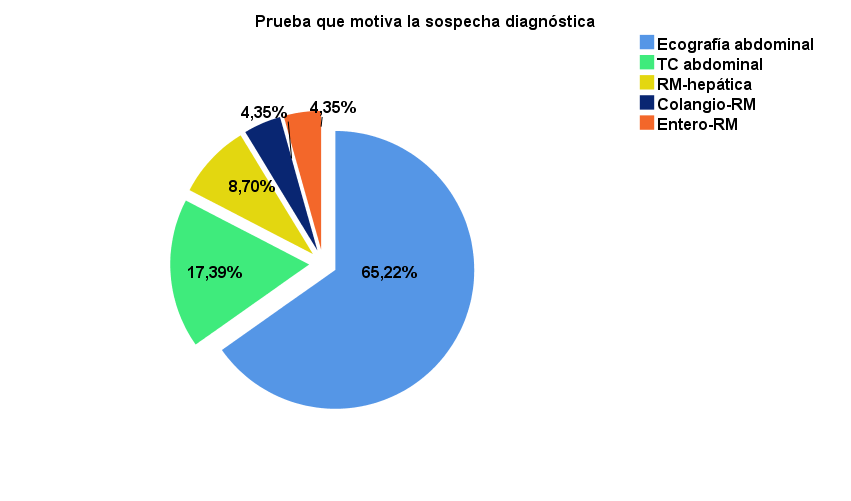
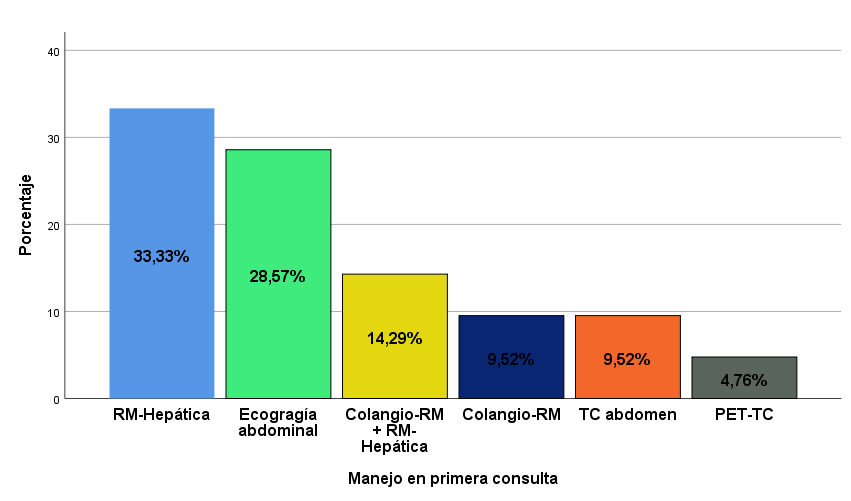
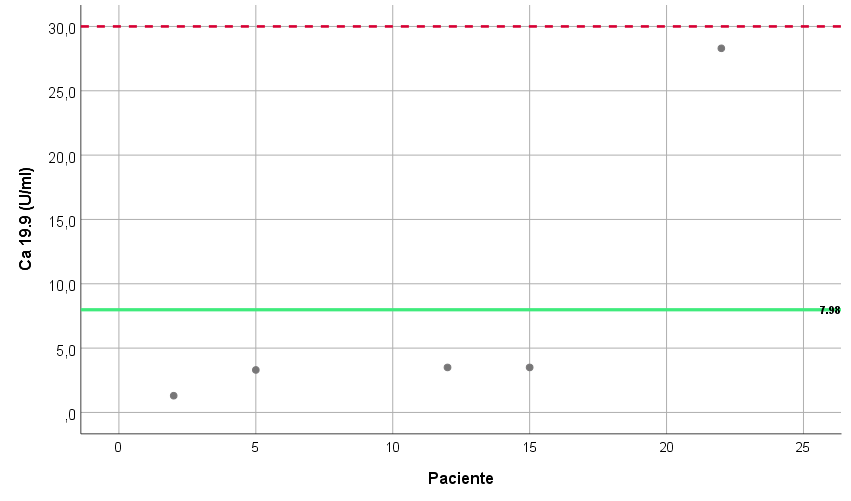
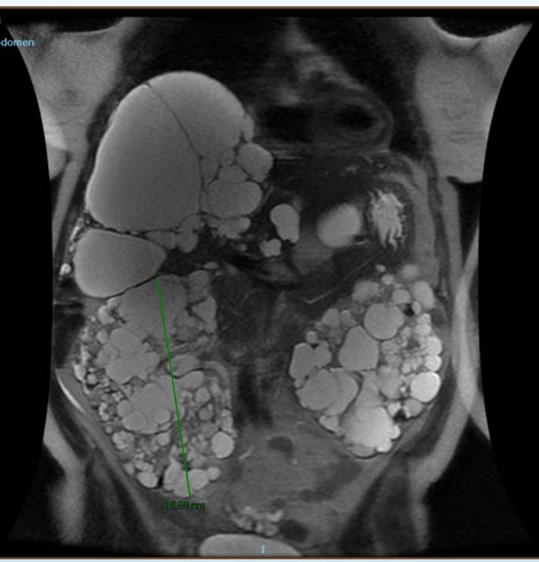
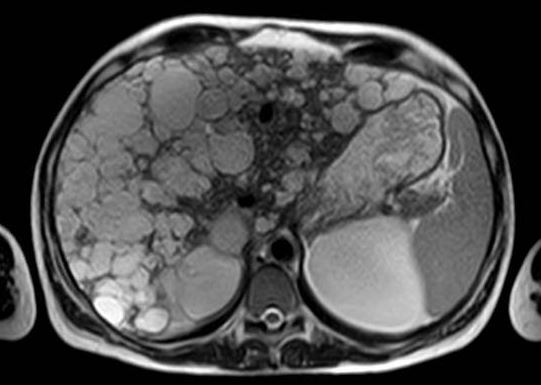
La primera prueba diagnóstica realizada fue la ecografía abdominal en un 65,2%, completándose el estudio diagnóstico con análisis de sangre en todos los casos y RMN-hepática (33,3%) (Fig. 2-3), si ésta no se había realizado previamente. Se mantuvo un seguimiento en consultas externas en el 73,9%, con una revisión a los 6 meses de media tras la primera valoración, espaciándose posteriormente el seguimiento cada 10 meses, con un tiempo de seguimiento medio de 45 meses. Entre los hallazgos analíticos no se identificó ningún patrón específico. Se realizó un estudio con marcadores tumorales en el 69,6%, de los que el Ca19.9 estaba presente en el 21,7% con unos valores medios de 7,9± 22,3U/ml (Fig. 4).
Durante el seguimiento se realizaron revisiones con análisis de sangre acompañados de pruebas de imagen, la ecografía abdominal en el 52,2% de los casos. No obstante, la RMN se llegaba a repetir hasta en el 21,7% de los pacientes durante el seguimiento.
Conclusiones
La hamartomatosis biliar es una enfermedad con predominio en mujeres, con una presentación en edades medias de la vida (58 años) y habitualmente como un hallazgo incidental en pruebas de imagen. La prueba diagnóstica que motiva la sospecha suele ser la ecografía abdominal, que posteriormente es confirmada mediante estudios de RMN. El seguimiento realizado en la mayoría de los casos es con ecografía abdominal y análisis de sangre con visitas de revisión cada 10 meses aproximadamente.
CP-055. ANILLO DE KAYSER FLEISCHER Y ENFERMEDAD DE WILSON. CASO PRAGMÁTICO DEL BENEFICIO DEL MANEJO MULTIDISCIPLINAR EN NUESTRA ESPECIALIDAD
Tenorio González E
Servicio Aparato Digestivo. Hospital Comarcal de la Axarquía, Vélez-Málaga.
Palabras clave: kayser fleischer, wilson, multidisciplinar.
Introducción
La enfermedad de Wilson se manifiesta por la disminución de la ceruloplasmina, proteína transportadora de cobre, y como consecuencia se genera acúmulo del metal en el cerebro, hígado y otros órganos, produciendo toxicidad y los síntomas que definen la enfermedad. El diagnóstico precoz tras cualquiera de ellos es imprescindible para mejorar el pronóstico y la calidad de vida del paciente.
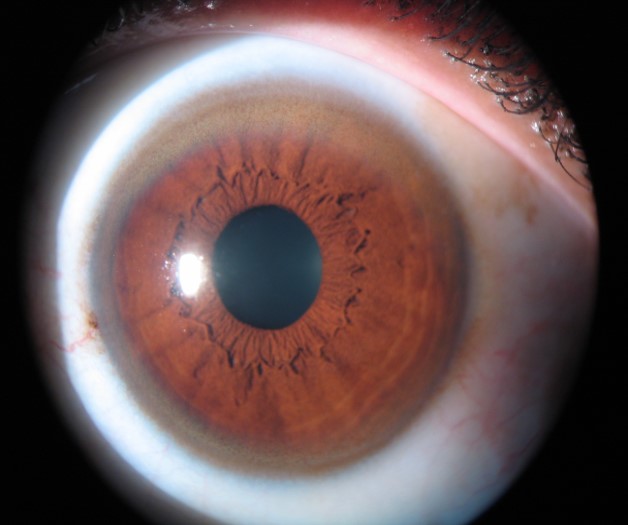
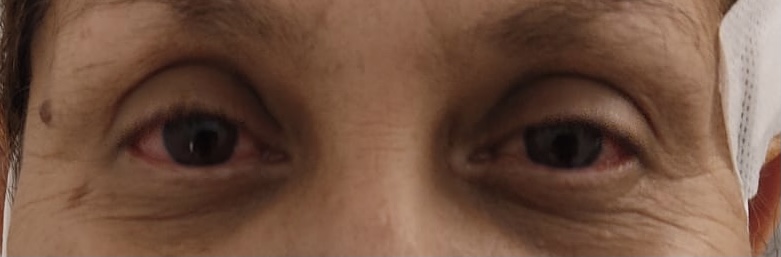
El anillo de Kayser-Fleischer es un signo ocular, típicamente bilateral y de color verdoso parduzco/dorado, producido por el acúmulo de cobre en la córnea. Está presente en el 90% de los pacientes con síntomas neuropsiquiátricos, y puede aparecer en otras patologías digestivas, como la cirrosis biliar primaria, hepatitis crónica activa, y colestasis intrahepáticas.
Caso clínico
Mujer de 27 años, estudiada por cambios en el carácter, consistentes en inhibición y anhedonía en los últimos 3 años, comenzando finalmente con temblor ocasional distal de extremidades y desequilibrio, que evolucionan a disartria y dificultad para la marcha, por lo que es derivada a consulta de Neurología.
A la exploración destacó sonrisa sardónica, hipofonía, bradicinesia de manos y marcha lenta con poco braceo. Ante la sospecha de enfermedad de Wilson, fue derivada a Oftalmología, donde identifican el anillo de Kayser-Fleischer bilateral mediante lámpara de hendidura.
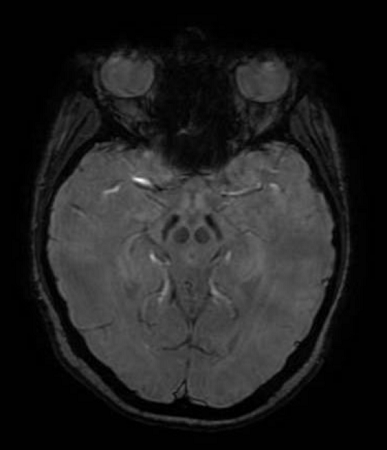
En Resonancia Magnética craneal se describe necrosis de la cabeza de los caudados y de los lenticulares. Los núcleos pálidos presentaron aumento de señal en T1.
En la analítica sanguínea, se expresan niveles de ceruloplasmina en suero bajos (3 mg/dL),cobre sérico bajo (21mmol/Dl) y cobre elevado en orina de 24 horas (207mg/dl).
En ecografía abdominal se apreció un hígado heterogéneo y esplenomegalia.
Mediante análisis genético se confirmó el diagnóstico de Enfermedad de Wilson, tratándose con D-penicilamina 250 mg/6h y piridoxina 300mg/día con buena tolerancia. El cuadro neurológico mejoró notablemente a los dos meses de iniciar el tratamiento.
Discusión
La identificación del anillo de Kayser-Fleischer en pacientes que presentan un cuadro neurológico no filiado, comúnmente confundido con alteraciones psiquiátricas, junto con alteraciones en la imagen neurológica y función hepática, constituye una herramienta fundamental en el diagnóstico de la enfermedad de Wilson.
Puede constituir la manifestación inicial de la enfermedad, siendo el papel del oftalmólogo crítico en el diagnóstico precoz. Además, la densidad del anillo se correlaciona con la duración de los síntomas, y su desaparición refleja en general una buena respuesta terapéutica a los fármacos quelantes o al trasplante hepático.
No siempre el paciente acude derivado inicialmente a la consulta de Digestivo y, de hecho, la sintomatología digestiva puede ser la última en manifestarse clínicamente, bien como insuficiencia hepática aguda o, más comúnmente, cirrosis. Es por ello especialmente importante la colaboración entre especialistas ante casos sospechosos, ya que el tratamiento precoz mejora su morbimortalidad, ralentizando su progresión.
CP-056. ANOREXIA NERVIOSA COMO CAUSA DE HEPATITIS AGUDA
Pérez Ramírez A1, López Bueno I1, Orti Cuerva F2, Sousa Martin JM1, Lara Romero C1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 2UGC Medicina Interna. Complejo Hospitalario Regional Virgen del Rocío, Sevilla.
Palabras clave: anorexia nerviosa, hepatitis aguda, fallo hepático.
Introducción
La anorexia nerviosa (AN) es un trastorno de la conducta alimentaria que se caracteriza por una pérdida autoinducida y significativa de peso asociada a una distorsión de la imagen corporal. Se asocia a múltiples complicaciones médicas relacionadas con la pérdida de peso y la desnutrición, incluyendo alteración de la función hepática.
Caso clínico
Se presenta el caso de una mujer de 19 años diagnosticada de AN desde marzo de 2021 con conductas restrictivas y atracones ocasionales, seguidos de conductas compensatorias (vómitos autoinducidos y ejercicio físico extremo). Índice de masa corporal (IMC) de 12 y amenorrea secundaria.
Acude a urgencias por astenia y bradipsiquia. Analíticamente se constató alteración de la función hepática, con hipertransaminasemia de patrón citolítico (AST 6280 U/L y ALT 5900 U/L), hiperbilirrubinemia (5.4 mg/dL) y ligero aumento de INR (1.33). Ausencia de datos de encefalopatía hepática. Dado el diagnóstico de hepatitis aguda y el estado grave de desnutrición se decidió ingreso hospitalario.
En el ingreso se descartó etiología vírica (VHA, VHB, VHC, VHE) y el estudio de autoinmunidad fue negativo. El metabolismo del hierro y cobre eran normales. La paciente afirmaba consumo muy ocasional de paracetamol e ibuprofeno, siendo los niveles sanguíneos de paracetamol normales. Seguía tratamiento con paroxetina y metilfenidato, aunque la probabilidad de hepatotoxicidad era muy baja tras consultar la bibliografía. Negaba consumo de tóxicos, así como productos de herboristería. Se realizó una ecografía abdominal que descartó origen biliar y evidenció normalidad del parénquima hepático, así como del estudio Doppler.
La paciente presentó durante el ingreso una pancitopenia por hipoplasia medular secundaria a la AN.
Tras soporte nutricional adecuado la función hepática y la pancitopenia mejoraron, trasladándose la paciente a su centro de referencia para continuar con el mismo. Al alta los parámetros de función hepática se habían normalizado.
Discusión
La elevación de transaminasas en un fenómeno común que afecta hasta el 60% de los pacientes con AN. El mecanismo fisiopatológico se desconoce, pero se ha relacionado con la deshidratación secundaria a la hipovolemia e hipotensión, la hipoxemia por hipoperfusión, acúmulo de grasa y estrés oxidativo. Se han descrito casos excepcionales de hepatitis aguda grave y fallo hepático asociados a la AN cuyo origen podría deberse a fenómenos de autofagia provocados por la inanición. La severidad del daño hepático es proporcional al estado de desnutrición. Aquellos con un IMC<13 kg/m2 parecen tener un mayor riesgo de hepatitis aguda, cuyo tratamiento se basa en un adecuado soporte nutricional.
CP-057. ASCITIS E HIDROTÓRAX: NO SIEMPRE ES LO QUE PARECE
Calderón Chamizo M1, Maraver Zamora M1, Ternero Fonseca J1, Naranjo Pérez A1, Quirós Rivero P1, Jaloud Saavedra E2
1Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Juan Ramón Jiménez, Huelva. 2Servicio Medicina Familiar y Comunitaria. Hospital Comarcal Infanta Elena, Huelva.
Palabras clave: síndrome de meigs, ascitis, hidrotórax .
Introducción
El síndrome de Meigs es una entidad infrecuente definida como la presencia de ascitis e hidrotórax asociado a tumores ováricos benignos (como los fibromas ováricos, tecomas, entre otros).
Caso clínico
Mujer de 73 años, con antecedentes de hipertensión arterial y dislipemia, refiere disnea a moderados esfuerzos, astenia y tos irritativa de un mes de evolución, acompañada de un aumento del perímetro abdominal. A la exploración, destaca la presencia de oleada ascítica. En radiografía de abdomen, no se muestran hallazgos significativos; sin embargo, en radiografía de tórax destaca la presencia de derrame pleural derecho significativo. Ante la sospecha de hepatopatía vs origen neoplásico, se realiza toracocentesis compatible con exudado sin evidencia de células neoplásicas en citología. Continuamos con el estudio de extensión realizando TAC de Tórax-Abdomen-Pelvis que descarta la presencia de nódulos pulmonares y datos de hipertensión portal; no obstante, describe una tumoración ovárica izquierda de 9 cm (sin poder descartar malignidad) con ascitis y gran derrame pleural derecho. Ampliamos estudio con una resonancia pélvica para una mejor caracterización de la lesión, que muestra hallazgos superponibles.
El Ca 125 se encontraba elevado (198mg/dl).
Ante la presencia de ascitis, hidrotórax derecha y lesión anexial, se sospecha un síndrome de Meigs/PseudoMeigs.
Se procede a la extirpación de la lesión obteniéndose el diagnóstico de fibroma ovárico tras el estudio anatomopatológico.
Tras la resección de la misma, tanto la ascitis como el derrame pleural derecho que presentaba la paciente se resolvieron, quedando asintomática.
Discusión
El síndrome de Meigs presenta una sintomatología muy inespecífica, desde disnea y astenia hasta molestias abdominales e irregularidad menstrual.
Su fisiopatología es aún desconocida. Rara vez asocian elevación del Ca 125 y, aunque ocasionalmente se eleva sin traducción maligna, el 80% suelen tener enfermedad diseminada. Las elevaciones de este marcador, aunque puede deberse a coexistencia de endometriosis, peritonitis o cirrosis, probablemente en algunos casos como el nuestro, se deba a la inflamación y secreción de las células del mesotelio, como ocurre en el sd. PseudoMegis (del que diferenciaremos dado que se asocia a enfermedad maligna).
El diagnóstico de confirmación lo obtendremos una vez analicemos la pieza quirúrgica. El fibroma ovárico es el tumor que con más frecuencia se asocia a dicha triada, aunque tan solo está presente en el 1% de ellos.
Destacar que aunque emula una enfermedad maligna, tiene un pronóstico excelente y tanto la ascitis como el derrame pleural (más frecuentemente de localización derecha) se resuelven tras la resección del tumor.
CP-058. ASOCIACIÓN DEL MIRNA-423-5P CON EL DAÑO HEPÁTICO EN UN MODELO PRECLÍNICO DE ENFERMEDAD HEPÁTICA METABÓLICA.
Montero Vallejo R1, Gallego Durán R1, López Bermudo L2, Gato S1, García Fernández V1, Maya D1, Muñoz Hernández R1, Gil Gómez A1, Rojas A1, Escudero B2, Cardenas García A2, Santos A3, Rodrigues C3, Martín Bermudo F2, Robles Frías MJ4, Ampuero J5, Romero Gómez M5
1Laboratorio Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 2Laboratorio Endocrinología y Nutrición. Centro Andaluz De Biología Molecular y Medicina Regenerativa (CABIMER), Sevilla. 3Grupo Cellular Function and Therapeutic Targeting. Research Institute for Medicines, Lisboa. 4Servicio Anatomía Patológica. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 5UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla.
Palabras clave: mirnas, nafld.
Introducción
La expresión del microRNA-423-5p en modelos animales bajo dietas ricas en grasas (HFD) varía con el daño hepático.
El objetivo principal de este estudio fue explorar el potencial uso diagnóstico del miRNA-423-5p como biomarcador no invasivo en un modelo de enfermedad hepática metabólica con dieta rica en grasas suplementada con metionina y deficiente en colina (CDA-HFD).
Material y métodos
Cuarenta y cuatro ratones C57BL/6J se incluyeron y se aleatorizaron en dos dietas diferentes: dieta control durante (n=19) y dieta alta en grasas suplementada con metionina al 0,1 % y deficiente en colina durante 16 semanas (n=25). Dentro de ambos grupos, un brazo del estudio incluyó animales tratados con sondas antisentido basadas en morfolinos contra un microRNA de interés relacionado con la enfermedad hepática metabólica (miRNA-X-3p). Por otro lado, se exploró un grupo control para evaluar la especificidad de este tratamiento antisentido (miRNA-X-5p). La expresión hepática del microARN miR-423-5p se evaluó en todos los ratones. Los hallazgos histopatológicos fueron evaluados por un patólogo que desconocía la procedencia de las muestras describiéndose Kleiner y NAS score. Se utilizó SPSS v24.0 para los análisis estadísticos.
Resultados
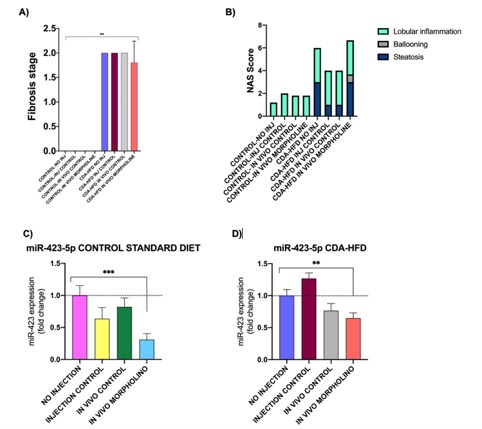
En este estudio, observamos niveles elevados de ALT en todos los ratones CDA-HFD con respecto a los controles, especialmente altos en el grupo miRNA-X-3p (195,86±25,38 vs 45,76±14,71 UI/mL; p=0,002). Además, se observó fibrosis hepática en ratones CDA-HFD vs controles (Figura 1A); así como un NAS score superior (Figura 1B). En este estudio se encontró que el NAS score y la fibrosis hepática estaban correlacionadas (r=0,868; n=44; p=0,0001). Después del sacrificio, se observó una disminución del miRNA-423-5p en los ratones a los que se le inyectó nuestro morfolino de interés (miRNA-X-3p) frente al grupo de control de dieta (fold change 0,31±0,09 vs 1±0,15; p=0,005) (Figura 1C). De manera similar, en el grupo CDA-HFD también se observó una disminución en la expresión de este microARN en el grupo de morfolinos en comparación con los controles (fold change 0,64 ± 0,08 vs 1 ± 0,09; p = 0,021) (Figura 1D).
Figura 1
Fibrosis hepática y NAS Score en el modelo preclínico en ambas dietas (1A, 1B) y fold change del microRNA 423-5p en un modelo animal con dos intervenciones dietéticas diferentes: dieta control (1C) y dieta alta en grasas deficiente en colina, y suplementada al 0,1% de metionina durante 16 semanas (1D)
Conclusiones
El microRNA-423-5p ser encontró disminuído en el modelo animal (tanto en el grupo control como en el de CDA-HFD) cuando se inyectó nuestro morfolino y se comparó con los controles. Se encontró que la expresión de este miRNA disminuía en paralelo con el aumento de la lesión hepática evaluada por el NAS Score.
Por lo tanto, las modificaciones epigenéticas pueden considerarse un objetivo terapéutico potencial en la enfermedad hepática metabólica.
CP-059. ATROFIA SEGMENTARIA DEL HÍGADO: UNA ENTIDAD INFRECUENTE, CON APARIENCIA RADIOLÓGICA DE MALIGNIDAD.
Lecuona Muñoz M, Tendero Peinado C, Rodríguez Gomez VM, Redondo Cerezo E, Valverde López F
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: elastosis nodular.
Introducción
La filiación de una lesión hepática incidental supone un reto diagnóstico cada vez más habitual debido a la implementación de las pruebas de imagen en la práctica clínica diaria.
Caso clínico
Mujer de 50 años con antecedentes de Colangitis Aguda de repetición, que ingresa de forma programada para colocación de prótesis biliar metálica. Tras el procedimiento, la paciente desarrolla una pancreatitis postCPRE con evolución tórpida, realizándose TC abdominal (Figura 1). Mediante esta técnica se identifica de forma incidental una lesión nodular hipodensa de 15 mm en el segmento 6-7 del hígado, visible únicamente en fase portal. Considerando el antecedente de Colangitis Aguda de repetición, se sospecha un origen infeccioso y se inicia tratamiento antibiótico. La paciente evoluciona favorablemente desde el punto de vista clínico y analítico. Dos meses después se solicita TC de control con hallazgos superponibles al estudio previo. Dada la ausencia de cambios pese a antibioterapia, se descarta etiología infecciosa y se solicita Ecografía con contraste (Figura 2). En esta exploración se visualiza una lesión sólida con captación en anillo tras administración de contraste, compatible con malignidad. Se completa el estudio mediante resonancia magnética nuclear (Figuras 3-4) con hallazgos sugerentes de neoplasia y se realiza BAG para estudio anatomo-patológico. A nivel histológico, se identifica un nódulo esclerosante compatible con atrofia segmentaria en fase de elastosis nodular. Actualmente, se realizan controles ecográficos cada seis meses para valorar evolución, hasta el momento sin cambios a nivel clínico-radiológico.
Figura 1
TC abdominal con contaste donde se objetiva una lesión nodular sólida hipodensa de unos 15 mm localizada en el segmento 6-7 del hígado visible únicamente en fase portal.
Figura 2
Ecografía con contraste. En fase arterial la lesión muestra captación de morfología en anillo en periferia del nódulo. Permanece hipogénica en fases portal y tardía.
Discusión
La atrofia segmentaria del hígado constituye un pseudotumor infrecuente recientemente descrito, caracterizado por una proliferación fibrosa tisular que se genera como consecuencia de un daño vascular. Afecta preferentemente a mujeres (72%) con una edad media de 60 años, y cursa habitualmente de forma indolente. Dada su escasa prevalencia, hasta el momento sólo se dispone de series de casos para su caracterización clínico-radiológica. A nivel histológico, inicialmente se produce un colapso del parénquima con cambios focales y posteriormente se genera un nódulo elastótico con fibrosis densa. Su importancia en la práctica clínica habitual reside en su apariencia sugerente de malignidad, presentando en ocasiones un aspecto superponible al de las lesiones metastásicas en los estudios radiológicos habituales, pese a tener un comportamiento aparentemente benigno.
CP-060. CAMBIO EN EL ABORDAJE TERAPÉUTICO DE PACIENTES CON HEPATOCARCINOMA EN ESTADIO AVANZADO. EXPERIENCIA CON ATEZOLIZUMAB-BEVACIZUMAB EN PRÁCTICA CLÍNICA
MOUHTAR EL HALABI SA, GARCÍA GARCÍA MD, FERNÁNDEZ ÁLVAREZ P, CORDERO RUIZ P, BELLIDO MUÑOZ F, CARMONA SORIA I
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: hepatocarcinoma, inmunoterapia, atezoluzimab-bevacizumab.
Introducción
Evaluar el manejo con terapia sistémica en pacientes con hepatocarcinoma en estadio avanzado desde la aprobación de Atezolizumab-Bevacizumab (AB), así como de estadios más precoces que reciben terapia sistémica.
Analizar las características clínicas de los pacientes que reciben cada una de las opciones terapéuticas, así como la eficacia y seguridad de la combinación Atezolizumab-Bevacizumab en práctica clínica real.
Material y métodos
Estudio observacional, prospectivo, descriptivo, no controlado y unicentro. Se incluyeron todos los pacientes con hepatocarcinoma en estadio avanzado y/o con indicación de terapia sistémica (migración de tratamiento) desde agosto del 2021 hasta septiembre del 2022, coincidiendo con la aprobación de AB en el centro hospitalario.
Resultados
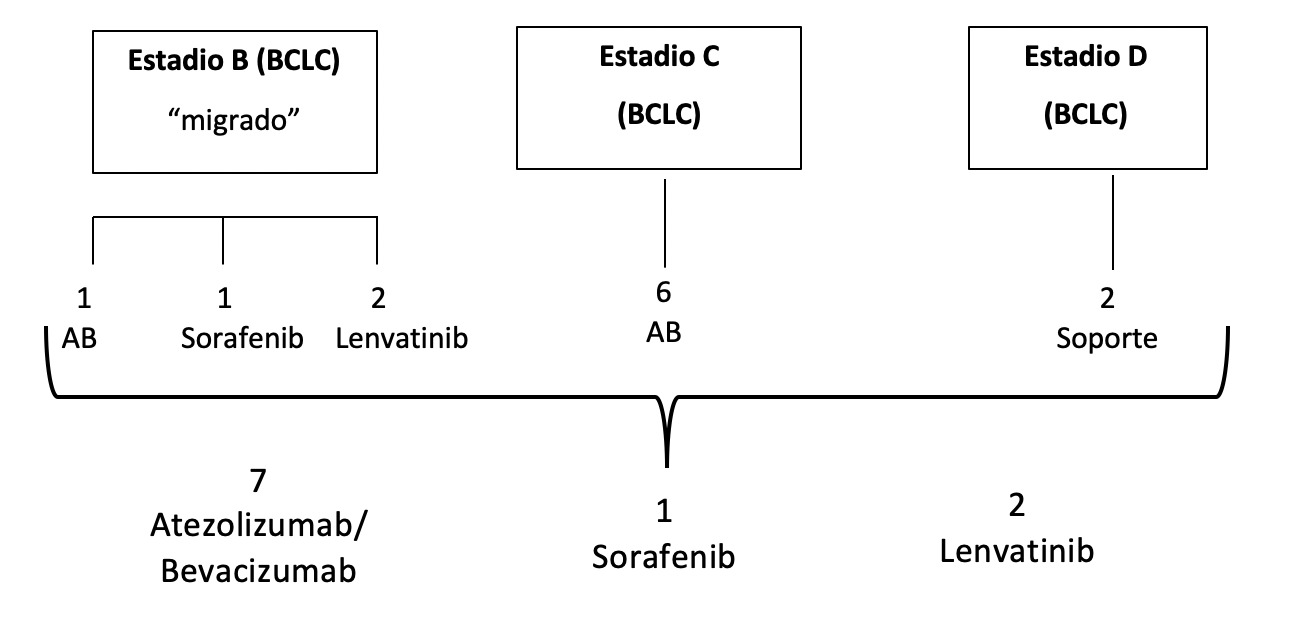
Se analizaron un total de 12 pacientes. En dos de ellos se indicó tratamiento de soporte por comorbilidades. Los 10 restantes recibieron terapia sistémica: 7 con AB, 1 con sorafenib y 2 con lenvatinib (Figura 1).
Figura 1
Distribución de pacientes según estadio de hepatocarcinoma por la BCLC y tratamiento recibido. AB: Atezolizumab-Bevacizumab
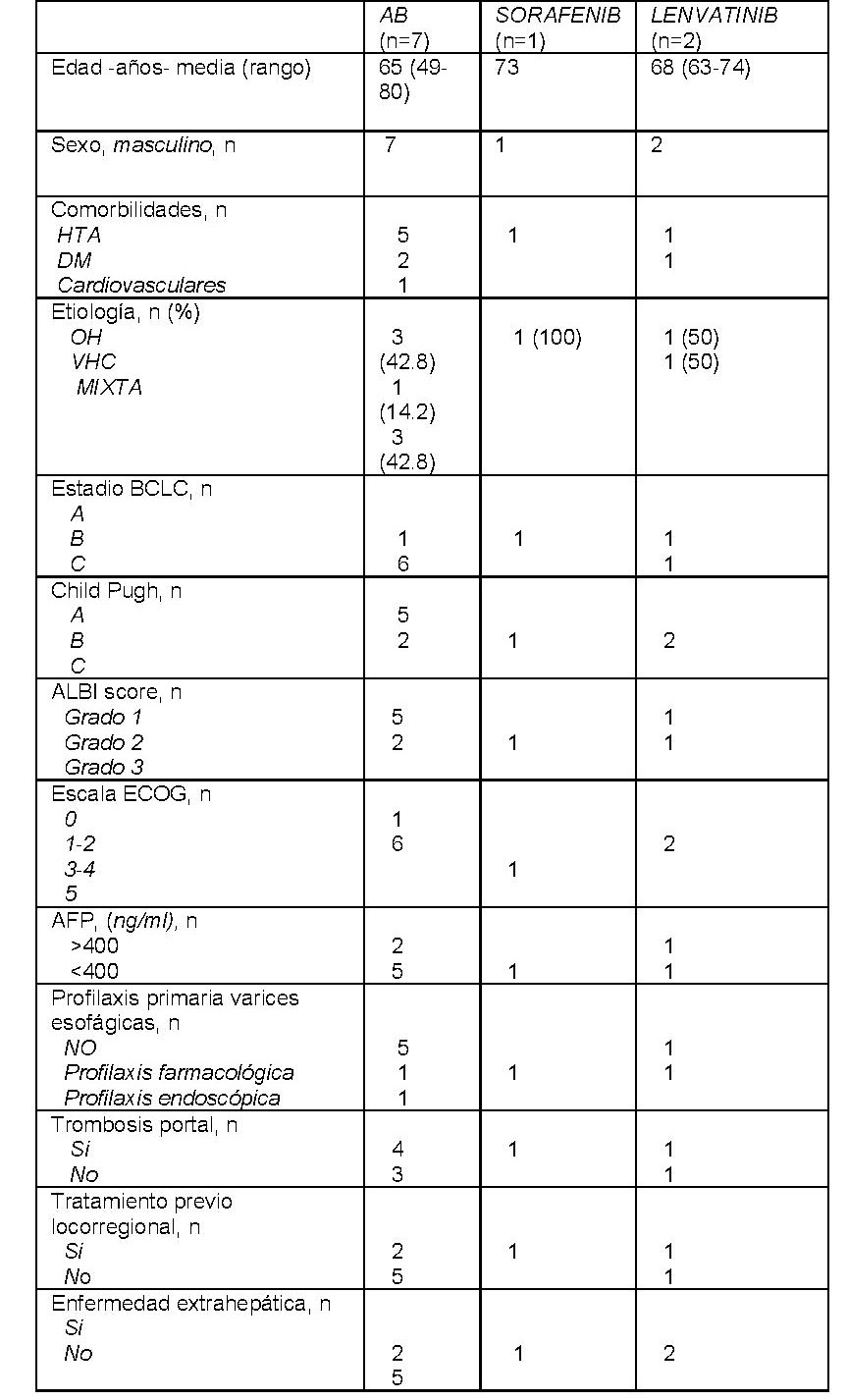
En la tabla 1 se resumen las características demográficas y clínicas de los pacientes incluidos. A destacar en el grupo de AB el alcohol y la infección por el virus de la hepatitis C como causas de hepatopatía mas frecuentes (85.6%). En dos pacientes se migró tratamiento tras fallo previo a terapia locorregional. La mayoría de los pacientes presentaban buena función hepática (Child-Pugh A/ALBI 1) y ausencia de varices gastroesofágicas. El tiempo medio de tratamiento con AB fue de 7,2 (2;14) meses. La respuesta radiológica ha sido evaluada en 5 pacientes, mostrando 2 de ellos progresión, 1 estabilidad y 2 pacientes respuesta, siendo una de ellas completa. Respecto a la seguridad, 5 pacientes desarrollaron efectos adversos leves (2 hipertiroidismo y 3 hipertensión arterial), todos controlados con tratamiento médico. Un paciente desarrolló fracaso renal grave en relación con nefritis tubulointersticial inmunomediada que obligó la retirada del tratamiento. Se suspendió la terapia en dos pacientes por progresión de la enfermedad. Un paciente falleció por descompensación hepática.
Conclusiones
La mayoría de los pacientes con hepatocarcinoma candidatos a tratamiento sistémico han podido realizar tratamiento de primera línea con AB.
En nuestra serie, la tolerancia al tratamiento ha sido aceptable, sin que se hayan producido complicaciones hemorrágicas. La hipertensión arterial y la toxicidad tiroidea inmunomediada ha sido el efecto adverso más frecuente.
CP-061. CARACTERÍSTICAS Y SUPERVIVENCIA DE LOS PACIENTES CON CARCINOMA HEPATOCELULAR EN HISTORIA NATURAL. ESTUDIO DE COHORTES.
González Sánchez MH1, Florez Díaz P1, Garcia Calonge M1, Muiño Dominguez D1, Celada Sendino M1, Castaño García A1, Álvarez Navascués C2, Franco L2, Cadahía Rodrigo V2, González Diéguez ML2, González Parra AC3, Varela M2
1Servicio Aparato Digestivo. Hospital Universitario Central de Asturias, Oviedo. 2Servicio Gastroenterología y Hepatología. Hospital Universitario Central de Asturias, Oviedo. 3Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: carcinoma hepatocelular, tratamiento, historia natural.
Introducción
El carcinoma hepatocelular (CHC) asienta sobre una cirrosis hepática en más del 80% de los pacientes y ésta puede condicionar el inicio y/o mantenimiento de su tratamiento. Asimismo, la comorbilidad puede obligar a hacer una migración en el estadio terapéutico y/o a dejar al paciente en historia natural (sin tratamiento específico para el tumor).
Objetivo: Conocer las características y la supervivencia de los pacientes con CHC en historia natural en nuestro medio.
Material y métodos
Inclusión consecutiva de pacientes con CHC desde 27-ene-15 hasta 27-dic-21 seguidos hasta 31-ene-22, cuyo primer y único tratamiento fue historia natural. Se registraron las variables basales, la razón de no tratamiento y el tiempo de seguimiento (periodo desde el diagnóstico hasta el fallecimiento / fin de seguimiento).
Resultados
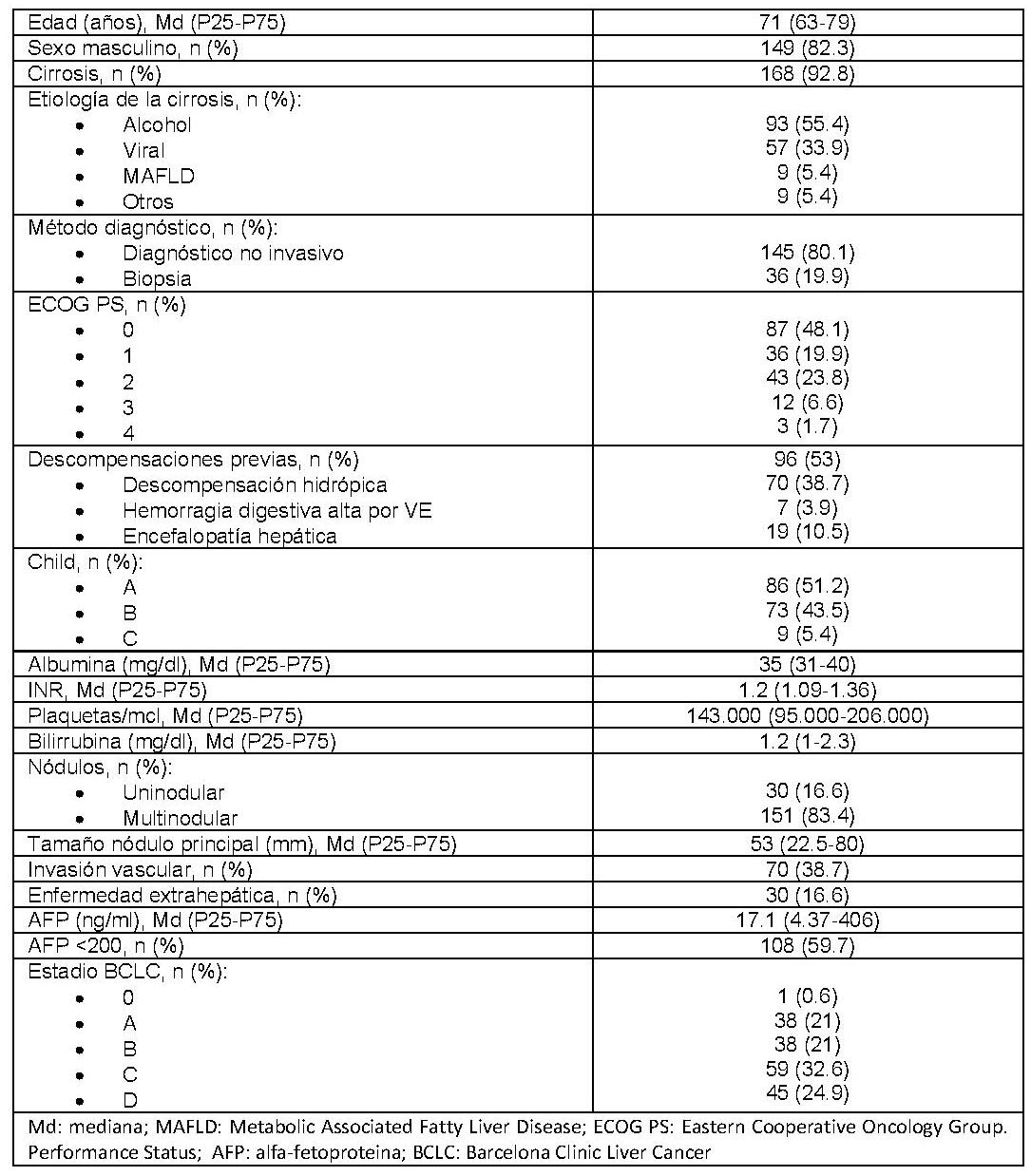
Se registraron 685 pacientes con CHC de los cuales 181 quedaron en historia natural: 82% varones, edad mediana 71 años, 93% con cirrosis, 55% de etiología alcohol vs 34% viral, 54% con descompensaciones previas (73% ascitis). Tras un seguimiento medio de 9,98 meses el 84% había fallecido.
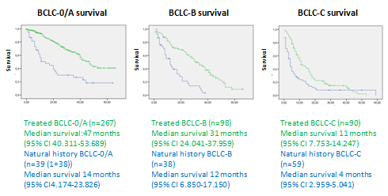
Hubo diferencias estadísticamente significativas en la mediana de supervivencia de acuerdo a 1) síntomas asociados al cáncer [ECOG PS-0: 13 meses, ECOG PS-1: 6 meses, ECOG PS >=2: 2 meses; p <001], 2) estadio tumoral [BCLC 0-A: 14 meses, BCLC-B: 12 meses, BCLC-C: 4 meses, BCLC-D: 2 meses; p <001], 3) AFP basal [AFP < 200 ng/mL: 9 meses vs AFP > = 200: 3 meses; p < 001] y 4) Child-Pugh basal [A:8 meses vs B:4 meses vs C:6 meses; p=0,003].
Las causas más frecuentes por las que no recibieron tratamiento fueron: descompensación de la cirrosis (33%), fragilidad / edad (34%), comorbilidad (21%) y negativa del paciente (11%).
Los factores basales asociados de forma independiente con la supervivencia fueron la ausencia de descompensación previa (HR 0.492, IC 95% 0.331-0.733, p< 0.001), el estadio BCLC (HR 0.389 IC 95% 0.183-0.813, p=0.012) y el diagnóstico en el seno del programa de cribado (HR 1.614, IC 95% 1.058-2.463, p = 0.026).
En pacientes diagnosticados dentro del programa de cribado (n=68), el principal motivo de no recibir tratamiento fue la fragilidad/edad avanzada (26.5%) y la presencia de descompensación de su cirrosis (26.5%).
Conclusiones
En nuestro medio el 26% de los pacientes con diagnóstico de CHC no recibe ningún tratamiento específico. La causa más frecuente de no recibir tratamiento es la fragilidad asociada a la edad seguida de la cirrosis descompensada y de la comorbilidad extrahepática. El estadio BCLC inicial, la ausencia de descompensaciones previas y el diagnóstico en el seno del cribado se asocian de manera independiente con una mayor supervivencia.
La inclusión o el mantenimiento de los pacientes en el programa de cribado de carcinoma hepatocelular debe ser re-evaluado atendiendo a la evolución clínica en cada momento de la enfermedad.
CP-062. CAUSA INUSUAL DE HEPATOMEGALIA: SÍNDROME DE MAURIAC
Martinez Burgos M1, Angulo McGrath I2, Bracho Gonzalez M3, Morales Bermudez AI3
1UGC Aparato Digestivo. Complejo Hospitalario Universitario de Cartagena, Cartagena. 2UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Virgen de Valme, Sevilla. 3UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: hepatomegalia; síndrome de mauriac; enfermedades por depósito.
Introducción
El síndrome de Mauriac se considera la máxima expresión de diabetes tipo 1 con mal control metabólico y se caracteriza por hepatomegalia por depósito de glucógeno, talla baja, hipertransaminasemia, dislipemia y pubertad retrasada. Se trata de una entidad infrecuente y que afecta en mayor grado al sexo femenino. Suele presentarse en la infancia o la adolescencia y es reversible si se consigue un adecuado control glucémico.
Caso clínico
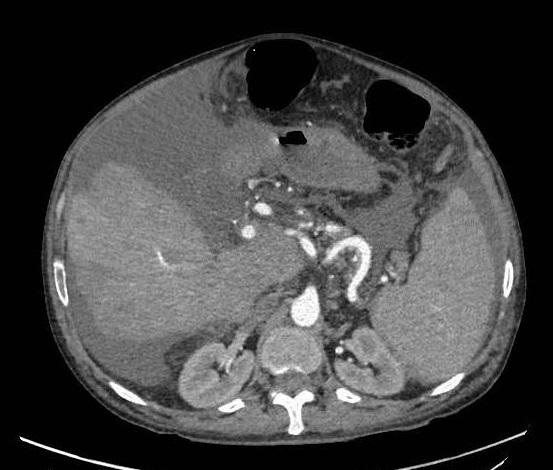
Mujer de 16 años. Antecedentes personales de diabetes mellitus tipo 2 y de nefrolitiasis con cólicos renoureterales. La paciente ingresa en UCI por cetoacidosis diabética con buena evolución posterior. Durante su estancia en planta presenta dolor abdominal en flanco derecho por lo que se decide realizar TC abdominal sin contraste por sospecha de litiasis obstructiva, que se descarta. En TC abdominal informan de hepatomegalia con aumento de la densidad del parénquima hepático sugestivo de enfermedad por depósito (Imagen 1). Solicitan ecografía abdominal que confirma hepatomegalia de 17 cm y descarta patología vascular. Se realiza analítica donde destaca discreta elevación de las transaminasas. Ante estos hallazgos realizan hoja de consulta a digestivo. Revisamos analíticas del paciente, perfil férrico e índice de saturación de transferrina descartan casi por completo hemocromatosis. Disponíamos de varias ecografías abdominales previas de la paciente por su patología renal donde el hígado presentaba tamaño y ecogenicidad normales. Valoramos a la paciente que presentaba excelente estado general por lo que se decidió seguimiento en consulta en 3 meses así como solicitar estudio de hepatopatías y nueva ecografía abdominal, insistiendo en importancia del control glucémico. La paciente acude a consulta 3 meses después con normalización analítica y ecografía abdominal que informa de hígado de tamaño y ecoestructura normal. Estudio de hepatopatías completo negativo.
Discusión
El hallazgo de una hepatomegalia aguda sugestiva de enfermedad por depósito en una prueba de imagen en un paciente joven con diabetes descompensada debe hacernos sospechar de la entidad conocida como Síndrome de Mauriac, donde el hígado aumenta de tamaño debido al depósito de glucógeno. El diagnóstico de confirmación es la biopsia hepática, que debe realizarse en caso de persistencia de las alteraciones en el tiempo a pesar de optimización de controles metabólicos.
CP-063. COLANGIOPATÍA PORTAL, COMPLICACIÓN EXTRAHEPÁTICA DE LA HIPERTENSIÓN PORTAL Y CAUSA POCO FRECUENTE DE COLANGITIS.
Requena De Torre J, Molina Villaba C, De La Cuesta Fernández I, Fernández López R, Jarava Delgado M
UGC Aparato Digestivo. Complejo Hospitalario de Poniente, Ejido, El.
Palabras clave: colangiopatía portal, colangitis, hipertensión portal, .
Introducción
La cavernomatosis portal se define como la presencia de alteraciones vasculares derivadas de la presencia de una trombosis portal crónica. La dilatación tortuosa a nivel de las venas paracoledocianas y epicoledocianas, en su progresión puede derivar en anormalidades colangiográficas definidas como colangiopatía portal.
Caso clínico
Presentamos el caso de un varón de 45 años, oriundo de Guinea Bissau con antecedente personal de infección crónica por virus de la hepatitis B, sin datos de fibrosis hepática, y diagnóstico previo de trombosis portal con cavernomatosis asociada, secundaria a déficit de proteína C y S.
Consulta por clínica de dolor abdominal en hipocondrio derecho, coluria y fiebre. En un primer test destaca hiperbilirrubinemia (8.1mg/dl) mixta, junto elevación de enzimas de citolisis (GOT-AST: 80 U/L, GPT-ALT: 70 U/L) y colestasis (GGT: 118 U/L, FA: 343 U/L).
Durante el ingreso hospitalario, se realiza estudio con colangio-resonancia magnética que identifica cavernomatosis poral ya conocida, condicionando la dilatación de la vía biliar intrahepática y del conducto hepático común.
Ante el diagnóstico de colangitis secundaria a colangiopatía portal se procede a realización de colangiografía retrógrada endoscópica (CPRE) que confirma la dilatación intrahepática y extrahepática con estenosis del colédoco. Se procede, tras esfinterotomía a la colocación de stent plástico biliar para el drenaje. En las horas posteriores, el paciente padece un nuevo episodio de colangitis que condiciona el recambio de prótesis. Concomitante a ello, se realiza gastroscopia con presencia de 4 varices esofágicas que se ligan mediante bandas elásticas. Completado el proceso diagnóstico y terapéutico se procede al alta para continuar seguimiento de manera ambulatoria.
Discusión
Si bien la mayoría de pacientes con esta afección permanecen asintomáticos a pesar de la dilatación del árbol biliar, tanto las malformaciones vasculares, como la propia ectasia pueden condicionar complicaciones, siendo la principal la colangitis derivada de las estenosis o por cálculos biliares de repetición. Por otro lado, como el caso de nuestro paciente, la propia trombosis puede traducirse en complicaciones derivadas de la hipertensión portal como la presencia de varices esofagogástricas.
Tanto en la identificación de la cavernomatosis portal y las alteraciones de la arquitectura biliar, como para descartar otras causas potenciales, la prueba diagnóstica de referencia es la colangiografía mediante resonancia magnética. La realización de CPRE se reserva para el intervencionismo, destinado a garantizar el adecuado drenaje biliar mediante el uso de prótesis y extracción de cálculos cuando sea preciso.
CP-064. CUANDO ES DEMASIADO TARDE: MALFORMACIÓN DE ABERNETHY
Pérez Campos E, Calvo Bernal MDM, Sánchez García O
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: abernethy, shunt portosistémico, hepatocarcinoma.
Introducción
La malformación de Abernethy es una enfermedad congénita que consiste en la persistencia de shunts portosistémicos. Para evitar la aparición de tumores hepáticos, es esencial un seguimiento exhaustivo en estos pacientes, especialmente teniendo en cuenta la gran diversidad de patrones de comportamiento radiológico, y el peligro que ello conlleva.
Caso clínico
Paciente varón de 38 años que desde la adolescencia comienza estudio de hipertransaminasemia y colestasis, siendo diagnosticado de malformación de Abernethy tipo Ib, con agenesia de la vena porta y shunt con drenaje de la circulación venosa portal hacia la vena renal. Inicia seguimiento, conservando buena función hepática, sin hipertensión portal.
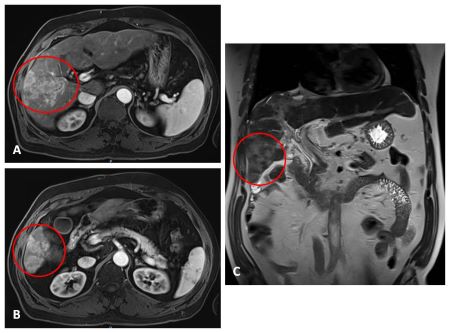
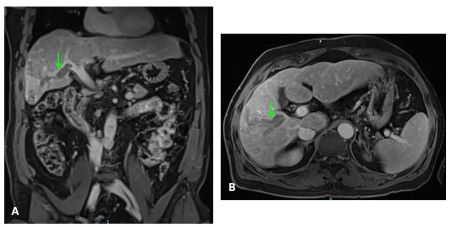
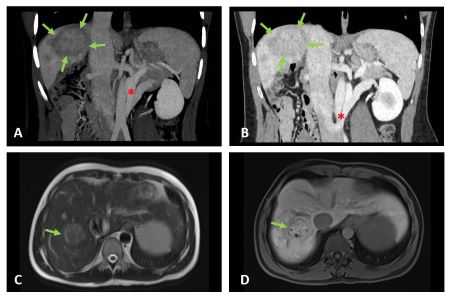
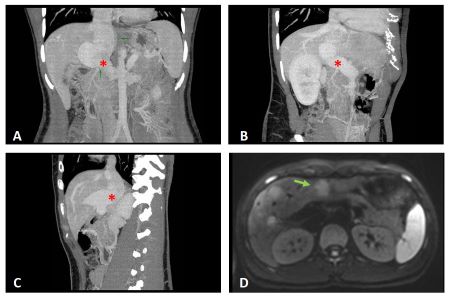
En la última resonancia se detectan lesiones hepáticas inespecíficas (interpretadas como nódulos de regeneración), además de una LOE pequeña con comportamiento vascular compatible con hepatocarcinoma (figura 1), confirmado histológicamente. Tras evaluación multidisciplinar, dado que la función hepática se encuentra mantenida, se decide realizar radiofrecuencia.
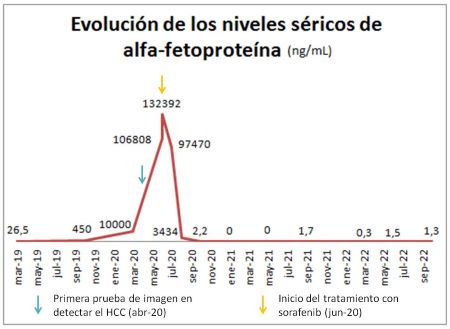
Cuatro meses después (y una semana antes de la sesión de radiofrecuencia) se detecta elevación desproporcionada de alfafetoproteína. Una segunda analítica corrobora los valores (>30.000 ng/ml), y un angioTC confirma la sospecha de progresión tumoral, describiendo un crecimiento muy significativo de la lesión que ya ocupa gran parte del parénquima y otras múltiples lesiones nodulares de nueva aparición, sugiriendo multicentricidad (figura 2). Además, se objetiva enfermedad pulmonar metastásica. Dada la progresión tumoral brusca e imparable, se desestima tratamiento curativo, iniciando en su lugar terapia sistémica.
Discusión
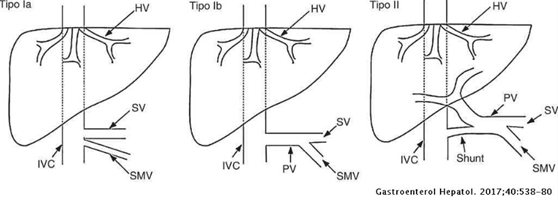
En el síndrome de Abernethy tipo I se produce agenesia portal, y con ello la desviación del 100% del que sería su flujo hacia la vena cava inferior (o renales), con formación o no de una confluencia venosa de drenaje portal antes de su desembocadura en la circulación sistémica (tipos Ib y Ia, respectivamente). En cambio, en el tipo II sí existe vena porta, aunque parte del flujo es desviado por un shunt extrahepático (figuras 3 y 4).
Figura 3
Extraído de Martín-Llahí et al. Esquema de los tipos de malformación de Abernethy descritos. En los tipos I existe agenesia de la vena porta intrahepática, mientras que en el tipo II hay vena porta pero un gran porcentaje del flujo portal bypasea el hígado por medio de un shunt.
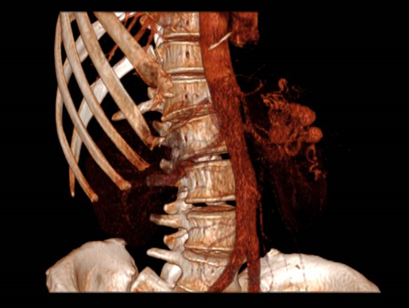
Figura 4
Reconstrucción virtual de la anatomía de nuestro paciente (tipo Ib). Se observa la presencia de una red de colaterales en la circulación esplácnica, y cómo el drenaje de las mismas recae sobre la vena renal derecha a través de un shunt, sin existencia de vena porta.
Dado el aumento del flujo arterial compensatorio y, con ello, una sobreexposición a factores de crecimiento, una de las posibles complicaciones es la degeneración hepatocelular, siendo el hepatocarcinoma su máxima expresión. Pero, puesto que existe alteración de los flujos arteriales y venosos, estos no siempre muestran comportamiento radiológico típico, por lo que la biopsia y el seguimiento exhaustivo de lesiones parenquimatosas inespecíficas resultan esenciales. Probablemente, este hecho explique la abrupta progresión radiológica en nuestro paciente, pudiendo haber llegado a infraestimar la enfermedad maligna en un primer momento.
CP-065. DÉFICIT DE ALFA-1-ANTITRIPSINA COMO CAUSA INFRECUENTE DE CIRROSIS HEPÁTICA
De La Cuesta Fernández I, Molina Villalba C, Requena De Torre J, Gallego Rojo FJ
Servicio Aparato Digestivo. Complejo Hospitalario de Poniente, Ejido, El.
Palabras clave: déficit aat, cirrosis.
Introducción
El déficit de alfa-1-antitripsina es una enfermedad hereditaria poco frecuente que se caracteriza por unos bajos niveles en sangre de dicha proteína. Puede producir daño pulmonar ocasionando enfisema y además causa de hepatopatía hepática crónica.
Caso clínico
Varón de 67 años, HTA y DM-2. Sin consumo de alcohol habitualmente. Ingreso por mareo y desorientación. Epigastralgia y vómitos en posos de café y melenas 48 horas antes. Taquicardia y a la exploración destacaba encefalopatía grado III y hepatomegalia.
Analíticamente glucosa 263, sodio 133, urea 168, creatinina 1.65, bilirrubina total 7 (directa 2.1, indirecta 4.9), GOT 67, GPT 53, Leucocitos 20.900, Hb 9.5, VCM 108, TP 24 %, INR 2.8, Fibrinógeno 96. Hemocultivos y urocultivos negativos.
Ecografía abdominal informa hígado cirrótico (no conocido) y ascitis moderada con datos de hipertensión portal. EDA con varices gástricas aisladas en fundus (VGA-1).
Buena respuesta al tratamiento conservador durante el ingreso con cese del sangrado de forma autolimitada y normalización de la función renal. Ceftriaxona empírica durante 5 días e inicio de betabloqueante como profilaxis secundaria de varices.
Estudio etiológico con virus hepatotropos, autoinmunidad y estudio genético HFE negativos y déficit de Alfa-1-antitripsina: 74 mg/dL (90-200) con fenotipo MZ.
Tras unos meses, vuelve a acudir a Urgencias por similar clínica. Nueva EDA que objetiva VGA-1/VEG-2 con signos de predictivos de sangrado. Embolización transarterial de varices con colocación de TIPS posterior. Tras unas semanas nuevo episodio de hematemesis, encefalopatía grado IV, esta vez con shock hemorrágico debido a HDA por ulcus bulbar Ib. Doble escleroterapia con adrenalina y etoxiesclerol y colocación de hemoclip. Ingreso en UCI con fracaso multiorgánico y posterior exitus.
Discusión
- El déficit de alfa-1-antitripsina surge de mutaciones en el gen que codifica la AAT (SERPINA1). Principalmente es causa de enfisema pulmonar y a nivel hepático condiciona un acúmulo de AAT que provoca estrés metabólico en el hepatocito y puede llevar a cirrosis o incluso tumores hepáticos.
- El diagnóstico se establece por una demostración de AAT < 100mg/dL junto con un estudio genético con variante genética compatible, la mayoría heterocigosis MZ, SZ u homocigosis ZZ.
- No se ha identificado ningún tratamiento específico para la afectación hepática en adultos. El manejo se basa en medidas de prevención o reducción de complicaciones derivadas de la enfermedad hepática crónica como ascitis, hemorragia por varices o encefalopatía. El trasplante hepático es una opción para aquellos en un estadio terminal de la enfermedad.
CP-066. DÉFICIT DE ORNITINA TRANSCARBAMILASA: UNA INDICACIÓN INFRECUENTE DE TRASPLANTE HEPÁTICO
León Sanjuan GF, Aguilar Martínez JC, Hernani Alvarez JA, Mateos Millan D
Servicio Aparato Digestivo. Hospital de Especialidades de Jerez de la Frontera, Jerez de la Frontera.
Palabras clave: ornitina transcarbamilasa, hiperamonemia, trasplante hepático .
Introducción
El déficit de ornitina transcarbamilasa (OTC) es un trastorno hereditario que afecta al ciclo de la urea, resultando en un incremento de niveles de amonio en sangre. Se manifiesta principalmente con sintomatología neurológica y su curso puede llegar a ser fatal si no se alcanza el diagnóstico con premura y se instaura el tratamiento adecuado.
Caso clínico
Mujer de 15 años, diagnosticada de déficit de OTC al nacimiento, que presenta en los últimos meses episodios de cefalea, comportamiento errático y disminución del nivel de conciencia, a pesar de realizar dieta restrictiva en proteínas y tratamiento con arginina, benzoato y fenilbutirato de sodio. En los análisis de sangre destaca únicamente una hiperamonemia, con función hepática normal. Tras valoración por Neurología y Salud Mental, que descartan patología por su parte, se propone valoración de trasplante hepático. Se realiza estudio pretrasplante hepático, sin contraindicaciones, y es incluida en lista de espera activa. En el postrasplante inmediato presenta disfunción grave del injerto, constatándose en ecografía doppler abdominal una trombosis completa de la arteria hepática, con necesidad de retrasplante urgente, que transcurre sin complicaciones. Desde entonces se mantiene clínicamente asintomática, sin incidencias durante su seguimiento posterior en consulta.
Discusión
El déficit de OTC es una enfermedad infrecuente de herencia ligada al cromosoma X. Se trata del trastorno del ciclo de la urea más común, que se caracteriza por interferir en la detoxificación de desechos de nitrógeno y en la biosíntesis de arginina endógena, lo cual resulta en un incremento en las concentraciones de amonio en sangre. Habitualmente la forma grave, por deficiencia completa, se presenta durante el periodo neonatal, mientras que la deficiencia parcial suele detectarse fuera del mismo. Como consecuencia de la hiperamonemia estos pacientes pueden desarrollar trastornos neurológicos o incluso la muerte si no se instaura tratamiento, el cual se basa inicialmente en una dieta restrictiva en proteínas. En casos seleccionados, sobre todo aquellos con evolución desfavorable a pesar del tratamiento conservador, el trasplante hepático es la alternativa de elección para prevenir el acúmulo de amonio, ya que la principal fuente de enzimas del ciclo de la urea es el hígado. En cuanto al pronóstico, la supervivencia a largo plazo de los pacientes que se trasplantan con esta indicación es mayor al 90%, siendo el único tratamiento que controla completamente la hiperamonemia grave causada por la deficiencia de esta enzima.
CP-067. DEL DICHO AL HECHO, HAY UN TRECHO: LA IMPORTANCIA DEL ESTUDIO HISTOLÓGICO DEL HEPATOCARCINOMA.
Carrillo Cubero B1, Ortiz Chimbo DS1, Valdivia Krag C1, Leiva-Cepas F2, Costán Rodero G1, Poyato González A1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba. 2UGC Anatomía Patológica. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: hepatocarcinoma, fibrolamelar, histología.
Introducción
EL hepatocarcinoma convencional (CHC) es una neoplasia primaria que se asocia entre un 60-90% a cirrosis hepática, siendo infrecuente su presentación sobre hígado sano. Cuando sucede, el diagnóstico diferencial debe hacerse con su variante fibrolamelar (CHC-FL), principalmente en personas jóvenes.
Caso clínico
Varón de 31 años sin antecedentes de interés, que consulta por dolor en hipocondrio derecho, náuseas, vómitos y pérdida de 8 kilogramos de peso en tres meses. A la exploración presentaba dolor a la palpación y sensación de masa a dicho nivel.
Presentaba discreta elevación de enzimas hepáticas, serologías virales hepáticas negativas y alfa-fetoproteína normal. En la ecografía abdominal, se objetivó una masa sólida, vascularizada, delimitada, con una zona central hiperecogénica con calcificaciones, que desplazaba estructuras vasculares y ocupaba los segmentos posteriores del lóbulo hepático derecho, sugestiva de neoplasia primaria hepática.
La Resonancia Magnética (RM) dinámica de hígado identificó una masa de 13x11 cm de diámetro en segmentos VI y VII hepáticos, en contacto con el polo superior renal derecho, cava intrahepática y porta derecha; sin signos de infiltración vascular, asentando sobre parénquima hepático sano, sugestivo de CHC-FL. El estudio de extensión fue negativo.
Se decidió hepatectomía derecha. En los hallazgos quirúrgicos, dicha tumoración comprometía los segmentos V a VIII hepáticos, rompía la superficie hepática e infiltraba la glándula suprarrenal, musculo esquelético y tejido adiposo. La biopsia fue compatible con CHC moderadamente diferenciado con invasión de glándula suprarrenal y grasa perirrenal derechas pT4 (8 Ed. AJCC).
Dados los hallazgos, se inició tratamiento con Atezolizumab y Bevacizumab.
Figura 1
RM hepática . Corte Coronal. Masa hepática de 13x11 cm en lóbulo derecho con área central de baja señal y realce heterogéneo en la periferia lesional.
Figura 2
RM hepática. Corte axial. Masa hepática de 13x11 cm en lóbulo derecho con área central de baja señal y realce heterogéneo en la periferia lesional.
Discusión
El diagnóstico de CHC, generalmente sobre hígados cirróticos, se basa en técnicas de imagen dinámicas, destacando el hiperrealce en fase arterial y lavado precoz en fase venosa. El CHC-FL suele aparecer en personas jóvenes con hígado sano, siendo habitual lesiones grandes, heterogéneas, con cicatriz central (65-70% de los casos), presencia de septos fibrosos y calcificaciones. En ambos casos se suele obviar la confirmación histológica. En nuestro caso, las pruebas de imagen eran características de CHC-FL, planteando directamente el abordaje quirúrgico. Sin embargo, los hallazgos histológicos demostraron la presencia de un CHC convencional. Una biopsia hepática previa podría haber modificado el planteamiento terapéutico y haber servido de base para la consideración de alternativas terapéuticas futuras. Tal como se ha planteando por otros grupos, habría que reconsiderar la biopsia en el abordaje inicial, especialmente en aquellos casos atípicos o pacientes sin cirrosis hepática.
CP-068. DEL GIMNASIO AL QUIRÓFANO: ADENOMATOSIS HEPÁTICA POR ESTEROIDES.
Ortiz Chimbo DS, Carrillo Cubero B, Valdivia Krag C, Rodríguez Perálvarez ML
UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: adenomatosis, esteroides, resección. .
Introducción
La adenomatosis hepática es una enfermedad rara, siendo tumores primarios benignos, normalmente asociados con enfermedades metabólicas de base o con la toma de esteroides anabolizantes o de anticonceptivos orales. Hay pocos casos descritos, siendo muy infrecuente en adolescentes y niños.
Caso clínico
Varón de 35 años, sin antecedentes de interés, militar de profesión, en buena forma física con realización de ejercicio diario extenuante y toma regular de esteroides anabolizantes por ciclos de 3 meses, durante los últimos 5 años. Acude a urgencias por sensación de malestar general y dolor en hipocondrio derecho, con sensación de empastamiento en dicho nivel.
Analíticamente destacaba ligera elevación de enzimas hepáticas con función hepática y alfafetoproteína normales. En la ecografía abdominal (US), se objetivaron varias lesiones homogéneamente ecogénicas. Se realizó resonancia magnética (RM) dinámica de hígado objetivándose gran hepatomegalia con múltiples lesiones, las de mayor tamaño localizadas en segmentos V-VI de 12 cm, que presentan áreas hemorrágicas y de aspecto inflamatorio sugestivo de adenomatosis hepática, confirmada mediante biopsia hepática.
Dado la posibilidad de malignización o rotura de alguna de las lesiones, se realizó Angio-tomografía TC en el que se aprecian los segmentos I-II-III libres de enfermedad, con lesiones en el resto de segmentos, así como TC con reconstrucción 3D, con volumen hepático suficiente, por lo que se decide hepatectomía derecha y extirpación de lesión en segmento IV por vía laparoscópica.
Figura 1.
AngioTC hepática. Adenomatosis hepática que afecta a todos los segmentos excepto al I, II y III.
Figura 2.
AngioTC hepática. Áreas hiperatenuantes en el interior de algunas lesiones sugestivas de sangrado intralesional más significativo en las lesiones de los segmentos IV-b, VI y VIII, donde se identifican vasos arteriales patológicos.
Figura 3.
RM dinámica de hígado. Múltiples lesiones hepáticas hipervasculares de diferente tamaño distribuidas por el parénquima, las mayores en segmentos IVb, V y VI, de hasta 87mm de diámetro máximo axial, con crecimiento exofítico.
Discusión
La adenomatosis hepática se trata de múltiples lesiones hepáticas benignas, pero con elevado riesgo de malignización y rotura pudiendo provocar hemorragia intraperitoneal e intratumoral. Las opciones terapéuticas pueden abarcar desde el seguimiento clínico, a la resección aislada de lesiones, las resecciones hepáticas mayores o la embolización arterial, hasta el trasplante hepático del que se describen pocos casos. El trasplante debe reservarse para los síntomas progresivos tras la resección parcial, o cuando se sospeche malignización.
En este caso dado que no objetivaron dichos datos, se optó por la resección hepática.
CP-069. EFECTIVIDAD DE LA BUDESONIDA COMO PRIMERA LÍNEA DE TRATAMIENTO DE LA HEPATITIS AUTOINMUNE
CORNEJO JIMÉNEZ A, PÉREZ RAMÍREZ A, RUÍZ PÉREZ R, GIRÁLDEZ GALLEGO A, FERRER RÍOS T, PASCASIO ACEVEDO JM, SOUSA MARTÍN JM
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla.
Palabras clave: hepatitis autoinmune, budesonida, efectividad.
Introducción
La hepatitis autoinmune (HAI) es una enfermedad inflamatoria crónica hepática cuya inducción de la remisión se realiza mediante corticoterapia, principalmente prednisona. La budesonida es otro glucocorticoide aceptado como primera línea en pacientes sin cirrosis ni HAI severa y con menos efectos secundarios; no obstante, su uso en práctica clínica es poco frecuente.
El objetivo del estudio fue analizar la efectividad de budesonida como tratamiento de primera línea en HAI.
Material y métodos
Estudio descriptivo, observacional y retrospectivo sobre 74 pacientes diagnosticados de HAI en nuestro centro entre junio 2011 y junio 2022 con un seguimiento mínimo de 3 meses. 24/78 (30%) fueron tratados con budesonida como primera línea.
Resultados
Se trataron con Budesonida como primera línea 24 pacientes, 17 mujeres (70,8%) y 7 hombres (29,2%) con una mediana de edad al diagnóstico de 53 (16-81) años. 5/24 (12%) presentaban un síndrome de solapamiento con colangitis biliar primaria (CBP). La mediana de seguimiento fue de 60 (6-126) meses.
El score diagnóstico de HAI pretratamiento fue probable en 8/24 (33.3%) y definitivo en 16/24 (66.6%). El grado de fibrosis basal fue 6/24 (25%) F0; 11/24 (46%) F1; 5/24 (21%) F2; y 2/24 (8%) F3. Solo 3 pacientes tenían bilirrubina elevada al inicio de tratamiento (los tres menor a 4 mg/dl). El 75% (18 pacientes) presentaba IgG elevada basalmente y el 91.6% (22 pacientes) presentaron autoanticuerpos positivos.
La tasa de respuesta a budesonida fue del 83.3% (20/24). Los 4 pacientes no respondedores sí respondieron a prednisona.
Al inicio de tratamiento la mediana de AST fue 112.5 (47-1310) U/L, ALT 164 (39-1458) U/L, bilirrubina total (BT) 0,71 (0.27-3.5) mg/dL, inmunoglobulina G (IgG) 1880 (717-4806) mg/dL.
A las 4 semanas del inicio, los valores medianos analíticos, de los 20 pacientes respondedores, fueron: AST 40.5 (20-143) U/L, ALT 52.5 (23-258) U/L, BT 0,62 (0.29-0.92) mg/dL, IgG 1560 (724-2474) mg/dL. A las 24 semanas: AST 27 (14-51 U/L, ALT 26 (13-58) U/L, BT 0,44 (0.20- 0.85) mg/dL, IgG 1187 (598-1881) mg/dL.
En 17 pacientes se añadió azatioprina o micofenolato de mofetilo de mantenimiento y 7 mantuvieron monoterapia a largo plazo con budesonida. Al final del seguimiento 19/24 (79%) de los pacientes mantenían la remisión sin haber precisado prednisona.
Conclusiones
La budesonida en un glucocorticoide eficaz como tratamiento de primera elección en HAI en pacientes bien seleccionados (formas leves sin fibrosis avanzada). Aunque su uso en práctica clínica no está muy extendido es una opción válida y con un espectro de efectos secundarios mucho menor a prednisona dada su baja biodisponibilidad sistémica.
CP-070. EFECTO DE LA METFORMINA EN UN MODELO DE RATÓN FVB/N OBESO INDUCIDO POR DIETA RICA EN GRASAS
Ojeda Pérez B, Hermán Sánchez N, Sarmento Cabral A, M. Luque R, Gahete MD
Grupo Investigación. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: metformina, hígado, obesidad.
Introducción
Explorar la implicación de la metformina en la modulación del metabolismo de la glucosa/insulina, la adiposidad, la función pancreática y hepática, las hormonas y los lípidos circulantes, la ingesta de alimentos y el gasto energético, ya que los datos existentes en la literatura son controvertidos.
Material y métodos
Se utilizó metformina administrada por vía oral (250 mg/kg/día) en ratones FVB/N obesos inducidos por dieta alta en grasa (HFD). Se analizaron los efectos de la metformina sobre el aumento y la composición del peso corporal, el metabolismo de la glucosa/insulina, la fisiología del hígado, la hormona del crecimiento y el eje IGF1 y la regulación transcripcional hepática usando animales alimentados con una dieta baja en grasas (LFD) como control.
Resultados
Los ratones alimentados con HFD exhibieron un peso corporal significativamente mayor en comparación con los ratones LFD, lo que fue acompañado por el aumento proporcional de la masa grasa total, evaluado por RMN. El aumento de peso corporal observado se debió a una mayor ingesta calórica. El consumo de HFD condujo a un aumento de la insulina y a un aumento no significativo de la glucosa. Los ratones alimentados con HFD también presentaron un deterioro en la tolerancia a la glucosa, aunque no se observaron alteraciones en la tolerancia a la insulina.
El tratamiento con metformina indujo efectos metabólicos paradójicos en ratones alimentados con HFD, sin un impacto importante en ratones alimentados con LFD. En concreto, el tratamiento con metformina no indujo cambios en el peso corporal, la ingesta de alimentos, la composición corporal o la glucosa en ayunas en condiciones de HFD o LFD, mientras que solo se observó una disminución de insulina en ratones HFD tratados con metformina.
Sin embargo, si se observó un efecto significativo a nivel hepático ya que los ratones HFD tratados con metformina exhibieron una proporción significativamente menor de esteatosis, inflamación y necrosis hepática, mientras que en ratones LFD exhibió un papel paradójico. Estos cambios fueron acompañados por cambios en la expresión de genes implicados en el control de la expresión génica, sugiriendo posibles biomarcadores en el desarrollo de esteatosis y/o respuesta a metformina.
Conclusiones
En modelos animales, la metformina ejerce un potente papel en la prevención y/o el desarrollo de patologías hepáticas, aunque su efecto sobre otros parámetros metabólicos es muy dependiente del contexto genético de los animales y de su estado metabólico.
Financiación: MINECO (FPU20/03957), ISCIII (PI20/01301), JdA (PEMP-0036-2020, BIO-0139), FSEEN y CIBERobn.
CP-071. EL PAPEL DE LA DENSITOMETRÍA ÓSEA EN VIDA REAL EN EL SEGUIMIENTO DE LOS PACIENTES CON COLANGITIS BILIAR PRIMARIA.
Sendra C, Silva-Ruiz MDP, Pérez-Palacios D
Unidad Aparato Digestivo. Hospital Comarcal Infanta Elena, Huelva.
Palabras clave: colangitis biliar primaria, osteoporosis, densitometría ósea..
Introducción
La osteoporosis es una complicación frecuente (20-45%) de los pacientes con colangitis biliar primaria (CBP). Su prevención, diagnóstico y tratamiento son fundamentales para mejorar la calidad de vida. Existen pocos datos sobre su monitorización y tratamiento en pacientes con CBP. Objetivos: 1) Analizar la monitorización de la enfermedad mineral ósea en pacientes con CBP; 2) Evaluar los factores relacionados con la presencia de osteopenia/osteoporosis en nuestra cohorte; 3) Analizar la estrategia terapéutica empleada.
Material y métodos
Análisis retrospectivo, descriptivo y observacional de los pacientes diagnosticados de CBP en el Hospital Infanta Elena entre 2002-2022.
Resultados
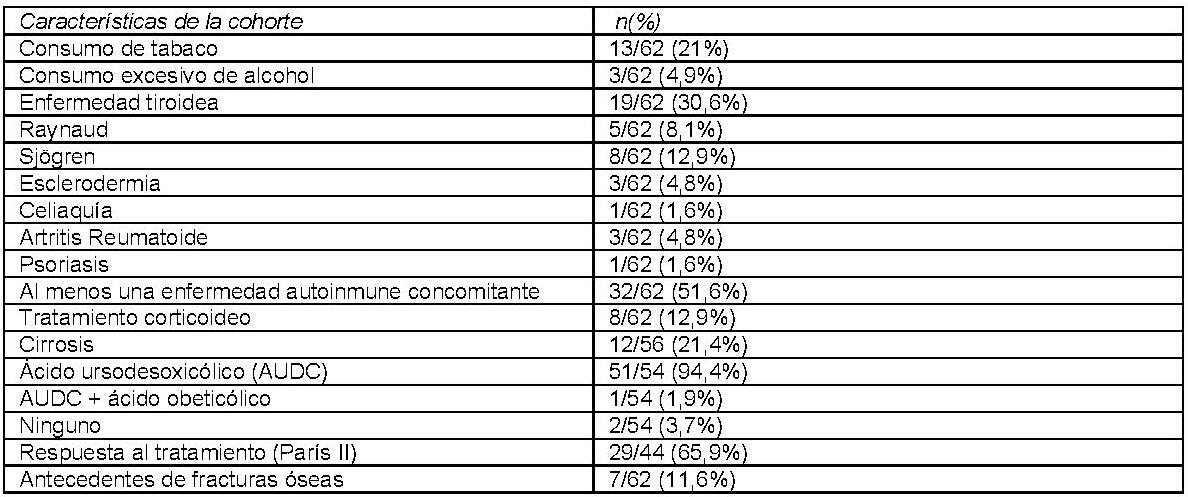
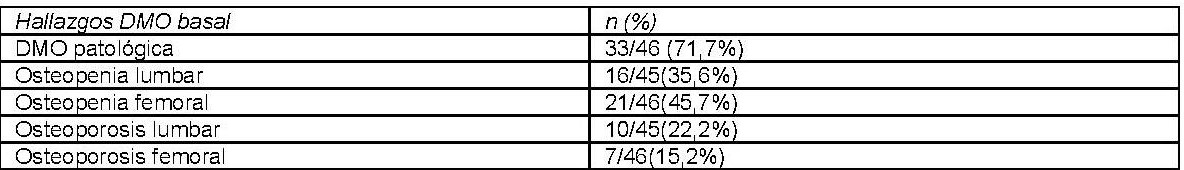
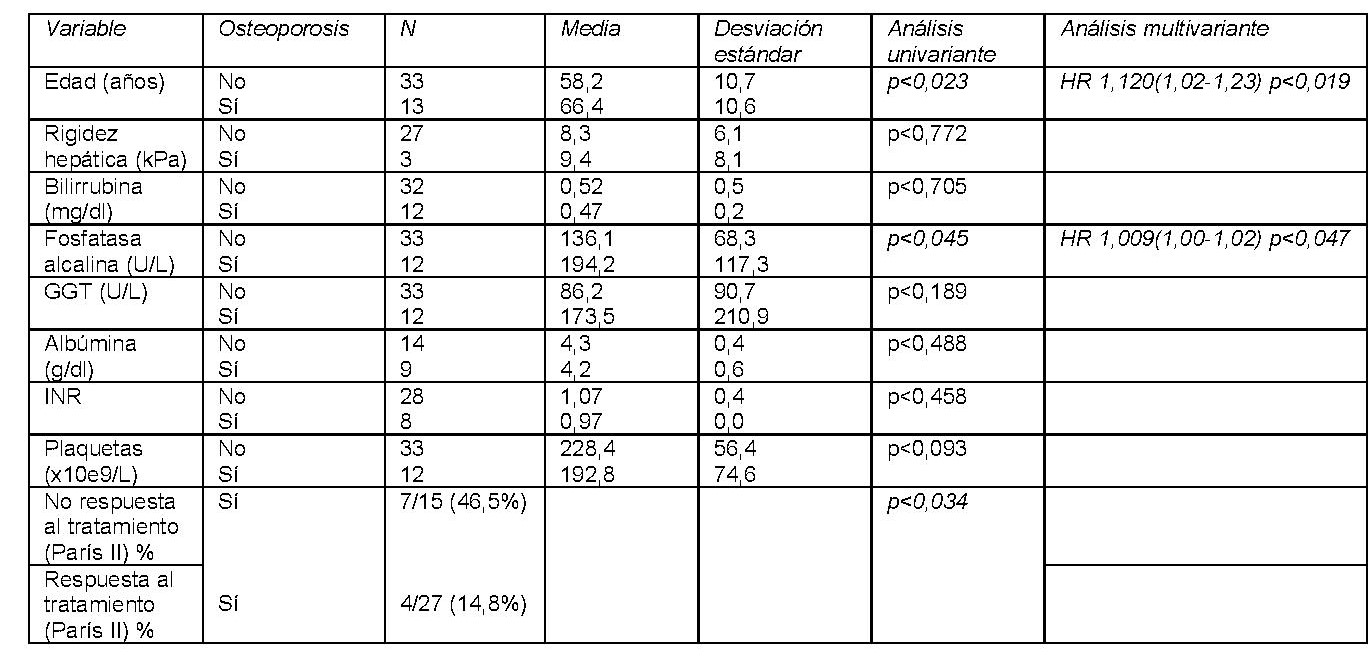
Se incluyeron 62 pacientes con CBP con una edad media de 60,213,6 años. El 91,1% eran mujeres (57/62). La mediana de seguimiento fue de 3,9 años. Las características de la cohorte se resumen en la tabla 1. El 74,2% (46/62) tenían realizada al menos una DMO. Solo en un 39,1% (18/46) se solicitó al diagnóstico de la CBP. La mediana de tiempo transcurrido desde el diagnóstico de CBP hasta la DMO basal fue de 12,6 meses. Al 62,5%(15/24) de los pacientes diagnosticados de 2018 en adelante se les pidió la DMO al diagnóstico frente al 13,6%(3/22) de los diagnosticados previamente (p<0,001). El 71,7%(33/46) tenía osteopenia u osteoporosis en la primera DMO solicitada. Tabla 2. El 28,3%(13/46) tenían osteoporosis. La presencia de enfermedad tiroidea (93,3%(14/15) vs. 60%(18/30); p<0,034) fue un factor de riesgo de tener una DMO basal patológica: 93,3%(14/15) vs. 60%(18/30); p<0,034, así como los niveles de FA elevados por encima del límite superior de normalidad (LSN) (80%(24/30) vs. 50%(7/14) respectivamente; p<0,042). En el análisis univariante, la edad (66,410,6 vs. 58,2 10,7 años; p<0,023), los niveles de fosfatasa alcalina (194,3117,3 vs. 136,168,3 U/L; p<0,045) y la ausencia de respuesta al tratamiento según París II (46,5%(7/15) vs. 14,8%(4/27); p<0,034) se relacionaron con más riesgo de osteoporosis. En el análisis multivariante la edad (HR 1,120(1,02-1,23) p<0,019) y la fosfatasa alcalina (HR 1,009(1,00-1,02) p<0,047) se relacionaron con el riesgo de osteoporosis. Tabla 3.
El 21,6%(8/37) de los pacientes, tras el diagnóstico de osteopenia/osteoporosis, no realizaba tratamiento correcto.
Conclusiones
Casi dos tercios de los pacientes con CBP tuvieron una DMO basal patológica. Sin embargo, su detección, monitorización y tratamiento no está generalizado en nuestras consultas. La presencia de enfermedad tiroidea y los niveles de fosfatasa alcalina elevados por encima del LSN se relacionaron con más riesgo de tener una DMO patológica. La edad y los niveles de fosfatasa alcalina fueron un factor de riesgo de osteoporosis.
CP-072. EL PAPEL DEL TIPS EN EL MANEJO DE LA HIPERTENSIÓN PORTAL. EXPERIENCIA EN NUESTRO CENTRO.
Berdugo Hurtado F1, Ortiz Sánchez A1, Ruiz Escolano E1, Cabrera Peña A2, Bailón Gaona MC1
1Servicio Aparato Digestivo. Hospital San Cecilio, Granada. 2Servicio Radiología Intervencionista. Hospital San Cecilio, Granada.
Palabras clave: hipertensión portal, derivación portosistémica intrahepática transyugular .
Introducción
La derivación portosistémica intrahepática transyugular (TIPS) es un procedimiento eficaz para el tratamiento de las complicaciones de la hipertensión portal (HTP), que incluyen la hemorragia por varices esofágicas (HDA VE), la ascitis y el síndrome hepatorrenal entre otros. Sin embargo, la prevalencia de efectos adversos ha limitado su uso en la práctica clínica.
El objetivo de nuestro estudio fue analizar la tasa de complicaciones y supervivencia de los pacientes de nuestro centro en los que se ha implantado un TIPS.
Material y métodos
Estudio observacional descriptivo retrospectivo de pacientes con HTP que requirieron de colocación de TIPS en nuestro centro entre 2018-2021.
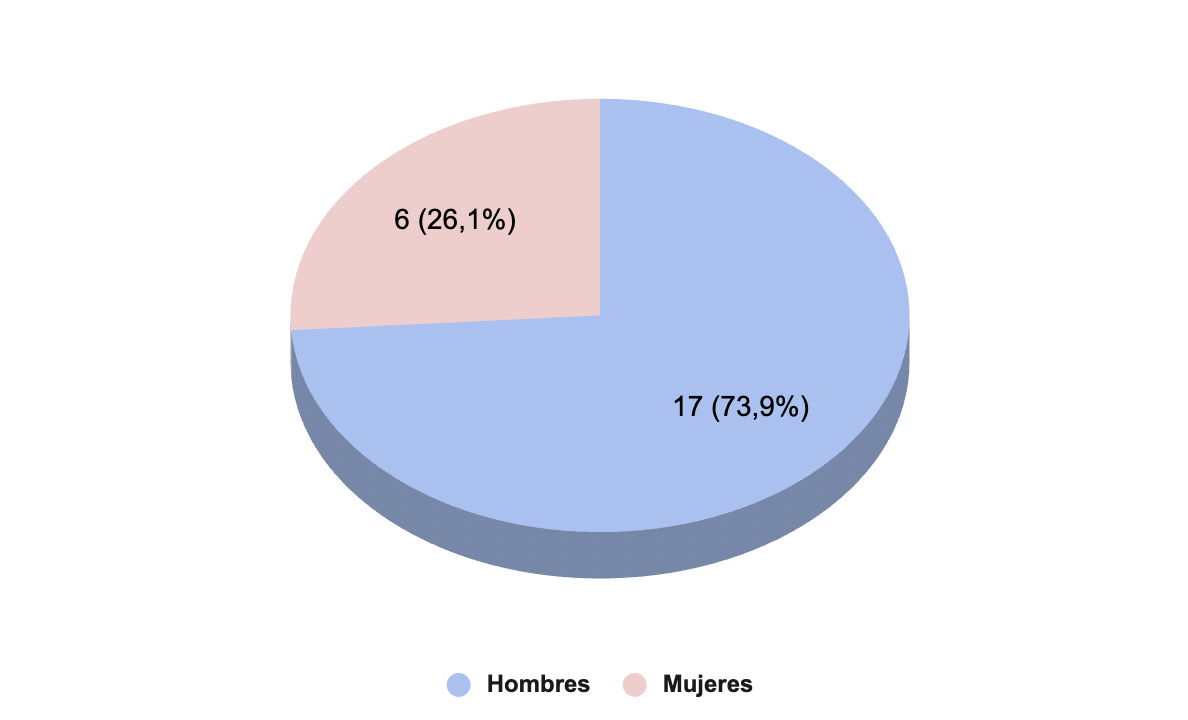
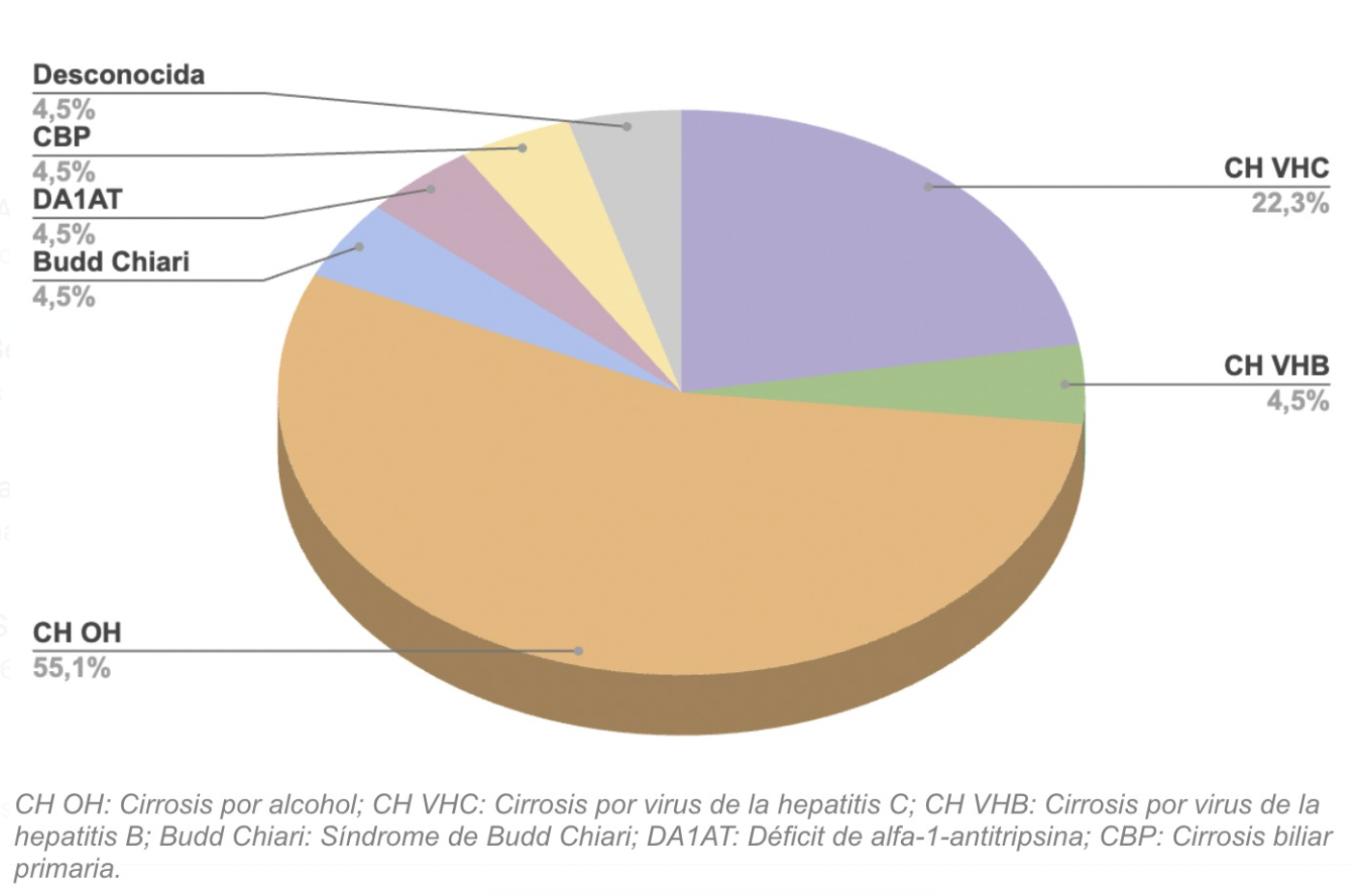
Se incluyeron 23 pacientes de entre 32 y 74 años (mediana: 62 años), 26.1% mujeres y 73.9% hombres. Entre sus causas de HTP, destaca como la más frecuente la cirrosis alcohólica (52.2%), seguida por cirrosis por VHC (26.1%).
En todos ellos, se colocaron TIPS recubiertos de politetrafluoroetileno(PTFE).
Resultados
Observamos un marcado incremento en la implantación de TIPS en el periodo 2020-2021 (69.5%), frente al 30.5% en 2018-2019.
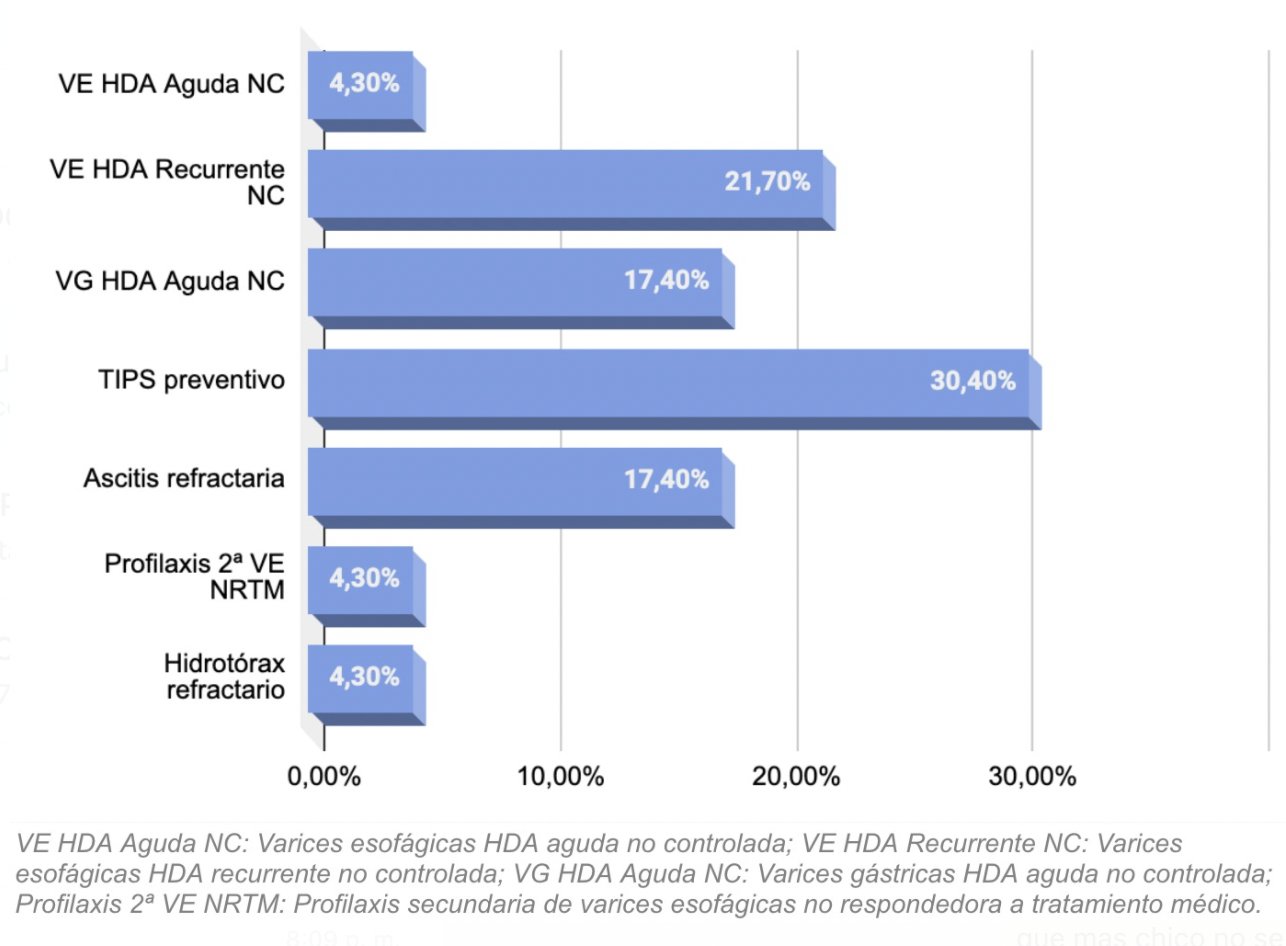
En cuanto a indicaciones destacar, en el 30.4% de los casos se colocó como TIPS preventivo en pacientes con alto riesgo de resangrado, seguido en un 21.7% por HDA VE recurrente no controlada y 17.4% en ascitis refractaria y hemorragia por varices gástricas no controladas respectivamente.
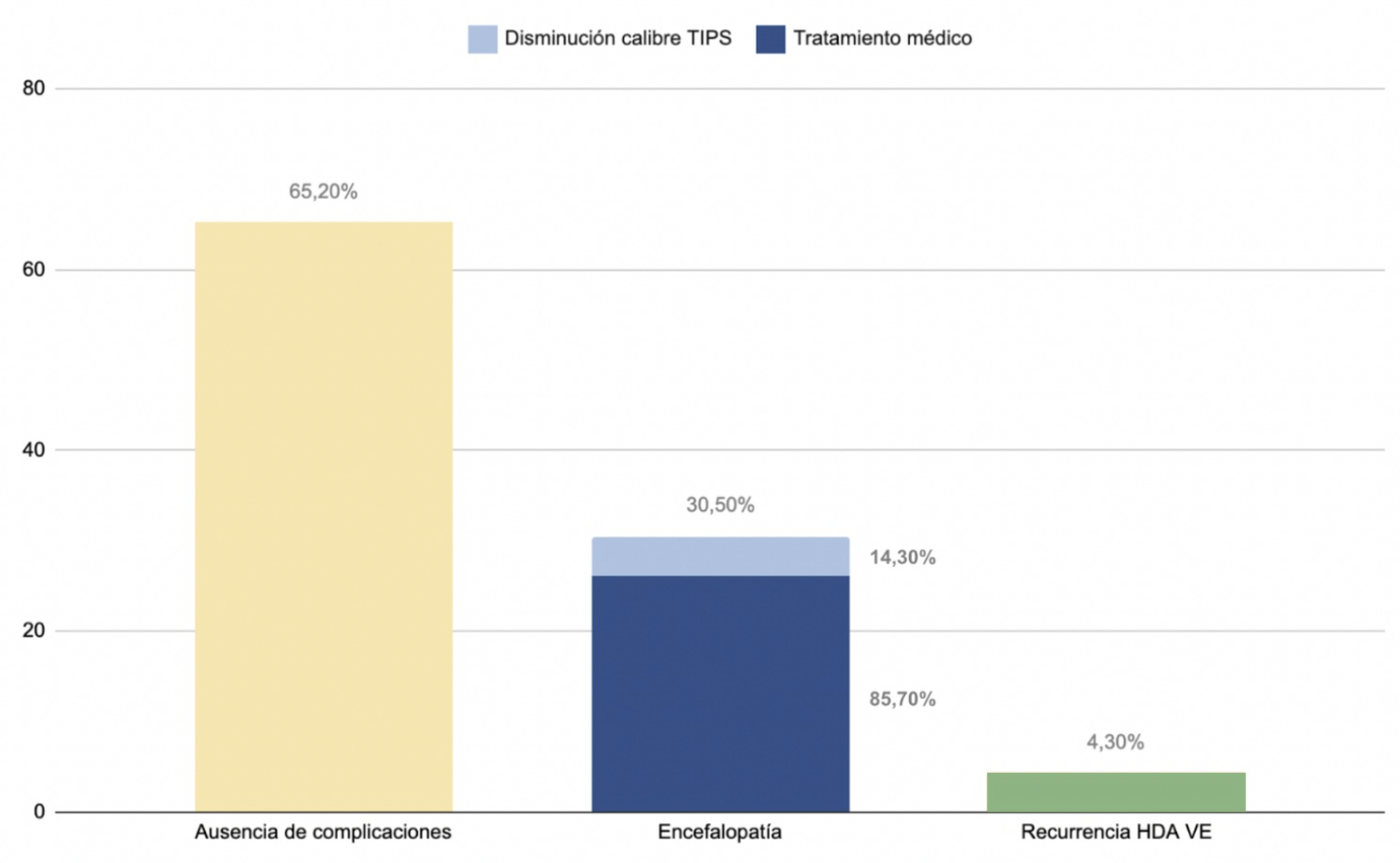
El 65.2% de los pacientes no tuvieron complicaciones relacionadas con el TIPS, presentándose estas en forma de encefalopatía en un 30.5% y como recurrencia de HDA VE en el 4.3%. En el 85.7% de los pacientes que presentaron encefalopatía, esta se resolvió de forma efectiva con tratamiento médico, precisando tan sólo un 14.3% de disminución del calibre del TIPS.
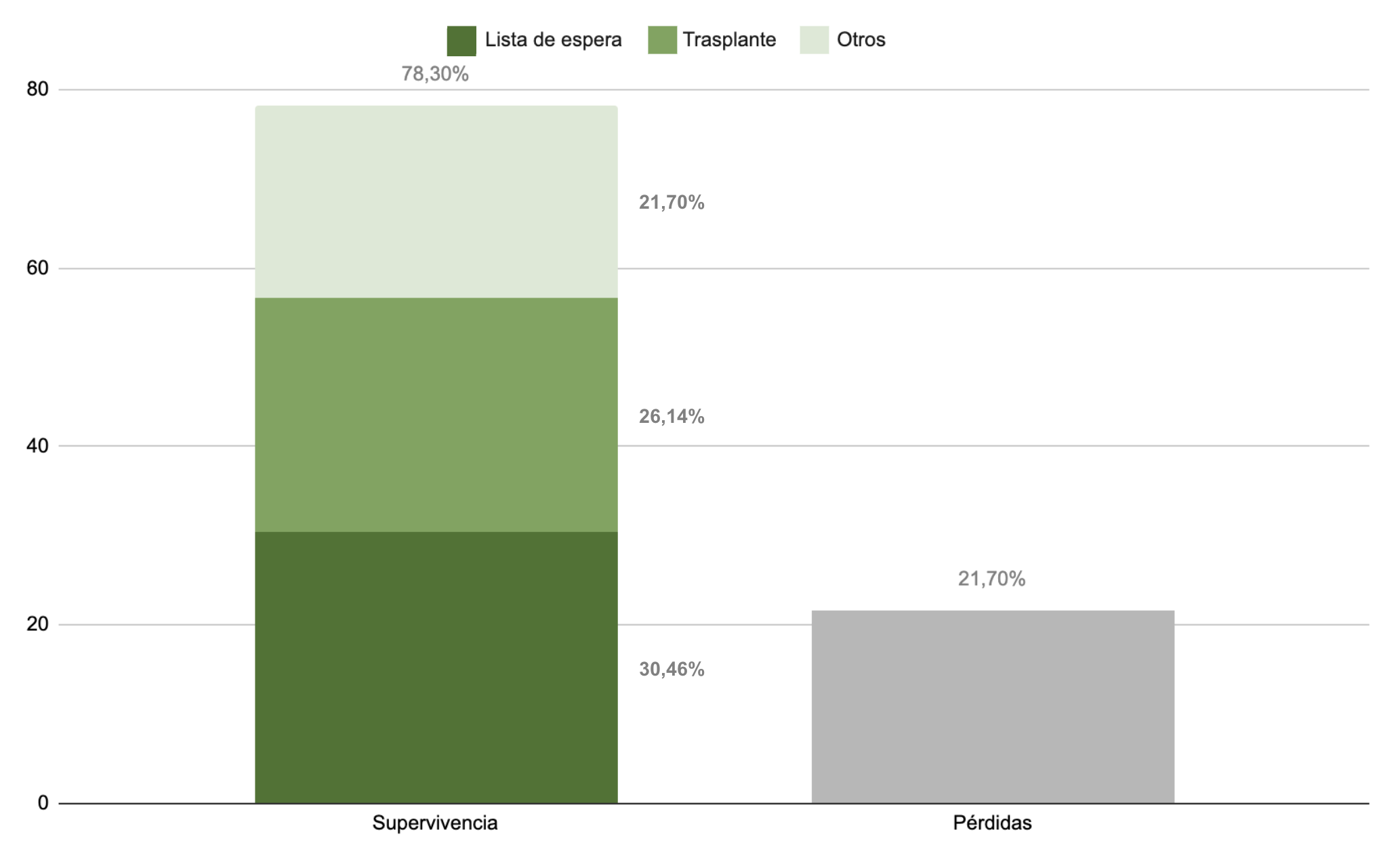
Actualmente, los pacientes incluidos en el estudio presentan una supervivencia del 78.3% . De ellos, un 26.1% se sometieron a trasplante hepático (TH) y el 21.7% se encuentra en lista de espera.
Conclusiones
Al inicio de la implantación del TIPS, se sugería que su uso era adecuado como terapia puente al TH dada su alta tasa de estenosis u oclusión. Sin embargo, el desarrollo de stent recubiertos de PTFE ha mostrado resultados alentadores en cuanto a permeabilidad, lo cual ha derivado en un aumento de la supervivencia y disminución de complicaciones. Permitiendo así, ampliar las indicaciones del TIPS como terapia a medio/largo plazo.
Podemos concluir, con los resultados de este estudio y las revisiones realizadas; que la implantación del TIPS debe considerarse activamente en la práctica clínica diaria del paciente cirrótico con HTP.
CP-073. EL SISTEMA SOMATOSTATINA COMO POTENCIAL FUENTE DE BIOMARCADORES EN ESTEATOSIS HEPÁTICA METABÓLICA Y HEPATOCARCINOMA
García Estrada A, Hermán Sánchez N, López Cánovas JL, Sáez Martínez P, Córdoba Chacón J, Sarmento Cabral A, Rodríguez Perálvarez M, Luque RM, Gahete MD
Grupo Investigación. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: somatostatina, esteatosis hepática metabólica, hepatocarcinoma.
Introducción
Evaluar la expresión de los ligandos y receptores del sistema somatostatina (SST) en esteatosis hepática metabólica (EHMet) y hepatocarcinoma (CHC), así como el efecto de péptidos naturales y sintéticos de este sistema sobre la proliferación de líneas celulares humanas de CHC.
Material y métodos
La expresión de la SST, de la cortistatina (CORT) y de sus receptores (SSTR1-5) se analizó en 2 cohortes retrospectivas de pacientes con enfermedad hepática crónica [cohorte 1: tejido tumoral vs. adyacente (n = 93), cohorte 2: tejido tumoral vs. adyacente (n = 58), cirrótico (n = 39) y sano (n = 5)] y en 7 cohortes de EHMet (E-MEXP-3291, GSE48452, GSE61260, GSE66676, GSE89632, GSE126848, GSE130970) y 6 cohortes de CHC (GSE6764, GSE14323, GSE14520, GSE164760, TCGA-GTex, CPTAC) disponibles online. Igualmente, se emplearon modelos murinos (C57BL/6J) que recapitulan la progresión de la EHMet a CHC a través de la dieta y líneas celulares de hepatoblastoma (HepG2) y CHC (Hep3B, SNU-387).
El impacto de la aplicación de péptidos naturales (SST, CORT) y sintéticos del sistema SST [BIM-23926 (agonista de SSTR1), octreótido (agonista de SSTR2), pasireótido (agonista de SSTR5)] en líneas celulares se midió a 0, 24, 48 y 72 horas mediante el ensayo de reducción de la resazurina.
Resultados
La expresión hepática de los SSTRs se observó alterada en la progresión EHMet-CHC. El desglose por estadios de la progresión en cohortes de muestras humanas reveló perfiles de expresión característicos para los receptores. Así, SSTR1 se observó sobreexpresado en tejido hepático en obesidad y esteatosis, SSTR2 en esteatohepatitis y SSTR5 en CHC, mientras que en el resto de estadios su expresión disminuyó. Por otro lado, la expresión de SST, CORT, SSTR3 y SSTR4 se vio disminuida en EHMet y su pérdida se acentuó en CHC. Estos resultados se corroboraron en los modelos murinos.
El análisis de la expresión de los SSTRs en líneas celulares demostró que Hep3B expresa y es ideal para el estudio de SSTR1, SSTR2 y SSTR5, mientras que HepG2 sobreexpresa SSTR5. De esta manera, el pasireótido redujo significativamente la proliferación en HepG2; BIM-23926 en Hep3B; el octreótido en ambas líneas y la SST en SNU-387.
Conclusiones
Nuestros resultados demuestran que existe una alteración profunda del sistema SST en modelos humanos, animales y celulares de la progresión EHMet-CHC con potencial diagnóstico, pronóstico y terapéutico en estas hepatopatías.
Financiación: MINECO (FPU20/03957, FPU21/04833), ISCIII (PI20/01301), JdA (PEMP-0036-2020, BIO-0139), FSEEN y CIBERobn.
CP-074. ENFERMEDAD DE CORI COMO CAUSA DE CIRROSIS HEPÁTICA Y HEPATOCARCINOMA
Plaza Fernández A, Moreno Moraleda I, Rodríguez Mateu A
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: (cirrosis hepática), (enfermedad de cori), (glucogenosis).
Introducción
La enfermedad por almacenamiento de glucógeno tipo III o enfermedad de Cori es una enfermedad rara, autosómica recesiva, que afecta al hígado, músculo cardíaco y músculo esquelético. Es causada por una actividad deficiente de la enzima desramificadora de glucógeno, clave en la degradación del mismo. En la infancia la afectación hepática se presenta como hepatomegalia y retraso del crecimiento, hipoglucemia cetósica en ayunas, hiperlipidemia y elevación de las transaminasas. Las complicaciones más frecuentes a largo plazo son la miocardiopatía y la cirrosis hepática sobre la que se puede desarrollar hepatocarcinoma, como ocurre con nuestro paciente.
Caso clínico
Paciente de 45 años con antecedentes familiares de glucogenosis que durante la infancia y la adolescencia se encuentra asintomático. A los 39 años acude a cardiología por clínica de disnea de esfuerzo, diagnosticándose de miocardiopatía hipertrófica (Figura 1). A los 43 años acude a consultas de digestivo tras objetivarse hipertransaminasemia en analítica de control. Se realiza estudio etiológico resultando negativo. En ecografía abdominal se objetivan signos de cirrosis, realizándose entonces biopsia hepática que muestra infiltrado inflamatorio secundario a esteatohepatitis. Se amplia estudio con TAC de abdomen en el que se objetivan LOEs hepáticas en segmentos VII y IV sospechosas de hepatocarcinoma (Figura 2). Dado los antecedentes, se realiza estudio genético en el que se confirma el diagnóstico de glucogenosis tipo III. En la biopsia hepática de las lesiones no se observan depósitos de glucógeno, pero dados los resultados del estudio genético, se relaciona su patología con la glucogenosis. Se decide tratamiento puente con quimioembolización y posteriormente trasplante hepático, sin evidenciarse en estudios de imagen postrasplante datos sugestivos de persistencia/recidiva tumoral.
Discusión
La importancia del caso clínico radica en el abordaje diagnóstico y terapéutico de una enfermedad secundaria a una metabolopatía difícil de diagnosticar si no se tienen en cuenta los antecedentes familiares.
El diagnóstico de la glucogenosis se realiza mediante pruebas de genética molecular, aunque la histología hepática puede ayudarnos al diagnóstico al evidenciar depósitos de glucógeno y fibrosis centrolobulillar y portal. En cuanto al tratamiento, el trasplante hepático se reserva para aquellos pacientes con cirrosis hepática avanzada, disfunción hepática y/o carcinoma hepatocelular, aunque puede exacerbar la miopatía y la miocardiopatía. En la glucogenosis tipo III, debido a que la alteración enzimática está localizada en el hígado no hay posibilidad de recurrencia de la enfermedad hepática primaria dentro del aloinjerto trasplantado, sin embargo no se corrigen con este tratamiento las manifestaciones esqueléticas o cardíacas.
CP-075. ENFERMEDAD HEPÁTICA METABÓLICA COMO SOLAPAMIENTO DE HEPATOPATÍA COLESTÁSICA AUTOINMUNE. UNA ASOCIACIÓN POCO DESCRITA EN LA LITERATURA.
Fernández Carrasco M, Sánchez García O, Navarro Moreno E
Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: síndromes solapamiento, colangitis biliar primaria, enfermedad hepática metabólica.
Introducción
Cuando hablamos de síndromes de solapamiento, nos referimos a la presencia simultánea de dos enfermedades hepáticas de origen autoinmune, como colangitis biliar primaria (CBP), hepatitis autoinmune (HAI), o colangitis esclerosante primaria (CEP).
Estos síndromes carecen de criterios diagnósticos establecidos, por ello para su diagnóstico, la biopsia hepática se vuelve imprescindible. A pesar de ser un diagnóstico infrecuente, dichas asociaciones están bien descritas en la literatura, no ocurriendo lo mismo cuando alguna de estas entidades se asocia a la enfermedad hepática metabólica.
Presentamos por tanto este caso de solapamiento de CBP y esteatohepatitis no alcohólica (EHNA), no existiendo apenas descripciones de esta asociación, a pesar de la gran prevalencia de la enfermedad hepática metabólica a nivel mundial.
Caso clínico
Se trata de una paciente de 54 años con antecedentes de vasculitis ANCA positivo-MPO por enfermedad de Wegener con afectación sistémica y gammapatía monoclonal IgG kappa. Se realiza seguimiento en hepatología por hipertransaminasemia y colestasis disociada progresiva, asociando astenia intensa, se realiza estudio autoinmunitario presentando anticuerpos ANA positivos.
La ecografía abdominal muestra signos de hepatopatía crónica con datos de hipertensión portal. Dada la sospecha de síndrome de solapamiento (hepatitis autoinmune y colangitis biliar primaria) se realiza biopsia hepática con hallazgos compatibles con hepatopatía crónica en relación con síndrome variante CBP más EHNA.
La paciente inicia tratamiento con ácido ursodesoxicólico (AUDC) así como control de factores de riesgo cardiovascular y medidas higiénico dietéticas; realizándose controles periódicos.
Discusión
La enfermedad hepática metabólica es el trastorno hepático más frecuente en occidente, está en relación con el sobrepeso, pero también ocurre en personas sin el mismo, siendo más frecuente dentro de este subgrupo en mujeres jóvenes.
El síndrome de solapamiento entre distintas enfermedades hepáticas de naturaleza autoinmune, como la CBP, HAI, CEP, se encuentran descritos en la literatura. Sin embargo, no existen estudios suficientes de la asociación del solapamiento entre la esteatosis hepática no alcohólica y colangitis biliar primaria.
En un estudio de pacientes con diagnóstico histológico de colangitis biliar primaria, en los que además se identifica esteatosis hepática y esteatohepatitis, concluye que la asociación entre ambas patologías presenta un peor pronóstico de la enfermedad, así como de respuesta a AUDC y un aumento de la mortalidad.
Dado el aumento progresivo de la prevalencia de EHNA en la población, resultaría de especial importancia el estudio de la asociación de ambas patologías, así como su implicación en el pronóstico e investigación de nuevas líneas de tratamiento.
CP-076. ENFERMEDAD VENOOCLUSIVA HEPÁTICA TRATADA CON TIPS
Rosa Sánchez C, López Vico M, García Aragón F, Pardo Moreno P, Redondo Cerezo E, López Garrido M
Departamento Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: enfermedad venooclusiva hepática, tips.
Introducción
La enfermedad venooclusiva hepática (EVOH), también conocida como síndrome de obstrucción sinusoidal hepática, es una patología resultante de la obstrucción de los sinusoides hepáticos de origen tóxico-metábolico, especialmente relacionado con el trasplante de progenitores hematopoyéticos (TPH) (hasta en el 3.4%) y el uso de quimioterapia en algunos tumores sólidos. Se caracteriza por la presentación de ictericia, hepatomegalia dolorosa, ascitis y trombocitopenia refractaria, y generalmente se trata de un cuadro de mal pronóstico cuyo único tratamiento médico con eficacia demostrada es el defibrotide, si bien algunos estudios sugieren el implante de una derivación intrahepática portosistémica transyugular (TIPS) como alternativa en pacientes refractarios al tratamiento farmacológico. Este es el caso de una paciente con una EVOH tratada con TIPS tras presentar una mala respuesta al tratamiento con defibrotide.
Caso clínico
Paciente de 26 años en seguimiento por Hematología por Linfoma de Hodgkin mediastínico refractario a varias líneas de quimioterapia y radioterapia, por lo que se decide realización de TPH autólogo, con respuesta inicial completa. Sin embargo, un año después presenta datos de recidiva tumoral diseminada, por lo que se inicia nueva línea de quimioterapia e ingresa para TPH alogénico. Durante dicho ingreso presenta cuadro de hepatomegalia dolorosa, alteración de la función hepática y ascitis rápidamente progresiva. Se realiza ecografía y TAC abdominal (Figura 1), con hallazgos sugerentes de EVOH. Ante la sospecha, se inicia tratamiento con defibrotide y corticoides a altas dosis, sin respuesta. Ante la refractariedad del cuadro, se decide finalmente realización de TIPS con endoprótesis tipo VIATOR, con buena respuesta clínica y analítica posterior. Dos meses después la paciente presenta un episodio de encefalopatía mixta por TIPS y sobredosificación de everólimus, que se resuelve tras el ajuste del inmunosupresor. Desde entonces presenta función hepática conservada, TIPS permeable, y remisión completa de su patología linfoproliferativa.
Discusión
La EVOH es una patología generalmente de mal pronóstico y que afecta habitualmente a paciente jóvenes, con una alta mortalidad (hasta del 41%) incluso pese al tratamiento con defibrotide. La existencia de una alternativa terapéutica en estos pacientes es crucial, y el TIPS representa una opción prometedora, tal como apreciamos en este caso. Sin embargo, a día de hoy la evidencia de este tratamiento es escasa, y serían necesarios más estudios para poder comprobar la eficacia y la seguridad del TIPS en este perfil de pacientes, si bien en casos sin otras opciones terapéuticas podría considerarse justificado el uso del TIPS como último recurso para intentar mejorar el pronóstico de estos pacientes.
CP-077. ESTADO NUTRICIONAL DE PACIENTES CON HEPATOPATIA CRONICA AVANZADA: DESCRIPTIVO BASAL DE UN ESTUDIO PROSPECTIVO.
Soria López E1, López Rodríguez C2, Costa Fernández JA3, Abilés Osinaga J2, Gálvez Fernández RM1, García Gavilán MC1, Rivas Ruiz F4, Rosales Zábal JM1
1Servicio Aparato Digestivo. Complejo Hospital Costa del Sol, Marbella. 2Servicio Farmacia. Complejo Hospital Costa del Sol, Marbella. 3Servicio Radiodiagnóstico. Complejo Hospital Costa del Sol, Marbella. 4Unidad Investigación. Complejo Hospital Costa del Sol, Marbella.
Palabras clave: nutrición, cirrosis.
Introducción
La desnutrición en pacientes con hepatopatía crónica avanzada es un factor pronóstico, frecuentemente olvidado en práctica clínica. Analizamos el estado nutricional de una cohorte prospectiva de nuestro ámbito.
Material y métodos
Análisis descriptivo basal de un estudio prospectivo para evaluar estado nutricional y evolución tras iniciar suplementación oral. Incluimos pacientes de hospital de día (unidad de ascitis) y consulta de hepatología, identificados en riesgo o desnutridos, previo consentimiento informado. Tras cribar nutricionalmente con VGS, MUST, RFH-NPT, realizamos antropometría, dinamometría (fuerza presión mano), analítica, test frecuencia crítica de parpadeo (FCP), cuestionario de salud SF-36 y determinación del índice musculoesquelético (IME) mediante medición masa muscular a nivel de L3 por TC.
Resultados
37 pacientes (30 varones). Mediana tiempo cirrosis 2 años. Lugar evaluación nutricional: 27 hospital de día, 9 consulta nutrición, 1 ingresado. Tabla 1.
Tabla 2. Test cribado nutricional.
Tabla 3. Situación nutricional.
Figura 1: correlación IME respecto a dinamometría (Pearson 0.515)
Conclusiones
La fiabilidad en la valoración del riesgo nutricional aumenta utilizando varias herramientas.
RFH-NPT sobreestima el riesgo de desnutrición en pacientes descompensados, frente a VSG y MUST, que son equiparables.
No hay diferencias en la distribución de desnutrición en función del Child-Pugh.
Es frecuente el déficit de micronutrientes y la fragilidad determinada por dinamometría; no así la sarcopenia, pero con buena correlación entre dinamometría y TC.
La desnutrición no parece influir en la FCP.
Actualmente en fase de evaluación del impacto de la implementación de un tratamiento nutricional.
CP-078. EVALUACIÓN BIOQUÍMICA Y DE FIBROSIS HEPÁTICA DE LOS PACIENTES CON CBP CON MÁS DE UN AÑO DE TRATAMIENTO
Lucena Valera A1, Sousa Martín JM1, Casado M2, Morales-Arraez D3, Moreno Moraleda I4, Arenas J5, Conde I6, Muñoz L7, Canillas L8, Fernandez E9, Quiñones R10, Simón MA11, Gómez E12, Gutierrez ML13, Fernández Rodríguez C13, Jorquera F10, García Buey ML9, García Retortillo M8, Morillas R7, Berenguer M6, Hernández Guerra M3, Molina E14, Ampuero J1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 2UGC Alto Riesgo. UGC Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería. 3UGC Aparato Digestivo. Complejo Hospitalario Universitario de Canarias, San Cristóbal de La Laguna. 4UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería. 5UGC Aparato Digestivo. Hospital Universitario Donostia-Donostia Unibertsitate Ospitalea, Donostia/San Sebastián. 6UGC Aparato Digestivo. Hospital Universitari I Politècnic la Fe, Valencia. 7UGC Aparato Digestivo. Hospital Universitari Germans Trias I Pujol de Badalona, Badalona. 8UGC Aparato Digestivo. Hospital del Mar, Barcelona. 9UGC Aparato Digestivo. Hospital Universitario de La Princesa, Madrid. 10UGC Aparato Digestivo. Complejo Asistencial Universitario de León, León. 11UGC Aparato Digestivo. Hospital Clínico Universitario Lozano Blesa, Zaragoza. 12UGC Aparato Digestivo. Hospital Universitario 12 de Octubre, Madrid. 13UGC Aparato Digestivo. Hospital Universitario Fundación Alcorcón, Alcorcón. 14UGC Aparato Digestivo. Complexo Hospitalario Universitario de Santiago, Santiago de Compostela.
Palabras clave: colangitis biliar primaria, fosfatasa alcalina, paris ii.
Introducción
La colangitis biliar primaria (CBP) debe ser evaluada sistemáticamente mediante los criterios de Paris II, que incluyen FA, AST, y bilirrubina, para determinar la respuesta al tratamiento y el control óptimo de la enfermedad. El objetivo fue determinar el porcentaje de pacientes con CBP sin respuesta al tratamiento, y analizar el control de la enfermedad según las características bioquímicas y de fibrosis hepática de los pacientes sin respuesta.
Material y métodos
Estudio retrospectivo multicéntrico, de naturaleza transversal, que incluyó a 817 pacientes de 13 hospitales españoles desde enero de 2020 a abril de 2021. La CBP se diagnosticó según las guías internacionales, mientras que la respuesta al tratamiento se evaluó siguiendo los criterios de Paris II.
Resultados
Las características de la cohorte general se recogen en la Tabla 1, destacando que el 97.7% de los pacientes estaban en tratamiento con ácido ursodesoxicólico y el 14.9% con bezafibrato. El 20,6% (156/796) de los pacientes no reunían criterios de respuesta. Además, el 35,1% (279/795) presentaba FA>LSN, y el 11,1% (88/795) incluso niveles de FA>1.5 LSN (Figura 1). Las características de los pacientes con FA elevada se describen en la Tabla 2. De forma particular, los pacientes con FA>LSN pero <1.5 LSN mostraron una prevalencia de cirrosis del 21,1% (59/279) frente al 29,5% (26/88) de los pacientes con FA>1.5 LSN, y el 52.6% (10/19) en pacientes con FA>2 LSN. Este hecho se observó también con el FIB-4 (FIB-4 1.86 en FA< LSN vs. FIB-4 3.5 en FA>3 LSN) (Figura 2). Respecto a la GGT, hasta el 87,2% (75/86) de los pacientes con FA>1.5 LSN tenía esta enzima también elevada, encontrando que hasta en el 69,8% (60/86) la elevación de GGT era >2 LSN (Figura 3). En pacientes con FA>1.5 LSN, en presencia concomitante de GGT>2 LSN la tasa de cirrosis fue 36,7% (22/60) vs. 18,2% (2/11) en aquellos con GGT normal (Figura 4). En pacientes con FA>3 LSN, los niveles medios de AST y GGT fueron 66 UL/L y 471 UL/L, respectivamente.
Conclusiones
Uno de cada cinco pacientes (20%) con CBP no presenta un adecuado control de la enfermedad a pesar del tratamiento. Aquellos sujetos con FA elevada muestran un aumento concomitante de AST y GGT, así como de FIB-4 y mayor prevalencia de cirrosis. De forma notable, la GGT elevada, parámetro no incluido en los criterios de respuesta Paris II, se asocia a mayor prevalencia de cirrosis en pacientes con FA elevada.
CP-079. EVALUACIÓN DE LA SECUENCIA DIAGNÓSTICA DEL CARCINOMA HEPATOCELULAR ÚNICO MENOR DE 3 CM. IMPACTO DE LA PANDEMIA COVID-19.
GARCIA CALONGE M1, FLOREZ DIEZ P1, GONZALEZ SANCHEZ H1, MUIÑO DOMINGUEZ D1, MARTINEZ CAMBLOR L2, MESA ALVAREZ A2, CASTAÑO GARCIA A1, CELADA SENDINO M1, GONZALEZ PARRA AC3, RODRIGUEZ M1, CADAHIA V1, VARELA M1
1Departamento Aparato Digestivo. Hospital Universitario Central de Asturias, Oviedo. 2Departamento Radiodiagnóstico. Hospital Universitario Central de Asturias, Oviedo. 3Departamento Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: carcinoma hepatocelular, tumor inicial, diagnóstico (covid-19).
Introducción
La finalidad del programa de cribado del carcinoma hepatocelular (CHC) es la detección de tumores en fase inicial/muy inicial para aplicar tratamiento con intención curativa y disminuir la mortalidad. En este estudio se evalúa: 1) el tiempo entre detección, diagnóstico y tratamiento en pacientes con CHC uninodular < = 3 cm; 2) número de pruebas y secuencia realizada; 3) impacto de la pandemia COVID-19 en los objetivos previos.
Material y métodos
Inclusión de pacientes consecutivos desde 27-ene-15 hasta 27-dic-21 con CHC único <= 3 cm. Se registraron las variables basales, la fecha de detección, diagnóstico, y tratamiento/entrada en lista de espera de trasplante, y la secuencia de pruebas realizadas (TC, RM, biopsia). Se definió tiempo hasta el diagnóstico (periodo desde la detección hasta el diagnóstico), tiempo hasta el tratamiento (desde el diagnóstico hasta la fecha del tratamiento/entrada en lista de espera para trasplante) y tiempo global (la suma de los previos). Se analizaron los resultados de forma global y divididos en dos periodos: era pre-COVID (ene-15 hasta feb-2020) y post-COVID (mar-20 hasta la actualidad).
Resultados
Se registraron 685 pacientes con CHC, de los cuales 128 fueron tumor único <= 3 cm, 18% en la era pre-COVID y 22% en la era post-COVID. Las características basales de los pacientes se muestran en la TABLA 1. Se llegó al diagnóstico por criterios no invasivos (imagen) en 112 pacientes y por biopsia en 16.
Las pruebas realizadas se muestran en la TABLA 2. No se hallaron diferencias estadísticamente significativas en la capacidad diagnóstica entre la TC multifásica (67,6%) y la RMN dinámica (73,3%), p-valor 0.113. No hubo diferencias en el método diagnóstico (imagen vs biopsia) según el tamaño del nódulo (21.43 mm vs 21.13 mm), p-valor 0.199; ni en el número de estudios realizados en función de la secuencia (TC-RM-Biopsia vs RM-TC-Biopsia vs otros), p-valor 0.746.
El tiempo al diagnóstico, al tratamiento y el tiempo global figuran en la TABLA 3. Se hallaron diferencias significativas en el tiempo al tratamiento entre la era pre-COVID y post-COVID; p-valor 0.038.
CP-080. HEMATOMA HEPÁTICO TARDÍO TRAS COLANGIOPANCREATOGRAFÍA RETRÓGRADA ENDOSCÓPICA (CPRE): UNA COMPLICACIÓN INFRECUENTE
Muíño Domínguez D1, Flórez Díez P1, Varela-Calvo M1, Garcia Calonge M1, González Sánchez MH1, González Parra AC2, Izquierdo Romero M1
1Servicio Aparato Digestivo. Hospital Universitario Central de Asturias, Oviedo. 2Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: cpre, hematoma, ecografía.
Introducción
El hematoma hepático tras la realización de una colangiografía retrograda endoscópica (CPRE) es una complicación rara con pocos casos descritos, pero que puede comprometer la vida del paciente, necesitando un diagnóstico preciso y precoz.
Caso clínico
Mujer de 88 años que ingresa por un cuadro de ictericia obstructiva, con ecografía abdominal urgente que objetiva coledocolitiasis en tercio proximal del colédoco, realizándose CPRE para limpieza de la vía biliar (Fig. 1). Durante la prueba se visualiza la papila desplazada en el borde de un divertículo duodenal, realizándose papilotomía y limpieza con balón de Fogarty de 12 mm en varios pases, extrayéndose varias litiasis. Tras 24 horas de observación la paciente es dada de alta.
37 días después acude nuevamente por dolor abdominal de 3 días refractario a analgesia oral, sin otro síntoma asociado. En la exploración presenta dolor en hipocondrio derecho. Analíticamente destaca únicamente una Hb de 10.2 g/dL (al alta 11.5 g/dL). La ecografía abdominal urgente muestra un hematoma intrahepático en segmento VI de 9x6x5 cm (Fig. 2). La paciente es ingresada para vigilancia, tratándose con éxito de forma conservadora.
Discusión
El primer caso de hematoma intrahepático tras CPRE se diagnosticó en 2001 y desde entonces se han publicado más de 30 casos, un número pequeño para el volumen de CPRE que se realizan. Habitualmente sucede entre horas y varios días después de la prueba. La sospecha clínica se obtiene cuando un paciente después de realizar una CPRE presenta dolor abdominal intenso acompañado en la mayor parte de los casos de una caída del hematocrito y de la Hb. El diagnóstico se realiza por ecografía, TAC o RNM. La fisiopatología no está clara, barajándose dos posibilidades: una relacionada con el daño de los vasos intrahepáticos por la guía metálica; otras, más probable, con la tracción ejercida por el balón en el pedículo, dañando los vasos intrahepáticos. Para pacientes hemodinámicamente estables y sin signos de infección se sugiere un tratamiento conservador, haciendo un abordaje más activo con drenaje percutáneo en casos complicados.
La particularidad de nuestro caso reside en la latencia entre la CPRE y la detección del hematoma, de más de un mes, al presentar síntomas inespecíficos y leve anemización para el tamaño del hematoma. Por tanto, parece relevantes tener presente la posibilidad de un hematoma intrahepático con clínica larvada y más tardíamente de lo publicado hasta la fecha.
CP-081. HEMOPERITONEO ESPONTÁNEO COMO DEBUT DE CARCINOMA HEPATOCELULAR.
Ortiz Chimbo DS1, Aparicio Serrano A1, Valdivia Krag C1, Leiva-Cepas F2, RodrÍguez Perálvarez ML1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba. 2UGC Anatomía Patológica. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: hepatocarcinoma, hemoperitoneo, embolización .
Introducción
El carcinoma hepatocelular es un tumor hipervascular que constituye la forma más frecuente de cáncer primario del hígado. El 90% se presenta sobre un hígado en estadio cirrótico. El aumento de carga vascular por hipertensión portal, conlleva al sangrado. Su ruptura espontánea se observa en el 3 - 15 % de los casos, siendo su rotura espontánea la principal causa de muerte(5). Por lo infrecuente y su relevancia clínica, presentamos el siguiente caso clínico.
Caso clínico
Se trata de un varón de 67 años con antecedente de hipertensión arterial, hepatitis aguda A en su infancia por consumo de agua contaminada y serología compatible con hepatitis B pasada con inmunidad, exbebedor hasta hace 20 años de 30-40 gramos/día y exfumador abusivo.
Acude por dolor abdominal en flanco derecho, malestar general y marcada hipotensión (80/40mmhg). Se realizó tomografía abdominal y se objetivó hemoperitoneo agudo, procedente de una lesión focal hepática de gran tamaño, que en la resonancia magnética se comporta como hipervascular con lavado en fase portal, junto a una masa de carácter neoplásico con posible origen en el cuerpo vertebral de la tercera vertebra lumbar con extensión al canal raquídeo y espacio paravertebral; además se objetivó signos radiológicos de hepatopatía crónica de base. Los marcadores tumorales fueron negativos, incluido alfafetoproteína.
Tras embolización urgente de la rama arterial de la lesión hepática que producía el hemoperitoneo, la evolución fue favorable. Posteriormente se realizó toma de biopsia de la lesión paravertebral, confirmándose que se trataba de una hepatocarcinoma avanzado, estadio C de la BCLC. El grado de diseminación tumoral desestimó cualquier intervención con intención curativa.
Figura 1
A: TC abdomen con contraste fase arterial. Corte coronal. Hemoperitoneo agudo con punto de sangrado activo en segmento VIII. B: Corte axial. En segmento VIII se observa captación irregular heterogénea y con contornos nodulares periféricos, que podría corresponder con una lesión focal hepática.
Figura 2
A: TC abdomen y pelvis con contraste fase arterial. Corte sagital. Masa vertebral/paravertebral izquierda, con probable origen en cuerpo vertebral L3. B: Corte axial. Dicha masa se extiende posteriormente hacia el canal raquídeo condicionando una estenosis del 50-60%.
Figura 3
Embolización arterial selectiva con microesferas. Gran tumoración hepática hipervascular central con lesiones satélites y sin visualizar sangrado activo. Dado el antecedente, se decide embolizar dicha porción con microesferas de 400 micras con buen resultado técnico.
Figura 4
A: RM de columna lumbosacra. Corte coronal. Gran masa retroperitoneal izquierda de 12 x 9 x 12 cm que desplaza el riñón izquierdo, psoas y grandes vasos, perdiendo planos de separación con el riñón y la musculatura. B:Corte sagital. Dicha masa invade la columna vertebral a la altura de L3.
Figura 5
A: RM dinámica de Hígado. Gran lesión hepática lobulada, en segmentos IV y VIII, en su parte más craneal zonas de aspecto necrohemorrágico y en su parte caudal un aspecto hipervascular que posteriormente lava el contraste. B y C : Varias lesiones nodulares en LHI de hasta 19 mm y en segmentos V-VI.
Discusión
En conclusión, la rotura espontánea del carcinoma hepatocelular con hemoperitoneo secundario, es infrecuente y constituye una urgencia vital. El riesgo de sangrado aumenta cuanto más grande es la extensión tumor y cuanto más periférico y exofítico protruye sobre el margen hepático.
Su síntoma principal es el dolor abdominal, seguido de repercusión hemodinámica e incluso shock hipovolémico, siendo en estos casos necesario un tratamiento hemostático intervencionista para evitar el sangrado continuo o repetido.
La ecografía abdominal y la tomografía computarizada helicoidal (TC), constituyen las técnicas de elección en su diagnóstico. El manejo implica la estabilización hemodinámica, corrección de la coagulopatía y lograr la hemostasia a través de medios médicos, radiológicos intervencionistas e incluso quirúrgicos.
CP-082. HEMOPERITONEO POR ROTURA DE HEPATOCARCINOMA, COMPLICACIÓN INFRECUENTE
González Parra AC, Fernández Mascuñano M, Mouhtar El Hálabi S, Castro Márquez C, Caunedo Álvarez A
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: hemoperitoneo, hepatocarcinoma, complicación.
Introducción
El hemoperitoneo secundario a rotura espontánea de carcinoma hepatocelular (HCC) es una rara complicación, estimándose una incidencia de 3%, con mortalidad de 25-75% según casos reportados. El cuadro clínico más frecuente consiste en dolor abdominal y ascitis hemorrágica. Se debe tener un alto índice de sospecha para plantear diagnóstico y tratamiento precoz.
Caso clínico
Varón de 50 años, antecedente de infección crónica por virus de la hepatitis C (VHC), tratado y curado con antivirales de acción directa en 2019, evolucionada a cirrosis hepática con hipertensión portal clínicamente significativa. Ingreso a finales de 2021 por hematemesis detectándose durante el mismo HCC multicéntrico con trombosis portal tumoral, estadio C de la BCLC. Función hepática estadio A de Child-Pugh, con buena situación basal (performance status 0). Se decidió inicio de terapia sistémica con Atezolizumab-Bevacizumab desde enero de 2022, suspendiéndose tras 5 meses por deterioro del estado general y progresión clínica de la enfermedad tumoral.
Acude a Urgencias tras cinco meses de la suspensión de inmunoterapia por dolor abdominal inespecífico, aumento de perímetro abdominal y encefalopatía hepática grado III. Al examen físico, estabilidad hemodinámica, abdomen distendido y doloroso de forma difusa sin peritonismo. Se realizó paracentesis evacuadora, con extracción de líquido hemorrágico en dos puntos distintos de punción no documentado previamente. Analíticamente, hemoglobina similar a previas, reactantes de fase aguda normales y fracaso renal agudo. Ante las características del líquido ascítico, a pesar de mantener estabilidad hemodinámica, se solicitó tomografía computarizada (TC) que confirmó colección hepática en relación a coágulo en íntima relación a foco de hepatocarcinoma excéntrico de 32 mm en segmento VII además sangre en zona pélvica, tratándose por tanto de rotura espontánea de foco de hepatocarcinoma sin sangrado activo (figura 1).
Por comorbilidades y enfermedad tumoral avanzada con mala función hepática se decidió actitud expectante, sin nuevos datos de resangrado y evolución favorable del proceso hemorrágico.
Discusión
Durante le evolución del HCC se han descrito numerosas complicaciones siendo las dos causas de muerte más frecuente consecuencia de su extensión a distancia o del deterioro de la función hepática.
La rotura espontánea con hemoperitoneo se debe sospecharse ante un cuadro agudo de dolor abdominal y evidencia de sangrado (anemización, inestabilidad hemodinámica, líquido ascítico hemorrágico). El diagnóstico se establece por prueba de imagen y el manejo depende de la situación basal del paciente así como el estadio tumoral, pudiendo plantearse tratamiento endovascular, quirúrgico o conservador en caso de enfermedad terminal.
CP-083. HEMORRAGIA DIGESTIVA ALTA COMO DEBUT DE PROTOPORFIRIA ERITROPOYÉTICA
Soler Góngora M, Gijón Villanova R, López Peña C, Caballero Mateos AM
Servicio Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: hepatopatía, protoporfiria, protoporfiria eritropoyética.
Introducción
Las porfirias son un grupo de enfermedades caracterizadas por alteraciones enzimáticas en la biosíntesis del grupo hemo. Las tres porfirias más frecuentes son la porfiria aguda intermitente, la porfiria cutánea tarda y la protoporfiria eritropoyética. Las manifestaciones clínicas pueden ser: cutáneas, neuroviscerales, hepáticas y eritropoyéticas.Las alteraciones hepáticas pueden ser variables, desde hipertransaminasemia leve hasta cirrosis y hepatocarcinoma. A continuación, se presenta un caso de protoporfiria eritropoyética cuya forma de debut fue un cuadro de dolor abdominal y hemorragia digestiva alta.
Caso clínico
Varón de 40 años natural de Senegal, sin antecedentes de interés, que acude a urgencias por dolor abdominal, hematemesis y deposiciones melénicas de 12 horas de evolución, manteniéndose hemodinámicamente estable.
Se realiza endoscopia digestiva alta (EDA) urgente, apreciándose tres cordones varicosos, uno grande y dos medianos, con puntos predictivos de sangrado en dos de ellos. Se colocan cinco bandas elásticas quedando la zona estable. Ante nuevo episodio de hematemesis se repite EDA bajo soporte de UCI sin evidenciar puntos de sangrado y con bandas normoposicionadas.
De forma ambulatoria se realiza estudio de hepatopatía con resultado negativo y AngioTC que demuestra hepatopatía crónica con trombosis parcial de la porta, esplenomegalia, múltiples colaterales porto-sistémicas y una incipiente cavernomatosis portal.
En control analítico posterior se objetiva anemia ferropénica microcitica, plaquetopenia de 57.000 y déficit de proteína S secundaria a hepatopatía. Con tal de completar el estudio se solicita estudio de porfirias, con hallazgo de un incremento de protoporfirinas libres (154,3) en plasma y heces.
Se realiza por tanto el diagnóstico de hepatopatía crónica secundaria a protoporfiria eritropoyética, iniciándose profilaxis secundaria de hipertensión portal con propranolol y anticoagulación con tinzaparina por parte de Hematología.
Discusión
La protoporfiria eritropoyética es la segunda de las porfirias más frecuente tras la porfiria cutánea tarda. Su origen reside en un déficit congénito de la enzima ferroquelatasa, que se transmite de forma autosómica dominante. Suele tener un curso clínico benigno con afectación cutánea como manifestación universal, aunque en nuestro caso lo principal que desencadenó el estudio fueron los datos de hipertensión portal. Hasta un 25% de los pacientes pueden tener algún grado de afectación hepática, de los que un 5% pueden presentar un cuadro rápidamente progresivo de insuficiencia hepática aguda, siendo indicación de trasplante hepático. Ningún tratamiento encaminado a disminuir la carga de protoporfiria en el hígado ha demostrado su utilidad, de ahí la importancia de vigilar la función hepática de estos pacientes para evitar el fallo hepático agudo.
CP-084. HEMORRAGIA DIGESTIVA MASIVA REFRACTARIA DE ORIGEN VARICEAL EN CIRROSIS HEPÁTICA CON HIPERTENSIÓN PORTAL.
Angulo McGrath I, Martínez Burgos M, Bracho González M, Bravo Aranda AM
Departamento Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: hemorragia digestiva, cirrosis hepática, hipertensión portal, .
Introducción
La cirrosis es una enfermedad crónica con una elevada mortalidad. Constituye la quinta causa de muerte en adultos.
Las varices gastroesofágicas están presentes en aproximadamente el 50% de los pacientes con cirrosis; del 30-40% de pacientes con cirrosis compensada, y hasta en el 85% de pacientes con cirrosis descompensada. La hemorragia digestiva (HD) de origen variceal es una complicación con elevada mortalidad.
Caso clínico
Varón de 48 años. Cirrosis hepática de origen enólico en abstinencia. Presenta cuadro de hematemesis y rectorragia con tendencia a la inestabilidad hemodinámica al ingreso. Hb de 10 gr/dL, que desciende a 7 gr/dL. Se inicia perfusión de somatostania a 6 mg/12 horas y se realiza gastroscopia urgente que identifica cordón varicoso único esofágico de pequeño tamaño que aplana con la insuflación, ausencia de varices subcardiales ni fúndicas, ni sangrado activo. En ileocolonoscopia programada se aprecian abundantes restos hemáticos y coágulos a lo largo de todo el colon sin identificarse lesiones que puedan ser causa de sangrado activo.
Tras 5 días de ingreso y bajada de dosis de somatostatina presenta rectorragia con inestabilidad hemodinámica. Hb de 5 gr/dL. AngioTC urgente que aprecia contraste a nivel de asa localizada en FII (fosa ilíaca izquierda), sugestivo de hemorragia digestiva a dicho nivel (Figuras 1 y 2). Divertículo en 4º porción duodenal. Arteriografía urgente no identificarse sangrado arterial activo. Se repite angioTC por persistencia de sangrado masivo, identificando contenido denso a nivel de asa ileal localizada en fosa ilíaca derecha, que se extiende hasta todo el marco cólico (Figura 3).
Realizamos enteroscopia intraoperatoia a través de enterotomía en intestino delgado, explorando desde válvula ileocecal hasta ángulo de Treitz, con abundante contenido hemático y coágulos, sin identificar punto de sangrado activo. Gastroscopia en mismo acto revela divertículo en 4º porción duodenal con gran coágulo en su interior sin visualizar lesiones potencialmente sangrantes. Enteroscopia de control a las 24 horas identifica impronta en divertículo duodenal que podría corresponder a variz a dicho nivel, sin identificarse sangrado activo.
Finalmente se decide colocación derivación portosistémica percutánea intrahepática (TIPS) (Figura 4) urgente, presentando reinicio de sangrado a las 72 horas. Ante fallo multiorgánico a pesar de medidas de soporte se decide limitación del esfuerzo terapéutico.
Figura 1.
AngioTC de aorta y bifurcación ilíaca. Corte axial. Se señala la presencia de contraste a nivel luminal en FII.
Figura 2.
AngioTC de aorta y bifurcación ilíaca. Corte coronal. Se identifica contrasta intraluminal. Diverticulo en 4º porción duodenal.
Discusión
La HD secundaria a colaterales desarrolladas por hipertensión portal es una complicación de elevada mortalidad. El objetivo con el caso expuesto es resaltar la gravedad de dicha entidad, en ocasiones aún no controlable en determinados cuadros clínicos a pesar del continúo estudio y avances en cuanto al manejo y prevención de la misma.
CP-085. HEPATITIS AGUDA DE ORIGEN TÓXICO SECUNDARIA A SUPLEMENTO DE PROTEÍNAS WHEY PARA GANANCIA DA MASA MUSCULAR
Benavente Oyega MA, García Martinez A
Servicio Aparato Digestivo. Hospital de Especialidades de Jerez de la Frontera, Jerez de la Frontera.
Palabras clave: hepatitis, tóxica, proteínas.
Introducción
La hepatitis aguda de causa tóxica es una entidad relativamente poco frecuente y cuyo diagnóstico se realiza mediante la exclusión de otras etiologías más frecuentes.
Caso clínico
Presentamos el caso de un varón de 60 años, sin antecedentes de interés que ingresó en nuestra unidad de Digestivo por ictericia mucocutánea desde hace dos semanas, así como coluria, molestias epigástricas postprandiales y pérdida de peso. La exploración física no aportó más información que la evidente ictericia. Analíticamente destacaba la elevación de la bilirrubina tanto directa como indirecta (BbT 6.37 mg/dl y BbD 4.6 mg/dl), así como hipertransaminasemia (GOT 780 U/L y GPT 859 U/L) y colestasis (GGT 1628 U/L y FA 555 U/L), siendo el hemograma y la coagulación normales. Se realizó una exhaustiva anamnesis descartándose la ingesta de alcohol, relaciones sexuales de riesgo, viajes recientes, fármacos, ingesta de agua o alimentos potencialmente contaminados. Sin embargo, refería haber comenzado un suplemento dietético proteico (proteína Whey) aproximadamente un mes antes del comienzo de la clínica, el cual sugirió ser el agente causante del cuadro actual. Se realizó estudio de serología viral, autoinmunidad y metabolopatías, las cuales resultaron negativas. Además, ecografía y TAC de abdomen, sin más alteraciones que colelitiasis sin datos de complicación y edema periportal.
Una vez comprobada la adecuada evolución del paciente se procedió al alta hospitalaria, suspendiéndose la toma del producto proteico y realizándose seguimiento ambulatorio donde se objetivó mejoría clínica y analítica progresiva.
Discusión
El origen tóxico de la hepatitis aguda debe tenerse en cuenta dentro del diagnóstico diferencial del daño hepático, bien sea agudo o crónico. La forma de presentación más común simula el cuadro clínico de una hepatitis aguda vírica, con ictericia, náuseas y en ocasiones dolor abdominal. Analíticamente el patrón de daño puede ser de tres tipos, bien hepatocelular, colestásico o mixto. El diagnóstico se alcanza mediante la identificación del potencial agente causante, presencia de una secuencia temporal plausible, así como la exclusión de otras causas más comunes de hepatitis aguda. En cuanto al tratamiento, resulta fundamental la retirada del fármaco o agente que haya podido causar el cuadro en cuanto sea identificado. Por último, la gravedad viene determinada por el estado clínico del paciente y de la coagulación, dado que en caso de encefalopatía hepática o tasa de protrombina inferior al 40%/INR> 1.5, el paciente debe ser trasladado a un centro de referencia donde pueda realizarse un trasplante en caso de ser necesario.
CP-086. HEPATITIS DE ORIGEN TÓXICO SECUNDARIA A TRATAMIENTO DE FERTILIZACIÓN IN VITRO
Benavente Oyega MA, García Martínez A
Servicio Aparato Digestivo. Hospital de Especialidades de Jerez de la Frontera, Jerez de la Frontera.
Palabras clave: hepatitis, tóxica, fertilización .
Introducción
La hepatitis aguda de origen tóxico es una entidad poco frecuente y que se diagnostica tras la exclusión de otras etiologías más frecuentes.
Caso clínico
Presentamos el caso de una mujer de 39 años, sin antecedentes de interés, que ingresa en nuestra unidad de Digestivo por clínica y analítica compatibles con hepatitis aguda. Un mes antes del ingreso realizó, por segunda vez, un tratamiento de fertilización in vitro con filotropina alfa, menotropina y acetato de Ganirelix, comenzando a la semana siguiente con coluria e ictericia conjuntival, así como aumento de la bilirrubina (BbT 4.8 mg/dl, BbD 3.9 mg/dl), hipertransaminasemia (GOT 1227 U/L, GPT 2471 U/L) y colestasis (GGT 113 U/L y FA 169), con hemograma y coagulación normales, que motivó el ingreso previo en otro hospital. Dos semanas más tarde se constató un aumento de los parámetros analíticos (destacando: BbT 26.3 mg/dl, BbD 15 mg/dl), siendo derivada a nuestro centro, hallándose además alteración de la coagulación (INR 1.25). A la exploración se encontró ictericia mucocutánea, sin signos de encefalopatía.
En cuanto a la anamnesis, se descartaron relaciones sexuales de riesgo, ingesta de alcohol, viajes o consumo de productos contaminados. Se realizó ecografía de abdomen sin hallazgos patológicos, así como serología de virus, autoinmunidad y estudio de metabolopatías, todos negativos.
Afortunadamente la evolución fue favorable, lo que permitió el alta hospitalaria. Descartando otras posibles etiologías, se consideró el tratamiento para fertilización in vitro como el causante del cuadro, desaconsejándose una nueva administración.
Discusión
El origen tóxico de la hepatitis aguda debe tenerse en cuenta dentro del diagnóstico diferencial del daño hepático tanto agudo como crónico. La forma de presentación más común simula el cuadro clínico de una hepatitis aguda vírica, con ictericia, náuseas y ocasionalmente dolor abdominal. Analíticamente encontramos tres patrones de daño: hepatocelular, colestásico o mixto. El diagnóstico se realiza mediante la identificación del posible agente causante, una secuencia temporal plausible, y la exclusión de otras causas más comunes de hepatitis aguda. En cuanto al tratamiento, resulta fundamental la retirada del agente que haya podido causar el cuadro en cuanto sea identificado. Por último, la gravedad viene determinada por el estado clínico del paciente y de la coagulación, dado que en caso de encefalopatía hepática o tasa de protrombina inferior al 40%/INR> 1.5, el paciente debe ser trasladado a un centro de referencia donde pueda realizarse un trasplante en caso de ser necesario.
CP-087. HEPATOCARCINOMA SOBRE HÍGADO CIRRÓTICO CON RESPUESTA TUMORAL COMPLETA TRAS TRATAMIENTO CON SORAFENIB
CASTRO RODRÍGUEZ J, ORTIZ CHIMBO DS, VALDIVIA KRAG C, BARRERA BAENA P, COSTAN RODERO G, RODRÍGUEZ PERÁLVAREZ ML, MONTERO ÁLVAREZ JL, POYATO GONZÁLEZ A
UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: hepatocarcinoma, sorafenib, respuesta completa.
Introducción
El hepatocarcinoma constituye la tercera causa de muerte por cáncer en el mundo. La cirrosis hepática es el principal factor de riesgo implicado en su desarrollo. El estadío avanzado (BCLC-C) se define por la presencia de invasión portal, diseminación extrahepática y/o performance status 1-2, con función hepática conservada (Child-Pugh A). También se incluyen los estadíos A/B que progresan a pesar de terapias locorregionales (migración de estadío). En estos pacientes está indicado el tratamiento con terapias sistémicas.
Caso clínico
Se expone el caso de un varón de 60 años, diagnosticado de cirrosis hepática de origen etílico y por VHC (con respuesta viral sostenida), y con función hepática conservada (Child-Pugh A5), únicamente con una descompensación previa en forma de ascitis. Como datos de hipertensión portal presentaba varices esofágicas grandes, por las que se encontraba en profilaxis primaria con propranolol, gastropatía leve y esplenomegalia.
Desde 2017 presentaba una elevación leve y fluctuante de alfa-fetoproteína (Fig.1), pero sin evidencia de hepatocarcinoma en las sucesivas pruebas de imagen realizadas (ecografía, TC y RM). Sin embargo en marzo de 2020 dicho marcador tumoral se eleva por encima de 10000, evidenciándose por primera vez por TC una lesión nodular hipervascular en segmento VI. Se completa estudio con RM, mostrando una lesión sugestiva de hepatocarcinoma con una trombosis portal adyacente, y por tanto en estadío avanzado BCLC-C (Fig.2-3).
Se decide iniciar tratamiento sistémico con Sorafenib 400mg/ 12 horas en junio de 2020. Como efectos secundarios el paciente desarrolla un síndrome mano-pie grado I-II que requiere la reducción de dosis a la mitad. La evolución del paciente hasta la fecha ha sido favorable, consiguiendo la normalización de los valores de alfa-fetoproteína (Fig.1), la práctica desaparición de la lesión hepática en la RM, quedando una pequeña imagen hipovascular residual en su lugar, así como la desaparición de la trombosis tumoral (Figs.4-5).
Figura 1
Gráfico que muestra la evolución en el tiempo de los niveles de alfa-fetoproteína en analíticas seriadas. Se puede visualizar el rápido descenso de los niveles séricos de dicho marcador tumoral tras iniciar el tratamiento sistémico con Sorafenib, manteniéndose en cifras normales hasta la actualidad.
Figura 2
RM T1 con contraste (mayo 2020), axial (A,B) y coronal (C). Hígado con signos de hepatopatía crónica, con lesión hipervascular en segmento VI de límites mal definidos y al menos 6 cm de eje axial máximo, sugestiva de hepatocarcinoma (circulo rojo). Porta permeable de 19 mm. Adenopatías periportales.
Figura 3
RM T1 con contraste (mayo 2020), coronal (A) y axial (B). La lesión se extiende a la rama portal derecha para el segmento VI, la cual se muestra aumentada de calibre, con un trombo en su interior (flechas verdes). Trombosis portal tumoral.
Figura 4
RM T1 con contraste (mayo 2021), axial (A,B): Signos de hepatopatía crónica, con atrofia del LHD e hipertrofia del LHI y caudado. Prácticamente ha desaparecido la lesión hipervascular en segmento VI, así como la trombosis tumoral de la rama portal derecha para el segmento VI, observadas en previo.
Figura 5
RM T2 (A) y T1 (B) (marzo 2022): sin cambios con respecto estudio previo. Ha desaparecido la lesión y la trombosis portal, quedando en su lugar una pequeña imagen hipovascular de aspecto residual en segmento VI y una línea hipointensa respectivamente (círculos amarillos). Sin nuevas lesiones.
Discusión
A pesar de la aparición de los nuevos tratamientos sistémicos para el hepatocarcinoma, el sorafenib continúa siendo una de las terapias de primera línea en estadíos avanzados. Es un inhibidor múltiple de tirosin-kinasa, usado por vía oral, y fue el primer fármaco en demostrar beneficio pronóstico en pacientes con hepatocarcinoma avanzado, con incremento de la supervivencia media en torno a 10 meses. No obstante resulta infrecuente alcanzar la respuesta tumoral y radiológica completa con sorafenib, y es por ello por lo que nuestro caso resulta excepcional.
CP-088. HIPERTRANSAMINASEMIA NO SIEMPRE ES SINÓNIMO DE HEPATOPATÍA
Asady Ben G, Fernández García F, Pinazo Bandera JM, Andrade Bellido RJ
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Virgen de la Victoria, Málaga.
Palabras clave: hiperckemia, hipertransaminasemia, miopatia.
Introducción
Presentamos el caso de un varón de 28 años, sin alergias medicamentosas ni antecedentes médico-quirúrgicos conocidos. Como hábitos tóxicos, bebedor ocasional de bajo riesgo y no consumidor de fármacos habitualmente. Trabaja como camarero.
Caso clínico
fluctuante de perfil citolítico (50-300 U/L), discreta hipercolesterolemia, molestias abdominales inespecíficas y coluria intermitente.
La exploración física es normal; normopeso y sin estigmas clínicos de cirrosis.
No existe relación directa con el consumo de medicamentos, productos herbales o anabolizantes. El estudio de hepatopatía resulta negativo (virus hepatotropos, autoinmunidad, celiaquía, alfa-1 antitripsina, perfil ferrocinético, tiroideo y del cobre); ecografía abdominal anodina y elastografía sin fibrosis significativa.
No se logra normalizar las alteraciones analíticas a pesar de medidas higienico-dietéticas instauradas, incluyendo abandono del alcohol. Indagamos entonces sobre otros hábitos de vida al reparar en una elevación paralela de creatina kinasa (2000-15000 U/L). El paciente reconoce practicar deportes de alta intensidad tipo artes marciales, a pesar de molestias musculares incluso con pequeños esfuerzos. Se deriva a Medicina Interna para descartar miopatías previo a plantear la realización de biopsia hepática como último eslabón del algoritmo diagnóstico. Dicho servicio completa el estudio con análisis de orina en el que se detecta mioglobinuria y test genéticos para despistaje de miopatías metabólicas. De esta forma se confirma mutación en el gen PYGM, compatible con enfermedad de McArdle.
Discusión
La enfermedad de McArle es una enfermedad rara, de herencia autosómica recesiva, que condiciona un déficit en la síntesis de la enzima miofosforilasa. Su función es la de degradar el glucógeno muscular para la obtención de energía, la cual en estos pacientes se encuentra limitada, traduciéndose en los síntomas y alteraciones analíticas previamente descritos. El interés del caso radica en la importancia de considerar estas entidades como causa de hipertransaminasemia, especialmente cuando existe una hiperCKemia asociada.
CP-089. HIPOGLUCEMIA SECUNDARIA AL USO DE SOMATOSTATINA: A PROPÓSITO DE UN CASO.
Rodríguez Gómez VM, López Vico M, Tendero Peinado C, Redondo Cerezo E, López González E
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: somatostatina, hipoglucemia..
Introducción
En pacientes cirróticos con hemorragia digestiva secundaria a varices esofágicas contamos con diversos abordajes terapéuticos: ligadura con bandas elásticas, shunts portosistémicos, taponamiento esofágico o métodos farmacológicos. Uno de los fármacos más empleados es la somatostatina, un vasoconstrictor esplácnico que ha demostrado eficacia en el control del sangrado digestivo secundario a hipertensión portal que cuenta con escasos efectos adversos graves. Un evento adverso poco frecuente son las crisis hipoglucémicas, como hemos objetivado en el caso que vamos a presentar a continuación.
Caso clínico
Paciente varón de 64 años con antecedentes personales de cirrosis hepática enólica y por VHC con hipertensión portal (gastropatía hipertensiva y varices esofágicas) que presenta cuadro de hemorragia digestiva alta. Tras tratamiento endoscópico urgente con ligadura con bandas elásticas, se inicia perfusión de somatostatina a dosis habitual de 6mg cada 12 horas. Al comienzo de la infusión, el paciente presenta episodio de sudoración, mareo y náuseas. Se mantiene normoconstante, sin cortejo vegetativo ni signos de sangrado. Se realiza glucemia capilar, objetivando glucosa de 40mg/dL. Tras tratamiento de soporte y reducción de dosis de somatostatina, el paciente queda asintomático. Tras 24 horas, el paciente presenta nuevo episodio similar con glucemia capilar de 52mg/dL; por lo que, dada la ausencia de signos de sangrado, se suspende la perfusión de somatostatina y el paciente recupera su estado basal.
Discusión
La somatostatina ha demostrado evidencia en el control del sangrado digestivo en pacientes con hipertensión portal, ya que reduce significativamente los valores de presión portal y portocolateral, siendo escasas y poco relevantes las complicaciones asociadas. Entre losefectos secundarios poco frecuentes encontramos la hipoglucemia (0.1-1% frente al 1-10% de la hiperglucemia), la cual se produce tras el comienzo de la infusión, seguida de una hiperglucemia compensatoria, por lo que se recomienda control glucémico estricto cada 3-4 horas durante el tratamiento. Asimismo, si la hemorragia se controla, es aconsejable reducir la dosis de forma progresiva para evitar el efecto rebote. En comparación con la terlipresina, otro de los fármacos empleados en hemorragia secundaria a hipertensión portal, ésta presenta una eficacia similar con menores eventos adversos metabólicos.
CP-090. ICTERICIA COMO MANIFESTACIÓN DE SÍNDROME PARANEOPLÁSICO
Tendero Peinado C, Rodríguez Gómez VM, García Aragón F, Redondo Cerezo E, Fernández Cano MC
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: ictericia, hiperbilirrubinemia, stauffer.
Introducción
Las neoplasias en ocasiones producen sintomatología a distancia de los tumores primarios o de sus metástasis, siendo esto conocido como síndrome paraneoplásico.
El síndrome de Stauffer corresponde a un conjunto de cambios clínicos y analíticos de naturaleza paraneoplásica en asociación principalmente con el carcinoma de células renales.
Caso clínico
Paciente de 88 años con antecedentes personales de adenocarcinoma de próstata con metástasis óseas que acude por coloración amarillenta de piel y conjuntivas y coluria de varios días de evolución. Niega dolor abdominal, náuseas o vómitos, fiebre u otra sintomatología.
Analíticamente destaca bilirrubina total en 9 a expensas de bilirrubina directa, GGT 780 y FA 420, plaquetas 400.000, PCR 45, Albúmina 3.2, TP 55% y resto de la analítica anodina. Se realiza Ecografía y TAC abdominal, descartándose en ambos dilatación de la vía biliar intra o extrahepática o la presencia de metástasis, objetivándose esplenomegalia.
A la anamnesis dirigida fueron descartadas otras causas de colestasis (fármacos, antecedentes epidemiológicos de interés, productos de herbolario…), siendo negativas las serologías de virus hepatotropos.
Discusión
El carcinoma de células renales es la neoplasia primaria que con más frecuencia se asocia con el Síndrome de Stauffer. Sin embargo, aunque existen menos casos descritos, puede aparecer en relación con otros tumores como el cáncer de próstata (nuestro caso), carcinoma de vejiga, leiomiosarcoma o disgerminoma ovárico, adenocarcinoma bronquial, enfermedad de Hodgkin…
Existe una versión clásica del síndrome de Stauffer y una variante del mismo (mucho menos frecuente), diferenciándose en que esta última contempla la elevación de bilirrubina, ictericia y prurito, siendo la versión clásica anictérica.
Los síntomas y cambios analíticos que caracterizan a ambos son la elevación de FA, GGT, plaquetas, tiempo de protrombina, alfa-2-globulina y VSG, así como la disminución de albúmina y la presencia de hepatoesplenomegalia.
La fisiopatología del síndrome no es bien conocida, aunque en diferentes estudios se ha objetivado una elevación de IL-6 inflamatoria.
Para su diagnóstico es necesario excluir previamente tanto colestasis iatrogénica como por otras causas, así como las metástasis hepáticas.
El tratamiento consiste en el control de la enfermedad (extirpación del tumor primario o tratamiento oncológico sistémico), siendo la reversibilidad una de sus características fundamentales.
Nuestro paciente, tras descartar otras causas posibles de colestasis, fue diagnosticado de la variante de síndrome de Stauffer.
Dada la frecuencia con la que nos enfrentamos a la hiperbilirrubinemia en Aparato Digestivo, es interesante conocer y tener en mente la posibilidad de encontrarnos ante este cuadro.
CP-091. IDONEIDAD DE LA UTILIZACIÓN DE TRES DETERMINACIONES EN LA MEDICIÓN DE LA ELASTICIDAD HEPÁTICA MEDIANTE ELASTOGRAFÍA DE TRANSICIÓN (FIBROSCAN®).
Valdivia Krag C, Ortiz Chimbo DS, Cerezo Ruiz A, Monrobel Lancho A, Reyes López A
UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: fibroscan, elasticidad hepática, mediciones. .
Introducción
Evaluar la correlación y grado de acuerdo entre la realización de tres mediciones frente a diez para determinar el grado de elasticidad hepática mediante Elastografía de Transición (ET).
Material y métodos
Se recogieron de forma prospectiva las diez mediciones preceptivas de elasticidad hepática obtenidas mediante ET (Fibroscan®) en 109 pacientes consecutivos que se realizaron la prueba diagnóstica por distintas indicaciones en nuestro centro, desde el 1 de abril al 23 de junio 2022. Se aplicó tanto el Coeficiente de correlación lineal de Pearson (r), como el Diagrama de Bland-Altman, para evaluar el grado de correlación y acuerdo respectivamente entre la mediana de dichas mediciones y la mediana resultante de las tres primeras medidas de los mismos pacientes.
Resultados
Se obtiene un Coeficiente de correlación lineal de Pearson de r = 0,978 (p<0.001) que muestra una alta correlación entre la mediana de las tres y las diez primeras medidas válidas, calculando la regresión lineal simple de la recta que ilustra dicha correlación (Figura 1).
Posteriormente, el Diagrama de Bland-Altman (Figura 2) muestra un buen grado de acuerdo con una media de la diferencia de elasticidad hepática entre las dos modalidades de medición de -0,509±2,105 KPa, estando los límites de acuerdo alrededor de la media situados entre -2,61 y 1,59 KPa con un 95% de confianza.
CP-092. IMPACTO DE LA PANDEMIA POR SARS COV-2 EN EL SEGUIMIENTO ENDOSCÓPICO DE VARICES ESOFÁGICAS
Librero Jiménez M, Herrador Paredes M, Sánchez Capilla AD, Redondo Cerezo E
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: varices esofágicas, sars-cov2.
Introducción
La pandemia por COVID-19 ha producido un colapso de la asistencia sanitaria a distintos niveles, incluyendo servicios de Aparato Digestivo de todo el mundo. Por ello AEG y SEED elaboraron un documento de consenso con el objetivo de priorizar las endoscopias no demorables. A pesar de esto, distintos motivos han llevado al retraso/falta de seguimiento endoscópico en pacientes incluidos en programa de ligadura endoscópica de varices esofágicas (LEVE). Nuestro objetivo fue analizar el impacto de la pandemia en dicho seguimiento.
Material y métodos
Se presenta un estudio observacional, retrospectivo, descriptivo donde se incluyeron pacientes que estuviesen en seguimiento endoscópico para LEVE antes del inicio de la pandemia (Marzo 2020). Se llevó a cabo un seguimiento hasta la actualidad (Febrero 2022), recabando datos demográficos y clínicos, así como documentando los que continuaron sus revisiones adecuadamente, los que no, y el motivo, así como los que desarrollaron complicaciones durante dicho periodo.
Resultados
Se incluyeron 22 pacientes (varones 65%, mediana 57 años (rango IQ 47.3-62.5 años)) de los cuales 17 (77,3%) perdieron el seguimiento endoscópico establecido, aunque en dos de ellos no fue precisa ligadura en última endoscopia realizada (y uno de ellos falleció por otra causa no relacionada con su cirrosis). De los 15 pacientes restantes (68,2%), los motivos de demora se recogen en la Tabla 1.
La mediana de tiempo de demora fue de 183 días (rango IQ 149-229) entre la última EDA del programa de cribado y la siguiente EDA de control.
Como consecuencia de ello dos pacientes de los que perdieron el seguimiento (13,3%) presentaron un episodio de Hemorragia Digestiva Alta secundaria a sangrado por varices esofágicas de gran tamaño que precisaron ingreso hospitalario. No obstante, solo uno de los pacientes (6,7%) precisó transfusión de hemoderivados (7 concentrados de hematíes) e ingreso en UCI, mientras que ninguno falleció por dicho motivo. Por el contrario, ninguno de los pacientes que continuaron el seguimiento presentaron complicaciones hemorrágicas derivadas de la HTPo.
Conclusiones
El impacto de la pandemia por COVID-19 en el seguimiento de pacientes con diferentes patologías crónicas continúa siendo un importante problema de gestión sanitaria. En el análisis de nuestra muestra comprobamos que la mayoría de pacientes (68,2%) perdieron el seguimiento endoscópico del programa de cribado de VE, con una mediana de demora de 183 días. Aunque la repercusión en términos de complicaciones mayores (HDA) o supervivencia no parece ser significativo, serían necesarios estudios multicéntricos con mayor número de pacientes para establecer conclusiones estadísticamente significativas.
CP-093. IMPORTANCIA DEL DIAGNÓSTICO Y TRATAMIENTO PRECOZ DE DISNEA EN UN PACIENTE CIRRÓTICO
Fernández García R1, Lecuona Muñoz M1, Alarcón Blanco PA2, Redondo Cerezo E1, López Garrido M1
1Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada. 2Servicio Medicina Interna. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: htpp, vhb, cirrosis.
Introducción
La hipertensión portopulmonar (HTPP) es una rara complicación de la cirrosis, con un curso y pronóstico sombríos sin tratamiento. Debemos descartarla en todo paciente cirrótico con disnea, ya que, es la única complicación pulmonar derivada de la hipertensión portal (HTP) que puede beneficiarse de tratamiento farmacológico. Este es el caso de una paciente con rápido diagnóstico de HTPP en el contexto de una cirrosis por VHB
Caso clínico
Mujer de 30 años, con antecedente de cirrosis por VHB (Child -Pugh A5) e HTP en tratamiento con entecavir. Acude a Urgencias, por cuadro de disnea progresiva, tras cesárea 12 días antes. En la exploración física destaca: saturación de oxígeno del 87% y edemas en MMII. Analíticamente presenta; BNP: 904 pg/ml y en GSV: pH 7,47 PaCO2: 24mmHg y PaO2: 59,3mmHg .
Para descartar disnea de origen cardiogénico se realiza ecocardiografía transtorácica (ETT) con dilatación de cavidades derechas y se completa estudio con ETT con contraste, que describe dilatación de ramas pulmonares y paso de burbujas de cavidades derechas a izquierdas entre el sexto y séptimo latido. Todo ello compatible con HTPulmonar. Se solicita cateterismo derecho que objetiva PCP de 15mmHg con PAP de 50mmHg que disminuye a 30mmHg tras administrar epoprostenol, manteniendo gasto cardiaco y resistencias vasculares de 8uw.
Se pauta precozmente, Tadalafilo, Macitentán y Trepostinil, produciéndose una importante mejoría sintomática y analítica: BNP: 120 pg/ml, PaO2: 88 mmHg .
Discusión
Los pacientes con hepatopatía grave pueden presentar alteraciones pulmonares. Estos síndromes pulmonares son: el síndrome hepatopulmonar y la HTPP. Ambos constituyen los extremos de un espectro de vasculopatía pulmonar que va desde la vasodilatación a la vasoconstricción. Si bien guardan relación patogénica con la hipertensión portal, tienen mecanismos fisiopatológicos opuestos.
La HTPP se produce por una vasoconstricción pulmonar persistente secundaria al hiperaflujo pulmonar en el contexto de la HTPortal. Entre los métodos diagnósticos encontramos la ecocardiografía con contraste que aportará signos sugestivos, y el cateterismo cardiaco derecho que es la prueba de referencia. Este síndrome, a diferencia del hepatopulmonar, presenta la posibilidad de tratamiento farmacológico mediante vasodilatadores, que permiten mejorar la sintomatología y enlentecer la progresión (disminuyendo la PAPm hasta en un 25%), pero de manera paliativa. En última instancia, en función de la PAPm, es posible la realización de trasplante hepático, que puede constituir un tratamiento definitivo.
Por tanto, si bien es infrecuente, debemos tener en mente este síndrome, ante todo paciente con cirrosis e HTPortal que debute con disnea, sin obviar en primer lugar otras causas frecuentes de la misma.
CP-094. INDAGAMOS EN EL ORIGEN DE UNA COLESTASIS DISOCIADA
Camacho Domínguez P, López Ocaña A, González Amores Y, Asady Ben GR
Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Virgen de la Victoria, Málaga.
Palabras clave: colestasis, vasculitis, diagnóstico diferencial.
Introducción
Las vasculitis sistémicas son un grupo de enfermedades complejas y heterogéneas que pueden afectar a cualquier sistema, y con frecuencia al aparato digestivo. Las manifestaciones clínicas son muy variadas e inespecíficas. Por lo tanto, descifrar si nos encontramos ante un paciente con este tipo de patología no conocida previamente, supone un reto para el gastroenterólogo.
Caso clínico
Mujer de 56 años con antecedente de Dengue, que acude por dolor en epigastrio e hipocondrio derecho de 4 días de evolución, asociando fiebre, ictericia y coluria. Analíticamente resaltaban hiperbilirrubinemia y elevación de FA, GGT y PCR. Se comenzó antibioticoterapia con Piperacilina-Tazobactam por sospecha de colangitis y se realizaron colangiorresonancia magnética y ecografía, observándose hallazgos sugestivos de hepatitis aguda, descartándose dilatación de la vía biliar y litiasis. Tras días de hospitalización, la ictericia desapareció pero persistieron picos febriles y datos analíticos de colestasis disociada. Además, la paciente comenzó a presentar debilidad de cintura escapular y pelviana (síndrome polimialgia-like), acompañado de escleritis y cefalea. Una exploración difícil de pulsos temporales, motivó realización de una ecografía Doppler de arterias temporales, obteniéndose un resultado anodino. Posteriormente, se llevó a cabo un estudio completo de autoinmunidad, serología viral, ecocardiograma, angioTAC y biopsia hepática, sin objetivarse alteraciones. Como tratamiento del cuadro inflamatorio presente, se iniciaron corticoides de forma empírica a dosis de mg/kg. Se decidió realizar biopsia de arteria temporal y PET TC, evidenciándose en ésta última, afectación inflamatoria de la aorta torácica ascendente. La biopsia fue negativa, sin poder descartar un resultado falseado por la corticoterapia y por la probable afectación arterítica parcheada. Tras una semana de tratamiento, se observó una importante mejoría de la clínica sistémica de la paciente, y un descenso de la colestasis y de parámetros inflamatorios. Finalmente, se concluyó como diagnóstico una vasculitis de grandes vasos, como es el caso de la arteritis de células gigantes. Se procedió al alta con Prednisona 60 mg. En la revisión, destacó franca mejora del estado general de la paciente, con desaparición de la cefalea y clínica ocular, y ausencia de colestasis.
Discusión
El diagnóstico de una vasculitis sistémica en un paciente cuyas manifestaciones iniciales se limitan al aparato digestivo (en nuestro caso, alteración hepática por afectación de grandes vasos abdominales), puede resultar complejo. En esto radica la importancia de realizar una exploración completa y un amplio diagnostico diferencial, no solo al inicio del cuadro, sino durante la evolución del mismo, permitiendo así obtener un diagnóstico definitivo temprano.
CP-095. INFECCIÓN POR LÚES. UNA ENTIDAD A CONSIDERAR EN EL CONTEXTO DE UNA HEPATITIS AGUDA.
Valdivia Krag C, Órtiz Chimbo DS, El Fallous El Mraghid M, Poyato González A
UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: sífilis, virus hepatitis b, infección de transmisión sexual. .
Introducción
Las infecciones de transmisión sexual (ITS) han experimentado un crecimiento progresivo en los últimos años. En concreto la sífilis presentó en España una tasa de incidencia de 13.29 casos por 100.000 habitantes en al año 2019, una cifra no vista antes. Muchas de las ITS, además de compartir mecanismos de transmisión, tienen tropismo hepático por lo que su cribado inicial, tanto en pacientes con hepatitis aguda como en aquellos con diagnóstico de ITS, es de gran interés.
Caso clínico
Varón de 55 años sin antecedentes de interés que consulta por coluria y acolia desde hacía una semana, junto con ictericia mucocutánea franca en las últimas 24 horas. Había consumido recientemente carne de caza, marisco crudo, así como productos de herboristería (Colestia®). Asimismo, refería exposiciones sexuales de riesgo con parejas masculinas no estables, la última hacía 3 meses, así como ingesta de hasta 60 gramos de alcohol los fines de semana. En la analítica destacaba una elevación de enzimas de citolisis (AST/ALT 1123/2210 U/l) y moderada colestasis (Tabla 1). Dado que no había coagulopatía ni presentaba signos de encefalopatía fue dado de alta con el diagnóstico de hepatitis aguda sin criterios de gravedad, pendiente de completar el estudio etiológico. En dicho estudio destacaba positividad para el antígeno de superficie e IgM frente al antígeno del VHB, así como anticuerpos RPR para la sífilis (título 1/64) (Tabla 1), siendo valorado posteriormente en consultas de Hepatología y Enfermedades Infecciosas para seguimiento de la hepatitis aguda por VHB y tratamiento y cribado de otras ITS, respectivamente.
En la tabla 1 se muestra la evolución de los datos analíticos destacando el aclaramiento del antígeno de superficie, pero sin desarrollar anticuerpos frente a éste y una cuantificación del DNA-VHB de 1.200 UI/ml que posteriormente se negativizó sin necesidad de recibir tratamiento antiviral, al tiempo que se producía una normalización de las enzimas de citólisis. Se descartaron otras ITS recibiendo tratamiento con tres dosis de penicilina G benzatina, con buena evolución clínica y analítica.
CP-096. ISQUEMIA HEPÁTICA Y ESPLÉNICA SECUNDARIA A ESTENOSIS DE TRONCO CELIACO POR ARTERIOSCLEROSIS SEVERA
Morales Bermúdez AI1, Bracho González M1, Palomino Luque P2, Jiménez Pérez M1
1UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga. 2UGC Aparato Digestivo. Hospital Comarcal de la Axarquía, Vélez-Málaga.
Palabras clave: isquemia, hígado, estenosis tronco celíaco.
Introducción
El tronco celiaco se origina de la arteria aorta abdominal y tiene tres ramas principales: arteria hepática común, esplénica y gástrica izquierda. Es responsable del suministro arterial de numerosas vísceras abdominales (hígado, vesícula biliar, páncreas, bazo, estómago, esófago distal y duodeno proximal). Presentamos un caso de isquemia hepática y esplénica por estenosis de tronco celíaco secundaria a arteriosclerosis severa.
Caso clínico
Mujer de 76 años. Hipertensa, dislipémica y diabética con afectación macrovascular. Polineuropatía diabética. Arteriopatía periférica. Ingresa en Cardiología por insuficiencia cardíaca congestiva secundaria a miocardiopatía dilatada de origen isquémico con enfermedad severa de 3 vasos. Ante la situación clínica de mejoría progresiva y estabilización con manejo médico, se decide tratamiento conservador inicial de su patología coronaria. En controles analíticos durante su hospitalización se objetiva empeoramiento agudo de perfil hepático (GOT 852, GPT 591, GGT 634, bilirrubina normal) y elevación de RFA (leucocitosis 31000 y PCR 210) sin clínica abdominal asociada, por lo que se solicita TC de abdomen: infarto hepático y esplénico con posible trombosis del eje esplenoportal. Arteriosclerosis de aorta, tronco celíaco, arteria mesentérica superior e iliacas. Posteriormente se realiza ecografía doppler abdominal, que descarta la presencia de trombosis esplenoportal y detecta pulso parvus tardus en arteria hepática y arteria esplénica en relación con estenosis de tronco celíaco. Radiología Vascular desestima intervención sobre la misma dado ausencia de clínica actual, mejoría analítica progresiva y valorando riesgo-beneficio. Fue dada de alta tras resolución de clínica congestiva y continúa seguimiento en consulta, sin incidencias hasta la fecha.
Discusión
La estenosis del tronco celíaco se puede deber a diferentes causas: extrínsecas (sd. del ligamento arcuato, invasión maligna, compresión por procesos inflamatorios como pancreatitis…), intrínsecas (arteriosclerosis) o idiopática. Se presenta con mayor frecuencia en mujeres con una edad media de 60 años. Solo un porcentaje pequeño de pacientes presentan síntomas debido al desarrollo de circulación colateral a lo largo del tiempo. En algunos casos pueden aparecer síntomas, como dolor difuso pospandrial y/o pérdida de peso. La enfermedad de dos vasos o una estenosis > 70 % producen síntomas susceptibles de tratamiento, siendo el tratamiento de elección la revascularización endovascular (angioplastia con balón o stent). En el caso de nuestra paciente no se llevó a cabo terapéutica ante la ausencia de clínica digestiva y por mayor riesgo que beneficio debido a la edad y comorbilidades asociadas.
CP-097. LEPTOSPIROSIS ICTÉRICA: A PROPÓSITO DE UN CASO.
Frutos Muñoz L, De Vicente Ortega A, Martín Marcuatu P, Rodriguez Tirado I
UGC Aparato Digestivo. Complejo Hospitalario de Jaén, Jaén.
Palabras clave: ictericia, leptospira.
Introducción
La enfermedad de Weil (leptospirosis ictérica) es una zoonosis potencialmente mortal que prevalece principalmente en los países tropicales y es causada por la infección por Leptospira interrogans (serovar icterohaemorrhagiae). Se caracteriza por una tendencia hemorrágica generalizada y ocasionalmente daño severo a muchos órganos, incluyendo el hígado, riñón, músculo esquelético, pulmón y sistema cardiovascular.
Caso clínico
Presentamos el caso de un paciente que consulta por ictérica franca y fiebre de hasta 38,7º. A su llegada mal estado general con hipotensión y taquicardia asociada. En analítica destacaba hiperbilurrubinemia a expensas de directa, alteración de transaminasas (mayor citólisis) sin estar en rango de hepatitis aguda, plaquetopenia y fracaso renal agudo.
Se realizó ecografía abdominal urgente, sin alteraciones significativas en la exploración. Posteriormente requiere ingreso en UCI, para soporte vasoactivo. Tras varios días en UCI con evolución tórpida, hemorragia alveolar con anuria completa que precisó terapia renal sustitutiva.
Tras solicitar estudio y realizar un amplio diagnóstico diferencial con otras patologías y alta sospecha de que se tratase se una leptospirosis se obtuvo serología positiva IgM positiva para la misma, recibiendo tratamiento dirigido con doxiciclina.
Discusión
La leptospirosis puede complicarse con ictericia e insuficiencia renal (¨enfermedad de Weil¨), hemorragia pulmonar, síndrome de dificultad respiratoria aguda (SDRA), uveítis, neuritis óptica, neuropatía periférica, miocarditis y rabdomiólisis.
La terapia de reemplazo renal de apoyo puede ser necesaria durante la fase aguda. La insuficiencia hepática es generalmente reversible y no es una causa de muerte.
CP-098. LINFANGIOMA CAVERNOSO COMO DIAGNÓSTICO DIFERENCIAL DE ASCITIS. A PROPÓSITO DE UN CASO.
NAVARRO MORENO E1, AMADO VILLANUEVA PP2, SANCHEZ MORENO S1
1UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería. 2UGC Aparato Digestivo. Hospital de la Cruz Roja Española, Palma de Mallorca.
Palabras clave: ascitis, quiste, lingangioma cavernoso.
Introducción
El linfangioma es una tumoración malformativa benigna del sistema linfático que se da con mayor frecuencia en la región craneo-facial o cervical. Se diagnostica habitualmente en la infancia. El diagnóstico se basa en pruebas de imagen, pero es necesaria la confirmación histopatológica y su tratamiento es la exéresis quirúrgica. Se presenta el caso de un paciente de 63 años con clínica de aumento progresivo del perímetro abdominal.
Caso clínico
Paciente de 71 años sin antecedente personales de interés. Como hábitos tóxicos es bebedor de un vaso de vino al día y ex fumador desde hace 5 años. Consulta por cuadro de aumento del perímetro abdominal de un año de evolución que actualmente le ocasiona dificultad respiratoria y molestias abdominales difusas. Niega pérdida de peso, alteración del hábito intestinal, hiporexia, vómitos u otra sintomatología. En analítica de sangre no se observan alteraciones significativas. Se realiza ecografía abdominal en urgencias que identifica gran cantidad de líquido libre intraabdominal por lo que se realiza paracentesis diagnóstica objetivando la salida de líquido marronáceo achocolatado que tras su análisis y cálculo del gradiente albúmina sérica, albúmina líquido ascítico (GASA) hace poco probable un origen por hipertensión portal. Durante el ingreso se realiza TC abdominal que muestra una ureterohidronefrosis izquierda G-III/IV secundaria a compresión de gran masa mesentérica, septada, de 36 x 28 x 22 cm con diagnóstico diferencial de mesotelioma o pseudoquiste no pancreático (Figura 1). El paciente es intervenido quirúrgicamente para exérisis de la masa con diagnóstico anatomopatológico (Figura 2) de malformación vascular, tipo linfangioma cavernoso, de larga evolución. Tras la exérisis el paciente evoluciona de forma favorable sin requerimiento de tratamiento posterior.
Figura 1
imagen de TC abdominal donde se observa masa que ocupa prácticamente la totalidad del abdomen y produciendo una ureterohidronefrosis izquierda.
Discusión
Los linfangiomas se consideran neoplasias benignas que se presentan habitualmente en la infancia. Si su crecimiento es lento, pueden presentarse en el adulto, siendo extremadamente raros. Se forman a partir de secuestros de vasos linfáticos primitivos o de anomalías en el desarrollo de espacios embrionarios. Se clasifican en tres tipos: capilar, quístico y cavernoso, siendo éste el más raro.
Suelen ser asintomáticos, pudiendo producir en algunos casos obstrucción intestinal o compresión extrínseca de las vías urinarias. El diagnóstico se realiza a través de pruebas de imagen, normalmente de TC y el tratamiento es la resección quirúrgica. La particularidad de nuestro caso y lo que lo hace de interés es la edad y modo de presentación, reforzando la importancia de un buen diagnóstico diferencial de las ascitis.
CP-099. LOE HEPÁTICA DE EXTRAÑA ETIOLOGÍA.
Soler Góngora M, Gutiérrez Holanda C, Barrientos Delgado A, López Peña C, Berdugo Hurtado B
Servicio Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: linfoma, tumor hepático, hígado.
Introducción
El linfoma de origen primario hepático es una entidad excepcional, representando el 0,016% de todos los linfomas no Hodgkin. Su patogenia no está claramente definida, relacionándose en ocasiones con procesos virales (VEB, VHC, VIH) y de inmunodeficiencia (cirrosis, LES, tratamiento inmunosupresor).
Caso clínico
Varón de 63 años, hipertenso, diabético y con antecedente de pericarditis aguda en 2013 que acude a consulta de Aparato Digestivo por epigastralgia posprandial irradiada a hipocondrio izquierdo de dos meses de evolución asociando náuseas sin vómitos. Tras estudio ecográfico, en TC abdominal se confirma una extensa lesión focal que ocupa el lóbulo hepático izquierdo (LHI), de 77x97x87 mm, con densidad y captación heterogéneas y áreas de aspecto quístico-necrótico en su interior. No se aprecian trombosis portal ni signos de hepatopatía crónica.
Se realiza toma de biopsia ecodirigida que muestra infiltración por una neoplasia linfoide (CD45+) de fenotipo B (CD20+ y PAX-5), con positividad para CD10 y Bcl-6 y en torno al 30-40% para c-myc con Ki-67 del 80-90%, diagnosticándose linfoma B difuso de células grandes, fenotipo centro germinal. Se deriva al paciente a Oncología para inicio de quimioterapia y se solicita PET-TC que informa de masa hipermetabólica en lóbulo hepático izquierdo, que invade parcialmente el segmento IV del derecho, junto con otro foco sobre un nódulo en el espacio precardiaco y refuerzo axilar bilateral sobre adenopatías de centro graso, confirmándose estadio IIIE-A de Ann Arbor, al encontrarse el paciente asintomático.
Se somete a tratamiento con seis ciclos de esquema R-CHOP comprobando en TC de control ausencia de afectación en ganglios linfáticos e hígado, con significativa reducción del volumen de LHI y LHD de contorno y densidad normales, sin identificar lesiones sospechosas.
Discusión
A pesar de su infrecuencia, el LHP debe incluirse dentro del diagnóstico diferencial de las lesiones ocupantes de espacio hepáticas. En el momento diagnóstico, para que un linfoma pueda ser considerado originario del hígado, los síntomas deben reflejar afectación de ese parénquima, sin detectarse alteraciones de ganglios linfáticos, sangre periférica ni médula ósea. Su diagnóstico requiere de una alta sospecha clínica y adecuadas imágenes, pero la histología es primordial para su confirmación y orientación del tratamiento. Aunque aún controvertido, la bibliografía apoya el uso de esquemas R-CHOP, alcanzando, si es identificado y tratado correctamente, mejor supervivencia que el carcinoma hepatocelular, con un promedio a 5 años del 83,1%.
CP-100. MANEJO DE LA ANEMIA CRÓNICA SECUNDARIA A GASTROPATÍA DE LA HIPERTENSIÓN PORTAL Y COLONOPATÍA DE LA HIPERTENSIÓN PORTAL EN PACIENTES CON CONTRAINDICACIÓN A BETABLOQUEANTES.
González Parra AC, Silva Albarellos E, Grande Santamaría L, Caunedo Álvarez A
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: gastropatía, octreótido, tips.
Introducción
La gastropatía de la hipertensión portal es una complicación descrita entre un 20-98% de los pacientes cirróticos. Su principal manifestación es anemización progresiva, estando presente entre un 3- 60% de los mismos. Sin embargo la colonopatía de la hipertensión rectal es mucho menos frecuente, identificándose en un 3-71% de los pacientes. En ambos casos los betabloqueantes es tratamiento de elección, situándose el TIPS como rescate en segunda línea.
Caso clínico
Se trata de un varón de 64 años, abstinente desde abril 2021, con antecedentes de hipertensión arterial y EPOC severo. En seguimiento por hepatología enfermedad hepática relacionada con alcohol (Child Pugh B8, MELD 9) con datos de hipertensión portal (varices esofágicas pequeñas y gastropatía severa de la hipertensión portal) hallazgos que, acordes a Baveno VII, son indicación de profilaxis primaria de sangrado con betabloqueantes. Sin embargo su patología pulmonar contraindica el betabloqueo. En colonoscopia se objetiva colonopatía de la hipertensión portal y varices rectales.
Acude en mayo 2022 a urgencias por hallazgo de anemia con Hb 7.6 (basal en torno a 8.5 g/dL). Se realiza endoscopia urgente, observándose sangrado difuso procedente de la gastropatía de la hipertensión portal, no subsidiario de tratamiento endoscópico (Figuras 1 –3). Clínicamente el paciente describe deposiciones melénicas de forma crónica.
Ante la situación de contraindicación a betabloqueo y anemización progresiva el paciente se planteó como candidato a TIPS. Mientras se realiza el estudio y tras realizar una revisión de la literatura, nos planteamos añadir de forma experimental un análogo de los receptores de somatostatina de forma domiciliaria, pautando octreótido a dosis empleadas en las angiodisplasias.
En sucesivas revisiones el paciente ha presentado algún episodio autilimitado de melenas pero sin mayor anemización, manteniendo cifras de Hb en torno a 8.5- 9.5 g/dL, sin efectos adversos y sin nuevas transfusiones en hospital de día. En endoscopia de control no se observó sangrado activo (Figura 4).
Figura 1
Gastropatía de la hipertension portal, mucosa congestiva con sangrado difuso no tratable endoscopicamente.
Discusión
El octreótido intravenoso es tratamiento de primera línea ante sangrado digestivo agudo por hipertensión portal. Respecto al octreótido subcutáneo no existen estudios suficientes en humanos para su recomendación en sangrados crónicos, sí está aceptado para el tratamiento de la hemorragia digestiva por angiodisplasias.
En nuestro paciente la contraindicación de betabloqueo y el difícil control del síndrome anémico por sangrado crónico nos hizo plantearnos una terapia puente al TIPS. Iniciamos tratamiento con octreótido subcutáneo (50 mcg /12 horas) durante 6 meses obteniendo una respuesta favorable, considerada como estabilización de anemización sin nuevos requerimientos transfusionales.
CP-101. MANIFESTACIONES DIGESTIVAS RELACIONADAS CON EL TRATAMIENTO CON PEMBROLIZUMAB
Barranco Castro D, García García MD, Castro Márquez C, Caunedo Álvarez A
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: pembrolizumab, colecistitis aguda inmunomediada, hepatitis aguda inmunomediada.
Introducción
Los inhibidores de puntos de control inmunitario (ICIs) han revolucionado la terapia antineoplásica en los últimos años. El anticuerpo monoclonal humanizado pembrolizumab genera una proliferación y activación permanente de los linfocitos T mediante la inhibición del receptor PD-1 presente en su membrana. Este mecanismo rompe con la tolerancia inmunológica frente a células cancerígenas, actuando así contra ellas. Sin embargo, esto puede desembocar en una reactividad inmunitaria excesiva frente a células propias, generando enfermedades autoinmunes inducidas por el fármaco.
Caso clínico
Mujer de 63 años sin antecedentes personales de interés, con diagnóstico reciente de adenocarcinoma de pulmón T4N3M0 estadio IIIC no resecable quirúrgicamente, en tratamiento por decisión de comité multidisciplinar con pembrolizumab y quimioterapia con pemetrexed y cisplatino.
Acude a urgencias por astenia, dolor en hemiabdomen superior y fiebre de hasta 39,5ºC de 15 días de evolución y de inicio 4 días tras la primera dosis de pembrolizumab, junto a ictericia mucocutánea las últimas 24 horas. Analíticamente presentaba hiperbilirrubinemia de 5,29mg/dL a expensas de directa, transaminasas diez veces por encima del valor normal (AST 2847, ALT 588), alargamiento de tiempos de coagulación (INR 1,44, tiempo de protrombina 16,7s), marcada respuesta inflamatoria (PCR 126,4mg/L, procalcitonina 19,7ng/mL) y deterioro agudo de la función renal (Cr 2,36mg/dL). El TC de abdomen realizado en urgencias, describía un engrosamiento de la pared vesicular, sin contenido en su interior, compatible con colecistitis aguda alitiásica (imagen 1). Ante estos hallazgos se inició antibioterapia empírica con piperacilina/tazobactam. Se solicitó además estudio completo de hepatopatía, descartándose virus hepatotropos y autoinmunidad como causa de hepatitis aguda asociada, y se realizó colangiorresonancia (imagen 2) y ecoendoscopia, que no evidenciaron colelitiasis ni coledocolitiasis. El estudio se completó con angio-TC, que excluyó una posible causa isquémica. Descartadas otras etiologías, ante la sospecha de colecistitis y hepatitis aguda inmunomediada por pembrolizumab, se inició tratamiento con metilprednisolona 2mg/kg/24h, añadiendo a las 48 horas micofenolato mofetilo 1g/12h por empeoramiento de la función hepática. Con este tratamiento, la paciente presentó una mejoría progresiva de la bioquímica y función hepática, suspendiendo micofenolato a los 10 días y finalizando corticoides en pauta descendente.
Discusión
La toxicidad hepática es un efecto secundario inusual del tratamiento con ICIs. La tasa de hepatitis aguda inmune inducida por pembrolizumab es <1%, y solo un 5% de los casos cursan con toxicidad grado 3-4. Mucho menos frecuente es la colecistitis aguda inmunomediada por ICIs, siendo este el primer caso de colecistitis inducida por pembrolizumab descrito hasta la fecha.
CP-102. MICROHAMARTOSIS BILIAR MÚLTIPLE O COMPLEJOS DE VON MEYENBURG: UNA ENTIDAD POCO FRECUENTE.
Arroyo Argüelles JM, Martín Marcuartu P, Rebertos Costela E, de Vicente Ortega A
Servicio Aparato Digestivo. Complejo Hospitalario de Jaén, Jaén.
Palabras clave: von meyenburg, hamartosis biliar.
Introducción
La microhamartosis biliar múltiple o complejos de Von Meyenburg suele ser un hallazgo incidental en pacientes asintomáticos, habitualmente de comportamiento benigno.
No obstante, es importante conocer esta entidad para diferenciarla adecuadamente mediante técnicas de imagen frente a una posible enfermedad metastásica hepática, cuyo pronóstico y manejo es radicalmente distinto.
Caso clínico
Se presenta el caso de una mujer de 57 años de edad que consulta por dolor abdominal.
Como antecedentes personales padecía un trastorno depresivo y dislipemia, en fármacos antidrepesivos y estatinas.
Ante el cuadro abdominal y elevación franca de reactantes de fase aguda se decide realizar un TC abdominal (Figura 1) en el cual se evidencia un hígado de tamaño y morfología normal, con múltiples pequeños nódulos hipodensos puntiformes que podrían corresponder a hamartomas biliares o complejos de Von Meyenburg.
Finalmente, el paciente fue diagnosticado de debut de enfermedad de Crohn, quedando los hamartomas biliares como un hallazgo incidental.
Discusión
La microhamartosis biliar múltiple o complejos de Von Meyenburg es una malformación biliar poco frecuente (incidencia < 1%), originada a partir de la placa ductal, generalmente con un comportamiento benigno.
Se trata de múltiples estructuras biliares quísticas dilatadas rodeadas de un estroma fibroso.
El paciente casi en la totalidad de los casos se encuentra asintomático, tratándose de un hallazgo casual en una prueba de imagen realizada por otro motivo.
En cuanto a sus características radiológicas, en el TC aparecen como lesiones hipodensas. Por otro lado, en la RM suelen verse como lesiones múltiples de pequeño tamaño y contorno irregular, hipointensas en T1 e hiperintensas en T2, sin apreciarse comunicación con los conductos biliares.
La importancia de conocer esta entidad radica en distinguirla de una enfermedad metastásica hepática para lo cual, aparte de las pruebas de imagen, el contexto clínico del paciente son de gran utilidad. Así mismo también se debe establecer diagnóstico diferencial con los quistes y abscesos hepáticos.
El manejo suele ser conservador mediante vigilancia con técnicas de imagen periódicas. La transformación neoplásica es posible, aunque verdaderamente infrecuente.
CP-103. NEFRITIS TUBULOINTERSTICIAL INMUNOMEDIADA GRAVE TRAS REPUESTA COMPLETA CON ATEZOLIZUMAB-BEVACIZUMAB EN HEPATOCARCINOMA AVANZADO.
MOUHTAR EL HALABI SA1, FERNÁNDEZ ÁLVAREZ P1, MACHUCA AGUADO J2, CORDERO RUIZ P1, BELLIDO MUÑOZ F1, CARMONA SORIA I1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla. 2UGC Anatomía Patológica. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: hepatocarcinoma, nefritis, atezolizumab.
Introducción
Atezolizumab-Bevacizumab (AB) se ha posicionado como el tratamiento de primera línea en el tratamiento del hepatocarcinoma (HCC) avanzado. Se han descrito numerosos efectos adversos asociados a esta inmunoterapia, algunos de ellos mas frecuentes y otros que solo se limitan a serie de casos.
Caso clínico
Varón de 66 años, hipertenso, diabético tipo 2. En seguimiento por cirrosis hepática de etiología mixta (virus de la hepatitis B, metabólico, enólico). Función hepática estadio A de Child-Pugh, escala ECOG 0. En eco de abdomen de control se observó lesión hepática de 93mm en segmento VII, confirmándose en tomografía computarizada (TC) dinámica lesión con comportamiento típico de HCC y trombosis portal tumoral (Figura 1), estadio C de la BCLC. Se inició tratamiento con Atezolizumab-Bevacizumab con buena tolerancia. Tras 6 meses de terapia se repitió estudio dinámico de hígado, evidenciando ausencia de realce de la lesión tumoral en todas las fases (Figura 2), y permeabilidad esplenoportal, traduciendo respuesta completa al tratamiento. Ingresa por deterioro de la función renal hasta alcanzar niveles de creatinina de 3,8mg/dl, descartándose causas más frecuentes de daño renal. Se realizó biopsia renal que demostró nefritis intersticial y glomerulopatía proliferativa probablemente secundaria a inmunoterapia y antiangiogénico (Figura 3). Se suspendió tratamiento y se inició corticoides. Mejoría progresiva de función renal sin alcanzar niveles basales, evolucionado a enfermedad renal crónica.
Figura 1
A: lesión hepática con hipercaptación en fase arterial. B: lesión hepática con lavado en fase portal. Comportamiento sugestivo de hepatocarcinoma.
Discusión
Los efectos adversos inmunomediados más frecuentes secundarios a AB son los dermatológicos, gastrointestinales y endocrinológicos. Los efectos adversos renales son raros (2%). El primer caso de nefritis tubulointesticial inmunomediada por Atelozolizumab fue descrito en 2018, caso que también alcanzó repuesta radiológica. Bevacizumab se ha relacionado a microangiopatía trombótica y proteinuria. La probabilidad de nefrotoxicidad es más alta en combinación con ambos fármacos. Se ha descrito relación entre el desarrollo de efectos adversos inmunomediados y beneficio clínico en la respuesta antitumoral. El tratamiento de los eventos inmunomediados graves consiste en suspensión de la inmunoterapia e inicio de corticoides. Destacar la importancia del abordaje precoz y multidisciplinar de los efectos adversos asociados a estos tratamientos que facilitarán la resolución de los mismos.
CP-104. NEUMATOSIS PORTAL. ¿SITUACIÓN DE EMERGENCIA?
Tendero Peinado C, Rosa Sánchez C, López Vico M, Redondo Cerezo E, Fernández Cano MC
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: gas portal, dolor abdominal.
Introducción
La neumatosis portal hace referencia a la presencia de gas en el sistema venoso portal, cuya etiología es poco conocida y probablemente multifactorial. En ausencia de sintomatología, puede tratarse de un hallazgo incidental sin repercusión, sin embargo, sumado a dolor abdominal intenso, peritonismo, acidosis metabólica y neumatosis intestinal puede representar una afección potencialmente mortal.
Caso clínico
Paciente de 60 años con antecedentes de dislipemia, infarto crónico cerebral y hernioplastia umbilical. Consulta por cuadro de un día de evolución de dolor mesogástrico intenso, náuseas e importante repercusión del estado general. En la exploración física presenta distensión abdominal y signos de peritonismo junto con datos analíticos de hiperlactacidemia. Se solicita tomografía computarizada que objetiva dilatación gástrica y de intestino delgado sin obstrucción mecánica identificada, con neumatosis portomesentérica, mural gástrica y yeyunal, en probable contexto de hipoperfusión sin objetivar defectos de depleción vascular. Finalmente se indica laparoscopia exploratoria que descarta isquemia intestinal, con hallazgo único de adherencias de epiplón a hernioplastia umbilical, que se liberan. Tras unos días de hospitalización con antibioterapia de amplio espectro y buena evolución, el paciente es dado de alta.
Discusión
La neumatosis portal presenta una repercusión clínica variable además de etiología heterogénea. Aunque la fisiopatología no está clara, se considera un mecanismo responsable el paso de gas intraluminal directamente al sistema vascular a través de puntos de ruptura de la mucosa intestinal y/o secundariamente a la invasión bacteriana de submucosa o planos más profundos de la pared. Entre las causas se incluyen: dilatación gástrica, endoscopia digestiva compleja, infecciones, enfermedad inflamatoria intestinal, traumatismo abdominal, tumores o isquemia intestinal aguda. Ante un paciente con factores de riesgo cardiovascular, sintomatología compatible y hallazgos sugerentes en prueba de imagen, es prioritaria la realización de una laparoscopia exploratoria, dada la alta mortalidad que conlleva, mayor aún si existe retraso diagnóstico.
En este caso, el cuadro adherencial actuó como promotor de la sintomatología, afortunadamente de forma reversible, sin causar daño orgánico establecido. La presencia de neumatosis portal ejerció una influencia clave en el procedimiento diagnóstico, que facilitó una actuación urgente con la minimización de repercusiones potencialmente letales. En práctica clínica, es esencial conocer las posibles etiologías de este hallazgo radiológico y tenerlas en consideración para un correcto diagnóstico diferencial.
CP-105. NO TODO ES HEPATOCARCINOMA. CASO DE UN TUMOR HEPÁTICO PRIMARIO ATÍPICO.
Silva Albarellos E1, Fernández Álvarez P1, Cordero Ruíz P1, Bellido Muñoz F1, Machuca Aguado J2, Carmona Soria I1
1Departamento Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla. 2Departamento Anatomía Patológica. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: tumor, hepático, atípico.
Introducción
Los tumores mesenquimales malignos hepáticos son neoplasias primarias infrecuentes que se originan en las células endoteliales del hígado.
Caso clínico
Varón de 73 años con antecedentes de diabetes mellitus, cardiopatía isquémica y enfermedad renal crónica que es remitido a nuestro servicio por hallazgos radiológicos de hepatopatía crónica avanzada y presencia de LOE hepática en segmento VII-VIII. En pruebas de imagen dinámicas sucesivas (Figura 1) y ecografía con contraste destaca un crecimiento acelerado de la lesión, así como un comportamiento radiológico atípico para hepatocarcinoma. Por este motivo se decide realización de biopsia hepática percutánea. Los hallazgos histológicos (Figura 2) son indicativos de neoplasia maligna de hábito mesenquimal con positividad para CD31, lo cual orienta a una estirpe vascular, existiendo dudas entre el diagnóstico definitivo de hemangioendotelioma y angiosarcoma. En estos momentos el paciente se encuentra pendiente de ser valorado en la Unidad de referencia Nacional de Sarcomas en el hospital Virgen del Rocío para plantear posibles opciones terapéuticas.
Discusión
Las neoplasias mesenquimales hepáticas de estirpe vascular son entidades muy poco frecuentes en la práctica clínica habitual.
Teniendo en cuenta la edad, género y el rápido crecimiento tumoral, la naturaleza mas probable de la afectación neoplásica de nuestro paciente sea el angiosarcoma. Este tumor hepático tiene una incidencia en el mundo occidental entre 0,5-1 por millón de habitante, el 1,8% de los tumores hepáticos malignos. Generalmente afecta a varones mayores de 60 años. Para su detección son necesarias pruebas de imagen que en la mayoría de los casos resultan inespecíficas, siendo fundamental el estudio histológico para el diagnóstico de confirmación. El tratamiento quirúrgico es de elección cuando la lesión es resecable, sin embargo las recurrencias son frecuentes. El trasplante hepático no está recomendado por la alta tasa de recidiva.
Los tumores vasculares, como el hemagioendotelioma son los que generan mas dudas en el diagnóstico diferencial. Esta entidad de lenta progresión y de bajo grado de malignidad, es aun más infrecuente, habiéndose reportado tasas de incidencia de 0,001% en la población general. Es más frecuente en mujeres y se ha asociado al uso de anticonceptivos orales, así como a la exposición a cloruro de vinilo, hepatitis virales y consumo de alcohol. Aunque la enfermedad intrahepática limitada ocurre en menos del 10%, es estos casos, el trasplante hepático es de elección debido a que la mayoría de pacientes presentan lesiones multifocales al momento del diagnóstico.
CP-106. PANCREATITIS AGUDA COMO MANIFESTACIÓN EXTRAHEPÁTICA POR VIRUS DE LA HEPATITIS E: A PROPÓSITO DE UN CASO
Rodríguez Gómez VM, Ortega Suazo EJ, Lecuona Muñoz M, Redondo Cerezo E, Abellán Alfocea P
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: hepatitis e, pancreatitis..
Introducción
La infección por el virus de la hepatitis E (VHE), se produce mayoritariamente en países subdesarrollados dados los menores recursos sociosanitarios, controles de calidad de los productos alimenticios y tratamiento de aguas de riego. En países desarrollados, se produce fundamentalmente por la ingesta de carne de cerdo, marisco o frutas y verduras regadas con agua contaminada. La repercusión clínica secundaria al VHE es poco frecuente y se suele producir en pacientes que presentan hepatopatía crónica de base.
Caso clínico
Hombre, 64 años, antecedente de hemocromatosis (heterocigoto C282Y/H63D) sin requerir sangrías en el último año, esteatosis hepática grado II-III, diabetes y dislipemia. Consumidor de 30 gramos de alcohol/día. Acude a Urgencias por cuadro de malestar general, astenia, hiporexia, ictericia progresiva, coluria y acolia de 2 meses de evolución asociando vómitos en la última semana. Analítica a su llegada: bilirrubina total 14.78 mg/dl (que asciende a 26), bilirrubina directa 8.16 mg/dl, GOT 2128 U/L, GPT 2845 U/L, GGT 443 U/L, FA 264 U/L, Lipasa 920 U/L, Amilasa 237 U/L, INR 1.37, triglicéridos 230. TAC abdomen: datos de hepatopatía crónica y signos compatibles con pancreatitis aguda (Fig. 1). Ecoendoscopia: datos de hepatopatía crónica, descarta colelitiasis y/o obstrucción biliar. IgM/IgG VHE positivas, confirmándose con PCR. Resto de estudio de hepatopatía negativo. Dada la mala evolución del cuadro y por presentar hepatopatía crónica de base comienza tratamiento con Ribavirina presentando evolución clínica y analítica favorable.
Discusión
La infección VHE, es una patología emergente en países desarrollados. En la mayoría de casos, se desarrolla de forma asintomática. La clínica fundamentalmente se produce en pacientes con hepatopatía crónica de base, inmunodeprimidos y embarazadas. Cuando causa sintomatología, se puede presentar con un amplio espectro de manifestaciones clínicas tanto a nivel hepático como extrahepático. Entre la clínica extrahepática, aunque poco frecuente, se encuentra la pancreatitis aguda que puede ser leve-moderada con pocos casos severos reportados y buena respuesta a tratamiento conservador, asimismo, la anemia hemolítica, trombocitopenia o alteraciones neurológicas, las cuales, se sugiere que puedan ser debidas a un mecanismo inmunomediado por replicación viral. El tratamiento antiviral se recomienda cuando se produce un caso de hepatitis aguda grave o de fallo hepático agudo sobre crónico.
La mortalidad es baja en pacientes inmunocompetentes, aumentado notablemente en mujeres embarazadas y en pacientes inmunodeprimidos.
CP-107. PBE POR LISTERIA MONOCYTOGENES
León Sanjuan GF, García Martinez A, Campos Gonzaga L, Hernani Alvarez JA
Servicio Aparato Digestivo. Hospital de Especialidades de Jerez de la Frontera, Jerez de la Frontera.
Palabras clave: pbe, listeria, cirrosis.
Introducción
La peritonitis bacteriana espontánea (PBE) es la infección del líquido ascítico (LA) en pacientes con hepatopatía crónica avanzada. Es una complicación frecuente y grave, con una incidencia del 5-25% en pacientes cirróticos hospitalizados con ascitis. Los agentes causales que se aíslan con mayor frecuencia en el cultivo del LA son las enterobacterias como Escherichia coli y Klebsiella pneumoniae, y cocos gram positivos como Streptococcus pneumoniae. Otro microorganismo menos frecuente es la Listeria monocytogenes cuya incidencia anual estimada es de 0.2 casos/100.000 habitantes en Europa y Estados Unidos.
Caso clínico
Varón de 49 años con cirrosis hepática de origen enólico (alcoholismo activo hasta hace 1 mes) con hipertensión portal asociada y dos episodios previos de descompensación hidrópica (el último hace un mes). Ingresa por aumento del perímetro abdominal acompañado de dolor abdominal y disnea de 2 semanas de evolución, afebril. A la exploración destacaba un abdomen con semiología ascítica pero no a tensión ni doloroso a la palpación.
Analíticamente, destacaba deterioro de función renal con creatinina de 2,58 mg/dL (creatinina basal 0,69 mg/dL), bilirrubina total/directa 5,74/3,30 mg/dL, hiponatremia de 121 mEq/L, PCR de 120,3 mg/l y leucocitos 22.27 x10^3/μl, neutrófilos 18.82 x10^3/μl. Se realizó paracentesis diagnóstica, así como evacuadora extrayéndose 4 litros de líquido turbio con 2710 x 1/μL leucocitos, 74% polimorfonucleares, 58 mg/dL glucosa y 1.9 g/dL proteínas totales. Tras ello se pautó tratamiento antibiótico empírico con piperacilina/tazobactam por ingreso reciente, con buena evolución clínica y analítica. No obstante, en el cultivo del LA se aisló Listeria monocytogenes, modificándose la antibioterapia a ampicilina 2 g cada 4 horas cumpliendo tratamiento durante 10 -14 días y mejorando la clínica y alteraciones analíticas.
Discusión
- Listeria monocytogenes aunque es causa poco frecuente de PBE, se debe sospechar si la evolución clínica y/o analítica no es favorable en 48-72 horas de tratamiento empírico, especialmente en presencia de factores de riesgo conocidos para listeriosis como cirrosis, alcoholismo activo, inmunodepresión celular, neonatos, embarazadas y ancianos. Su identificación precoz permitiría una terapia antimicrobiana dirigida adecuada reduciendo la tasa de morbimortalidad.
- Profilaxis secundaria de PBE por microorganismos habituales: norfloxacino oral 400 mg/día. Esto se basa en la tasa de recurrencia de hasta el 70%/año, reduciéndose la morbimortalidad de estos pacientes con dicha terapia antimicrobiana.
- Existe controversia acerca de la profilaxis secundaria con cotrimoxazol en caso de PBE por Listeria monocytogenes, ya que no es un microorganismo habitual en la flora intestinal y serían necesarios más estudios al respecto.
CP-108. PERITONITIS SECUNDARIA A ROTURA DE QUISTE HEPÁTICO INFECTADO
Morales Bermúdez AI, Bracho González M, Bravo Aranda AM, Jiménez Pérez M
UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: quiste hepático, rotura, peritonitis.
Introducción
Los quistes hepáticos simples son formaciones quísticas rellenas de líquido presentes en el hígado. Constituyen la patología más frecuente del hígado, con una prevalencia del 2,5-5% y de predominio en mujeres. La mayoría son asintomáticos y se diagnostican de forma incidental en pruebas de imagen. No es necesario ningún tratamiento salvo que sean sintomáticos o presenten complicaciones.
Caso clínico
Mujer de 86 años. Hipertensa en tratamiento con un fármaco, sin otros antecedentes de interés. Acude a urgencias por distensión abdominal progresiva de 2 meses de evolución con episodios de dolor abdominal en los últimos días. No fiebre ni otra clínica asociada. No antecedente de traumatismo. A la exploración abdominal se objetiva hepatomegalia y dolor a la palpación de forma generalizada, sin signos de irritación peritoneal. En analítica destaca deterioro de la función renal (Cr 1,6) y elevación de reactantes de fase aguda (leucocitos 15900 y PCR 320) con perfil hepático normal. Se realiza TC de abdomen, donde se objetiva hígado con múltiples lesiones quísticas, colección de 19 cm que parece corresponder con quiste hepático del LHI complicado con rotura y ascitis generalizada secundaria. Se cubre empíricamente con piperacilina-tazobactam. Se realiza paracentesis diagnóstica con crecimiento en cultivo de liquido ascítico de Enterobacter cloacae sensible a antibioterapia prescrita. Además, se realiza drenaje percutáneo de líquido ascítico y del quiste hepático infectado. La paciente presenta buena evolución clínica y analítica y tras 10 días de antibioterapia dirigida y drenajes, se comprueba buena evolución radiológica, con disminución del tamaño de la colección, siendo posible retirar los drenajes y alta hospitalaria.
Discusión
Las complicaciones de los quistes hepáticos simples son poco frecuentes. La hemorragia intraquistica y la infección son las más frecuentes, aunque también pueden aparecer otras como rotura a la cavidad peritoneal o el conducto biliar o compresión del árbol biliar. La rotura de un quiste puede producirse como consecuencia de infección, traumatismo o iatrogenia, u ocurrir de forma espontánea.
No existe tratamiento estándar ante un quiste hepático roto. El tratamiento conservador parece ser la mejor opción en pacientes sin semiología de abdomen agudo; sin embargo en caso contrario, se recomienda tratamiento quirúrgico. Entre los procedimientos invasivos encontramos opciones que van desde el drenaje percutáneo hasta la hepatectomía. En nuestro caso, optamos por el tratamiento antibiótico debido a que la rotura del quiste era secundaria a infección del mismo, junto con drenaje percutáneo del quiste infectado y de la ascitis secundaria, ya que la paciente no presentó abdomen agudo a lo largo de su evolución.
CP-109. POLIQUISTOSIS HEPATORENAL HEREDITARIA NO CONOCIDA: CAUSA INFRECUENTE DE DOLOR ABDOMINAL
Martín-Lagos Maldonado A, Díaz Alcázar MDM, Bergudo Hurtado F, Ortiz Sánchez A
UGC Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: poliquistosis, quiste hepático, dolor abdominal.
Introducción
La poliquistosis renal hereditaria del adulto es una causa frecuente de enfermedad renal crónica. Su diagnóstico derivado de los síntomas asociados a la afectación hepática es poco común.
Caso clínico
Mujer de 33 años consulta por síntomas dispépticos desde hace 2 meses consistente en distensión abdominal y pesadez postpandrial. En los últimos días comenta episodio de dolor abdominal agudo en hipocondrio derecho que cedió con analgesia. Abdomen: sensación de masa en hipocondrio derecho, levemente doloroso a dicho nivel, sin peritonismo. Analítica: Hemograma y perfil hepático normales; creatinina 2-2.16 mg/dl (2 determinaciones). Ecografía abdominal: Hígado con presencia de múltiples quistes simples bilobares no complicados. Ambos riñones nefromegálicos con distorsión de su arquitectura por la presencia de múltiples quistes en su interior (Figura 1). Resonancia magnética nuclear abdominal: Hepatomegalia con longitud craneocaudal de 22 cm. Sustitución del lóbulo derecho por innumerables quistes, uno mayor a 16 cm de diámetro. Colelitiasis. Nefromegalia bilateral con innumerables quistes de diámetros variables que sustituyen por completo al parénquima renal (Figura 2). La paciente es derivada a Nefrología donde se completa estudio de insuficiencia renal y se solicita estudio genético que muestra la presencia de una mutación en el gen PKD2 y confirma el diagnóstico de Poliquistosis hepatorrenal hereditaria del adulto, con herencia autosómica dominante. Desde entonces realiza seguimiento conjunto en nefrología y hepatología, sin necesidad de inicio de sesiones de diálisis. Se realizó estudio genético a sus familiares de primer grado que resultó negativo, tratándose de una mutación de novo.
Discusión
La poliquistosis renal autosómica dominante es la enfermedad renal genética más frecuente. Los quistes hepáticos suponen la principal forma de manifestación extrarrenal, afectando a más del 90% de los pacientes en la quinta década. Suele ser asintomática, pero hasta un 20% de los casos desarrollan síntomas relacionados con el crecimiento de los quistes hepáticos, que incluyen dolor abdominal, saciedad precoz, reflujo gastroesofágico o complicaciones como la infección, hemorragia o ruptura de un quiste. El diagnóstico derivado de la afectación hepática es infrecuente. Sin embargo, se ha sugerido que los pacientes con mutaciones en el gen PKD2 podrían tener un curso más indolente y no requerir trasplante renal. El volumen hepático y renal son marcadores pronósticos y pueden medirse mediante TC o RMN. Aunque existen opciones de tratamiento para disminuir el volumen suelen reservarse para los pacientes sintomáticos con enfermedad moderada o severa que afecten a su calidad de vida o el manejo de complicaciones. El trasplante hepatorrenal es la única opción curativa que mejora la supervivencia.
CP-110. POLIQUISTOSIS HEPATORRENAL COMO CAUSA DE DOLOR ABDOMINAL.
López Peña C, Berdugo Hurtado F, Gijón Villanova R, Ruiz Escolano EM
Servicio Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: dispepsia, poliquistosis hepatorrenal. .
Introducción
La poliquistosis renal autosómica dominante (PQRAD) es un trastorno común que afecta aproximadamente a 1 de cada 1000 nacidos vivos. Está causada en su mayoría por mutaciones en el gen PKD1 (cromosoma 16) o el PKD2 (cromosoma 4).
Caso clínico
Paciente de 40 años, fumadora e hipertensa, tratamiento con enalapril 20 mg/24h. Remitida a consultas de Aparato Digestivo por dolor abdominal de un año de evolución. Refiere aumento del perímetro abdominal, sensación de plenitud, saciedad precoz y vómitos de contenido alimentario ocasionalmente. Niega pérdida ponderal. No alternancia del hábito intestinal ni productos patológicos en las heces. No asocia otra sintomatología.
Exploración física normal salvo hepatomegalia dolorosa de unos cinco traveses de dedo.
Se realiza análisis de sangre, presentando hemograma, coagulación, perfil férrico, tiroideo, estudio de celiaquía, hepatopatía y autoinmunidad normales, únicamente GGT 55. Helicobacter pylori en heces negativo.
Se realiza gastroscopia, toma de biopsias duodenales y gástricas sin alteraciones. La ecografía de abdomen muestra múltiples quistes hepáticos simples y complejas que sustituyen en su gran mayoría al parénquima hepático, las mayores de 8.5 y 11 cm localizadas en epigastrio. Riñones aumentados de tamaño a expensas de múltiples quistes simples. Se realiza resonancia de abdomen confirmando dichos hallazgos y derivación a consultas de Nefrología. Tras estudio genético, se diagnostica de poliquistosis renal autosómica dominante (PQRAD), heterocigosis en el gen PKD1 con afectación hepática.
Actualmente se encuentra en seguimiento por Aparato Digestivo y Nefrología, mantiene adecuada función renal y sin complicaciones digestivas.
Discusión
Los pacientes afectos de PQRAD por mutaciones en el gen PKD1 presentan hipertensión arterial e insuficiencia renal a edades más tempranas. También pueden presentar síntomas secundarios a quistes en hígado, páncreas, bazo o epidídimo.
La prevalencia de quistes hepáticos aumenta con la edad, detectándose hasta en el 83% de casos. Las mujeres tienen más probabilidad de presentar quistes grandes, especialmente aquellas con embarazos múltiples, pudiendo deberse a una sensibilidad de los quistes a las hormonas femeninas.
La mayoría de pacientes permanecen asintomáticos con función hepática conservada. El dolor agudo, requiere descartar complicaciones: infección, rotura, hemorragia o torsión de los quistes. Los síntomas por efecto masa pueden tratarse con drenaje percutáneo, escleroterapia o cirugía.
El trasplante hepático o en combinación con el renal se ha realizado en casos sintomáticos graves. En no candidatos a cirugía, la embolización de la arteria hepática transcatéter es una opción. El inmunosupresor sirolimus y análogos de la somatostatina como el octeótride pueden disminuir el volumen del hígado poliquístico.
CP-111. POTENCIAL DIAGNÓSTICO Y TERAPÉUTICO DE EIF4A3 EN ENFERMEDAD HEPÁTICA METABÓLICA Y CARCINOMA HEPATOCELULAR
Hermán-Sánchez N1, López-Cánovas JL1, Sánchez-Frias ME2, Amado V3, Ciria R4, Briceño J4, De La Mata M3, Rodriguez-Perálvarez M3, Luque RM1, Gahete MD1
1Grupo Investigación. Complejo Hospitalario Regional Reina Sofía, Córdoba. 2Grupo Anatomía Patológica. Complejo Hospitalario Regional Reina Sofía, Córdoba. 3Unidad Gastroenterología y Hepatología. Complejo Hospitalario Regional Reina Sofía, Córdoba. 4Unidad Cirugía General y Digestiva. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: carcinoma hepatocelular, eif4a3, diana terapéutica.
Introducción
Explorar el potencial diagnóstico, pronóstico y terapéutico de las proteínas responsables del proceso celular de splicing del ARNm en la enfermedad hepática metabólica (EHmet) y el carcinoma hepatocelular (CHC).
Material y métodos
Se evaluó la expresión (ARNm/proteína) de componentes de la maquinaria de splicing (n=72) en pacientes con CHC de dos cohortes retrospectivas (n=154 y n=172) y seis cohortes in silico. El potencial diagnóstico de EIF4A3 se evaluó mediante ELISA en plasma y orina de pacientes con enfermedad hepática [sano, n=12; NAFLD, n=28; cirrosis, n=26; CHC=16]. El papel funcional de EIF4A3 en CHC se evaluó in vitro mediante silenciamiento, sobreexpresión y bloqueo farmacológico (IN-1-EIF4A3) en líneas celulares hepáticas (HepG2, Hep3B y SNU-387) e in vivo, en un modelo xenógrafo inducido por Hep3B. El potencial terapéutico del bloqueo combinado de EIF4A3 y FGFR4 se evaluó con un inhibidor específico del receptor (BLU-9931).
Resultados
Los resultados mostraron una desregulación en la expresión del 41,42% de los componentes de la maquinaria de splicing analizados (ARNm/proteína) en CHC frente a los tejidos de control. Entre ellos, EIF4A3 fue el factor más consistentemente alterado y relacionado con parámetros clínicos de agresividad (supervivencia, recurrencia), alcanzando altos niveles de discriminación entre tejido tumoral y tejido adyacente no tumoral en todas las cohortes analizadas (AUC: 0,718-0,943). Ensayos de ELISA demostraron, además, una alta capacidad de discriminación entre pacientes con enfermedad hepática metabólica (EHmet) y CHC en plasma (AUC: 0,7038) y orina (AUC: 0,7440).
Experimentalmente, el silenciamiento y/o el bloqueo farmacológico (IN-1-EIF4A3) de EIF4A3 in vitro redujo la proliferación, la migración y la formación de tumorosferas/colonias, así como el crecimiento tumoral in vivo, mientras que su sobreexpresión tuvo el efecto contrario in vitro. Además, el silenciamiento de EIF4A3 en líneas celulares aumentó la sensibilidad de estas a tratamientos de uso común en la práctica clínica (Lenvatinib, Sunitinib). Mediante análisis de RNAseq se identificó FGFR4 como uno de los genes modulados por EIF4A3, de tal forma que el silenciamiento de EIF4A3 combinado con el bloqueo de FGFR4 (BLU-9931) no tuvo un efecto sinérgico. Por lo tanto, el bloqueo de EIF4A3 podría ser una alternativa a la inhibición de FGFR4.
Conclusiones
En conjunto, estos resultados demuestran una amplia desregulación de la maquinaria de splicing del ARNm en CHC y el potencial de estas proteínas, especialmente EIF4A3, como biomarcador y diana terapéutica en EHmet y CHC.
Financiación: MINECO (FPU20/03957), ISCIII (PI20/01301), JdA (PEMP-0036-2020, BIO-0139), FSEEN y CIBERobn.
CP-112. PREVALENCIA Y PATRÓN DEL CONSUMO DE ALCOHOL EN PACIENTES CON HEPATOCARCINOMA
Muíño Domínguez D1, Mínguez Sabater A2, Castaño García A1, García Calonge M1, González Sánchez MH1, Junquera Alonso E3, Piedra Cerezal AM1, Rodríguez M1, González Parra AC4, Varela Calvo M1
1Servicio Aparato Digestivo. Hospital Universitario Central de Asturias, Oviedo. 2Servicio Aparato Digestivo. Hospital Universitari I Politècnic la Fe, Valencia. 3Servicio Aparato Digestivo. Hospital San Agustín, Avilés. 4Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: hepatocarcinoma, consumo de alcohol, audit.
Introducción
Determinar la prevalencia de consumo de alcohol (CA) en pacientes con CHC independientemente de su etiología, presencia de cirrosis y CA previo; evaluar la utilidad del AUDIT-C para detectar cualquier CA en pacientes con CHC; comparar AUDIT-C con otros métodos de uso común (CAGE) y marcadores biológicos.
Material y métodos
Estudio transversal de 102 pacientes consecutivos con CHC que acuden a consulta.
Criterios de exclusión: encefalopatía hepática en el momento de la entrevista, pacientes con CHC en lista de espera o seguidos tras trasplante hepático.
Se recogieron variables clínicas y sociodemográficas. El AUDIT-C, el cuestionario CAGE y el CA se recogieron mediante una encuesta estructurada en todos los pacientes. También se registro el consumo de cerveza sin alcohol.
Resultados
Se incluyeron prospectivamente 102 pacientes con CHC. Las características basales se recogen en la tabla 1. El tiempo medio desde el diagnóstico del CHC hasta entrar en el estudio fue de 25 meses (rango 1-72). El alcohol fue la causa subyacente del CHC en 60 (58.8%) pacientes, bien solo o combinado con otras causas. La prevalencia de consumo de cerveza sin alcohol fue del 49.02% (n=50).
No hubo diferencias en CA por edad, nivel educativo o consumo de psicofármacos. Sin embargo aquellos que viven en áreas urbanas tienen más CA que los que viven en zonas rurales (p 0.04), y los que nunca fumaron beben significativamente menos que los fumadores/ex-fumadores (p 0.002).
CA no fue diferente si cirrosis de base (p 0.35), causa alcohólica del CHC (p 0.66) o en pacientes con tratamiento activo vs pacientes en vigilancia de recidiva (p 0.32). Por contra, CA fue más alto en varones (p <0.001), pacientes diagnosticados hace más de un año vs nuevos diagnósticos (p<0.01), y en pacientes con estadios BCLC precoces/muy precoces vs otros estadios (p<0.05).
En cuanto al consumo de cerveza sin alcohol, los pacientes con etiología alcohólica consumen más que los de otras causas (p 0.0001).
La puntuación AUDIT-C 3 (AUROC 0,849) predice cualquier CA con una sensibilidad (S) del 75% (IC 95%: 59,47-90,53%) y una especificidad (E) del 84% (IC 95%: 74,70-94,05%). En cambio CAGE y los marcadores analíticos (VCM y GGT) tienen baja sensiblidad y especificidad para discriminar cualquier CA: CAGE>1 (AUROC 0,626) S: 72,22%, E: 53,03%; CAGE>2 (AUROC 0,615) S: 47,22%, E: 75,76%; VCM>85 fL (AUROC 0,509) S: 0,81%, E: 21,2%; GGT>40 UI/L (AUROC 0,487) S: 75%, E: 33%.
Conclusiones
Un tercio de los pacientes con CHC consumen alcohol. El consumo es mayor en áreas urbanas, fumadores/ex-fumadores, CHC diagnosticado hace más de 1 año y en estadio precoz/muy precoz. La puntuación AUDIT-C ≥ 3 discrimina cualquier CA con una sensibilidad del 75% y una especificidad del 84% en esta población.
CP-113. PSEUDOTUMOR INFLAMATORIO HEPÁTICO, EL GRAN SIMULADOR: A PROPÓSITO DE UN CASO.
Guerrero Palma E, Sotomayor Orellana MA, Hidalgo Blanco A, Macías Rodríguez MA
UGC Aparato Digestivo. Hospital Puerta del Mar, Cádiz.
Palabras clave: pseudotumor inflamatorio hepático, metástasis, benigno .
Introducción
El pseudotumor inflamatorio (PTI) hepático es una entidad rara, de etiología desconocida y naturaleza benigna, que se caracteriza por la infiltración crónica de células inflamatorias y áreas de fibrosis. Las manifestaciones clínicas y hallazgos de imagen son similares a los de un tumor maligno, particularmente colangiocarcinoma, metástasis o hepatocarcinoma, siendo el diagnóstico diferencial un reto diagnóstico.
Caso clínico
Paciente de 59 años consumidor de tabaco y alcohol en cantidades tóxicas. En seguimiento en nuestras consultas por hepatopatía y pancreatitis crónica calcificante con reagudizaciones frecuentes y presencia secundaria de colangiopatía intrapancreática, dilatación de wirsung <10mm y pseudoquistes en cabeza, cuerpo y cola. Ingresa en 2020 por cuadro compatible con colangitis aguda por Streptococcus anginosus con presencia de adenopatías múltiples mediastínicas y abdominales que se biopsian aislando el mismo gérmen que en sangre, descartándose sospecha inicial de neoplasia primaria pancreática Vs proceso linfoproliferativo. En control posterior, se realiza TC toracoabdominal donde se evidencia mejoría de las adenopatías, pero nueva aparición de múltiples lesiones hepáticas sugestivas de metástasis. Mediante ecografía con contraste las lesiones se muestran hipervasculares con lavado posterior y los resultados de la biopsia son compatibles con pseudotumor inflamatorio. Se completa estudio con colangioscopia observando estenosis de colédoco distal sin signos de malignidad y citología negativa, dejándose colocada prótesis plástica de drenaje. En TC de revisión a los 3 meses hay regresión espontánea completa de las lesiones hepáticas y el paciente persiste asintomático desde el punto de vista digestivo.
Figura 1
Páncreas atrófico con calcificaciones milimétricas dispersas por todo el parénquima glandular. Dilatación del conducto pancreático principal, de aspecto discretamente arrosariado, de unos 6 mm de calibre. Lesión quística en cola pancreática de 1,2 cm.
Figura 2
Corte axial de RMN de páncreas y corte coronal de TAC abdominal donde se visualiza una colección de 3.4 x 6.7 cms., de intensidad heterogénea, con tabiques, situada craneal a la cabeza pancreática, con extensión al espacio retropancreático en relación a cuadro de pancreatitis aguda.
Figura 3
Hepatomegalia, de predominio en lóbulo hepático izquierdo, con contornos lobulados, en relación a cirrosis hepática. Varias lesiones hipodensas, de bordes mal definidos, algunas con claro realce periférico en anillo, sugestivas de lesiones de naturaleza metastásica, localizadas en segmentos II, III,
Discusión
El PTI hepático representa el 8% de los PTI extrapulmonares, siendo el pulmón la localización más frecuente. Son lesiones ocupantes de espacio de naturaleza benigna, consideradas como una condición reactiva-inflamatoria no neoplásica, aunque pueden tener a veces comportamiento agresivo. La etiología y patogénesis continúan siendo desconocidas, aunque la obstrucción crónica y estasis parecen ser factores etiológicos importantes. Otras causas posibles son la etiología infecciosa y autoinmune. La TC revela lesiones con realce de contraste variable, a veces con carácter hipovascular. La RMN muestra lesiones hipointentas en T1 e hiperintensas en T2. Estos hallazgos pueden ser similares a los de los tumores malignos o abscesos. La biopsia está indicada cuando el diagnóstico es incierto. En la mayoría de las ocasiones regresan con tratamiento conservador, antibiótico o AINEs. La resección quirúrgica se reserva para lesiones que no regresen, aumenten de tamaño, produzcan sintomatología o ante la incertidumbre diagnóstica.
CP-114. REACTIVACIÓN DE LA HEPATITIS C EN EL PACIENTE ONCOLÓGICO ¿PENSAMOS EN ELLO?
Sánchez Moreno S, Calvo Bernal MDM, Casado Martín MM, Pinochet Almonacid S
Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: reactivación, hepatitis c, quimioterapia.
Introducción
El uso de terapias inmunosupresoras supone un alto riesgo de reactivación en pacientes portadores de la hepatitis B.
Sin embargo, en el caso del virus de la hepatitis C (VHC), la reactivación viral es extremadamente rara.
Reportamos el caso de una paciente con reactivación del VHC tras tratamiento con quimioterapia
Caso clínico
Mujer de 58 años, fumadora, con diagnóstico de adenocarcinoma de pulmón estadio IIIA en octubre de 2021, intervenido quirúrgicamente, con posterior inicio de quimioterapia (cisplatino y vincristina) en enero de 2022.
Derivada a nuestra consulta de hepatología por hallazgos analíticos de hipertransaminasemia en rango de hepatitis aguda (GOT 930 U/L, GPT 822 U/L) tras haber recibido tres ciclos de tratamiento citostático. El análisis de sangre mostró además elevación de enzimas de colestasis (GGT 2700 U/L y FA 728 U/L) con hiperbilirrubinemia (BT 4 mg/dL), sin deterioro de la coagulación y resultado positivo para los anticuerpos contra el virus de la VHC, con carga viral (ARN) de 4.080.000 UI/mL.
Se realizó una ecografía abdominal que no mostró alteraciones, y se solicitó una biopsia hepática ante la duda de tratarse de una hepatitis tóxica o una reactivación viral, con hallazgos histológicos concordantes con hepatitis crónica de naturaleza viral (virus C) en fase de agudización.
Una vez establecido el diagnóstico, y tras haberse suspendido la quimioterapia, iniciamos tratamiento antiviral con sofosbuvir y velpatasvir durante doce semanas, con respuesta analítica satisfactoria, con normalización de los niveles de transaminasas y negativización de la carga viral al finalizar el tratamiento.
Discusión
La reactivación del virus de la hepatitis C en pacientes en tratamiento inmunosupresor es rara pero puede ocurrir, por lo que debemos pensar en ella en casos de hepatitis aguda en pacientes que estén en tratamiento con inmunosupresión o quimioterapia.
Este hecho permite la recomendación de que se haga un cribado del VHC a todos los pacientes que se van a someter a tratamiento inmunosupresor.
Además es interesante destacar la utilidad que puede tener la biopsia hepática en casos de hepatitis aguda en pacientes que están en tratamiento con quimioterapia para diferenciar que sea una hepatitis tóxica como consecuencia del tratamiento o que pueda ser una reactivación del VHC, dado que el hecho de que un paciente presente una serología positiva para el virus C no obliga a que la hepatitis aguda sea por ello.
CP-115. SÍNDROME DE ABERNETHY: DERIVACIÓN PORTO-SISTÉMICA EXTRAHEPÁTICA CONGÉNITA. SERIE DE CASOS EN NUESTRO CENTRO
CASTRO RODRÍGUEZ J1, TEJERO JURADO R1, RODRÍGUEZ PERÁLVAREZ ML1, LEAL TÉLLEZ J2, BLANCO RODRÍGUEZ MJ3, JAMAL ISMAIL S4, DOMÍNGUEZ JIMÉNEZ JL5, MONTERO ÁLVAREZ JL6
1UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba. 2Servicio Aparato Digestivo. Hospital Comarcal La Línea de la Concepción, Línea de la Concepción, La. 3Servicio Aparato Digestivo. Hospital de Especialidades de Jerez de la Frontera, Jerez de la Frontera. 4Servicio Aparato Digestivo. Complejo Hospitalario de Jaén, Jaén. 5Servicio Aparato Digestivo. Hospital Alto Guadalquivir, Andújar. 6Servicio Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: síndrome de abernethy, shunt porto-sistémico, neoplasias hepáticas.
Introducción
El síndrome de Abernethy (SA o shunt portosistémico extrahepático) es una malformación congénita infradiagnosticada e infrecuente, en la cual existe una agenesia o hipoplasia de la vena porta (VP), de modo que la sangre venosa esplácnica drena directamente en la circulación sistémica a través de comunicaciones anormales, creándose una derivación portosistémica que excluye el paso hepático (Figura 1).
Caso clínico
Nuestro registro lo conforman cuatro pacientes (Figuras 2-6). Los tres varones jóvenes, con edades entre 18 y 23 años, se realizaron ecografía abdominal por aumento de enzimas hepáticas, confirmando la malformación portal por angio-TC. Nuestro primer paciente posee además una cardiopatía congénita; los otros dos jóvenes tienen un ecocardiograma normal. Nuestro cuarto caso trata de una mujer adulta que, a raíz de dolor y palpación de masa abdominal, es diagnosticada e intervenida de un hepatocarcinoma, siendo el SA reconocido posteriormente en un angio-TC de control. En 2016 inicia Sorafenib por una adenopatía supracavicular izquierda positiva para hepatocarcinoma, siendo suspendido en 2018 por efectos adversos y por permanecer libre de enfermedad.
Todos nuestros pacientes se encuentran asintomáticos y tienen una función hepática conservada, de modo que ninguno ha requerido intervención terapéutica del shunt portosistémico. No obstante todos, menos el segundo, poseen lesiones hepáticas potencialmente malignas por la que se encuentran en seguimiento estrecho mediante alfa-fetoproteína y RM cada 3-6 meses, planteándose resección hepática ante signos de malignidad. En el primer paciente con adenomas hepáticos múltiples se descartó inicialmente el trasplante dada su complejidad técnica.
Figura 1
Clasificación anatómica del síndrome de Abernethy (tipo I, con los subtipos Ia y Ib, y tipo II).
Figura 3
Paciente 1. TC abdominal coronal (A, B): el sistema venoso esplénico, mesentérico y renal izquierdo drenan a través de un tronco común retroaórtico a VCI (*). RM abdominal axial (C T2, D T1): lesión discretamente hipervascular con contenido graso intracelular sugestiva de adenoma (flechas verdes).
Figura 4
Paciente 2. TC abdominal coronal (A), sagital (B), oblicuo (C): De la confluencia de la VMS y VE se origina la VP troncular de 20 mm, con shunt hacia la VCI retrohepática (*). RM abdominal axial (D T1): imágenes hipervasculares discretamente hiperintensas en T1 sugestivas de HNR (flecha verde).
Figura 5
Paciente 3. TC abdominal axial (A), coronal (B), sagital (C): shunt portosistémico directamente a aurícula derecha (*). RM abdominal T1, axial (D), coronal (E, F): lesión en segmento VII con cicatriz central, hiperintensa con contraste hepatoespecífico, sugestiva de HNF (flechas verdes).
Figura 6
Paciente 4. TC abdominal (2014), axial (A), coronal (B): gran masa heterogénea necrótico-quística en LHI (flechas verdes), que desplaza órganos abdominales. Angio-TC (2022), coronal (C), axial (D): shunt portosistémico a VCI (*). Lesión focal de 22 mm en segmento VI/VII medial (flecha amarilla).
Discusión
Los pacientes diagnosticados de SA pueden permanecer asintomáticos o desarrollar complicaciones y síntomas de encefalopatía hepática o disnea secundaria a hipertensión pulmonar o síndrome hepatopulmonar. Es común la presencia de lesiones nodulares hepáticas, generalmente benignas, no obstante se han descrito adenomas y hepatocarcinomas, entre otras neoplasias. Con frecuencia el SA se asocia a otras anomalías congénitas, sobre todo cardiacas (también genitourinarias, musculoesqueléticas, gastrointestinales, hepatobiliares,etc). El diagnóstico del SA suele ser incidental por pruebas de imagen realizadas en la infancia o juventud. El cierre del shunt mediante ligadura quirúrgica o por vía endovascular percutánea constituye una medida terapéutica y a la vez profiláctica de las complicaciones derivadas. Por otro lado, aunque el trasplante hepático puede estar dificultado por las alteraciones anatómicas propias de esta malformación, puede suponer una opción terapéutica en caso de complicaciones refractarias a tratamiento médico o presencia de hepatocarcinoma.
El conocimiento de esta entidad resulta importante para tratar y prevenir el desarrollo de complicaciones y neoplasias hepáticas.
CP-116. SÍNDROME DE DELECIÓN DEL GEN HNF1B. UNA CAUSA INFRECUENTE DE COLESTASIS.
Santa Bárbara Ruiz J, Pinazo Bandera JM, Toro Ortiz JP, Andrade Bellido RJ
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Virgen de la Victoria, Málaga.
Palabras clave: colestasis, hepatologia, genetica.
Introducción
La colestasis es el déficit del flujo biliar del hígado hacia el tubo digestivo, pudiendo ésta tener origen intrahepático o extrahepático. Dentro de las intrahepáticas, existen causas genéticas como el déficit de HNFs (factores nucleares del hepatocito), que son reguladores clave en la transcripción genética en el hepatocito y células epiteliales de la vía biliar, tanto durante el desarrollo embrionario y fetal como durante la adultez, jugando un papel crucial en la organogénesis y transporte de sales biliares. El déficit de este gen, al expresarse también en riñones, tracto urogenital y células beta pancreáticas puede ocasionar colestasis, poliquistosis hepatorrenal y DM tipo MODY 5, entre otras.
Existen diferentes fenotipos a nivel hepático desde una colestasis neonatal (la más grave) hasta una colestasis de presentación en edad adulta/adolescencia.
Caso clínico
Paciente varón de 34 años sin antecedentes de interés que acude a urgencias por cuadro de 3-4 días de náuseas, astenia, prurito intenso e ictericia mucocutánea, sin fiebre ni dolor abdominal. Realizándosele anamnesis detallada, el paciente niega tatuajes, transfusiones, viajes recientes, ingesta de fármacos, productos de herbolario o carne de caza y comportamientos sexuales de riesgo. Analíticamente se evidenció una AST 111, ALT 309, GGT 375, FA 269, bilirrubina total 11.99 a expensas de directa, con hemograma y coagulación normales (figura 1). Con la sospecha de hepatitis aguda, se inicia el estudio con serología de virus hepatotrópos y autoinmunidad, resultando negativos, y descartándose razonablemente otras entidades menos frecuentes como la hemocromatosis, enfermedad de Wilson o porfirias. Además se descartó mediante colangioRM la obstrucción de la vía biliar.
Dados estos resultados, se realiza biopsia hepática sin evidenciar datos de inflamación ni de fibrosis: únicamente datos de colestasis (figura 2), por lo que se solicitó estudio genético diagnosticándosele de colestasis biliar genética por síndrome de delección de 17q12 (ausencia de expresión del gen HNF1B). El paciente además fue diagnosticado de diabetes mellitus tipo MODY y atrofia pancreática.
Inició Ácido Ursodesoxicólico (AUDC), mejorando cifras de bilirrubina y Rifampicina, como segunda línea terapéutica del prurito. Actualmente se encuentra asintomático tomando únicamente AUDC.
Discusión
Las colestasis biliares de causa genética son entidades cuya forma de presentación abarca un amplio espectro y que, al ser poco frecuentes, deben diagnosticarse una vez descartadas otras etiologías más frecuentes. La instauración de colestasis, una biopsia sin datos de inflamación/necrosis y la presentación concomitante de diabetes mellitus o poliquistosis renal, debe hacernos pensar en el déficit del gen HNF1B.
CP-117. SÍNDROME DE RENDU-OSLER-WEBER: FORMA DE PRESENTACIÓN INUSUAL
Librero Jiménez M, Rodríguez Gómez V, García Aragón F, Espinosa Aguilar MD, Redondo Cerezo E
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: rendu-osler-weber.
Introducción
La Telangiectasia Hemorrágica Hereditaria (THH) o Rendu-Osler-Weber es una rara enfermedad genética autosómica dominante caracterizada por la aparición de malformaciones arterio-venosas (MAVs) o telangiectasias a nivel cutáneo, mucoso o visceral. La afectación hepática afecta a un 41–74% de los casos, generalmente es difusa y pueden aparecer desde pequeñas telangiectasias a grandes MAVs, llevando en estadios avanzados al desarrollo de Insuficiencia Cardiaca Congestiva y complicaciones derivadas de la hipertensión portal.
Caso clínico
Presentamos el caso de un varón de 43 años sin antecedentes de interés que ingresa en Neurología por un ictus isquémico subagudo vértebrobasilar en territorio de la arteria cerebelosa superior derecha (ACS). Durante el estudio etiológico se realiza ecocardiograma con hallazgo de Foramen Oval Permeable (FOP), siendo catalogado como ictus de origen embólico en probable relación con embolismo paradójico (shunt derecha-izquierda) asociado a FOP.
Durante el ingreso se evidencia en analíticas seriadas una hipertransaminasemia (GOT 106, GPT 102, GGT 415, FA 130) sin hiperbilirrubinemia, si bien el paciente no disponía de controles previos con los que comparar. Ante la sospecha de hepatopatía congestiva en el contexto de insuficiencia cardiaca asociada al FOP, se deriva a consultas de Hepatología donde se realiza estudio completo de hepatopatías (que resulta normal), así como ecografía doppler hepática. Esta última se completa con un TAC abdominopélvico donde se evidencian múltiples fístulas arteriovenosas hepáticas con hipertrofia secundaria de la arteria hepática (Figura 1), así como una fístula arteriovenosa pulmonar en lóbulo medio, con sospecha de Sd. de Rendu-Osler-Weber. El paciente cumplía los criterios de Curaçao para dicha enfermedad y el posterior estudio genético confirmó el diagnóstico de THH tipo 2.
Discusión
A pesar de que inicialmente se asumiera que el ictus isquémico se había producido en el contexto de un embolismo paradójico secundario al FOP, fue el estudio de la hipertransaminasemia hallada durante el ingreso lo que llevó al diagnóstico no solo de las MAVs hepáticas sino también de la pulmonar, pasando a ser más plausible el origen isquémico del ictus en el contexto de la fístula arteriovenosa pulmonar. Por dicho motivo, y como prevención secundaria de nuevos accidentes cerebrovasculares, finalmente se llevó a cabo el cierre endovascular de la fístula pulmonar, con buen resultado. En conclusión, con este singular caso queremos destacar la importancia de prestar atención a cada uno de los síntomas y signos que presentan los pacientes, con el objetivo de lograr que finalmente todas las piezas del puzzle encajen entre sí.
CP-118. TRATAMIENTO DE LA HEPATITIS C Y USO DE TIAMAZOL
Grilo Bensusan I
Unidad Aparato Digestivo. Hospital de Alta Resolución de Écija, Écija.
Palabras clave: hepatitis c, hipertiroidismo, tiamazol.
Introducción
La hepatitis C tiene actualmente un tratamiento oral muy efectivo. En el proceso de selección de dicho tratamiento es necesario la comprobación de la existencia de interacciones con otros fármacos que esté tomando el paciente. En este sentido, se dispone de una herramienta muy útil desarrollada por la universidad de Liverpool en la que se pueden comprobar la existencia de dichas interacciones. Aunque la lista de fármacos es muy amplia, en este caso no existía información acerca del fármaco que tomaba el paciente, ni en la literatura médica, ni en el departamento médico del laboratorio. Se describe el caso de un paciente con hepatitis C y en tratamiento con tiamazol ,tratado exitosamente con la combinación sofosbuvir-velpatasvir.
Caso clínico
Un paciente varón de 39 años es remtido por el médico de Atención Primaria por serología positiva para el VHC. Se confimó en la analítica la existencia de infección activa por el VHC genotipo 1b, con una carga viral de 4710000 UI/ml . Se descartaron otras causas de hepatopatía. La valoración del grado de fibrosis situaban al paciente con un nivel F2, con un FIB4:1,5 y con una elastografía hepática con valores de 7,7 Kpa con IQR: 1,6. El paciente estaba en tratamiento con tiamazol a dosis de 5 mg/24h/voral por un hipertiroidismo autoinmune con niveles estables de hormonas tiroideas previo al tratamiento. Explicándole al paciente la ausencia de información acerca de las interacciones de los fármacos antivirales y el tiamazol, y la necesidad de un seguimiento más estrecho, se le indicó tratamiento con sofosbuvir 400 mg/Velpatasvir 100 mg durante 12 semanas. El paciente negativizó la carga viral en la semana 4, siendo también negativa en la semana 8 ,al final del tratamiento y las 3 meses del mismo obteniendo una respuesta virológica sostenida. Durante el tratamiento no presentó efectos secundarios y los niveles de hormonas tiroideas y TSH permanecieron sin alteraciones durante el tratamiento (semanas 4, 8 y 12) y 3 meses finalizado el mismo.
Discusión
Se trata del primer caso descrito de tratamiento oral de la hepatitis C con la combinación sofosbuvir/ velpatasvir junto con el tratamiento con tiamazol. En este caso no se observaron ni efectos secundarios, ni pérdida de efectividad de los fármacos, con la consecución de la respuesta virológica sostenida del paciente.
CP-119. TROMBOSIS PORTAL POST COVID-19 EN AUSENCIA DE OTROS FACTORES DE RIESGO
GARCÍA ARAGÓN F, LANCHO MUÑOZ A, RODRÍGUEZ GÓMEZ VM, LECUONA MUÑOZ M, REDONDO CEREZO E, CABELLO TAPIA MJ
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: trombosis, covid.
Introducción
La trombosis del eje espleno-portal no asociada a cirrosis o neoplasias cumple los criterios de enfermedad rara de la OMS. Si se realiza un estudio exhaustivo, hasta en 2/3 de los pacientes se logra identificar un factor etiológico predisponente a la trombogénesis.
Por otro lado, como se ha descubierto durante los últimos dos años, la infección COVID-19 puede provocar un estado inflamatorio excesivo acompañado de hipercoagulabilidad, aumentando el riesgo de aparición de tromboembolismos venosos y arteriales.
Caso clínico
Varón de 40 años, sin antecedentes hematológicos ni hepáticos familiares o personales. Infección COVID-19 leve en el mes previo, la cual no precisó de medicación específica. Acude a urgencias por dolor epigástrico irradiado a hipocondrio derecho de 3 semanas de evolución, sin relación con la ingesta, deposiciones o movimientos, y sin otra sintomatología acompañante. Analítica anodina sin alteraciones de la coagulación.
Se realiza ecografía (Figuras 1-3) y TC abdominal con hallazgo de trombosis aguda casi completa de vena porta, con extensión a ramas intrahepáticas, y trombosis parcial de la vena esplénica. Tras inicio de anticoagulación terapéutica se realiza angio-TC de control, evidenciándose resolución de la trombosis esplénica, con persistencia de la trombosis portal e intrahepática.
El paciente fue derivado posteriormente a consultas de hematología, donde se realizó estudio de trombofilias con resultado negativo, describiéndose la infección SARS-CoV2 como la causa más probable del fenómeno trombótico.
Figura 1
Imágenes de ecografía y eco-Doppler hepáticos, observándose el defecto de repleción a nivel portal.
Discusión
La trombosis del eje espleno-portal no asociada a cirrosis hepática o neoplasias es una enfermedad rara, con una prevalencia inferior al 3.7/100.000 habitantes. No obstante, constituye la segunda causa de hipertensión portal. Hasta el 70% de los afectados presentan algún tipo de factor protrombótico subyacente, siendo frecuente la coexistencia de varias entidades etiológicas.
La clínica depende del momento evolutivo y de la extensión del trombo, desde dolor abdominal inespecífico en el momento agudo, hasta la aparición de cavernomatosis e hipertensión portal si evoluciona hacia la cronicidad. Es esencial el inicio precoz de la anticoagulación para conseguir la revascularización portal y mejorar el pronóstico del paciente.
El riesgo de enfermedad tromboembólica venosa en pacientes con COVID-19 ha constituido un problema importante desde el inicio de la pandemia. La inmovilización asociada a la enfermedad, la deshidratación, el estado inflamatorio agudo, y la presencia de otros factores de riesgo cardiovascular, así como antecedentes de trombofilia, pueden incrementar su potencial aparición, que si bien ha demostrado ser más frecuente en aquellos casos de infección grave, no deja exentos de riesgo a los casos más leves como el que presentamos.
CP-120. TUMOR NEUROENDOCRINO HEPÁTICO PRIMARIO: UNA ENTIDAD INFRECUENTE.
Gutiérrez Holanda C1, Soler Góngora M1, Vicente Gutiérrez MDM2
1Servicio Aparato Digestivo. Hospital San Cecilio, Granada. 2Grupo Gastroenterología y Hepatología. Hospital San Cecilio, Granada.
Palabras clave: tumor neuroendocrino, tumor carcinoide, hígado.
Introducción
El tumor neuroendocrino hepático primario (TNEHP) constituye una entidad rara, representando el 0,3% del total de tumores neuroendocrinos, con menos de 200 casos reportados en la literatura. Presentamos el caso de un TNEHP de rápido crecimiento y síndrome carcinoide asociado.
Caso clínico
Mujer de 66 años sin antecedentes personales de interés, que acude a Urgencias por epigastralgia y pérdida ponderal de 10 kg en los últimos 6 meses. Se realizan ecografía y TC abdominal, revelando una masa hepática sólida y heterogénea de 7x10x13 cm, hiperdensa respecto al parénquima en fase arterial, con lavado portal, leve dilatación de radicales biliares y adenopatía sospechosa locorregional. Como primera posibilidad sugieren neoplasia hepática primaria LI-RADS 4 (hepatocarcinoma vs. colangiocarcinoma). Se decide, tras presentar el caso en Comité Multidisciplinar, realizar RM, sin poder definir criterios definitivos de una u otra etiología. Asimismo, se realiza estudio de extensión torácica, que resulta negativo. Se biopsia la LOE revelando infiltración por neoplasia neuroendocrina de células pequeñas y medianas grado 3 de la OMS, con índice proliferativo -Ki67- entre 20 y 50%. Se corrobora positividad para INSM1 confirmando así la etiología neuroendocrina.
Dos meses después, ingresa por ictericia con hiperbilirrubinemia de 14,15, de componente mixto. Destaca la aparición de crisis de “flushing” tras la ingesta, con 5-hidroxiindolacético en orina elevado y consiguiendo control de los síntomas con octreótido.
Para completar estudio, se solicita Octreoscan, que muestra dos lesiones óseas sospechosas de metástasis.
Se consensua con Radiología Intervencionista proceder al drenaje biliar por CTPH para poder iniciar quimioterapia neoadyuvante, de cara a una eventual cirugía paliativa. Desafortunadamente, no se alcanza un nivel aceptable de bilirrubina para quimioterapia.
La paciente evoluciona desfavorablemente con exitus por insuficiencia hepática.
Discusión
El diagnóstico de TNEHP es complejo, debido a las similitudes con otros tumores primarios intrahepáticos más frecuentes y a la ausencia de factores de riesgo y marcadores tumorales específicos. La positividad para INSM1 en estudio histológico, es el marcador actualmente más sensible para la procedencia neuroendocrina. Su abordaje requiere de una adecuada evaluación anatomopatológica y de la exclusión de otro tumor neuroendocrino primario. Actualmente, no se dispone de una guía para su tratamiento, siendo la resección completa el único curativo y de primera elección.
CP-121. UN TUMOR INFRECUENTE: PECOMA HEPÁTICO
Gutiérrez Martínez F1, Gil Ayuso J1, Asady Ben GR1, Dawid De Vera MT2, Andrade Bellido RJ1
1Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Virgen de la Victoria, Málaga. 2Servicio Anatomía Patológica. Complejo Hospitalario de Especialidades Virgen de la Victoria, Málaga.
Palabras clave: tumor, histología, pecoma.
Introducción
El Pecoma es un tumor infrecuente de estirpe mesenquimal con marcadores inmunohistoquímicos específicos que puede aparecer en cualquier localización. La mayoría tienen un comportamiento benigno aunque hay variantes que pueden llegar a malignizar. A nivel hepático suele presentarse como hallazgo incidental en pacientes asintomáticos aunque puede producir dolor abdominal e ictericia por compresión sobre la vía biliar o complicaciones locales del tumor.
Caso clínico
Mujer de 47 años hipertensa y dislipémica con obesidad tipo I sin otros antecedentes de interés en tratamiento con anticonceptivos orales en seguimiento por Urología por disinergia vesical que en ecografía de abdomen rutinaria se objetiva LOE hepática como hallazgo incidental (Figura 1).
Asintomática desde el punto de vista digestivo y analíticamente sin alteraciones relevantes. Serología infecciosa negativa para virus y parásitos. Se realiza TC focal hepático visualizándose lesión sólida bien definida de 68x53 mm en lóbulo caudado sin datos de infiltración de estructuras vasculares con realce difuso en fase arterial e isodensidad en fase portal y tardía (Figuras 2 y 3); hallazgos sugerentes de Adenoma hepático.
Se presenta en comité médico-quirúrgico y se decide tratamiento conservador con medidas higiénico-dietéticas, suspensión de tratamiento anticonceptivo y control radiológico en 6 meses. Tras dicho periodo se repite TC hepático permaneciendo la lesión con tamaño y características similares. Se vuelve a presentar el caso en comité y se decide cirugía.
En la anatomía patológica de la pieza quirúrgica se informa de tumor de células epitelioides perivascular positivo para marcadores melanocíticos y musculares sin datos de invasión linfovascular (Figuras 4, 5 y 6).
Actualmente, asintomática y con controles radiológicos cada 6 meses.
Figura 1
Imagen ecográfica de lesión sólida hipoecogénica con pequeños focos hiperecogénicos (línea punteada)
Figura 2
Corte axial de TC en fase arterial que muestra lesión hepática de 68x53 mm con realce difuso (líneas verdes)
Figura 3
Corte axial de TC en fase portal que muestra misma lesión hepática de aspecto isodenso (flecha negra)
Figura 5
Estudio microscópico con tinción hematoxilina-eosina con evidencia de celulas epitelioides con citoplasmas claros y nucleolos
Discusión
En el caso de nuestra paciente se enfocó inicialmente como adenoma hepático dada la compatibilidad de las pruebas radiológicas y la presencia de factores predisponentes a este tipo de lesiones (mujer en edad fértil, obesidad y toma de anticonceptivos orales).
Los adenomas hepáticos de pequeño tamaño sin datos sugerentes de malignidad en mujeres se suelen manejar de forma conservadora incidiendo en la pérdida de peso y los hábitos saludables. No obstante, dado el tamaño de la lesión y la invariabilidad del mismo tras medidas higiénico-dietéticas, se decidió cirugía.
El PEComa es un tumor tan infrecuente que no tiene establecido un claro protocolo de actuación y seguimiento, pero por lo general, se opta por la opción quirúrgica. En caso de irresecabilidad o enfermedad a distancia se puede optar por terapia sistémica con quimioterapia convencional o con inhibidores de la vía mTOR.
CP-122. VASCULITIS LEUCOCITOCLÁSTICA POR SORAFENIB
Fernández Cornax A1, Gómez Rodríguez P1, González García J2, Bracho González M1
1Servicio Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga. 2Servicio Anatomía Patológica. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: sorafenib, hepatocarcinoma, vasculitis.
Introducción
El sorafenib es un fármaco indicado en el tratamiento del hepatocarcinoma en estadio avanzado, con aumento de supervivencia en pacientes adecuadamente seleccionados.
Son varios los efectos secundarios descritos en pacientes tratados con este fármaco, habitualmente a nivel sistémico, gastrointestinal y cutáneo. En este caso nuestro paciente desarrolla afectación cutánea al introducir Sorafenib, con necesidad de suspensión del tratamiento.
Caso clínico
Paciente varón de 66 años con cirrosis por infección crónica de VHB e hipertensión portal establecida. Antecedentes de HDA secundaria a varices esofágicas, motivo por el que es ingresado para control del sangrado. Durante el ingreso se realiza TC de abdomen, en el cual se aprecian hallazgos compatibles con hepatocarcinoma con datos de infiltración vascular extensa.
Tras completar el estudio y presentar el caso en comité oncológico, se decide que el paciente se encuentra en un estadio C de la BCLC, siendo candidato a tratamiento sistémico con Sorafenib, iniciándose a dosis de 200 mg cada 12h.
Al mes siguiente el paciente acude a Urgencias, refiere astenia intensa en los últimos días y aparición de lesiones puntiformes, eritematosas y levemente sobreelevadas, con predominio en región de manos y pies (FIGURA 1), así como aparición de lesiones ampollosas en dorso de ambas manos (FIGURA 2). Analíticamente destaca PCR en 116, sin leucocitosis asociada.
Se retira Sorafenib por sospecha de síndrome mano-pie grado III, y se deriva al paciente a Dermatología, donde se realizan biopsias cutáneas de las lesiones, con AP compatible con Vasculitis leucocitoclástica de pequeños vasos (FIGURAS 3 y 4). Se mantiene suspensión del fármaco y se plantea el inicio de inmunoterapia.
Discusión
Las manifestaciones cutáneas en el contexto de tratamiento activo con Sorafenib no son infrecuentes, siendo la más típica el síndrome mano-pie. En el caso de nuestro paciente, además aparecen lesiones petequiales en el contexto de una vasculitis cutánea asociada al inicio del tratamiento.
En el contexto de aparición de lesiones cutáneas severas, se recomienda reducción o suspensión del tratamiento al menos durante una semana, con reintroducción posterior del fármaco a menor dosis si fuera posible.
CP-123. ¿LA HEMOGLOBINA GLICOSILADA PUEDE IDENTIFICAR EL RIESGO DE FIBROSIS HEPÁTICA EN PACIENTES CON DIABETES TIPO 2?
Torres Domínguez A1, Saldaña García L1, Hernández Pérez AM1, Cantero Sánchez FM2, García Gavilán MC1, Gálvez Fernández R1, Rivas Ruíz F3, Rosales Zábal JM1
1Unidad Aparato Digestivo. Complejo Hospital Costa del Sol, Marbella. 2Unidad Análisis Clínico. Complejo Hospital Costa del Sol, Marbella. 3Unidad Investigación. Complejo Hospital Costa del Sol, Marbella.
Palabras clave: enfermedad hepática metabólica, diabetes mellitus, fibrosis hepática.
Introducción
La enfermedad hepática metabólica (EHmet) es la enfermedad hepática crónica más frecuente del mundo, con una alta prevalencia en diabetes mellitus tipo 2 (DM-2). La hemoglobina A1c (HbA1c) proporciona información sobre el control glucémico en los últimos 2-3 meses, permitiendo dirigir los tratamientos.
Objetivo: Evaluar la relación entre el control glucémico y la presencia de fibrosis hepática en la DM-2. Secundariamente analizamos prevalencia de riesgo de fibrosis, factores asociados al mismo y la tasa de seguimiento por Digestivo.
Material y métodos
Estudio retrospectivo unicéntrico en el que se analizaron pacientes con DM-2 de consultas ambulatorias en enero de 2021. Se recogieron datos demográficos, analíticos con HbA1c, enfermedades de base y el servicio responsable del seguimiento del paciente. Definimos “buen control glucémico” con HbA1c <7% y “riesgo de fibrosis” con un FIB4 >1,3 en <65 años o > 2 en >65 años.
Resultados
Se analizaron 123 pacientes con DM (62,6% varones), edad media 65,4 años. El 53,7% tenían obesidad con un IMC medio de 30,8 y el 76,4% cumplían criterios de síndrome metabólico. El 50,4% tenían buen control glucémico. Presentaron riesgo de fibrosis 21 pacientes (17,1%), de los que el 71,4% eran seguidos por Medicina Interna, 23,8% por Cardiología, 47,6% por Nefrología y el 9,5% por Digestivo. El 80,9% cumplían criterios de síndrome metabólico. No hubo diferencias estadísticamente significativas entre los niveles de HbA1c y el riesgo de fibrosis (p=0,90). La presencia de enfermedad renal crónica se asoció a un mayor riesgo de fibrosis (p<0,05; OR 10,2 [IC 95% 2,9-36,1]), así como los niveles de AST (p=0,026; OR 1,1 [IC 95% 1-1,11]).
Conclusiones
La hemoglobina glicada no permite identificar riesgo de fibrosis hepática en DM-2, aún cuando presenten un mal control glucémico.
Un 17% de diabéticos están en riesgo de fibrosis por FIB-4.
La enfermedad renal crónica y los niveles de AST son factores de riesgo para fibrosis significativa en DM-2. La primera, incrementa más de 10 veces ese riesgo.
Sólo el 9,5% de los pacientes en riesgo de fibrosis significativa estaban en seguimiento por Digestivo, por lo que es imprescindible implementar de estrategias de formación en el uso de métodos no invasivos de fibrosis y adecuar la derivación.

 Descargar número completo
Descargar número completo Download full issue
Download full issue