CP-124. NECROSIS INTESTINAL SECUNDARIA A VÓLVULO DE SIGMA
López Peña C, Berdugo Hurtado F, Soler Góngora M, García Verdejo FJ
Servicio Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: dolor abdominal, vólvulo de sigma, necrosis intestinal. .
Introducción
El vólvulo sigmoideo generalmente ocurre en adultos de edad avanzada, con mayor incidencia en hombres. Los pacientes a menudo están institucionalizados, tienen antecedente de enfermedad neurológica o psiquiátrica y estreñimiento. Se han descrito casos en pacientes más jóvenes con motilidad colónica anormal, enfermedad de Crohn y Chagas.
Caso clínico
Mujer de 50 años con antecedentes de estreñimiento crónico y retraso mental, dependiente e institucionalizada. Acude a Urgencias por vómitos, dolor abdominal, ausencia de deposiciones y ventoseo desde 72 horas.
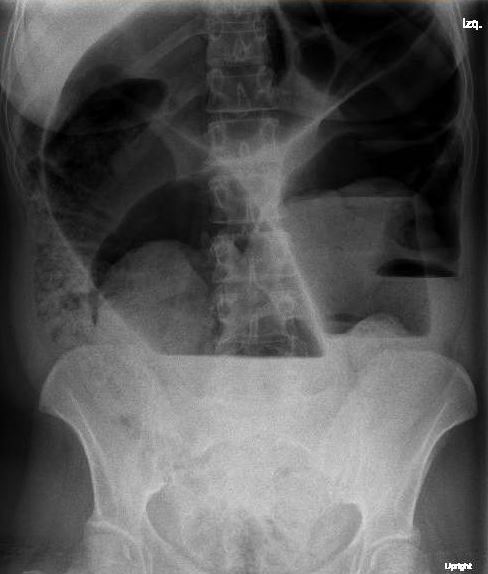
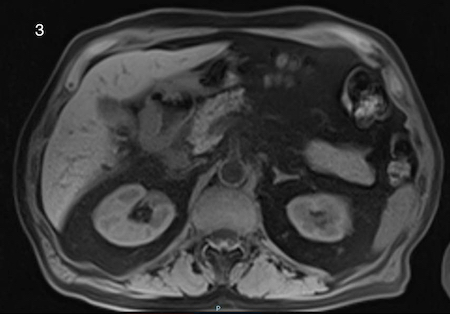
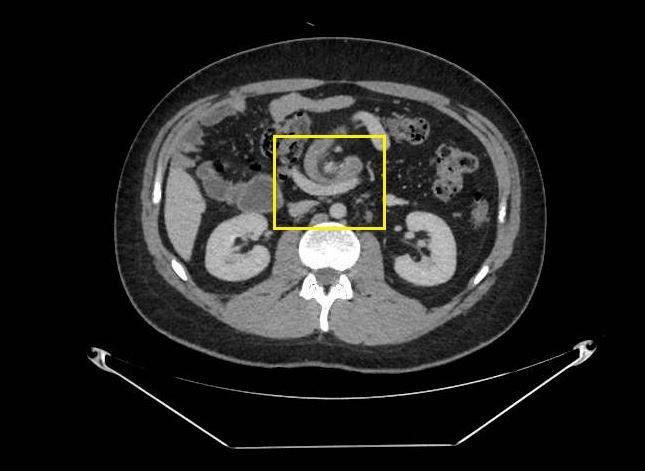
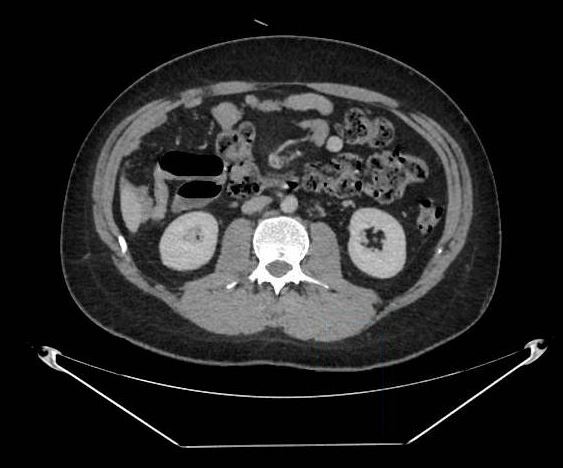
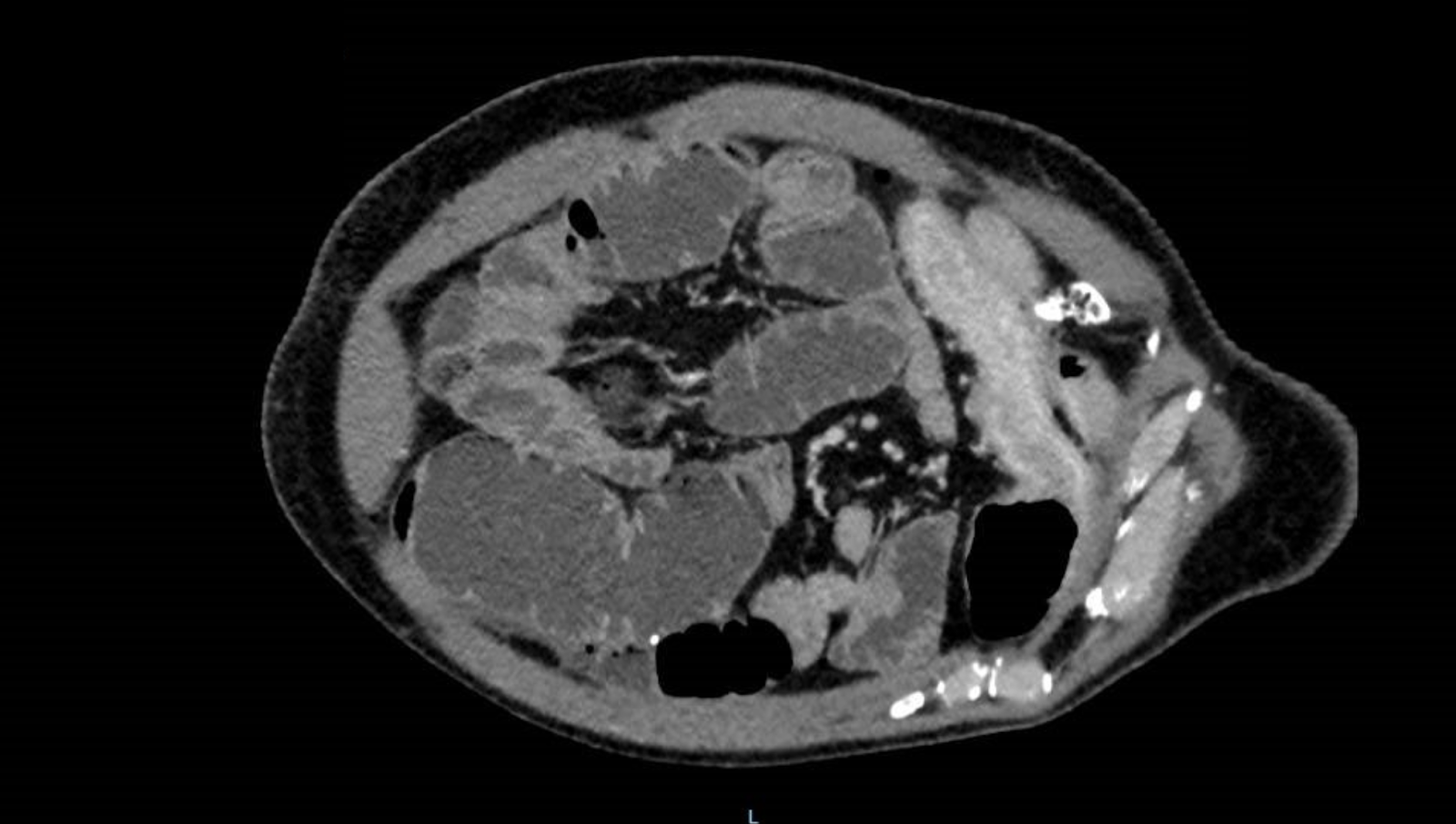
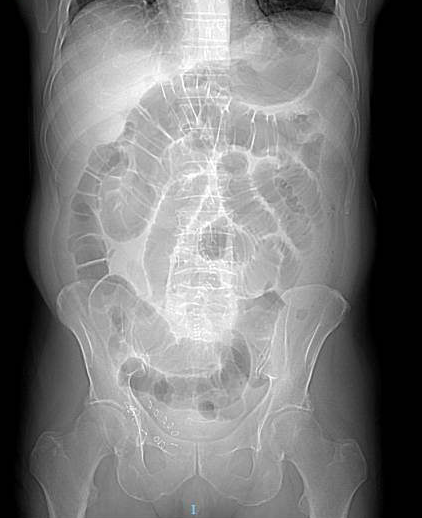
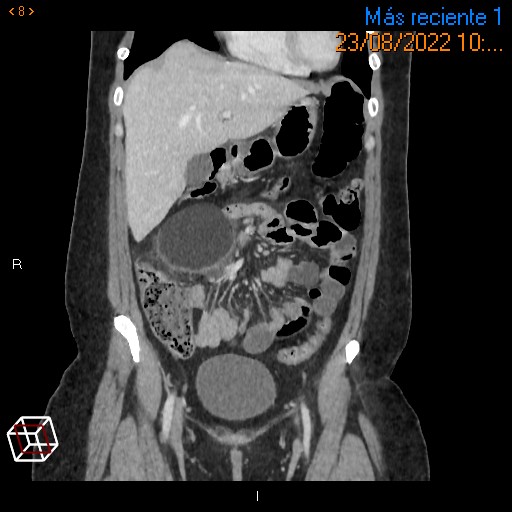
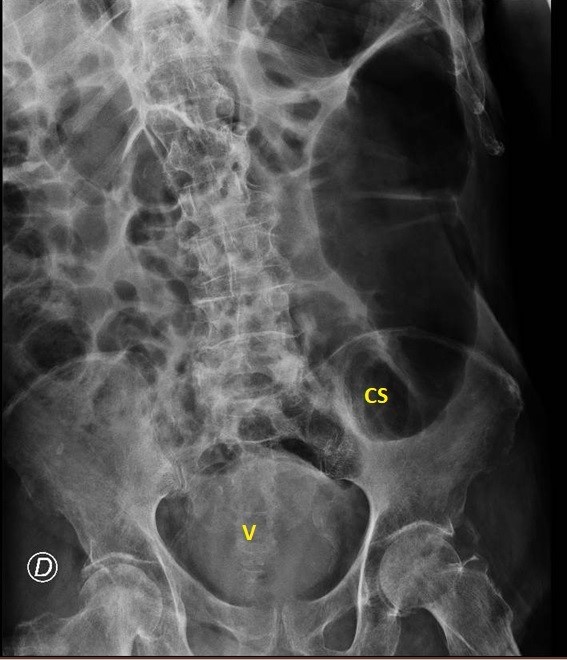
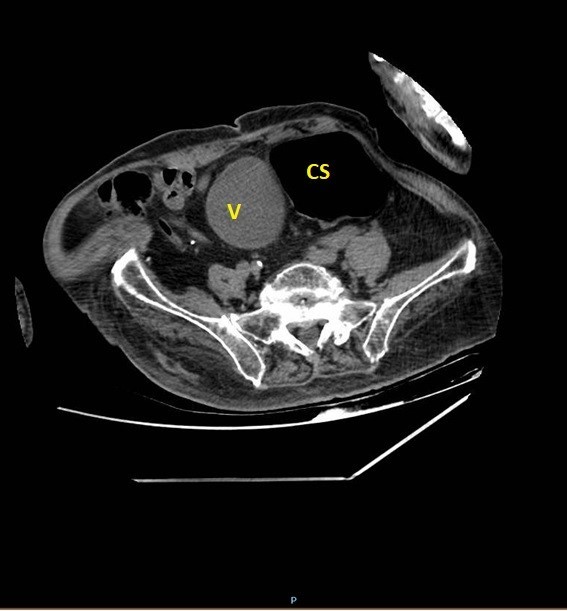
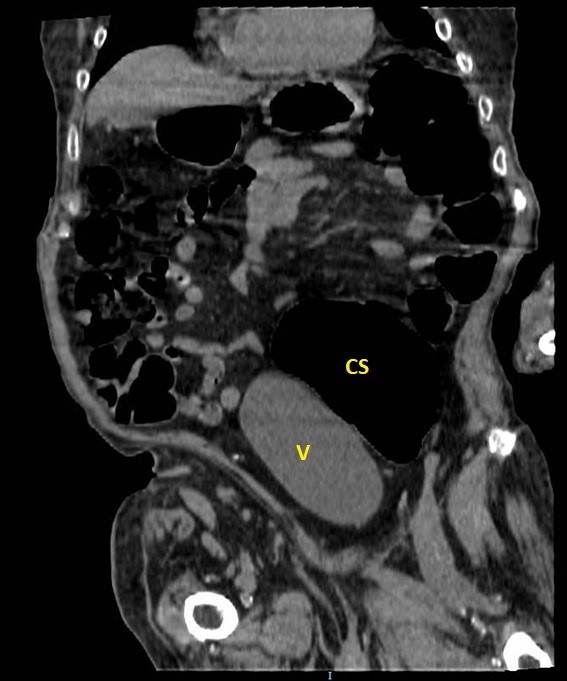
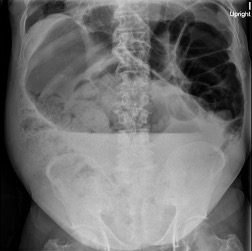
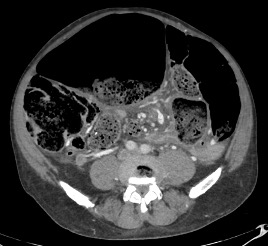
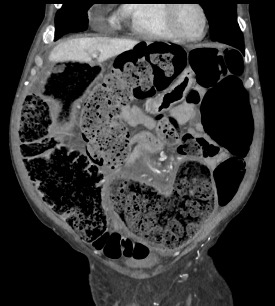
A la exploración física, presenta regular estado general. Se encuentra normotensa, taquicárdica y apirética. Auscultación cardiorrespiratoria normal. Abdomen distendido, timpanizado y muy doloroso a la palpación generalizada con dudosa defensa. En análisis de sangre destaca leucocitosis de 12000/μL con neutrofilia, LDH 350 U/L, hipopotasemia de 3 mEq/L y PCR 105 mg/L. Gasometría venosa con pH 7.26 y ácido láctico 5. La radiografía de abdomen muestra imagen compatible con vólvulo de sigma.
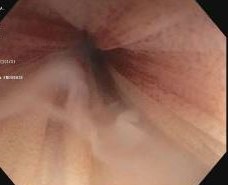
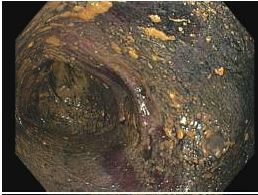
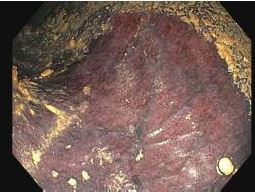
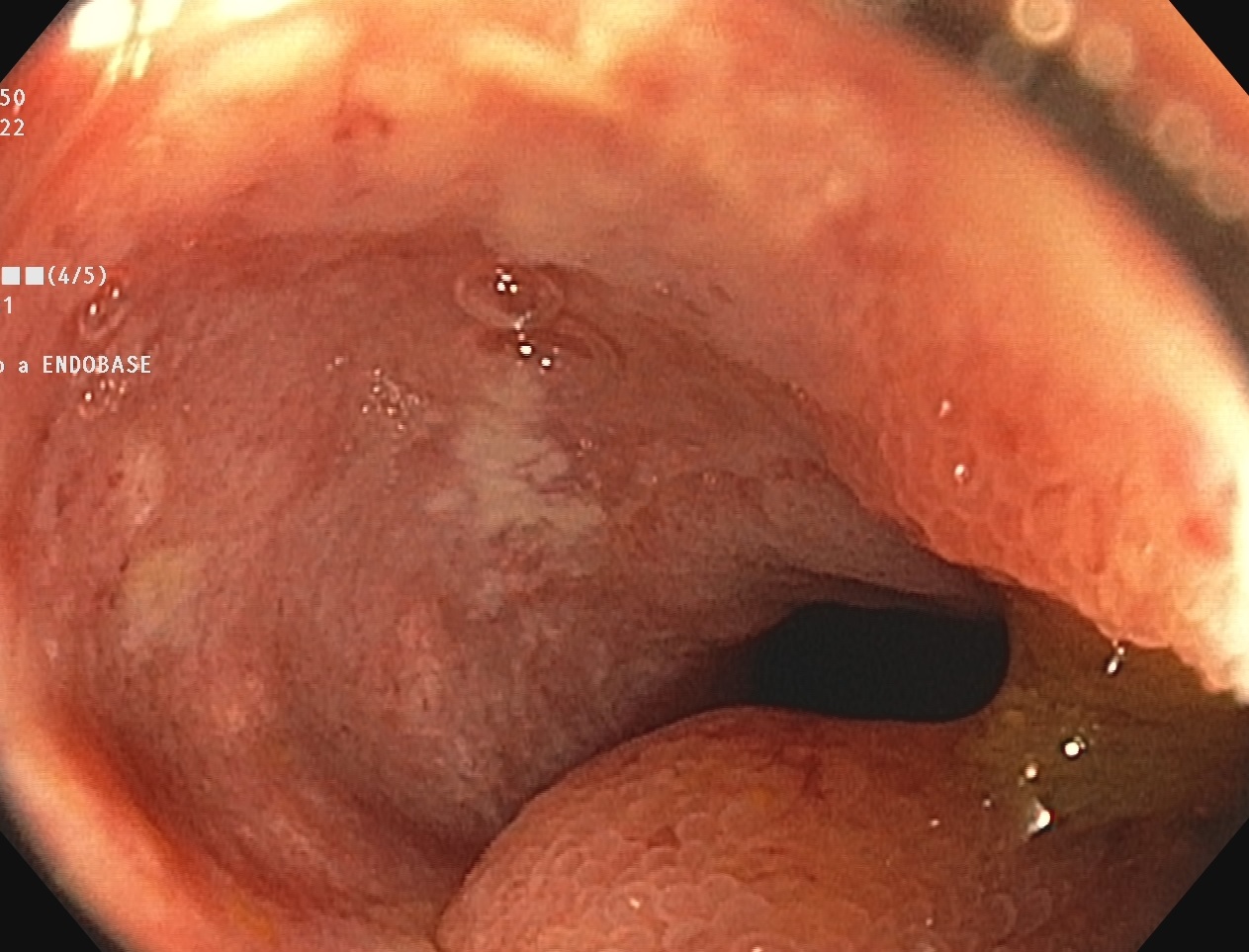
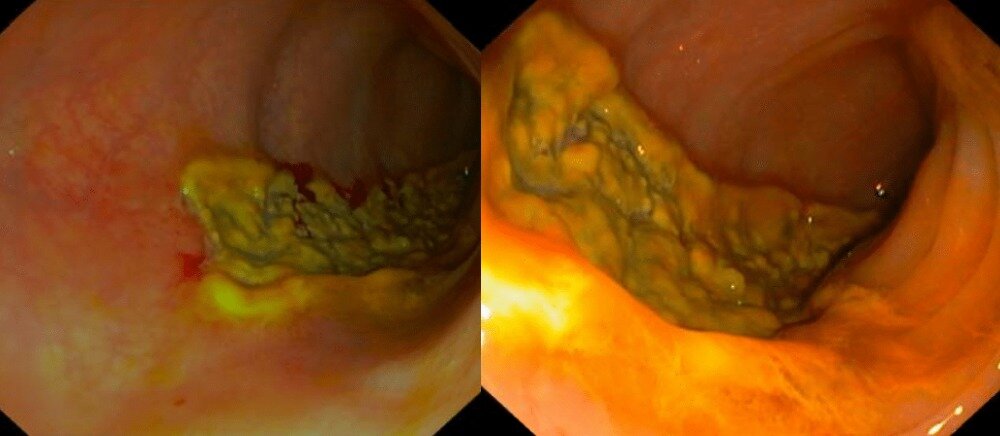
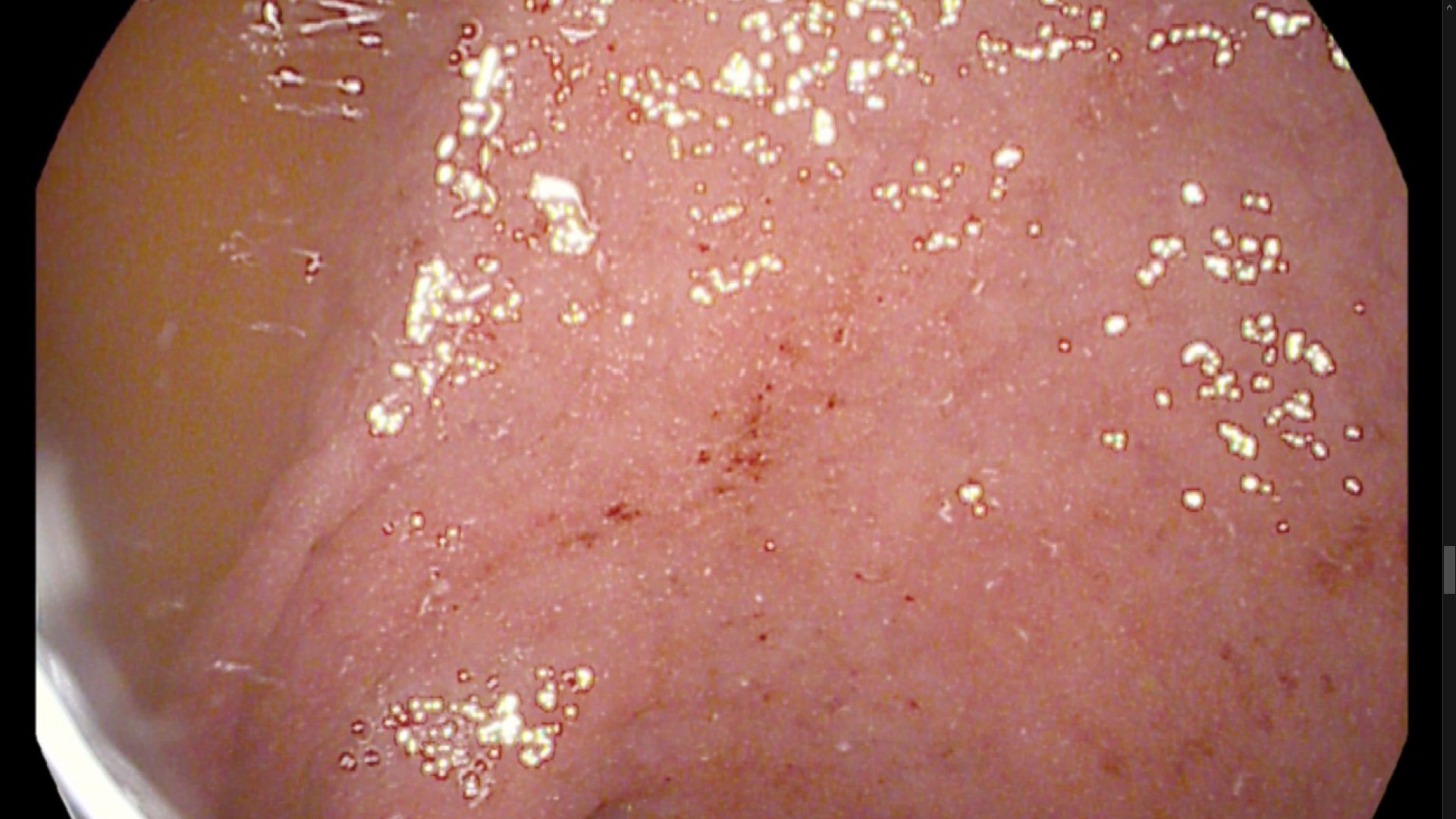
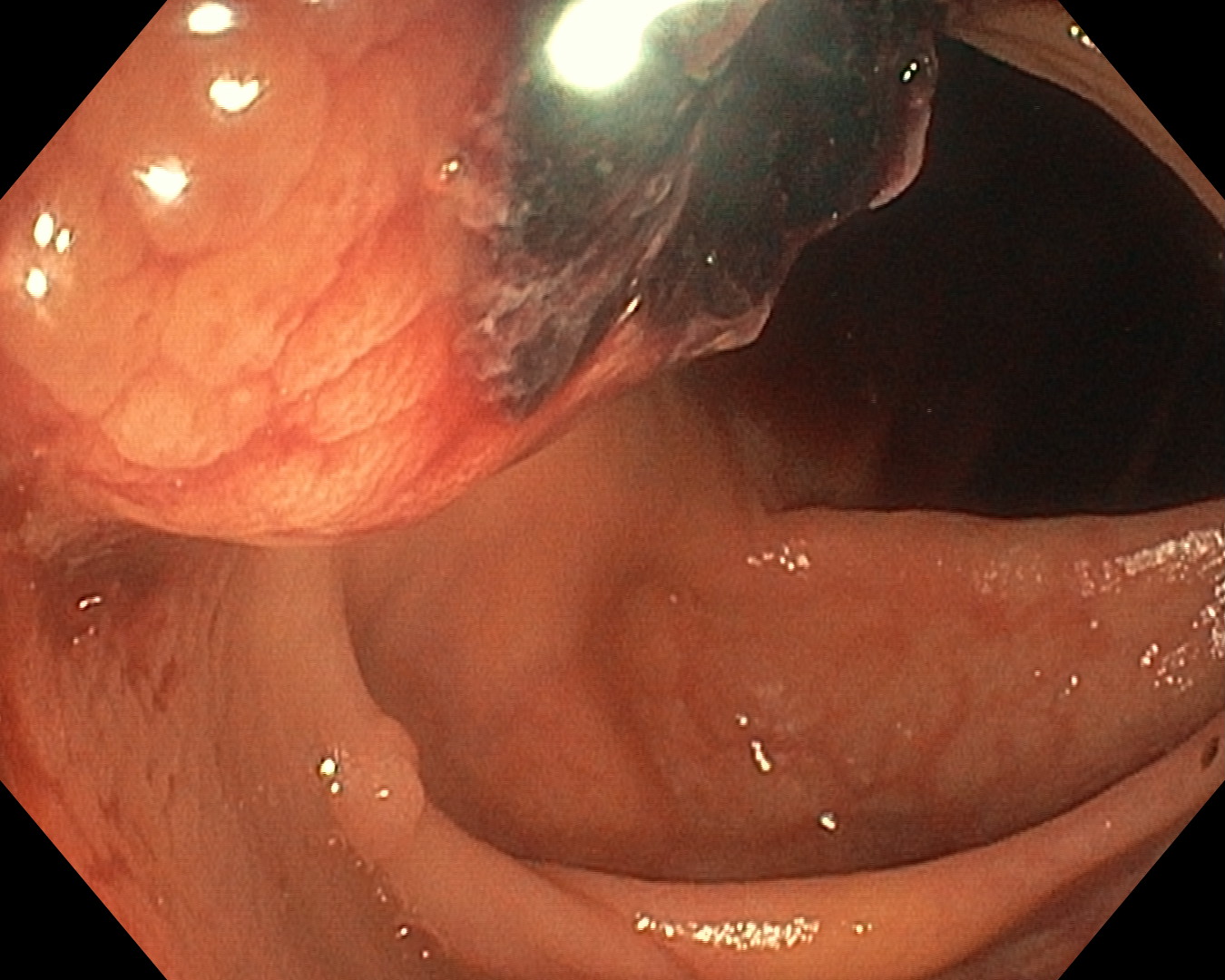
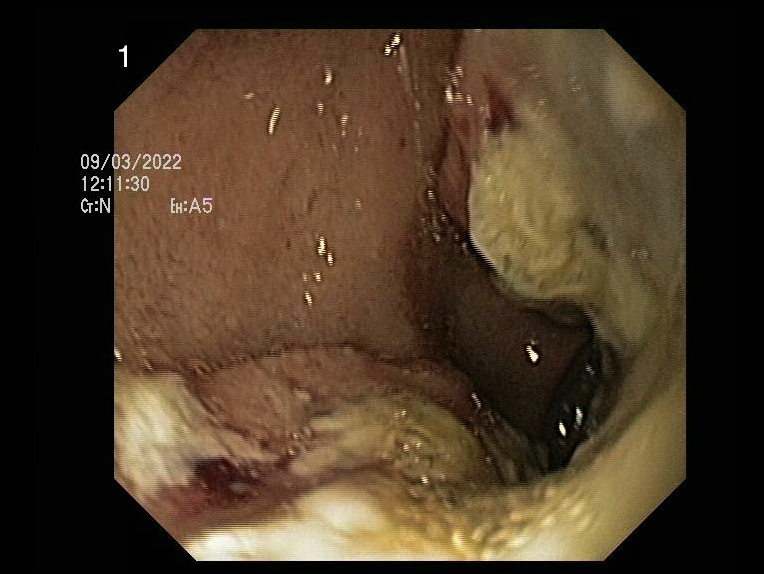
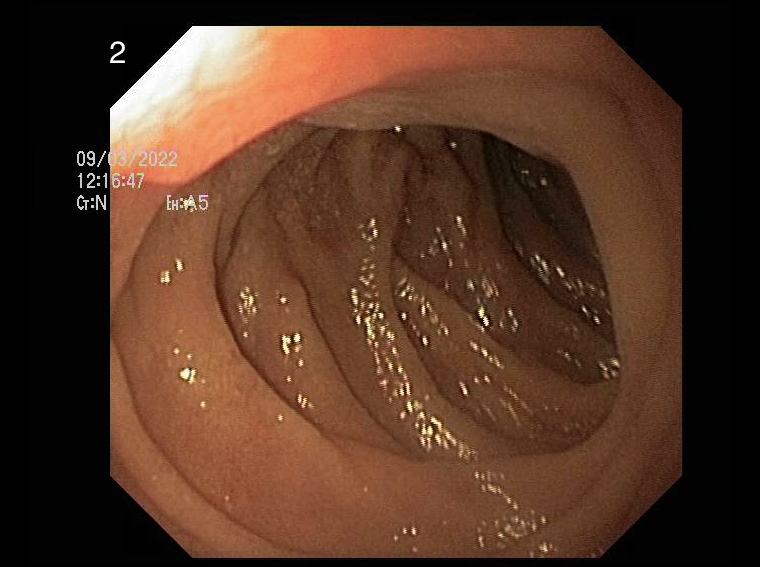
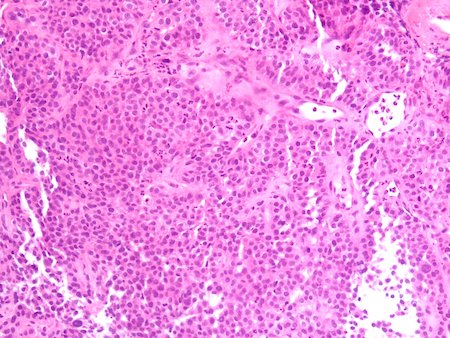
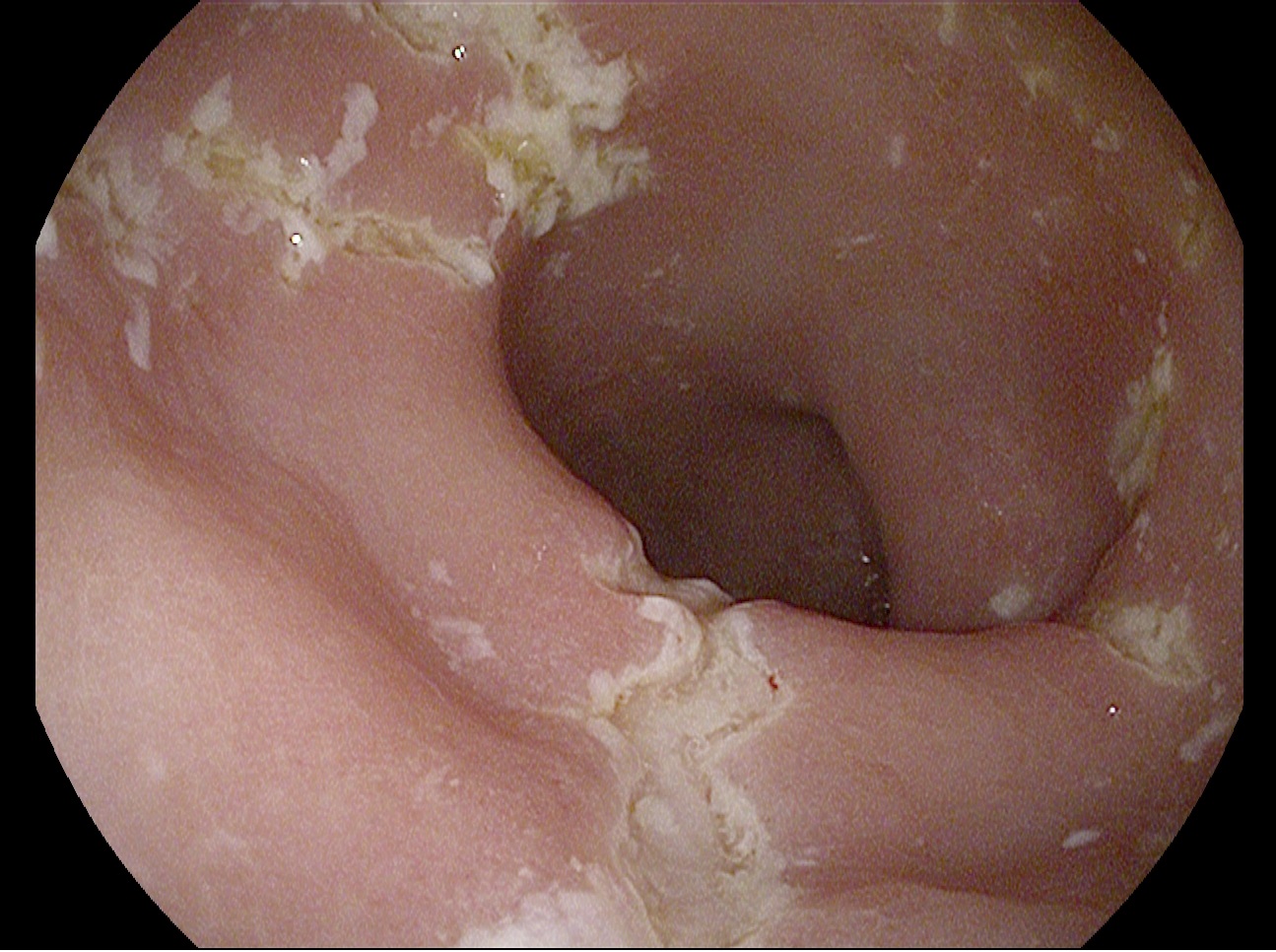
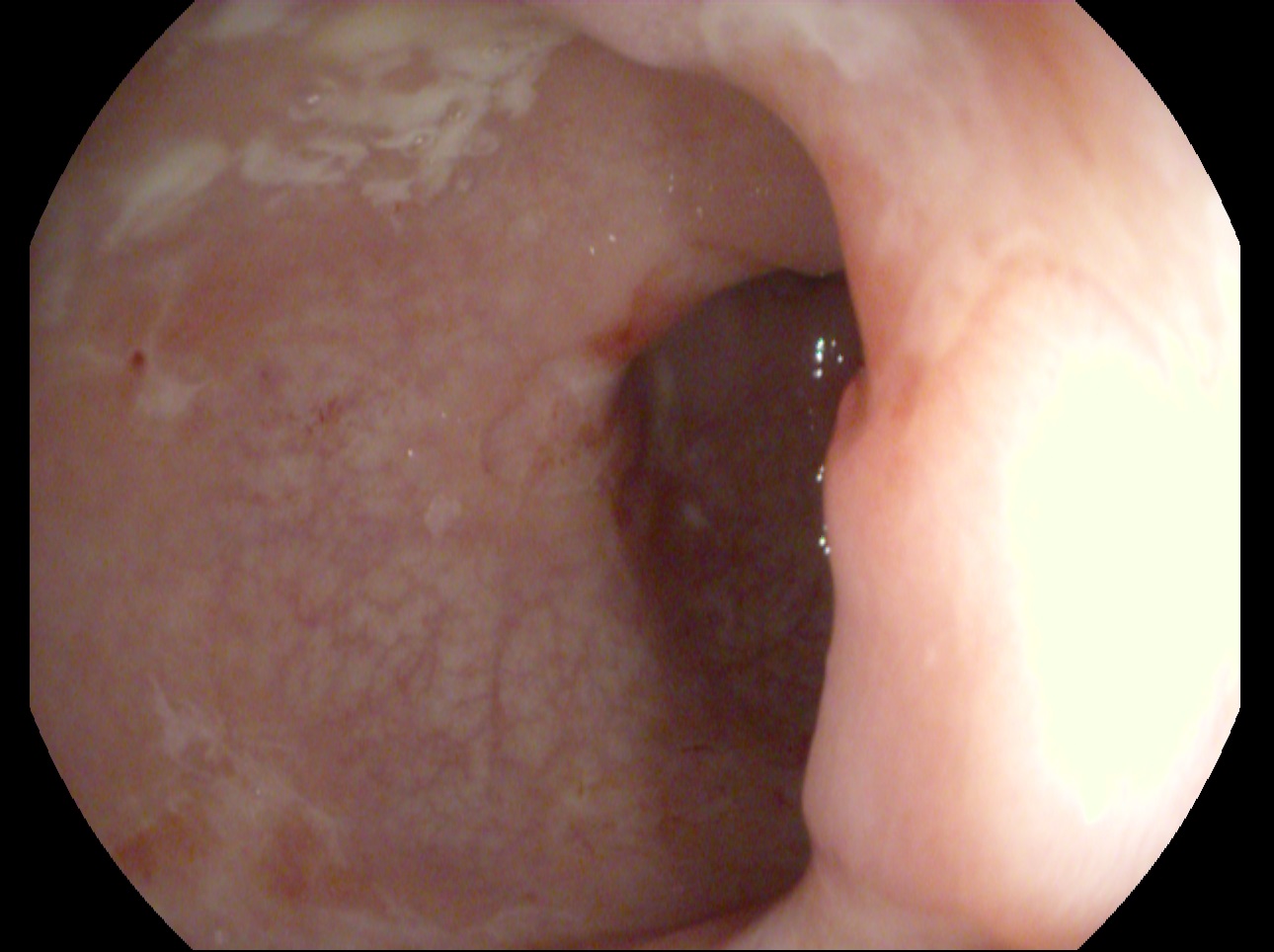
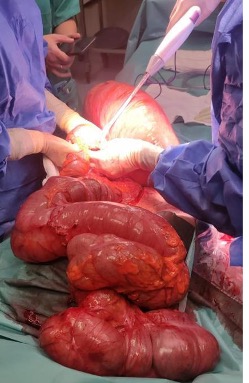
Se contacta con Aparato Digestivo decidiéndose realizar colonoscopia descompresiva que muestra a 15 cm del margen anal un fruncimiento con mucosa distal sana que comienza a presentar datos de isquemia conforme se progresa hasta llegar a porción proximal de fruncimiento apareciendo mucosa de aspecto necrótico. Una vez franqueado, da paso a luz colónica con gran dilatación y mucosa necrótica logrando desvolvulación parcial con mejora clínica inicialmente.
Ingresa en Cirugía General para vigilancia, presentando evolución tórpida por lo que se realiza finalmente sigmoidectomía y colostomía terminal.
Discusión
El vólvulo sigmoideo ocurre cuando un asa del sigma llena de aire se retuerce alrededor de su mesenterio. La obstrucción de la luz intestinal y el deterioro de la perfusión se producen cuando el grado de torsión supera los 180 y 360 grados, respectivamente. La fisiopatología precisa no está bien establecida, pero se han descrito factores de riesgo como un sigma redundante largo con una unión mesentérica estrecha y la dismotilidad colónica. Clínicamente se caracteriza por dolor abdominal progresivo y distensión, náuseas y estreñimiento. Posteriormente, pueden aparecer vómitos. En ocasiones, el compromiso de la perfusión puede provocar gangrena, peritonitis y sepsis. Los pacientes jóvenes pueden presentar crisis de dolor abdominal con resolución por detorsión espontánea. Se diagnostica mediante radiografía o TAC de abdomen.
En pacientes sin complicaciones como peritonitis o perforación intestinal, el tratamiento de primera línea se basa en la detorsión endoscópica seguida de cirugía programada si ha tenido éxito de desvolvulación endoscópica. En caso de complicación o fracaso del tratamiento endoscópico, se realizará sigmoidectomía urgente.
CP-125. AFECTACIÓN COLÓNICA EN ENFERMEDAD GRANULOMATOSA CRÓNICA.
Fernández Cornax A1, Díaz Barbero N2, León Valenciano L2, Mongil Poce LL2
1UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga. 2Servicio Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: colonoscopia, enfermedadgranulomatosa, granuloma.
Introducción
La enfermedad granulomatosa crónica (EGC), es una entidad infrecuente englobada dentro de las inmunodeficiencias primarias que predispone al desarrollo de infecciones graves, siendo diagnosticada frecuentemente en la infancia.
Fisiopatológicamente, existe un defecto funcional de un complejo enzimático clave en la fagocitosis, favoreciéndose la formación de granulomas en el organismo. Clínicamente destaca la aparición de infecciones recurrentes, aunque también es característica la aparición de granulomas a distintos niveles.
Caso clínico
Nuestro paciente es un varón de 31 años, diagnosticado de EGC en la adolescencia y que presenta un cuadro de meses de evolución consistente en diarrea sin aparición de productos patológicos. En el estudio destaca calprotectina fecal elevada, por lo que se decide realización de colonoscopia diagnóstica.
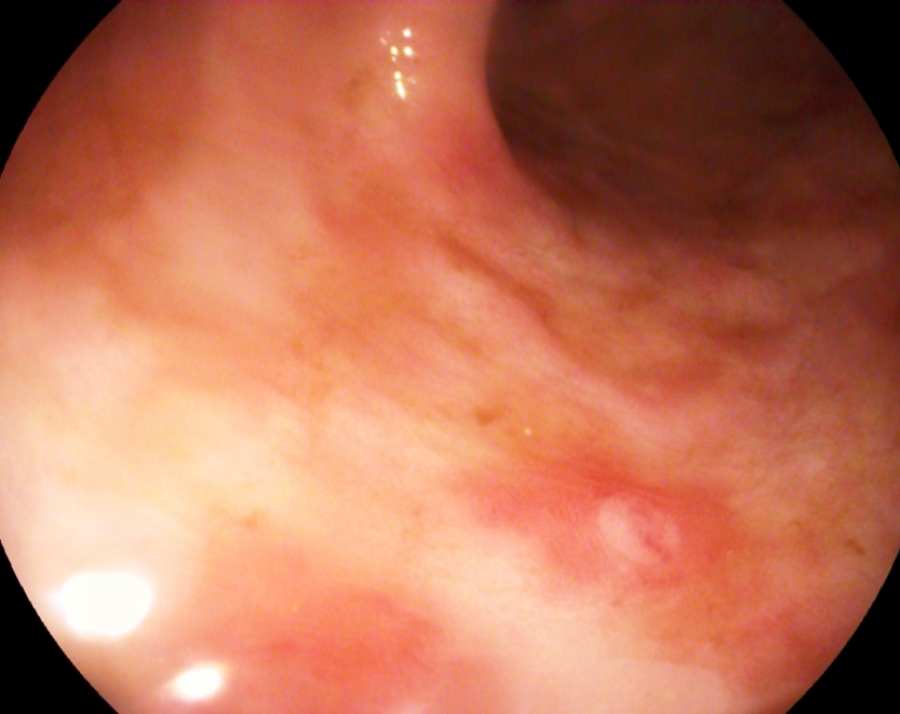
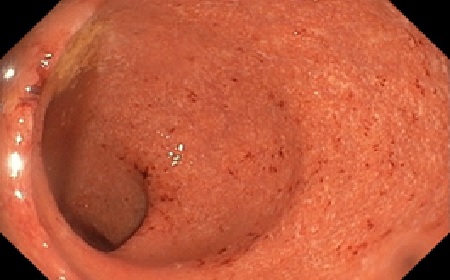
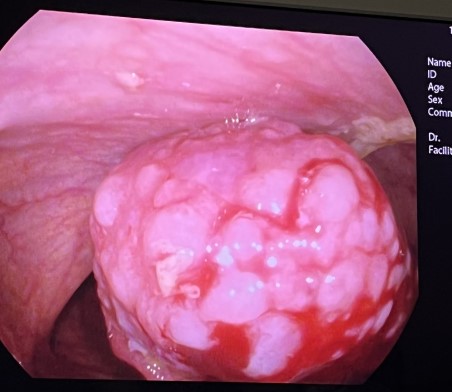
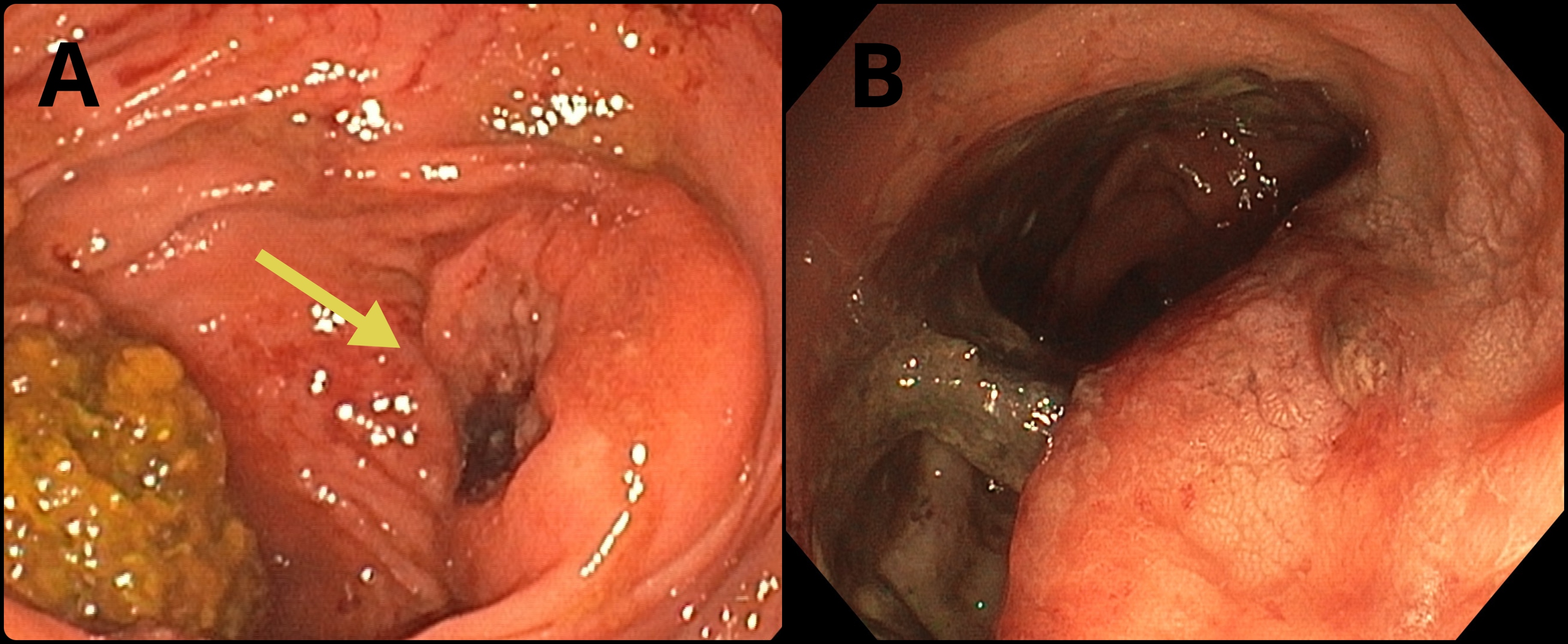
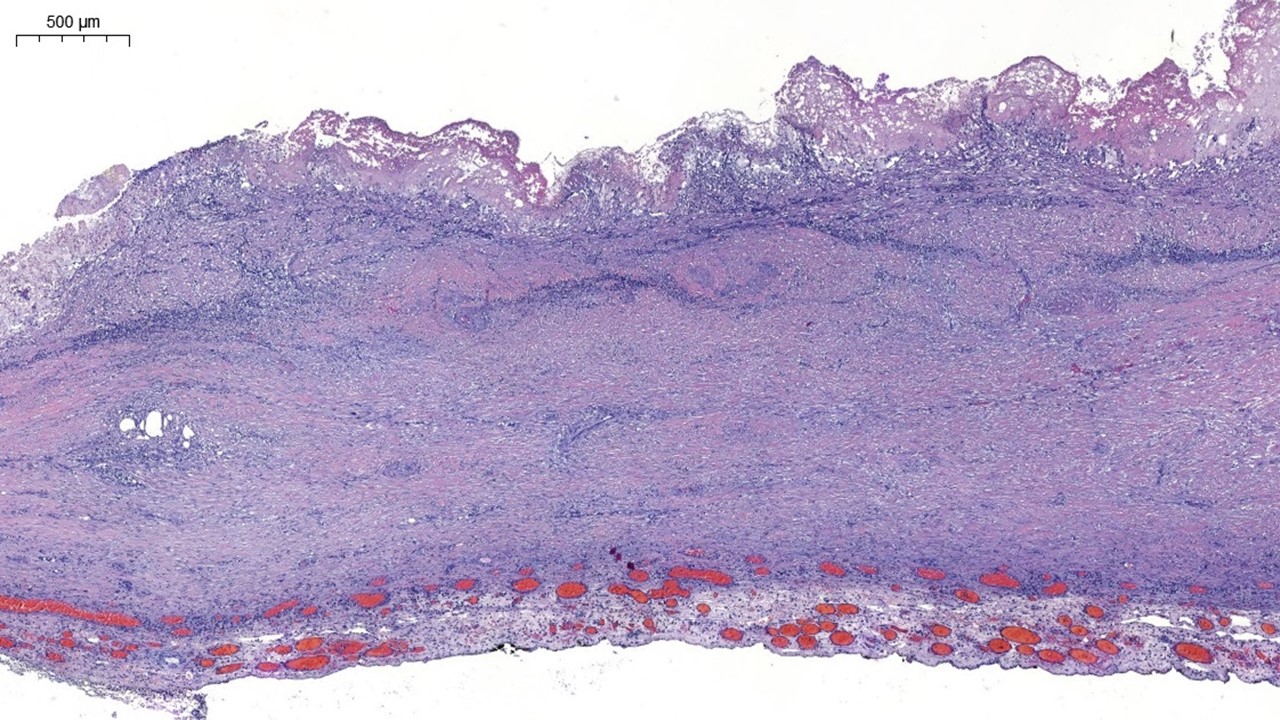
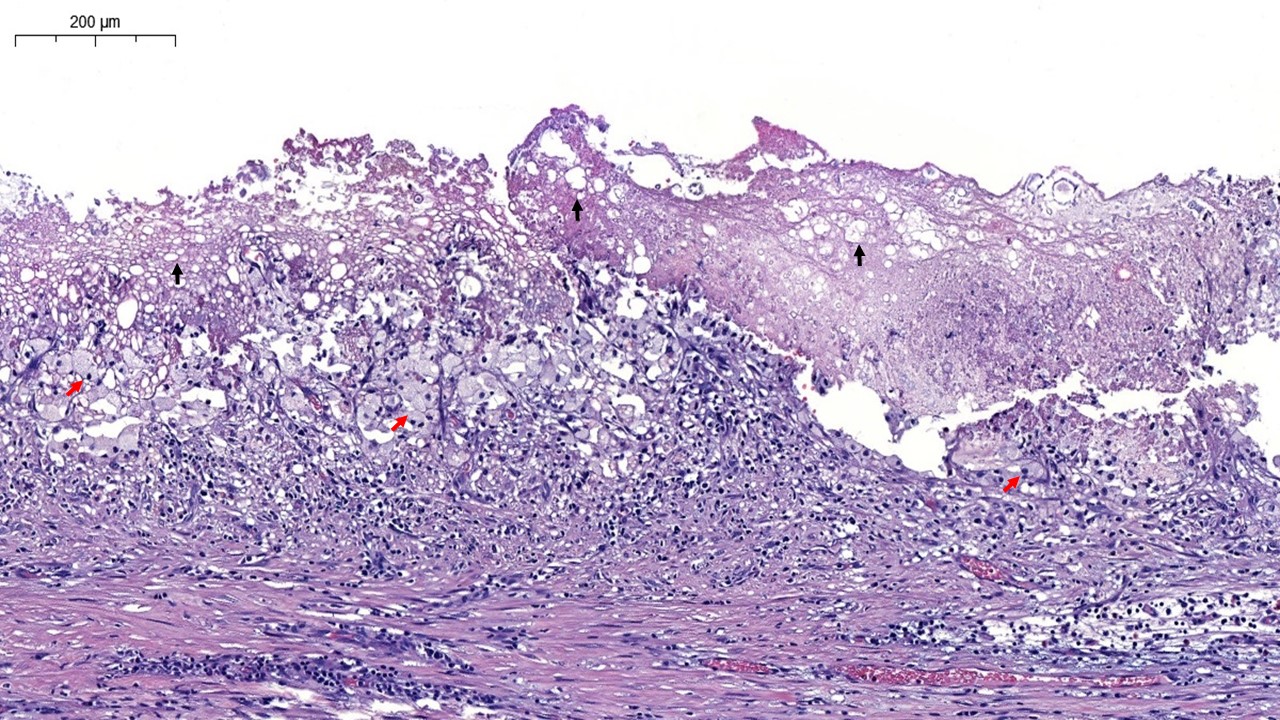
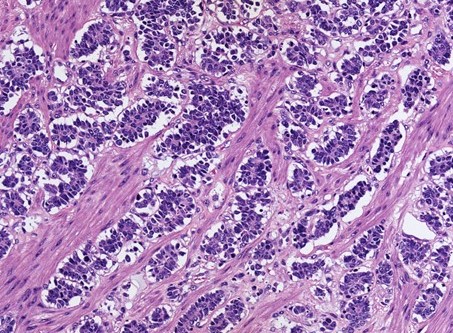
Se introduce endoscopio, observándose a 4 cm de margen anal una lesión nodular, polilobulada e irregular, sin ulceraciones en su superficie, de unos 20 mm y que ocupa más del 50% de la circunferencia rectal (Figura 1), se aplica cromoendoscopia virtual para mejor visualización de la lesión (Figura 2). Se toman múltiples biopsias de la lesión descrita. Resto de la exploración sin hallazgos relevantes.
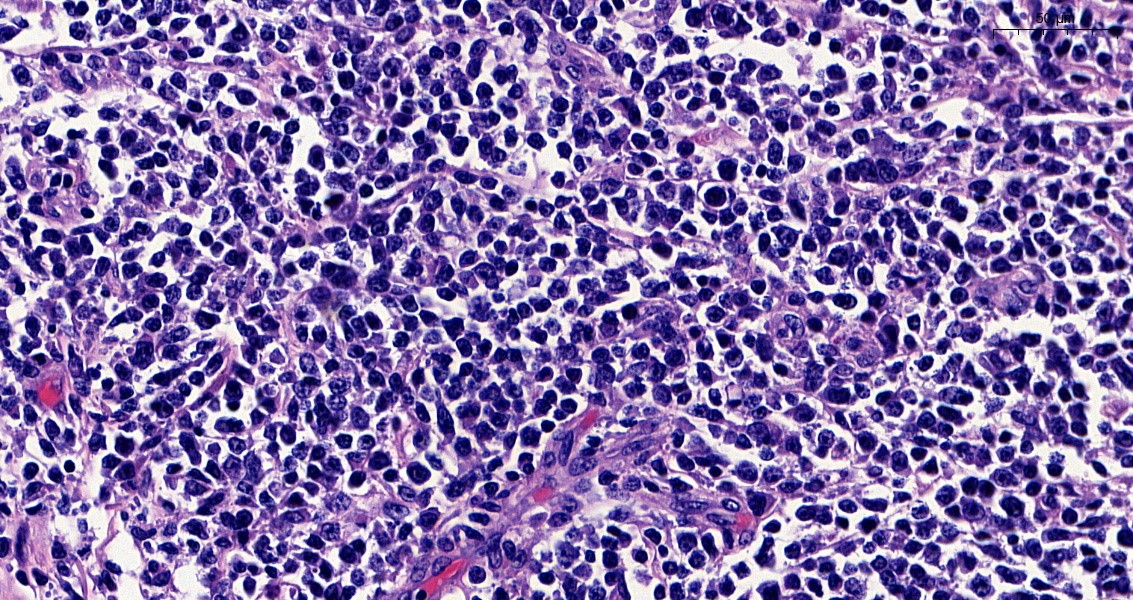
El estudio de AP informa de colitis crónica granulomatosa no necrotizante con actividad leve, sin observar signos de displasia en la muestra. Se realiza seguimiento endoscópico de la lesión, que mantiene estabilidad en cuanto a tamaño y morfología, repitiéndose biopsias con resultados similares.
Discusión
La EGC es una inmunodeficiencia poco común que puede cursar con la aparición de granulomas gastrointestinales. Pese al aspecto irregular de las lesiones, los granulomas no comportan riesgo de progresión a displasia. Infrecuentemente los granulomas pueden aumentar su tamaño condicionando problemas locales como la obstrucción intestinal.
CP-126. AFECTACIÓN GASATROINTETINAL EN PACIENTE CON CÁNCER DE MAMA, ¿SE DEBE SOSPECHAR METÁSTASIS?
Díaz Alcázar MM, López Peña C
UGC Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: cáncer de mama, metástasis, íleon..
Introducción
El cáncer de mama es uno de los tumores más frecuentes a nivel mundial. En casos avanzados suele metastatizar en hueso, pulmones e hígado. Sin embargo, las metástasis de esta neoplasia en el tracto gastrointestinal son raras.
Caso clínico
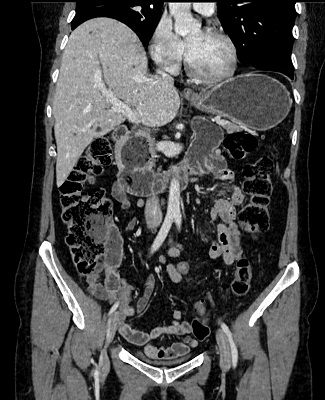
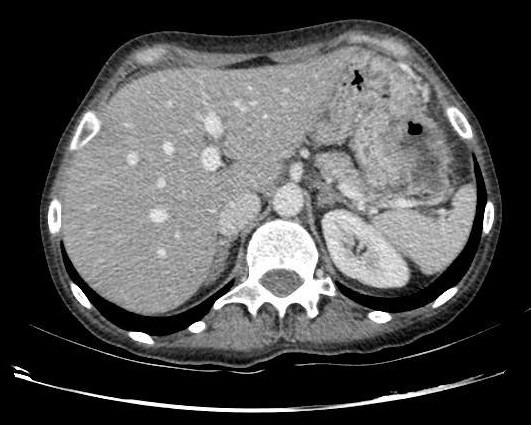
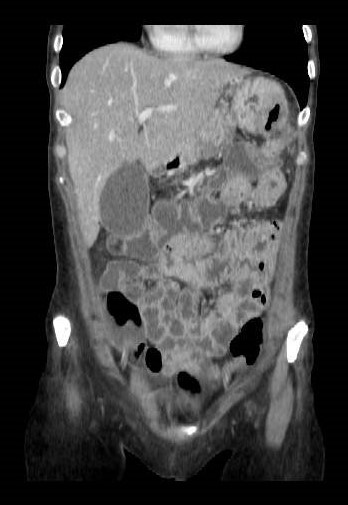
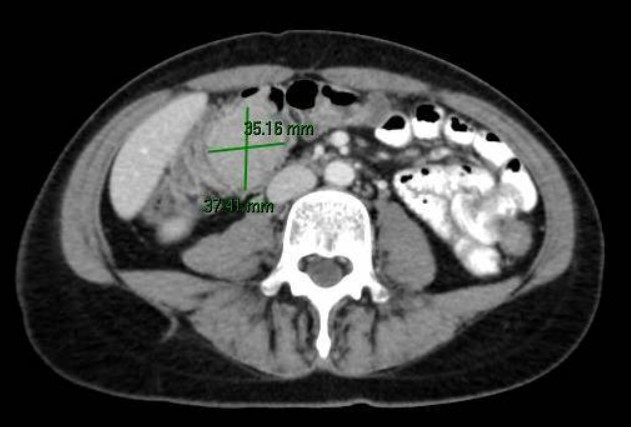
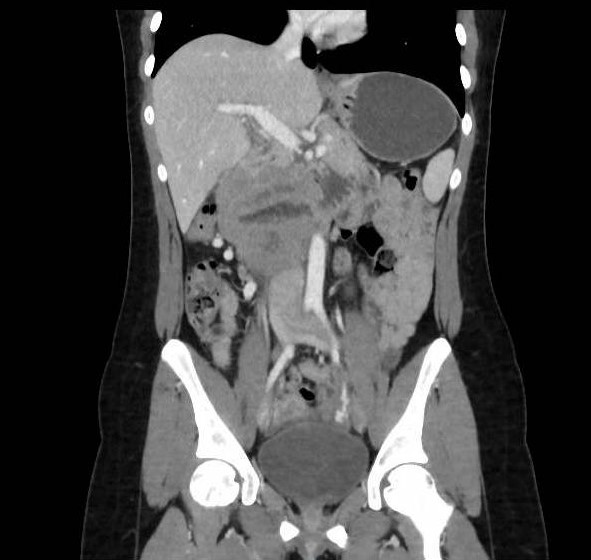
Mujer de 71 años diagnosticada de cáncer de mama. Se realiza estudio de extensión con tomografía computarizada toraco-abdomino-pélvica con contraste detectando en íleon terminal segmento corto de unos 3 cm con engrosamiento concéntrico e hipercaptación. La paciente niega clínica digestiva. Se plantea en primer lugar ileocolonoscopiam en la que se observa en colon derecho, en haustra inmediatamente distal a válvula íleocecal, una úlcera fibrinada. En íleon terminal,la mucosa está ulcerada, de aspecto cavitado, friable al roce y pétrea a la toma de biopsias. El estudio histológico de las biopsias de colon derecho e íleon es compatible con infiltración de la lámina propia por carcinoma lobulillar metastásico triple negativo (receptor de estrógenos y progesterona y producción de HER2 negativos). La paciente no presenta afectación metastásica a otro nivel. Se decide tratamiento oncológico sistémico.
Discusión
El patrón metastásico del cáncer de mama se relaciona con el receptor de estógenos y el tipo histológico de tumor. Los tumores que expresan receptor de estrógenos metastatizan más en hueso, mientras que los que no tienen receptor presentan más afectación visceral. Con respecto al tipo histológico, el cáncer lobulillar tiene más tendencia a metástasis gastrointestinales, afectación ginecológica y enfermedad peritoneal que el ductal, que se extiende más a hígado, pulmones y cerebro.
Las metástasis del cáncer de mama en el tracto gastrointestinal se consideran muy raras (<5%), aunque se han publicado series de autopsias con metástasis a este nivel en hasta el 15-16% de los casos. El diagnóstico de la afectación metastásica puede ser complejo, ya que la clínica es inespecífica y las biopsias pueden ser negativas en hasta el 50% de los casos porque el tumor invade desde la serosa y puede no llegar a afectar a la mucosa.
El caso presentado, además de por ser un lugar infrecuente de metástasis del cáncer de mama, destaca también porque las metástasis solitarias en el tracto gastrointestinal son extremadamente poco comunes.
CP-127. AFECTACIÓN INTESTINAL SECUNDARIA A PÚRPURA DE SCHÖNLEIN-HENOCH
Mata Perdigón FJ1, Viejo Almanzor A2, Abraldes Bechiarelli AJ2
1UGC Aparato Digestivo. Hospital de Especialidades de Puerto Real, Puerto Real. 2UGC Aparato Digestivo. Hospital Puerta del Mar, Cádiz.
Palabras clave: púpura de schölein-henoch, hemorragia digestiva.
Introducción
La púrpura de Schölein-Henoch es una vasculitis sistémica de pequeño vaso ocasionada por el depósito de inmunocomplejos IgA en la pared vascular. Ocurre principalmente en la infancia, la mayoría de las ocasiones tras una infección respiratoria, siendo poco frecuente en el adulto.
Caso clínico
Mujer de 66 años hipertensa, dislipémica y obesa que ingresa en Dermatología por pápulas purpúricas de una semana de evolución, algunas con centro necrótico y ampollas hemorrágicas, afectando a miembros superiores, inferiores y región abdominal. Las biopsias de las lesiones confirmaron una vasculitis leucocitoclástica con depósito de IgA en las paredes vasculares compatible con púrpura de Schölein-Henoch.
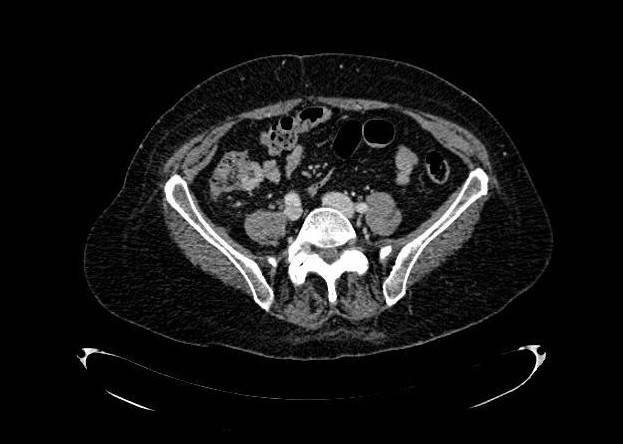
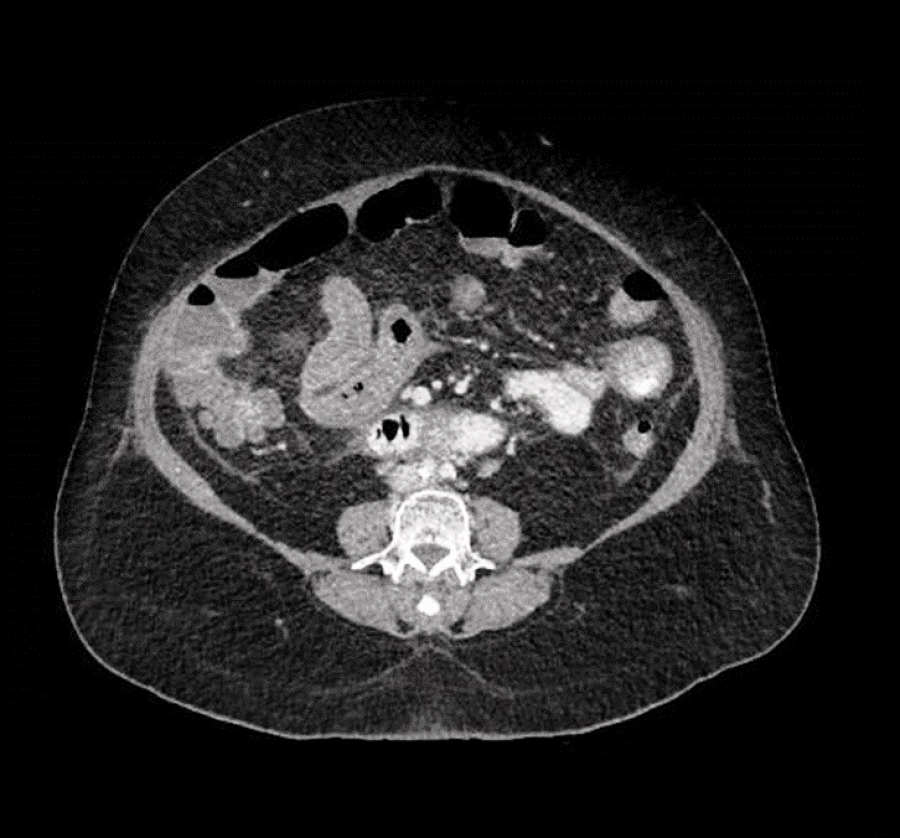
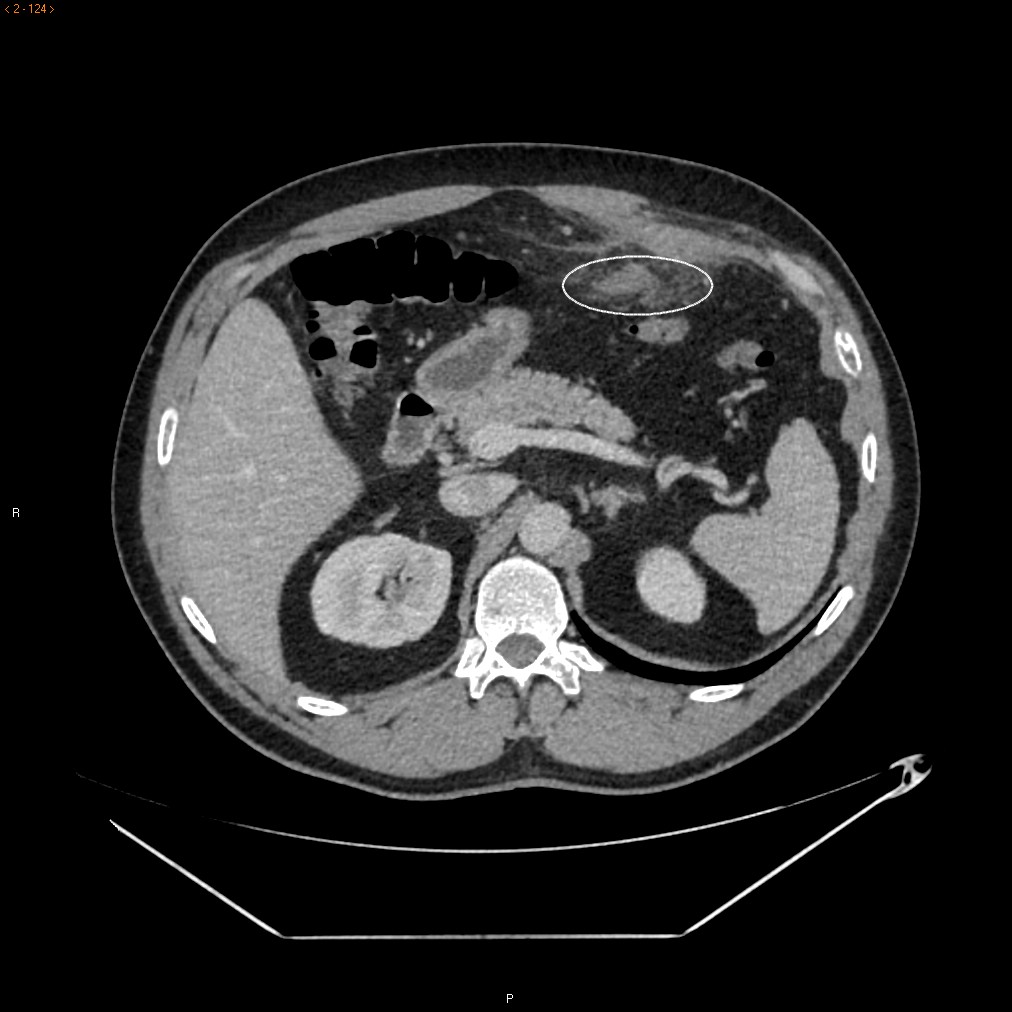
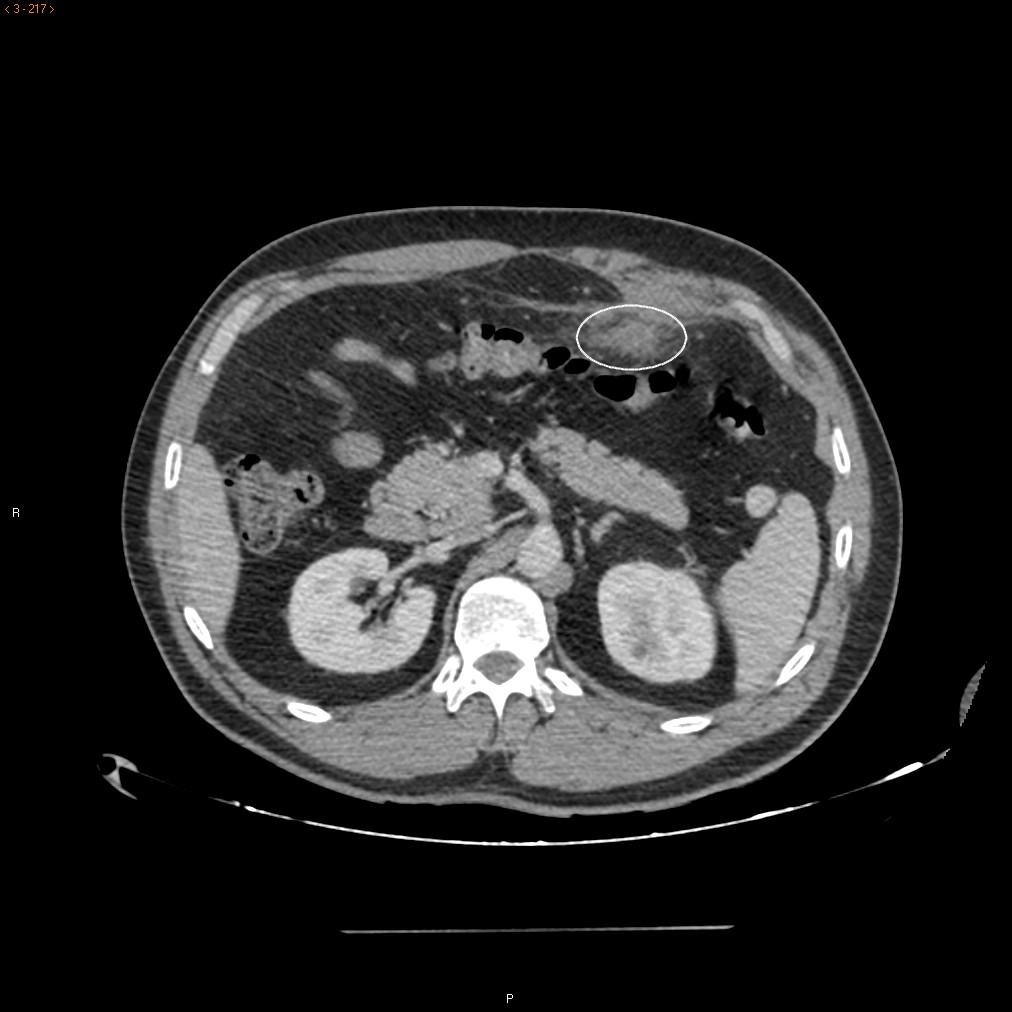
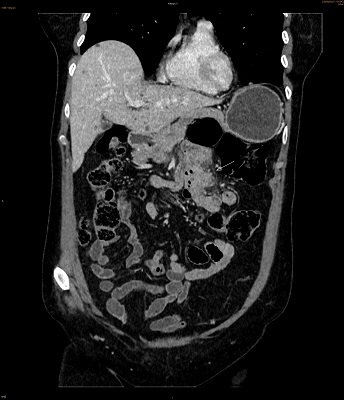
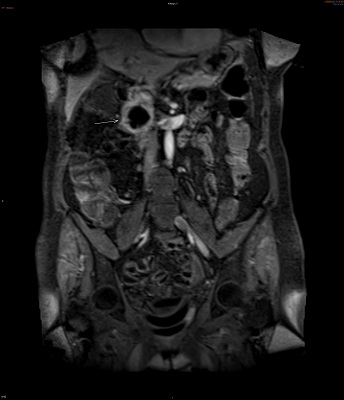
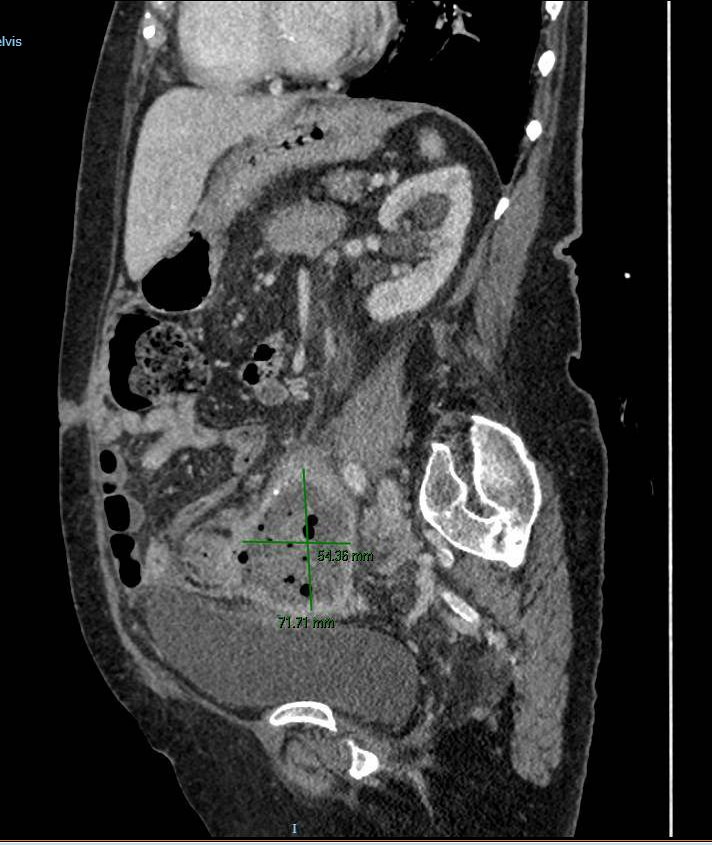
Se administraron bolos de metilprednisolona con mejoría parcial de las lesiones cutáneas pero la paciente comenzó con dolor abdominal y rectorragia no anemizante al quinto día del ingreso. Se realizó estudio con TC abdominal informando de cambios inflamatorios a nivel de íleon terminal y ciego, con líquido libre así como divertículos en colon descendente sin signos de complicación (Figura 1).
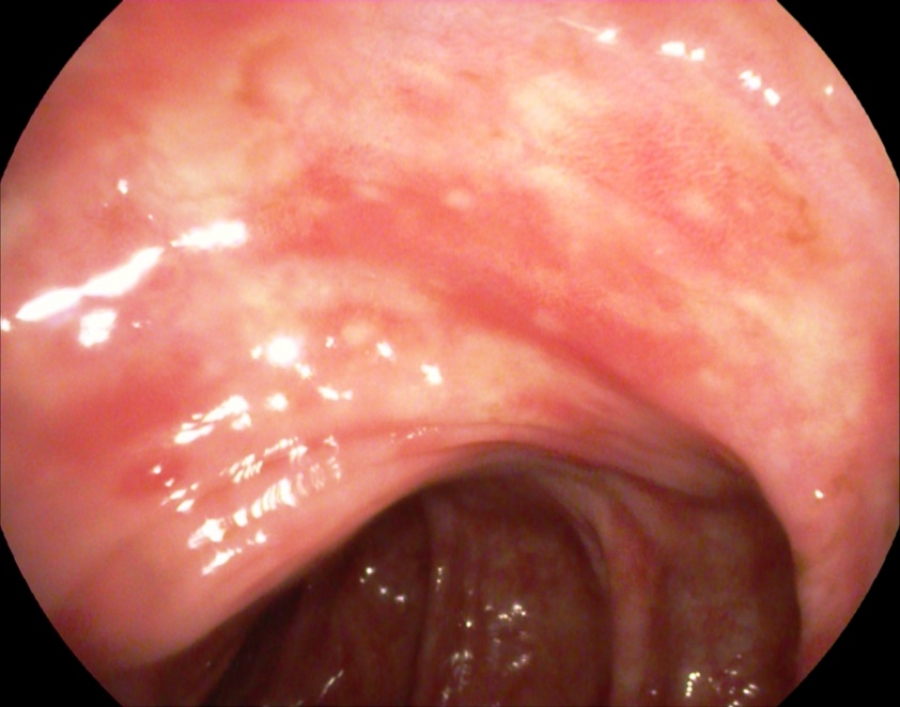
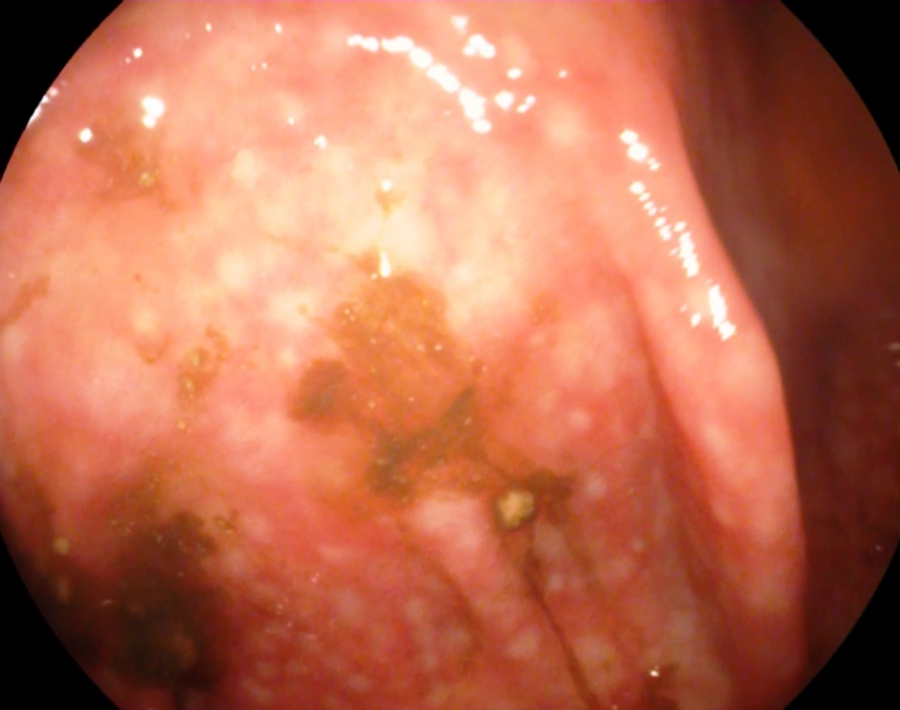
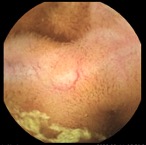
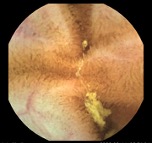
Se completó estudio con colonoscopia evidenciando edema, eritema y pérdida del patrón vascular con lesiones purpúricas en diana en todo el tramo colónico, más marcado a nivel de ciego y colon derecho con una válvula ileocecal edematosa que resultó imposible intubar (Figuras 2, 3, 4). Además, se realizó endoscopia oral sin hallazgos patológicos.
Las biopsias de las lesiones colónicas fueron inespecíficas y fue precisó la escalada del tratamiento con inmunoglobulinas, micofenolato mofetilo y posteriormente rituximab. La paciente evolucionó desfavorablemente desarrollando una insuficiencia respiratoria y una aplasia medular siendo finalmente exitus.
Figura 1
Corte transversal de TC abdominal donde puede observarse un engrosamiento de íleon terminal con pequeña cantidad de líquido libre.
Figura 2
Lesiones eritematosas en diana en colon derecho, de distribución parcheada, afectando a la totalidad de la circunferencia colónica.
Discusión
La púrpura de Schölein-Henoch es una vasculitis sistémica con afectación principalmente cutánea. Los síntomas gastrointestinales en forma de dolor abdominal, náuseas, vómitos y alteración del ritmo intestinal pueden aparecer en el 50% de los pacientes y normalmente preceden a las manifestaciones cutáneas.
Sin embargo, la presencia de hematoquecia o rectorragia solo está presente en un 25% de los pacientes y en el estudio endoscópico pueden observarse lesiones purpúricas en diana en cualquier tramo digestivo pudiendo asociar edema y ulceración mucosa.
El diagnóstico anatomopatológico de la púrpura se suele realizar por biopsia cutánea y las muestras a nivel endoscópico no suelen ser confirmatorias al tomar solo tejido mucoso.
El tratamiento en los casos de afectación sistémica precisa de inmunosupresores. En torno al 90% de los pacientes adultos se recuperan de la enfermedad, pero hasta en un tercio de los enfermos se produce recidiva con la sintomatología de debut pero de menor intensidad.
CP-128. ANÁLISIS DEL SÍNDROME DE LYNCH-LIKE EN LA CONSULTA DE ALTO RIESGO DEL HOSPITAL TORRECÁRDENAS
Hallouch Toutouh S, Diéguez Castillo C, Navarro Moreno E
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: lynch-like, alto riesgo, inestabilidad de microsatélites. .
Introducción
El síndrome Lynch-like (SLL) se define por la presencia de inestabilidad de microsatélites en la pieza tumoral, sin identificar mutaciones en línea germinal. Existen multitud de explicaciones que puede justificar dicha entidad, pero ante la situación de incertidumbre que genera las guías actuales recomiendan un vigilancia endoscópica similar al síndrome de Lynch. El objetivo de nuestro estudio es valorar las características clínicas de los pacientes diagnosticados de SLL en nuestra consulta.
Material y métodos
Presentamos un estudio descriptivo, en el que se incluyen los pacientes con diagnóstico de SLL, que se encuentran en seguimiento en la consulta de Alto Riesgo de Aparato Digestivo del Completo Hospitalario Torrecárdenas. Se recogieron las siguientes variables: demográficas (edad y sexo), del CCR (edad del diagnóstico, localización, pérdida de expresión, estadiaje postquirúrgico), agregación familiar para CCR (número y grado de parentesco), así como, tipo de vigilancia endoscópica (periodicidad) y hallazgos.
Resultados
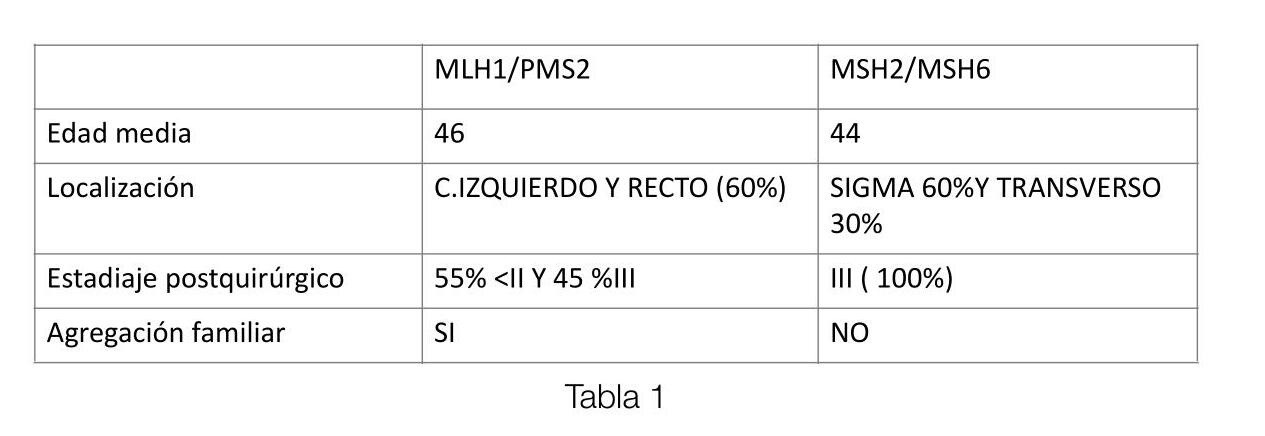
Se incluyen 14 pacientes, con una edad media de 52 años siendo el 50% mujeres. Respecto al diagnóstico de CCR, se diferenciaron las características entre los casos con pérdida de expresión en MLH1/PMS2 ( 11/14) y MSH2MSH6 ( 3/14), las cuales figuran en la tabla 1. En cuanto a la presencia de agregación familiar para CCR, el 21% (3/14) presentaban otros casos en la familia, siendo mayoritariamente de 2ª o 3ª grado (4/6). Todos los casos de agregación familiar se objetivaron entre los casos con pérdida de expresión en MLH1/PMS2.
El 57% ( 8/14) cumplía los criterios revisados de Bethesda, el 35% (5/14) presentaba un PREMM > 5% , y solo el 7% (1/14) cumplía los criterios Amsterdam II.
Respecto a la vigilancia endoscópica, en un 60% se realiza colonoscopia anual y en el resto cada 2 años. Durante el seguimiento el 85% de las colonoscopias fueron normales (12/14), un solo paciente presentó un neoplasia metacrónica colónica y otro desarrolló lesiones de bajo riesgo. Dos pacientes ( 14%) presentaron tumores extracolónicos ( ovario y endometrio).
Conclusiones
El SLL engloba a individuos con gran heterogeneidad clínica cuyo riesgo puede ser muy variable dependiendo de la historia personal y familiar, por lo que, a pesar de las recomendaciones generales se requiere de un asesoramiento individualizado. La determinación de la mutación V600F del BRAF en los casos de pérdida de expresión en MLH1, es una herramienta útil para identificar pacientes con mutaciones esporádicas y realizar una vigilancia endoscópica menos intensiva, no obstante, para protocolizar el abordaje del síndrome de LL se necesita un mejor conocimiento de su patogenia y por ende más investigación en este campo.
CP-129. CARACTERIZACIÓN DEL PERFIL LIPÍDICO DE TEJIDO INTESTINAL
Chica Cid T1, Agulleiro Beraza I1, Reyes Díaz ML2, Muñoz García-Borruel M3, Caunedo Álvarez A3, Gómez Rosado JC4, Rodríguez Téllez M3, Rico Gutiérrez MC1, Pizarro Moreno A1, Gómez Izquierdo L5, Garzón Benavides M1, León Camacho M6, Giráldez Jiménez MD1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 2UGC Cirugía General y Digestiva. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 3UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla. 4UGC Cirugía General y Digestiva. Complejo Hospitalario Regional Virgen Macarena, Sevilla. 5UGC Anatomía Patológica. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 6Laboratorio Bioquímica. Csic Centro Superior de Investigaciones Científicas, Madrid.
Palabras clave: lípidos, intestino, cromatografía.
Introducción
El análisis del perfil lipídico en muestras intestinales está ganando una atención creciente ya que enfermedades como el cáncer colorrectal (CCR) se asocian con una alteración del metabolismo lipídico a nivel intestinal. Los objetivos son: 1) desarrollar un procedimiento analítico para caracterizar el perfil lipídico de muestras intestinales y 2) comparar el perfil lipídico del intestino grueso vs. delgado e identificar una firma lipídica capaz de discriminar entre ambos tipos de tejido.
Material y métodos
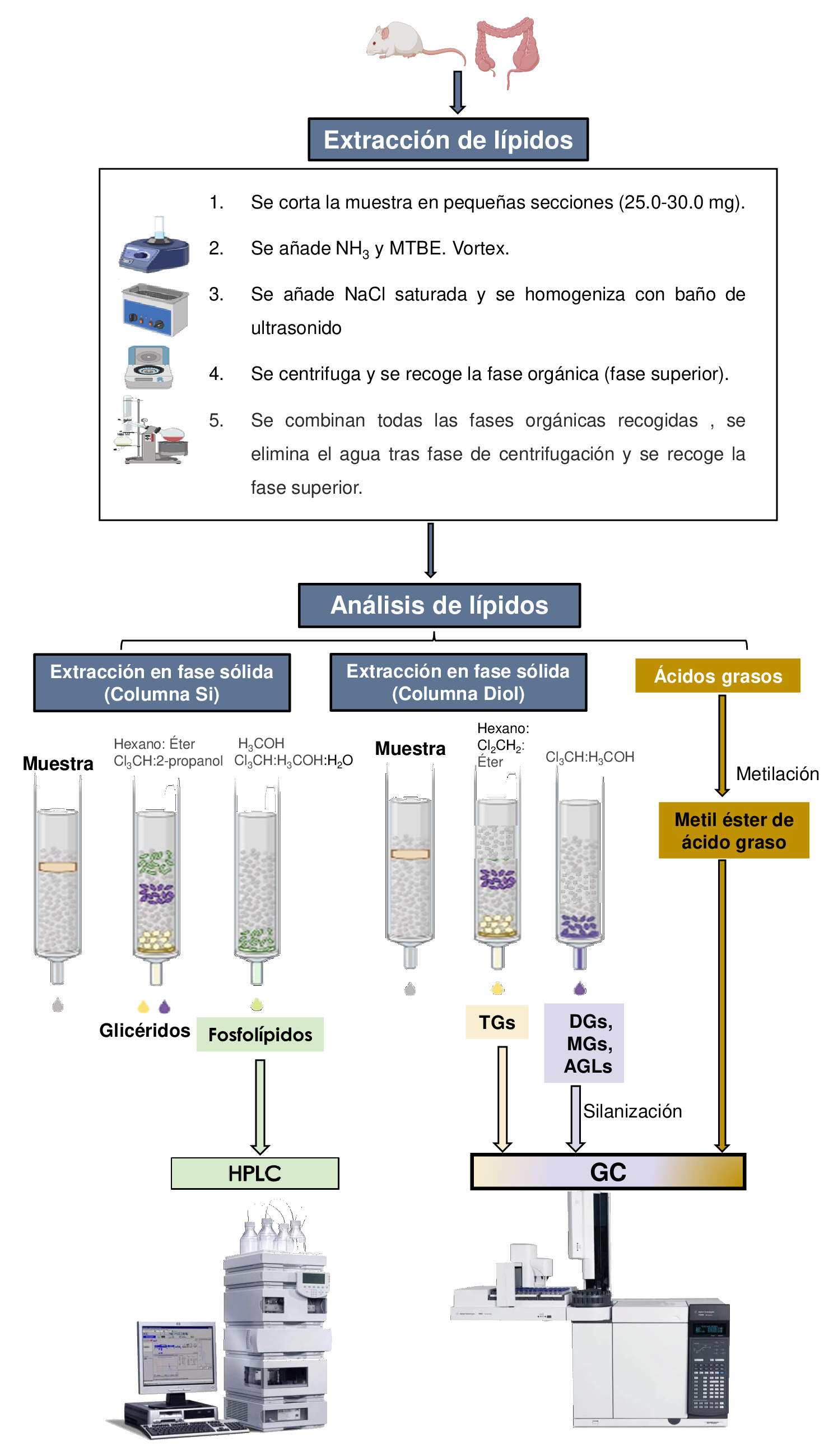
Para optimizar el procedimiento analítico, se utilizaron muestras de intestino grueso y delgado de ratones C57BL6/J. Se realizó la extracción de lípidos con metil-terc-butil-éter (MTBE) a partir de 25 mg de tejido. Los ácidos grasos se analizaron por cromatografía de gases y el resto de la fracción lipídica se aisló por extracción en fase sólida. Los triglicéridos, diglicéridos, monoglicéridos y ácidos grasos libres se analizaron por cromatografía de gases y los fosfolípidos por cromatografía líquida de alto rendimiento (Figura 1). Se utilizó el test ANOVA para comparar la composición lipídica del intestino grueso frente al delgado y se realizó un análisis discriminante lineal para identificar una combinación de lípidos capaz de discriminar entre ambos tipos de tejido.
Resultados
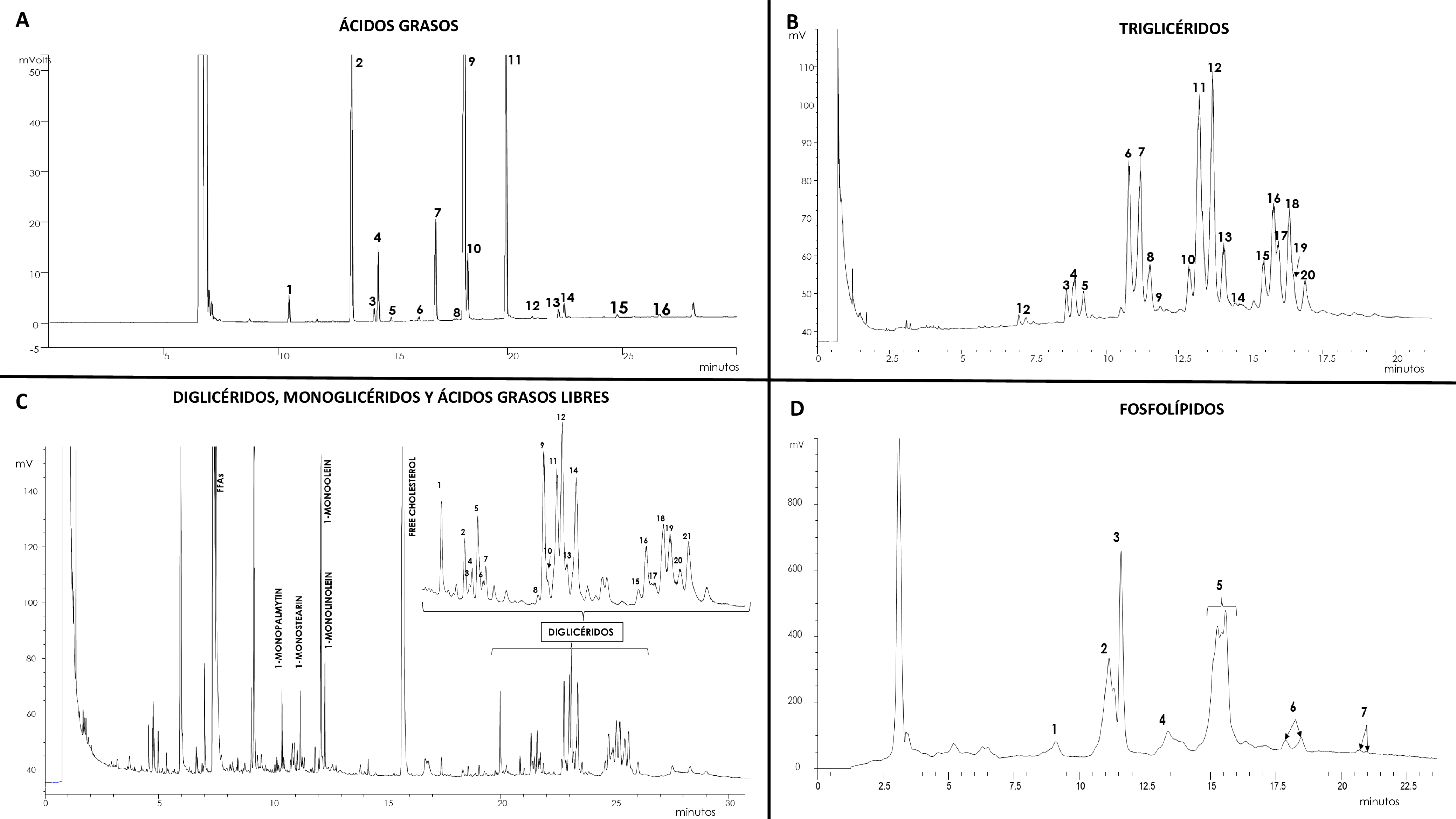
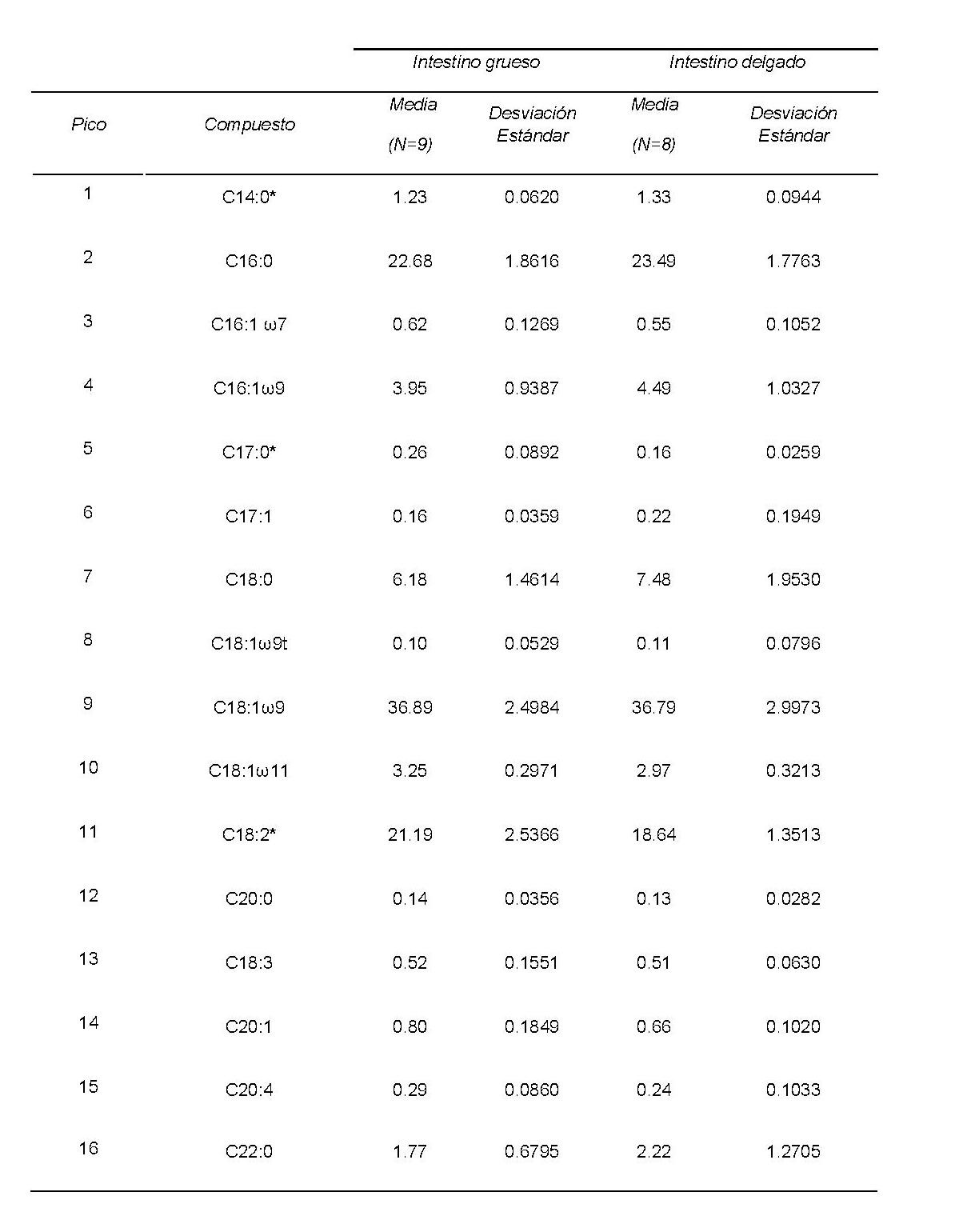
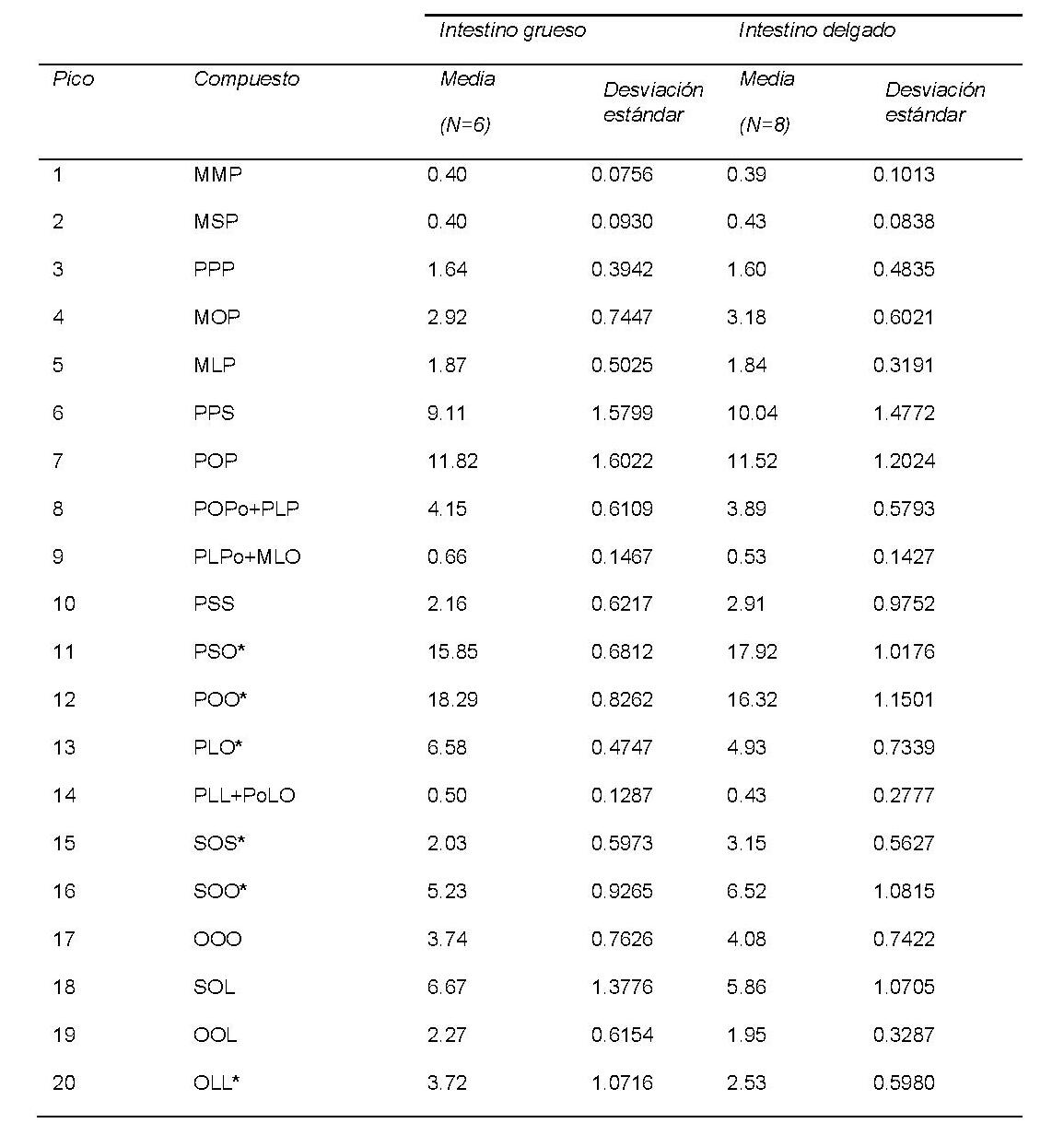
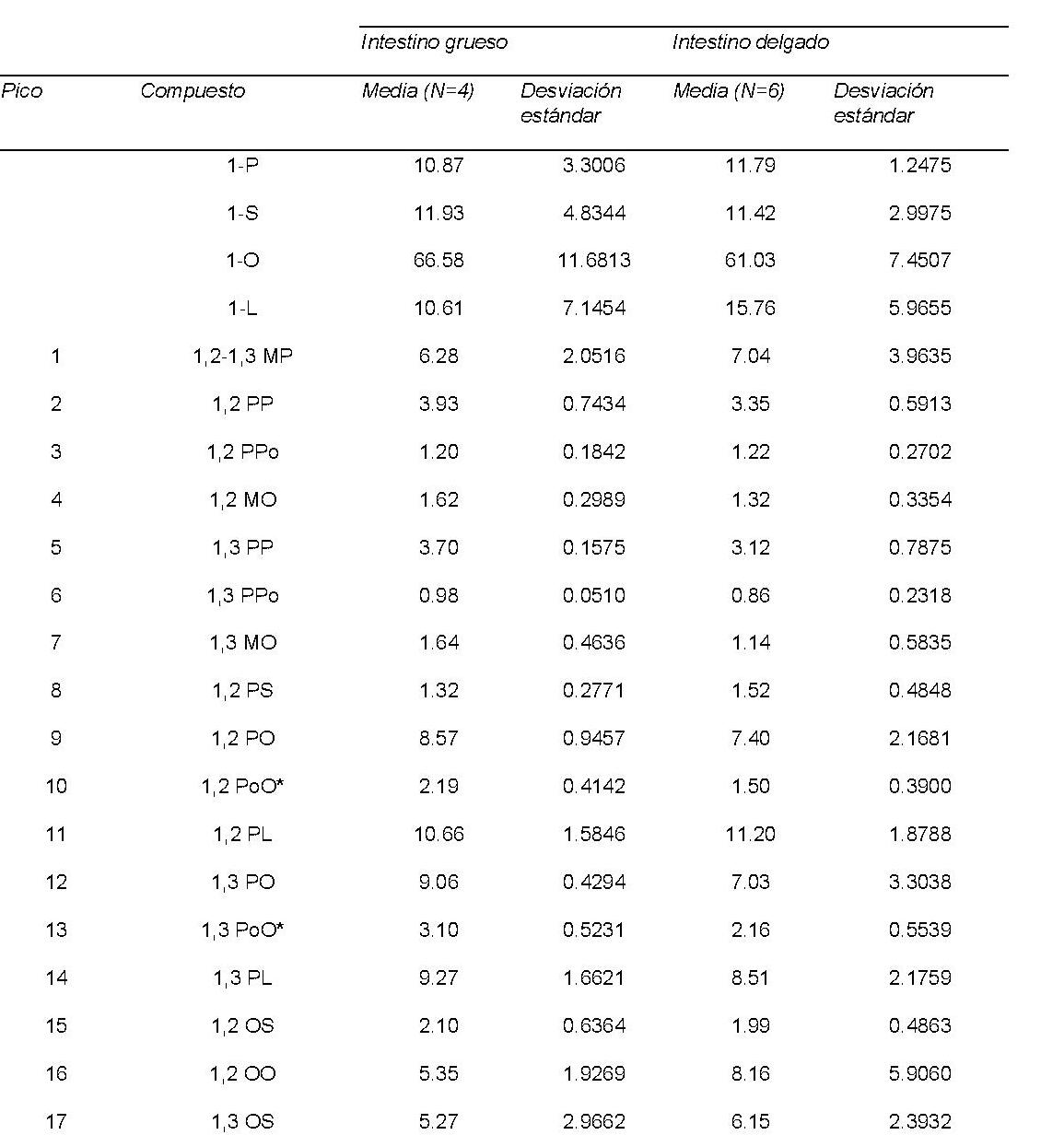
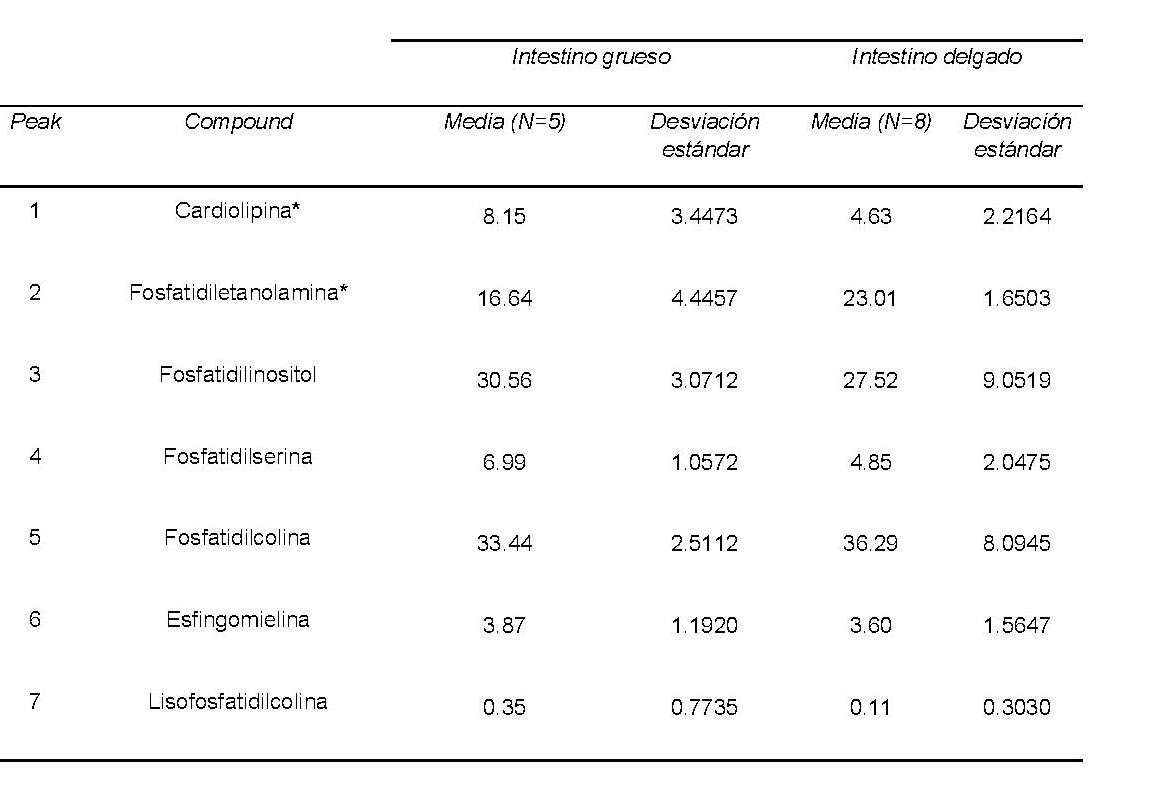
Se identificaron 16 ácidos grasos en muestras de intestino delgado y grueso, siendo el ácido oleico el más abundante en ambas (Figura 2A; Tabla 1). El principal triglicérido identificado varió en función del tipo de tejido (palmitoil-dioleoil glicerol en el intestino grueso y palmitoil-estearil-oleoil glicerol en el intestino delgado) (Figura 2B; Tabla 2). En cuanto a los diglicéridos, los monoglicéridos y los ácidos grasos libres, el principal compuesto fue el 1,2-palmitoil-oleilglicerol tanto en intestino delgado como grueso (Figura 2C; Tabla 3). La fosfatidilcolina fue el fosfolípido más abundante en ambos tejidos (Figura 2D; Tabla 4). Tres ácidos grasos, seis triacilgliceroles, dos diacilgliceroles, la cardiolipina y la fosfatidiletanolamina mostraron diferencias significativas entre el intestino grueso y el delgado. Obtuvimos una separación completa de ambos tejidos utilizando la combinación de seis compuestos lipídicos (C17:0, el C14:0, el C18:2, cardiolipina, fosfatidiletanolamina y distearyl-oleilglicerol).
Figura 2
Perfiles cromatográficos de ácidos grasos (A), triglicéridos (B), diglicéridos, monoglicéridos y ácidos grasos libres (C) y fosfolípidos (D). La identificación de los picos se incluye en las Tablas 1, 2, 3 y 4, respectivamente.
Tabla 1
Identificación y composición (en porcentaje) de la fracción total de ácidos grasos en tejido intestinal de ratón. *Diferencias significativas entre I. grueso y delgado (p<0.05).
Tabla 2
Identificación y composición (en porcentaje) de la fracción total de triglicéridos en tejido intestinal de ratón. M: mirístico; P: palmítico; Po: palmitoleico; S: esteárico; O:oleico; L:linoleico. *Diferencias significativas entre I. grueso y delgado (p<0.05).
Tabla 3
Identificación y composición (en porcentaje) de la fracción total de diglicéridos, monoglicéridos y ácidos grasos libres en tejido intestinal de ratón. M: mirístico; P: palmítico; Po: palmitoleico; S: esteárico; O: oleico; L: linoleico. *Diferencias significativas entre I. grueso y delgado (p<0.05).
CP-130. CAUSA INFRECUENTE DE ABDOMEN AGUDO TRAS INTERVENCIÓN QUIRÚRGICA: APENDAGITIS AGUDA
Navajas Hernández P, Belvis Jiménez M, Muñoz García-Borruel M, Caunedo Álvarez Á
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: apendagitis epiploica, abdomen agudo.
Introducción
La apendagitis epiplóica (AE) es una enfermedad benigna que ocurre como consecuencia de la torsión o trombosis del pedículo vascular de un apéndice epiploico causando isquemia o infarto del mismo. Clínicamente es similar a un cuadro de apendicitis o diverticulitis, siendo el TAC el método diagnóstico de elección. Su evolución suele ser autolimitada, recomendándose inicialmente manejo conservador.
Caso clínico
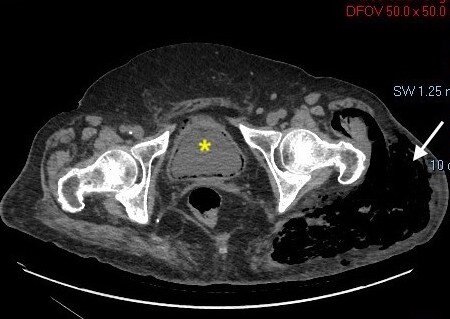
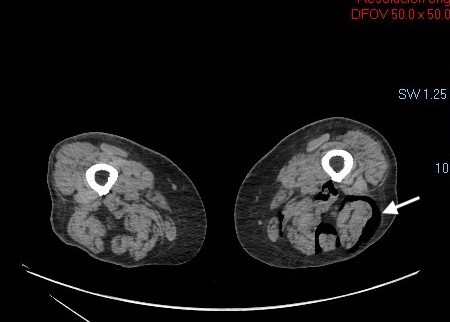
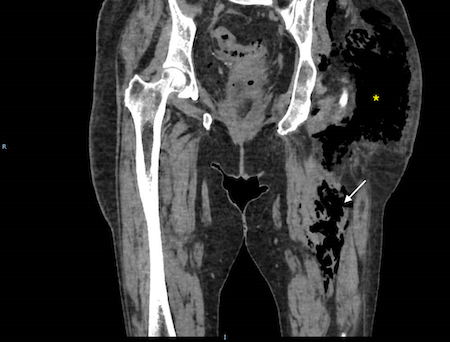
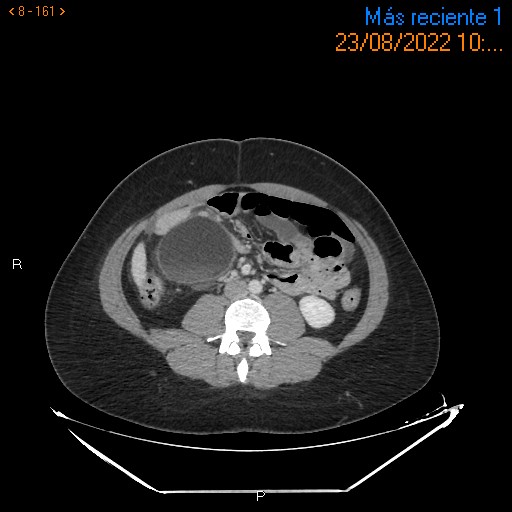
Varón de 41 años con antecedentes de apendicectomía laparoscópica que posteriormente se complicó con hemoperitoneo, requiriendo lavado y drenaje de la cavidad abdominal. Cuatro meses más tarde acude a Urgencias por dolor abdominal intenso en hipocondrio izquierdo irradiado al resto del abdomen junto a sensación febril no termometrada y náuseas. Se realiza analítica con discreta leucocitosis y TAC de abdomen con contraste donde se aprecian cambios inflamatorios en epiplón mayor en flanco izquierdo con edema de la grasa adyacente compatibles con infarto de apéndice epiploico. Se ingresa al paciente en planta de Digestivo y se comienza tratamiento con analgesia, presentando una evolución favorable, pudiendo darse de alta a los tres días de ingreso. Posteriormente, en TAC de abdomen de control a los 3 meses, se aprecia aumento del componente inflamatorio a nivel del área del infarto omental descrito en prueba previa, optándose por laparoscopia exploradora para excisión de epiplón y lavado de la cavidad abdominal. En revisiones posteriores el paciente se mantiene asintomático.
Primer TAC abdomen
Se aprecian cambios inflamatorios en epiplon mayor, en región del vacío izquierdo con edema de la grasa adyacente compatibles con infarto omental o de apéndice epiploico
Discusión
La incidencia verdadera de la AE es desconocida. Ocurre con mayor frecuencia en hombres entre 20-50 años. Clínicamente se caracteriza por dolor abdominal bajo de inicio subagudo o agudo, siendo la exploración desde poco llamativa a presentar signos de alarma (abdomen agudo). En cuanto a la etiología, puede ser primario (idiopático) o secundario (más frecuentes) tras intervenciones quirúrgicas o patologías abdominales como tumores, hernias o adherencias entre otras. El diagnóstico diferencial se realizará con otras causas de abdomen agudo como la apendicitis o la diverticulitis siendo el diagnóstico de confirmación mediante TAC. El tratamiento de elección es conservador (principalmente analgesia) y se reserva el tratamiento quirúrgico en casos de empeoramiento o no resolución del cuadro. Sin embargo, debido a las tasas de recurrencia (en torno al 40%) y que el seguimiento de estos pacientes conlleva la exposición constante de radiaciones ionizantes a través de los TAC de control, algunos autores plantean la cirugía de entrada como solución definitiva de la AE permitiendo la reincorporación temprana del paciente a su vida, especialmente si se opta por un abordaje laparoscópico.
CP-131. CITOLOGÍA DEL LÍQUIDO PERITONEAL EN ASCITIS MALIGNA SECUNDARIA A TUMORES DIGESTIVOS: ¿PODRÍA REDUCIR EL TIEMPO DE DEMORA DEL DIAGNÓSTICO DEL TUMOR PRIMARIO?
Torres Domínguez A1, Saldaña García L1, Hernández Pérez AM1, Rivas Ruíz F2, Rosales Zábal JM1
1Unidad Aparato Digestivo. Complejo Hospital Costa del Sol, Marbella. 2Unidad Investigación. Complejo Hospital Costa del Sol, Marbella.
Palabras clave: ascitis maligna, citología peritoneal, neoplasia digestiva.
Introducción
Analizar si la positividad para células malignas de una citología en el líquido ascítico en los pacientes con ascitis secundaria a tumores digestivos reduce el tiempo de demora hasta el diagnóstico del tumor primario.
Material y métodos
Estudio descriptivo retrospectivo y unicéntrico en el que se analizaron todas las citologías del líquido ascítico solicitadas en el Área Hospitalaria Costa del Sol entre los años 2014 y 2018, seleccionando aquellas cuya causa era tumoral y la neoplasia primaria fue de origen digestivo. Se recogieron los resultados de la citología, las fechas de solicitud y del resultado de la citología del líquido ascítico, y la fecha de solicitud y del resultado del análisis de la muestra histopatológica del tumor primario que dio el diagnóstico definitivo.
Resultados
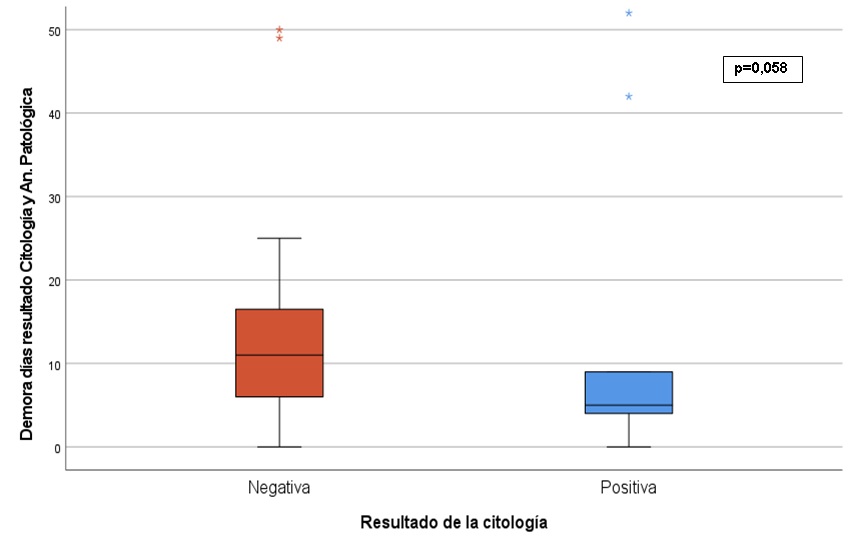
Se analizaron un total de 146 pacientes que presentaron ascitis maligna por neoplasia digestiva, siendo la citología positiva para células malignas en el 32,9% de los casos. En 11 pacientes (7,7%) se realizó el diagnóstico definitivo del tumor primario únicamente con el resultado de la citología. El 45,9% de los pacientes a los que se solicitó la citología del líquido ascítico ya se habían diagnosticado previamente del tumor primario. En los pacientes que aún no tenían un diagnóstico conocido de neoplasia digestiva (53,4%), la citología fue positiva en el 21,8% de los casos, siendo la mediana de tiempo transcurrido desde el resultado de la citología del líquido ascítico hasta el resultado de la anatomía patológica definitiva de 11 días en los pacientes con citología negativa y de 5 días en los pacientes con citología positiva, aunque esta diferencia no fue estadísticamente significativa (p<0.058).
Conclusiones
La citología del líquido ascítico se recomienda como parte del estudio inicial de un paciente con ascitis, sin embargo su sensibilidad para malignidad es baja según los estudios publicados. Aunque podría disminuir los tiempos de demora del diagnóstico del tumor primario de origen digestivo, nuestros resultados muestran que la mayoría de éstas se solicitan en pacientes que ya tienen un diagnóstico previo lo que disminuye su utilidad diagnóstica y podría estar asociado a mayor gasto sanitario.
CP-132. COLITIS ISQUÉMICA INDUCIDA POR CLOZAPINA.
Ruz Zafra P1, Orti Cuerva F2, Rosado Bellido C1, Trigo Salado C1, Herrera Justiniano JM1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 2UGC Medicina Interna. Complejo Hospitalario Regional Virgen del Rocío, Sevilla.
Palabras clave: colitis isquémica, neurolépticos atípicos, clozapina..
Introducción
La clozapina es un antipsicótico atípico empleado en la esquizofrenia resistente al tratamiento. Dentro de los eventos adversos gastrointestinales descritos en el tratamiento con antipsicóticos atípicos se encuentra con mayor frecuencia el estreñimiento, siendo otro mucho menos usual pero potencialmente grave la colitis isquémica. Ello se debe a la acción antiserotoninérgica y anticolinérgica de dichos fármacos que provocan paresia gastrointestinal grave, condicionando vasoespasmo e hipoperfusión a nivel de la mucosa colónica, que está más predispuesta a la isquemia que el resto del intestino. El riesgo de desarrollar colitis isquémica aumenta cuando se asocian fármacos anticolinérgicos.
Caso clínico
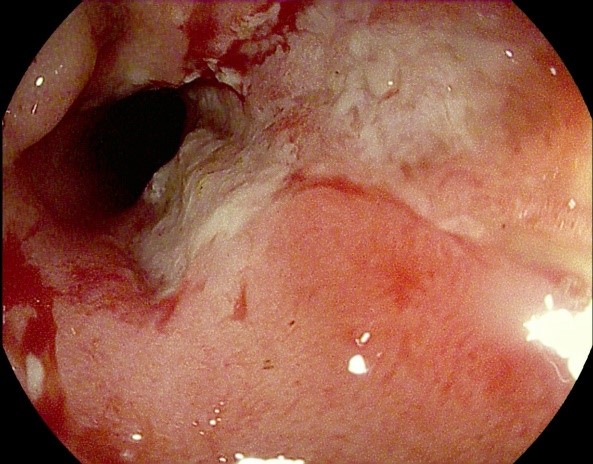
Mujer de 49 años diagnosticada de esquizofrenia hebefreno-paranoide en 2016 con evolución tórpida y necesidad de varios ingresos involuntarios en unidad de agudos de psiquiatría, en tratamiento con ácido valproico 500mg/8h, clonazepam 2mg/8h, Sertralina 50mg/12h y Clozapina 375mg/24h. Acudió a urgencias por dolor abdominal de un mes de evolución en flanco izquierdo, afebril y diarrea líquida asociada. Analíticamente destacaba leucocitosis de 20830/µL y PCR de 507 mg/dl. En la exploración física presentaba distensión abdominal, dolor en zona referida sin peritonismo. Se realizó un TC de abdomen con contraste objetivando colitis izquierda de probable etiología infecciosa/inflamatoria. La colonoscopia posterior constató en colon descendente ulceraciones longitudinales, anchas, excavadas y confluyentes con áreas necróticas en relación con colitis isquémica severa (Figura 1). Ante sospecha de bajo gasto, se solicitó un angio-TC sin objetivarse defectos de repleción en vascularización mesentérica y el estudio de trombofilia fue negativo. Ante estos hallazgos y tras descartar etiología infecciosa asociada, se postuló el probable origen farmacológico secundario a clozapina, por las características del fármaco, decidiéndose retirada del mismo siguiendo indicaciones de psiquiatría. Progresivamente presentó mejoría clínica y analítica, aunque paralelamente se produjo una reagudización de la patología psiquiátrica basal, precisando ingreso en la unidad de agudos de salud mental.
Discusión
Los neurolépticos atípicos, como la clozapina, deben contemplarse como posible causa de colitis isquémica en pacientes que los reciban como tratamiento habitual, habiendo descartado previamente etiologías más frecuentes como situaciones de bajo gasto, o alteración de la vascularización intestinal. Ante esta sospecha se requiere retirada del fármaco para mejoría del cuadro clínico, que ha de realizarse de manera progresiva y asesorada por la unidad de psiquiatría por probable descompensación de patología psiquiátrica basal. La interrupción de la clozapina se ha relacionado con episodios de psicosis asociada a la abstinencia con rebote colinérgico, catatonia y síntomas de discontinuación serotoninérgicos.
CP-133. COLITIS POR CITOMEGALOVIRUS: UNA CAUSA RARA DE HEMORRAGIA DIGESTIVA BAJA GRAVE EN PACIENTES INMUNOCOMPETENTES
González Sánchez MH1, CELADA SENDINO M1, García Calonge M1, Carballo Folgoso L1, Argüelles Estrada P1, López Mourelle A1, Lamas Álvarez S1, González Parra AC2, Muiño Domónguez D1
1Servicio Aparato Digestivo. Hospital Universitario Central de Asturias, Oviedo. 2Servicio Aparato Digestivo. Hospitales Universitarios Virgen Macarena - Virgen del Rocío, Sevilla.
Palabras clave: colitis, rectorragia, hemorragia digestiva.
Introducción
La colitis por citomegalovirus (CMV) es una entidad poco frecuente en sujetos inmunocompetentes.
Caso clínico
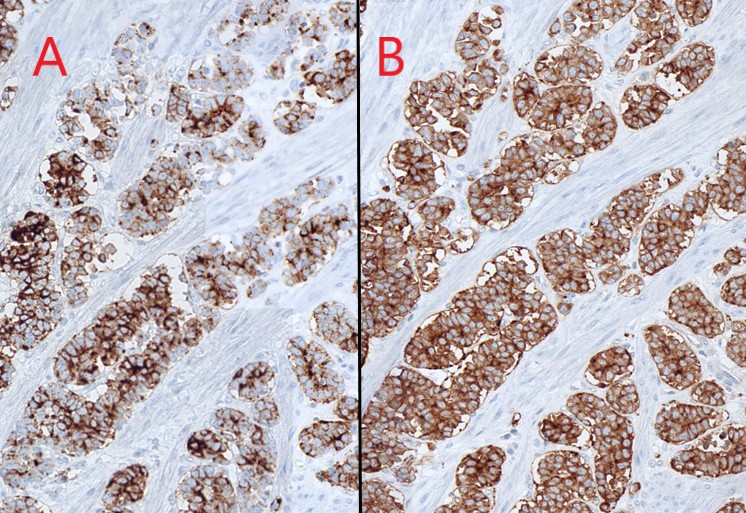
Varón de 85 años, hipertenso, diabético y anticoagulado por fibrilación auricular, que ingresa por presentar desde hace un mes diarrea con sangre. Como antecedentes digestivos, señalar cuadro de colitis isquémica en 2015 y otro episodio de colitis de etiología indeterminada en 2019. Analíticamente, destaca anemia severa de perfil ferropénico. El coprocultivo y la detección de Clostridium en heces resultaron negativos. Por rectorragias francas con repercusión hemodinámica, se realiza colonoscopia urgente, observando estenosis y ulceraciones grandes en sacabocados en un segmento de 5 centímetros de sigma distal, sin objetivar otro tipo de lesiones en el resto del colon e íleon (Fig.1). El estudio histológico y microbiológico muestra colitis activa severa ulcerada con presencia de CMV y cambios isquémicos secundarios, por lo que recibe ganciclovir intravenoso. Se solicita estudio de inmunodeficiencia y serologías, con único resultado positivo de IgG CMV. Además, valorado por Medicina Interna, se descarta inmunodeficiencia primaria. El paciente evoluciona favorablemente, por lo que es alta con tratamiento antiviral. Tras 4 semanas, se reevalúa endoscópicamente, observando mejoría de las lesiones ulcerativas, persistiendo pequeñas erosiones que se biopsian (Fig.2), con hallazgos histológicos reparativos y estudio inmunohistoquímico para CMV negativo.
Discusión
La colitis por CMV, aunque rara, es una entidad potencialmente grave que debe ser considerada en el diagnóstico diferencial de colitis en pacientes ancianos inmunocompetentes. Los hallazgos endoscópicos pueden ser indistinguibles de la enfermedad inflamatoria intestinal, por lo que el estudio histológico y microbiológico resulta fundamental.
CP-134. COLITIS SECUNDARIA A NIVOLUMAB EN PACIENTE DIAGNOSTICADO DE MELANOMA FUSOCELULAR
Rebertos Costela E, Frutos Muñoz L, Martín Marcuartu P, Ojeda Hinojosa M
Servicio Aparato Digestivo. Complejo Hospitalario de Jaén, Jaén.
Palabras clave: colitis, nivolumab, melanoma.
Introducción
El Nivolumab pertenece a un grupo de fármacos que se conocen como inhibidores de puntos de control inmunitario (inmune checkpoint inhibitor/ICIs); estos puntos se consideran proteínas elaboradas por células inmunitarias con el fin de evitar respuestas inmunes farragosas. Son producidas también por las células cancerígenas como mecanismo de evasión del sistema inmune. La unión de la proteína PD-L1 en células tumorales con PD-1 en linfocitos T evita la respuesta inmune. El Nivolumab tiene la capacidad de inhibir la unión de las proteínas punto de control inmunitario PD-1 y PD-L1. Entre sus efectos secundarios destacan los digestivos, como es el caso de la colitis, así como reacciones dermatológicas en forma de rash o prurito.
Caso clínico
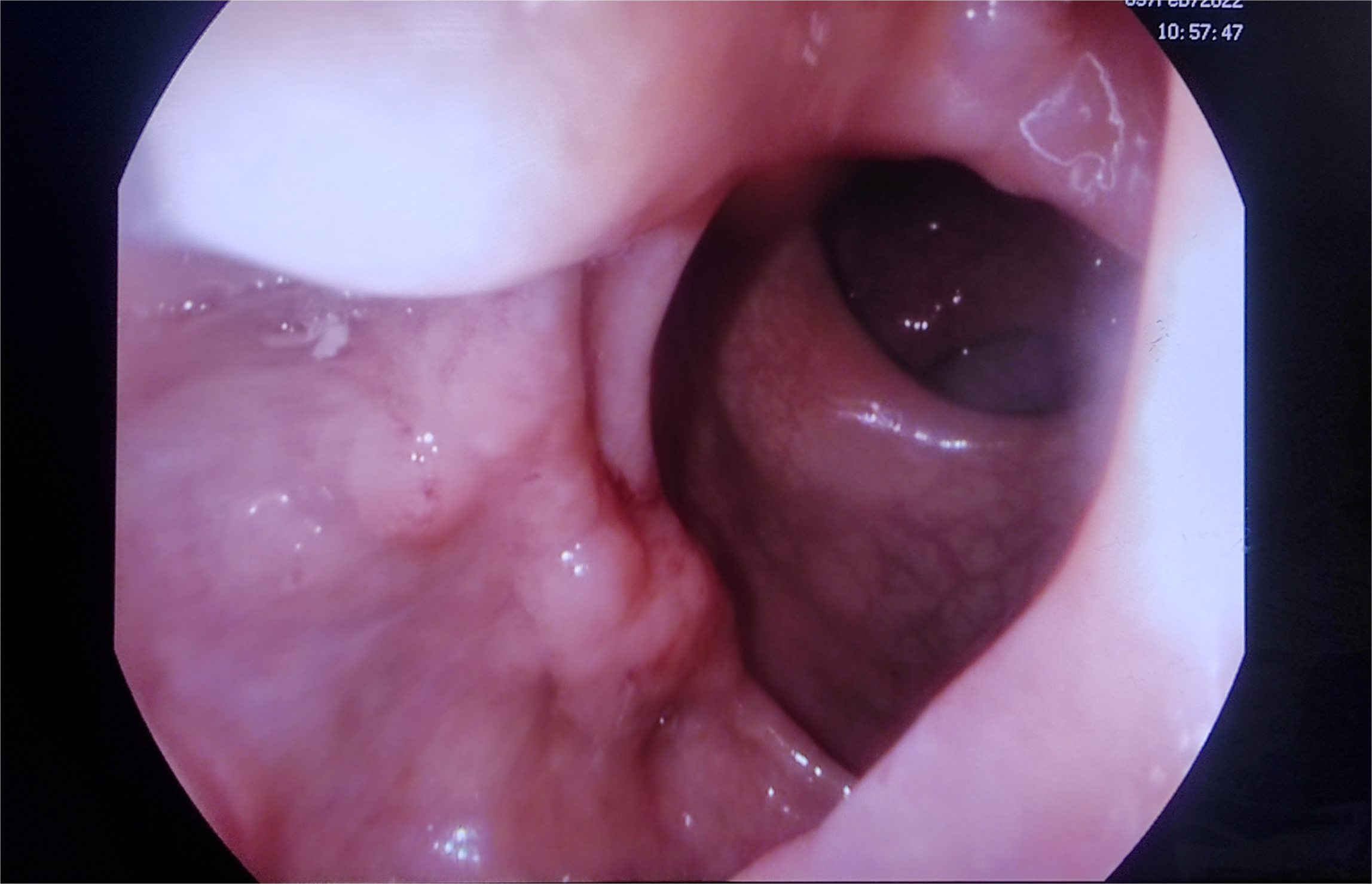
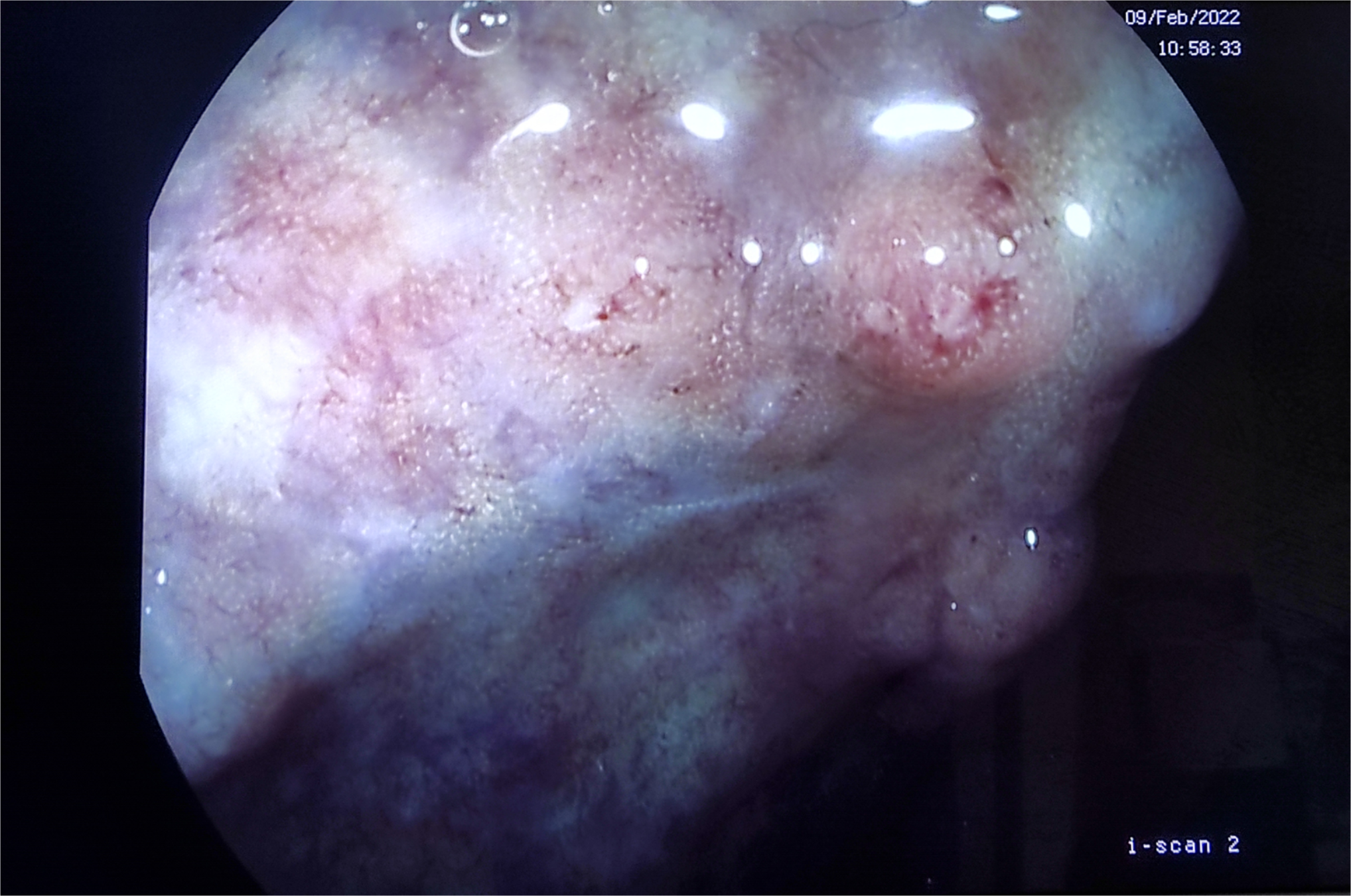
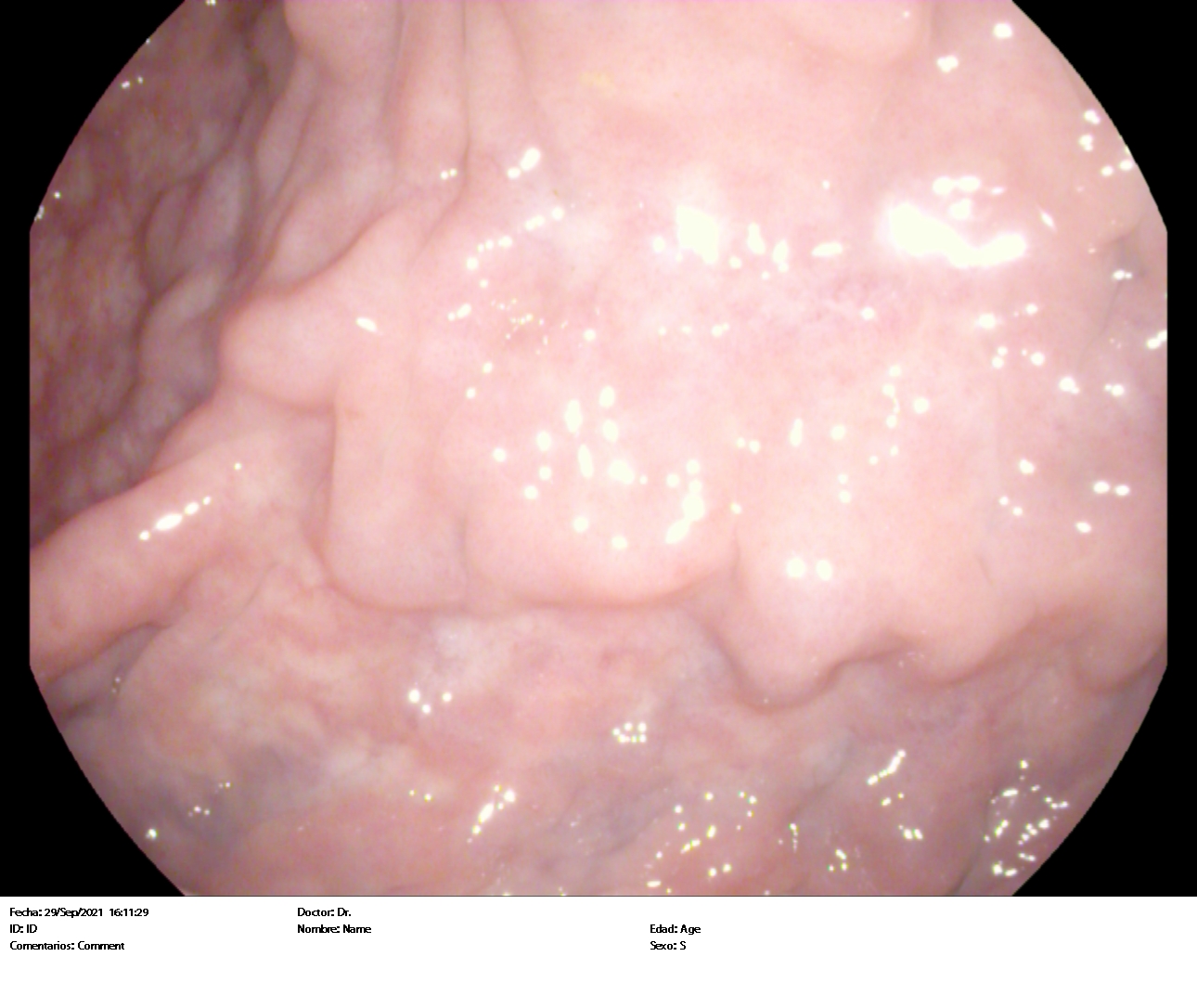
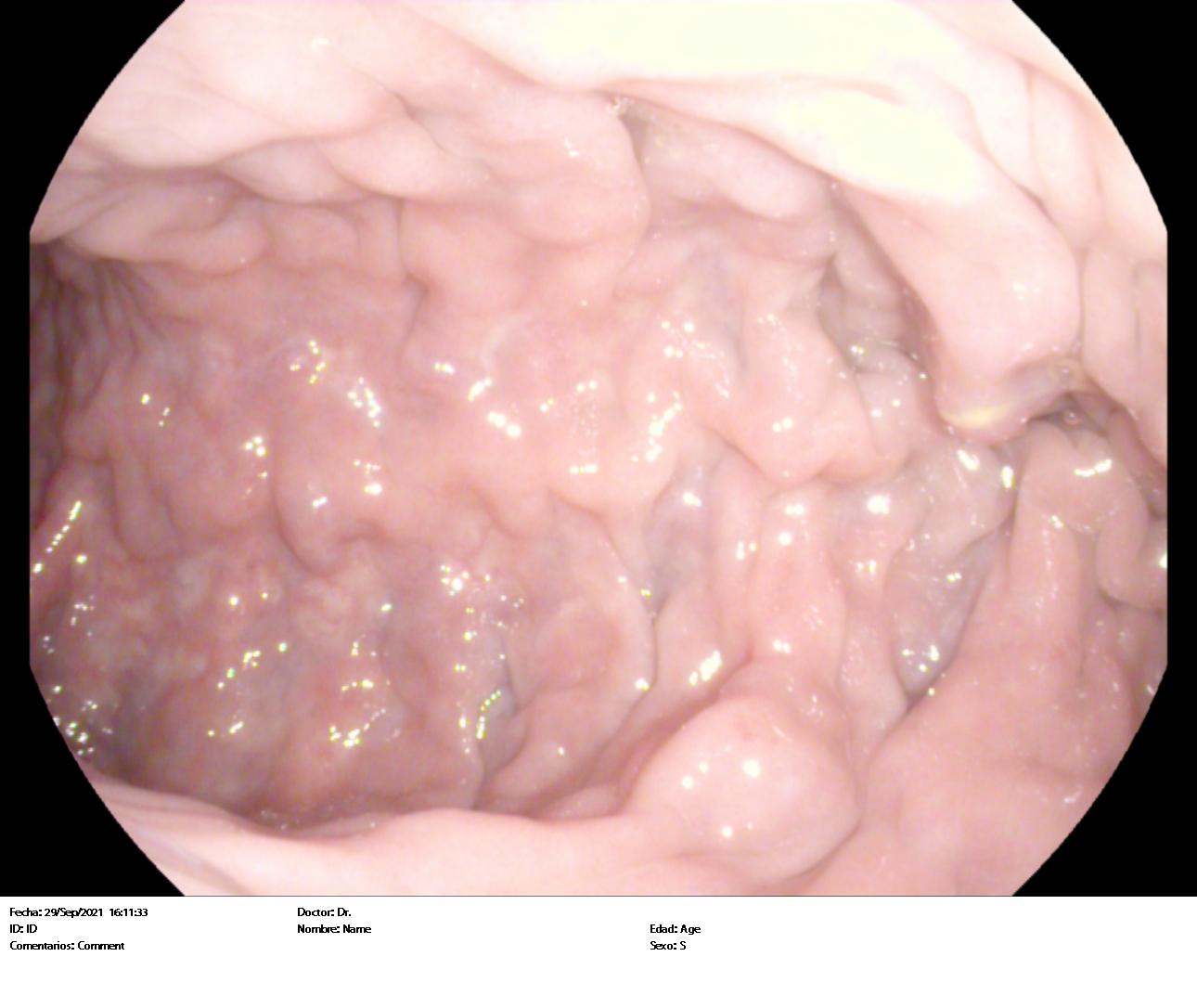
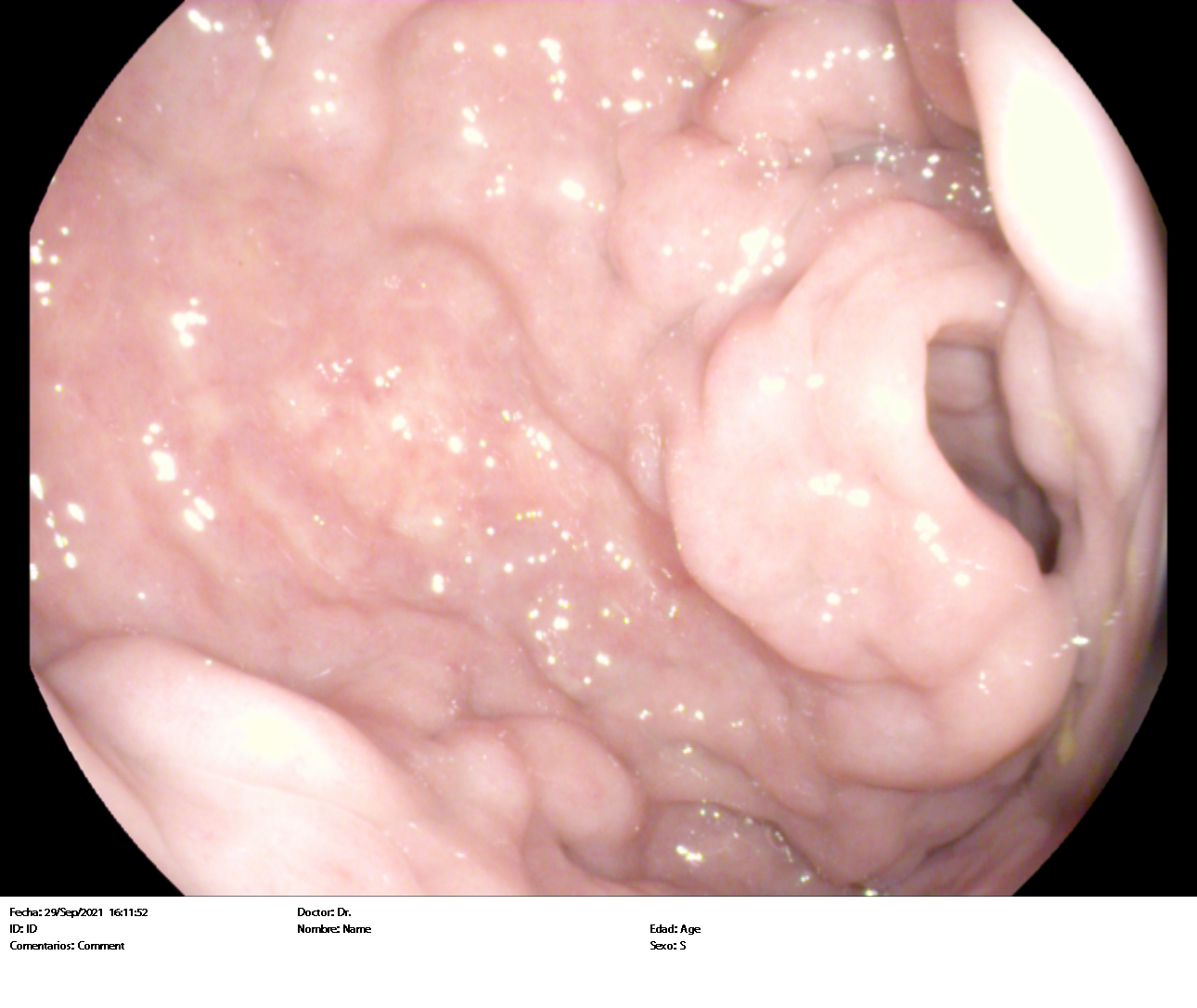
Hombre de 55 años de edad fumador. Diagnosticado en noviembre de 2021 de melanoma fusocelular interescapular estadio IIIC (T4a N+ M0). En febrero de 2022 participa en ensayo clínico, recibiendo tratamiento con Nivolumab 480mg/ 4 semanas. Tras recibir 4 ciclos de tratamiento sin incidencias, el paciente acude a urgencias en julio por aumento del número de deposiciones diarias con restos hemáticos. Se suspende tratamiento y comienza corticoterapia ambulatoria no satisfactoria que deriva en ingreso en Oncología por colitis inmunomediada pautándose metilprednisolona 1mg/kg durante 6 días. Se da de alta y se cita para colonoscopia en agosto que evidencia pancolitis crónica activa con grado 3 de actividad inflamatoria, objetivándose principalmente en colon descendente perdida de trama vascular, eritema, cierto edema y micro úlceras (Figura 1 y 2).
Discusión
Los ICIs han sido una revolución en el tratamiento de melanomas, cáncer renal o cáncer pulmonar no microcítico. Se piensa que la causa de muchos de los efectos adversos que producen estos fármacos se relaciona con la gran estimulación del sistema inmune que producen. Destacan por frecuencia las reacciones cutáneas en forma de rash o prurito. También hay que resaltar los efectos adversos gastrointestinales, teniendo la colitis una incidencia del 0,7% al 1,6%.
La colitis suele manifestarse con malestar abdominal y un aumento del número de deposiciones respecto a lo normal para el paciente. El diagnóstico definitivo se alcanza realizando una biopsia mediante colonoscopia. En las imágenes de colonoscopia se puede evidenciar eritema, pérdida del patrón vascular, edema etc.
El tratamiento de la colitis se basa en la corticoterapia y en la retirada del fármaco.
Como alternativa a los IPIs se puede valorar el uso de fármacos anti-TNF de los cuales se goza de más experiencia.
CP-135. CONSEJO GENÉTICO EN EL CÁNCER COLORRECTAL DE DEBUT PRECOZ
Agulleiro Beraza I1, Chica Cid T1, Reyes Díaz ML2, Rico Gutiérrez MC1, Pizarro Moreno A1, Gómez Izquierdo L3, Fernández García R1, Garzón Benavides M1, Giráldez Jiménez MD1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 2UGC Cirugía General y Digestiva. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 3UGC Anatomía Patológica. Complejo Hospitalario Regional Virgen del Rocío, Sevilla.
Palabras clave: genética, cáncer hereditario, cáncer colorrectal de debut precoz.
Introducción
El cáncer colorrectal (CCR) de debut precoz (diagnosticado <50 años) es sugestivo de predisposición hereditaria por lo que es crucial la realización de consejo genético. El síndrome de CCR hereditario más frecuente es el síndrome Lynch debido a mutaciones germinales en los genes del sistema reparador MMR. De forma reciente, la introducción de paneles de genes ha puesto de manifiesto la implicación de mutaciones en otros genes en el CCR hereditario. Nuestros objetivos fueron evaluar el porcentaje de pacientes con CCR de debut precoz que han recibido consejo genético en nuestro centro y analizar la frecuencia de mutaciones germinales en esta población.
Material y métodos
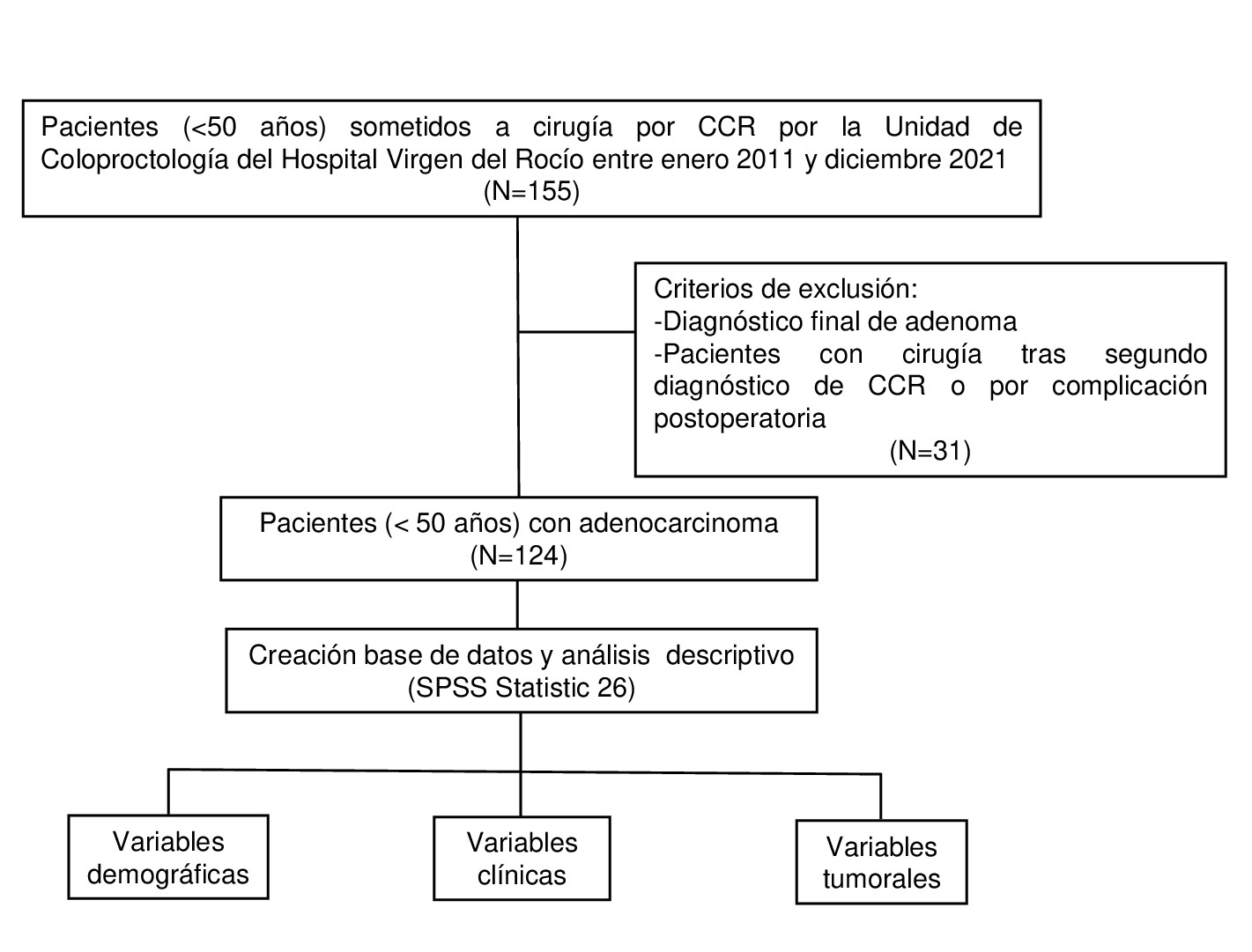
Se incluyeron los pacientes diagnosticados de CCR de debut precoz tratados quirúrgicamente por la Unidad de Coloproctología del Hospital Universitario Virgen del Rocío, entre enero 2011-diciembre 2021. Se recogieron los antecedentes familiares, resultados de los estudios moleculares tumorales y del estudio genético. Se realizó el análisis estadístico utilizando SPSS v26.0.
Resultados
Se incluyeron 124 pacientes. En 16 casos no se realizó ningún estudio molecular en el tumor para evaluar el sistema MMR. En el resto de casos se realizó inmunohistoquímica identificando un 17.75% de tumores con sistema reparador deficiente (pérdida MLH1/PMS2=8, pérdida MSH2/MSH6=8, pérdida MSH6=1, pérdida PMS2=1, perdida de las cuatro proteínas=1) (Fig1). Tres pacientes tenían diagnóstico previo de síndrome de Lynch. Del resto de pacientes, se derivó a consejo genético únicamente un 57%, identificando mutaciones germinales en 21 de ellos (7 en MLH1, 4 en MSH2, 2 en MSH6, 2 en APC, 2 en ATM, 1 en PALB2, 1 en PMS2 y 2 con mutaciones bialélicas en MUTYH) (Fig2). Cinco casos con diagnóstico de síndrome de Lynch presentaban sistema reparador normal. En el 86% de los pacientes en los que no se identificaron mutaciones se realizó el estudio mediante un panel de al menos 18 genes asociados a cáncer hereditario (Tabla1). Solo un 33% de los pacientes con mutaciones presentaba antecedentes familiares de primera generación de CCR y un 9.5% de tumores del espectro Lynch. La existencia de antecedentes familiares de primera generación de CCR fue significativamente más frecuente en los pacientes diagnosticados de síndrome de Lynch que en aquellos con cualquiera de los otros síndromes hereditarios (46.2 vs. 12.5% p<0.01) (Fig3).
CP-136. DIAGNÓSTICO ENDOSCÓPICO DEL MUCOCELE APENDICULAR.
Tenorio González E
Servicio Aparato Digestivo. Hospital Comarcal de la Axarquía, Vélez-Málaga.
Palabras clave: mucocele apendicular, moco.
Introducción
El mucocele apendicular es una entidad infrecuente (0,2–0,3% de todas las apendicectomías realizadas y del 8–10% de los tumores apendiculares)que consiste en la dilatación de la luz apendicular por secreción mucosa secundaria a la obstrucción de ésta, pudiendo convertirse en una masa quística con riesgo de perforación y diseminación del contenido de mucina (pseudomixoma peritoneal) en la cavidad abdominal, por lo que tiene siempre indicación quirúrgica.
Histológicamente, engloba tanto procesos benignos (hiperplasia focal o difusa de la mucosa apendicular y cistoadenoma) como malignos (cistoadenocarcinoma apendicular),y se puede presentar con una variedad de manifestaciones clínicas, siendo más frecuentemente un hallazgo incidental.
Caso clínico
Mujer de 81 años que acude a realización de colonoscopia tras episodio de diverticulitis aguda resuelta con antibioterapia.
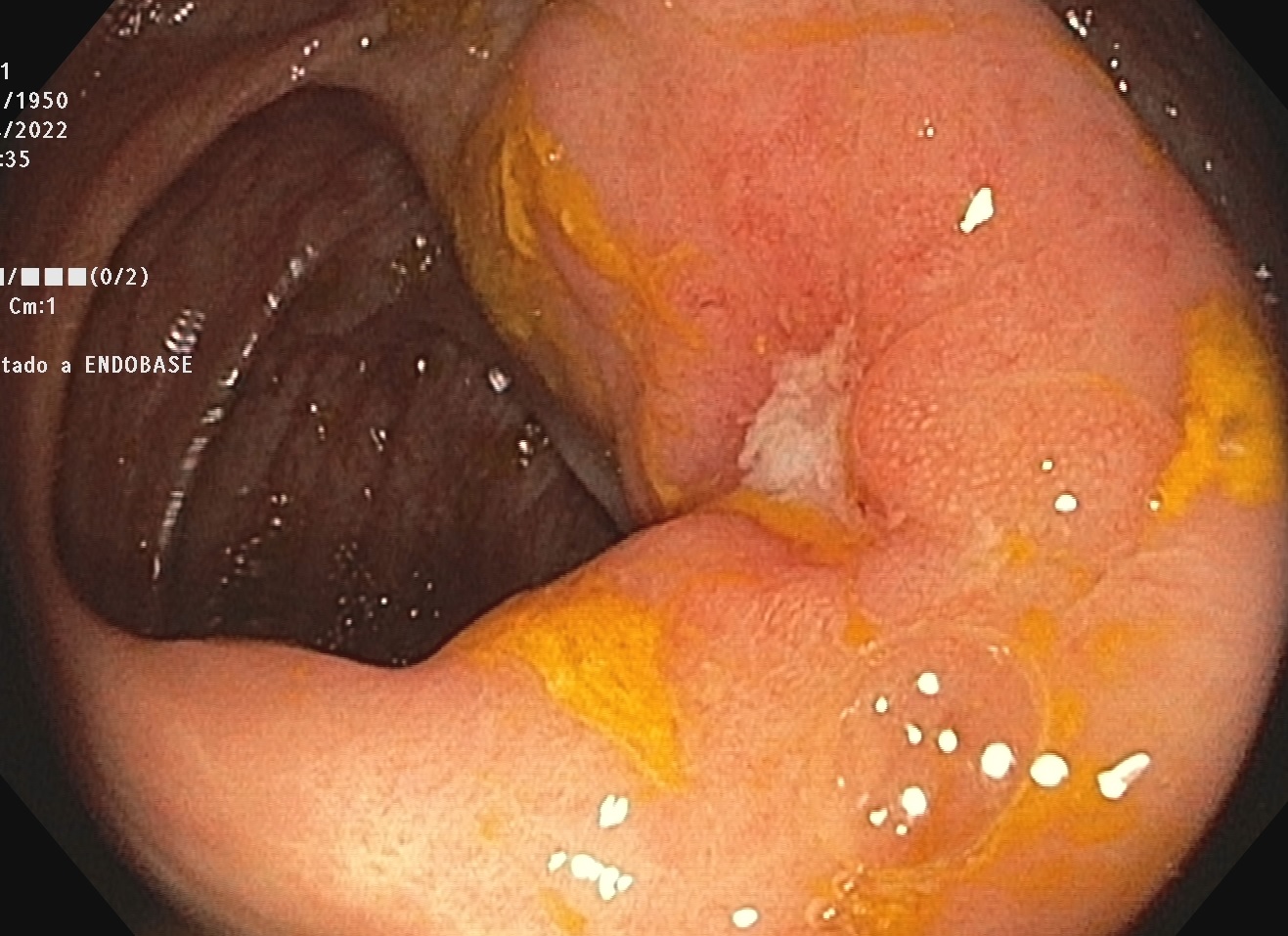
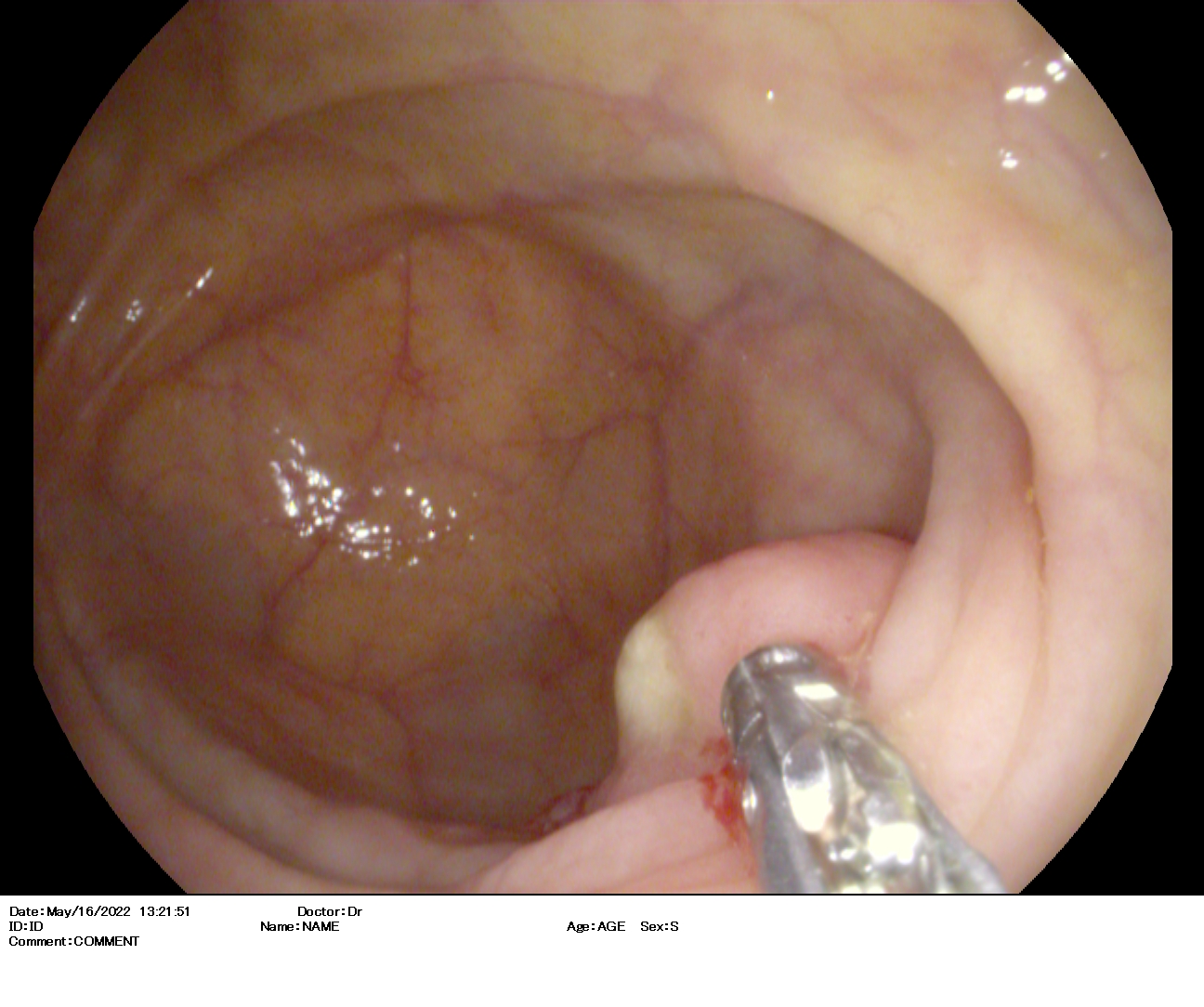
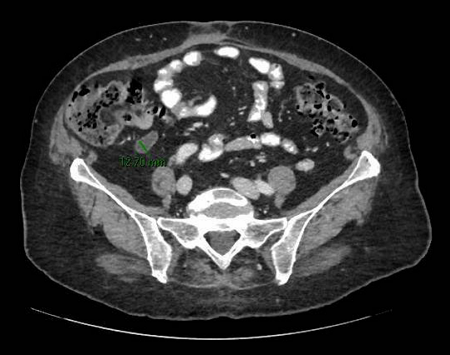
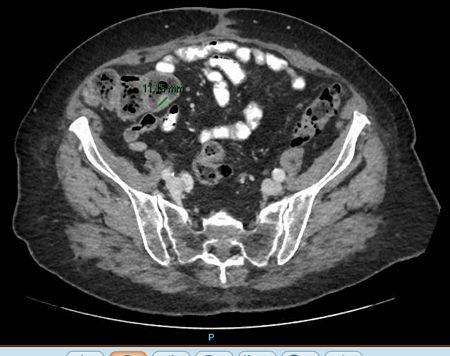
En fondo cecal se observa apéndice evertido, en cuyo vértice emana una sustancia amarillenta sugestiva de moco/pus. Se toman biopsias para descartar mucocele apendicular, y en el informe anatomopatológica se describen únicamente cambios glandulares hiperplásicos focales, pero ante la sospecha endoscópica se solicita TAC abdomen con contraste que evidencia dilatación quística del apéndice de 12mm,con captación en la base, sugestivo de mucocele apendicular.
Se realiza apendicectomía programada, con diagnóstico en pieza quirúrgica de neoplasia mucinosa apendicular de bajo grado con extensión extraapendicular al tejido adiposo de mucina y tejido neoplásico, así como margen quirúrgico afecto, por lo que se decide realización de hemicolectomía derecha, sin evidencia neoplásica ni afectación ganglionar (pT3),y sin precisar así tratamiento adyuvante.
CP-137. DIARREA SECUNDARIA A ESPIROQUETOSIS INTESTINAL, ¿DEBEMOS PENSAR EN ELLO?
Calvo Bernal MDM1, Moreno Moraleda I1, Sánchez Moreno S1, Gil Belmonte MJ2
1UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería. 2UGC Anatomía Patológica. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: diarrea crónica, espiroquetosis, brachyspira.
Introducción
La espiroquetosis intestinal (EI) se define como una colonización de la mucosa colónica por espiroquetas. Es un hallazgo muy poco frecuente en nuestro medio, pudiendo ser superior al 40% en hombres que practican sexo con hombres y pacientes VIH positivos.
Caso clínico
Paciente de 57 años derivada a consultas externas para estudio de diarrea (5-6 deposiciones blandas sin productos patológicos) de un año de evolución. Como antecedentes destacan HTA y dislipemia. Viuda, niega relaciones sexuales en los últimos 5 años.
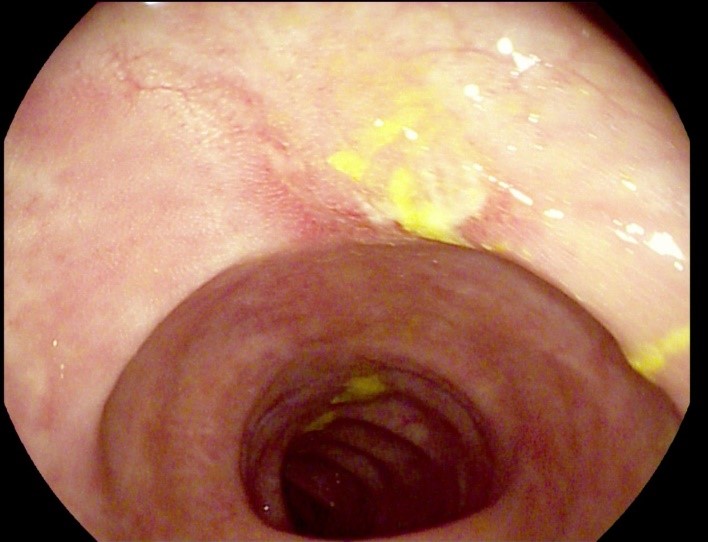
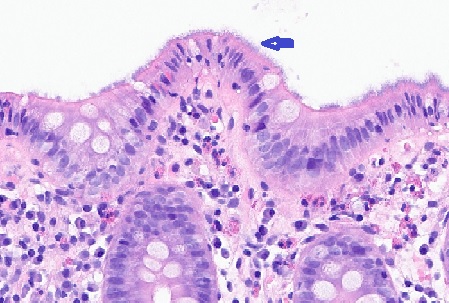
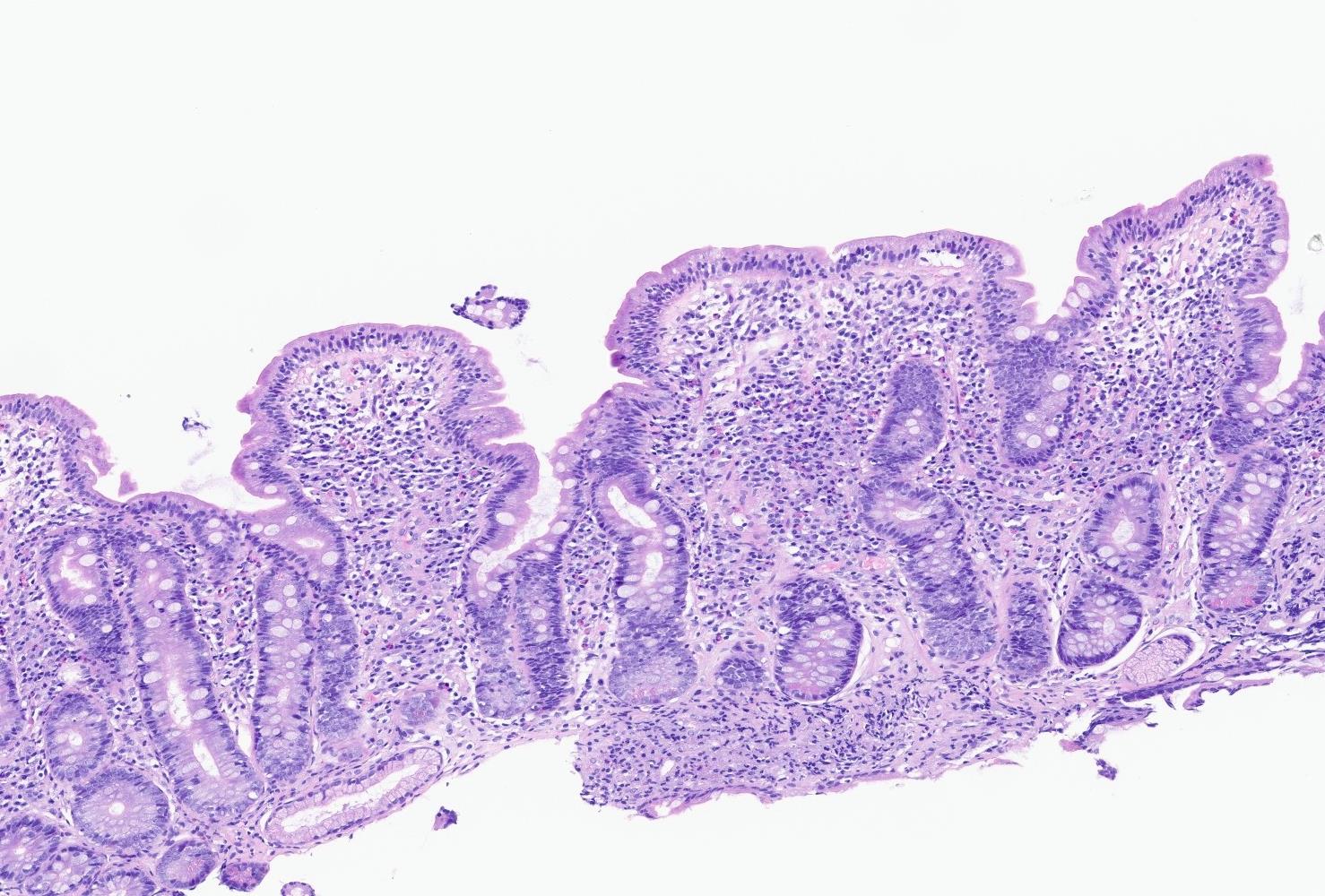
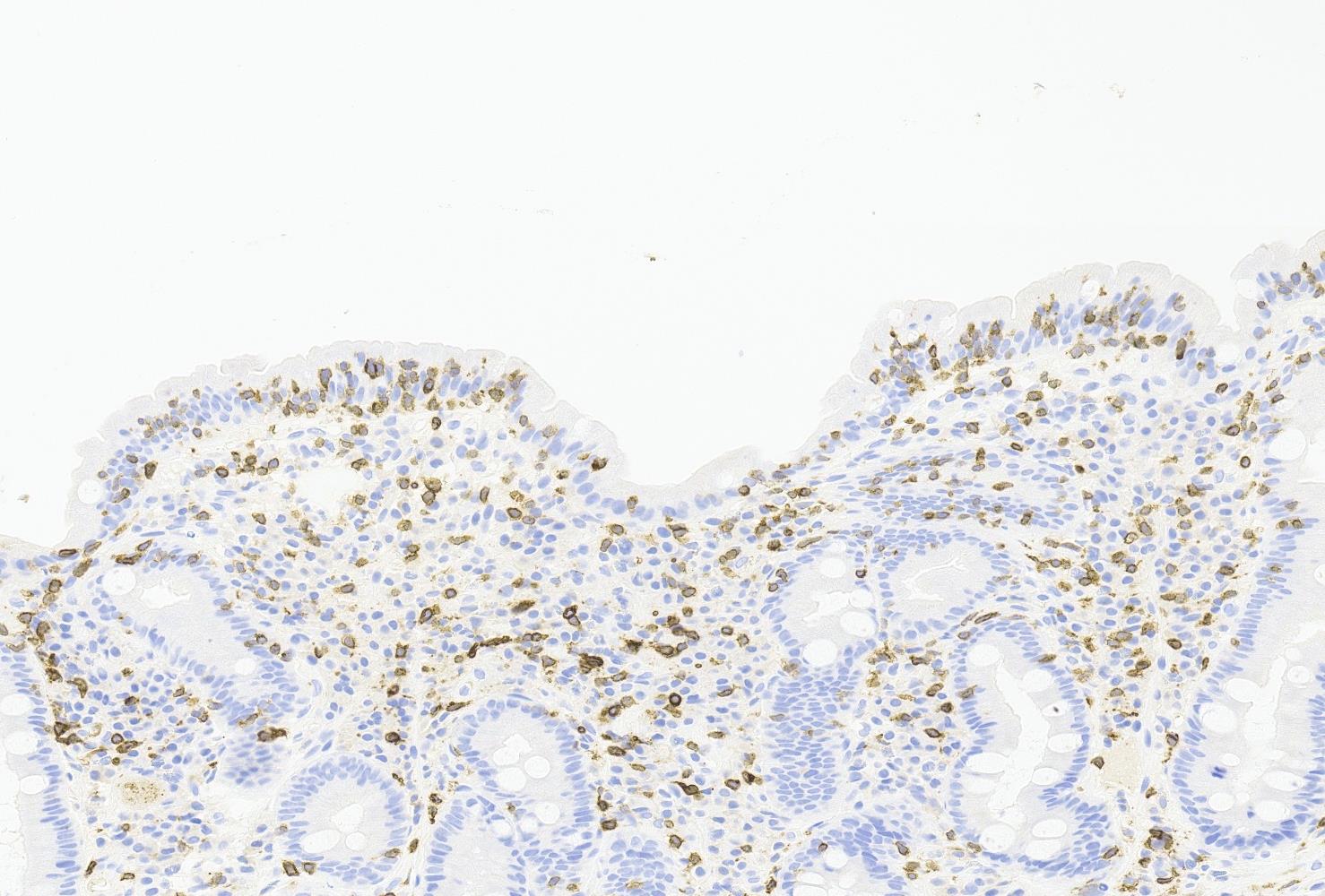
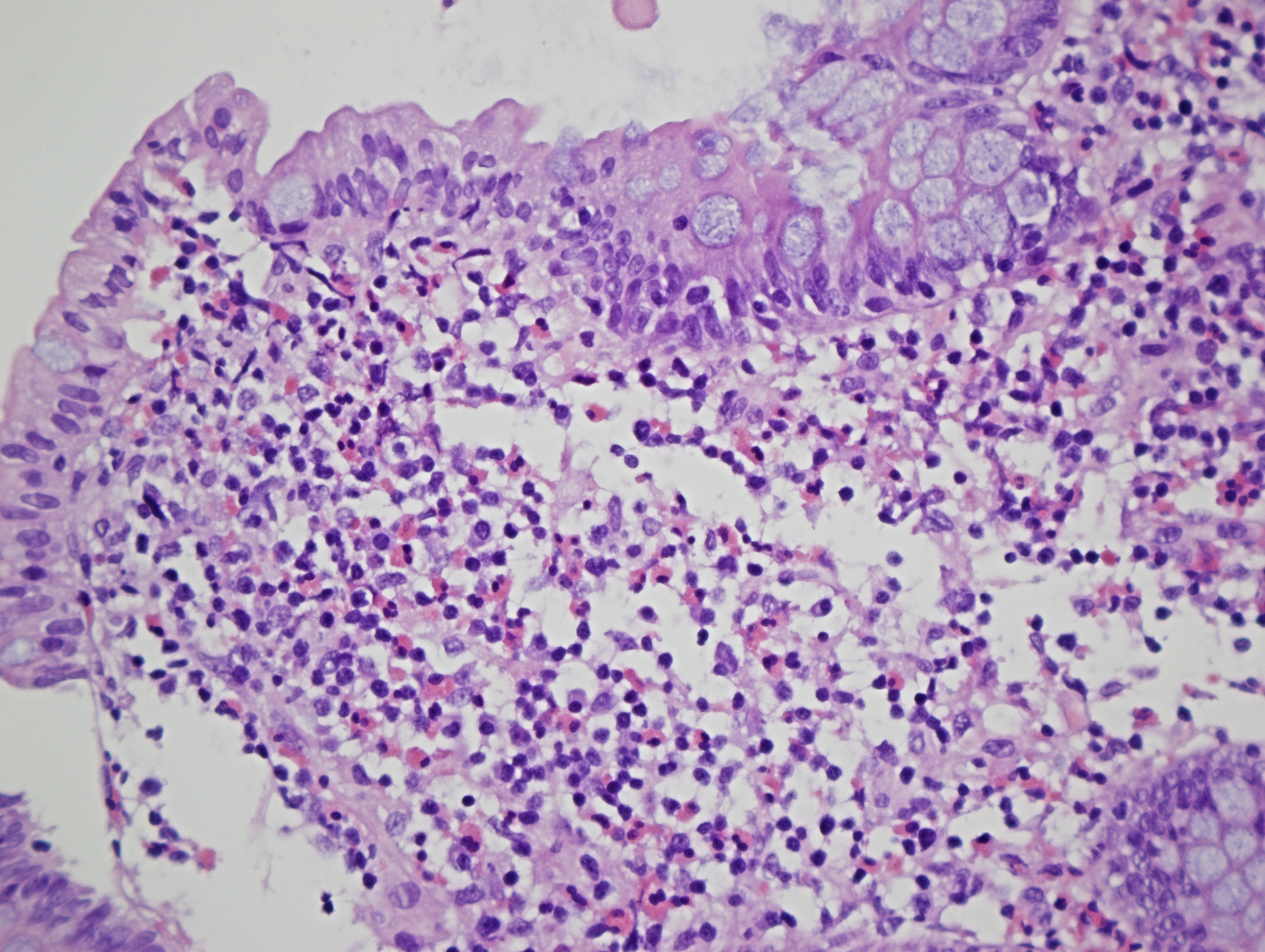
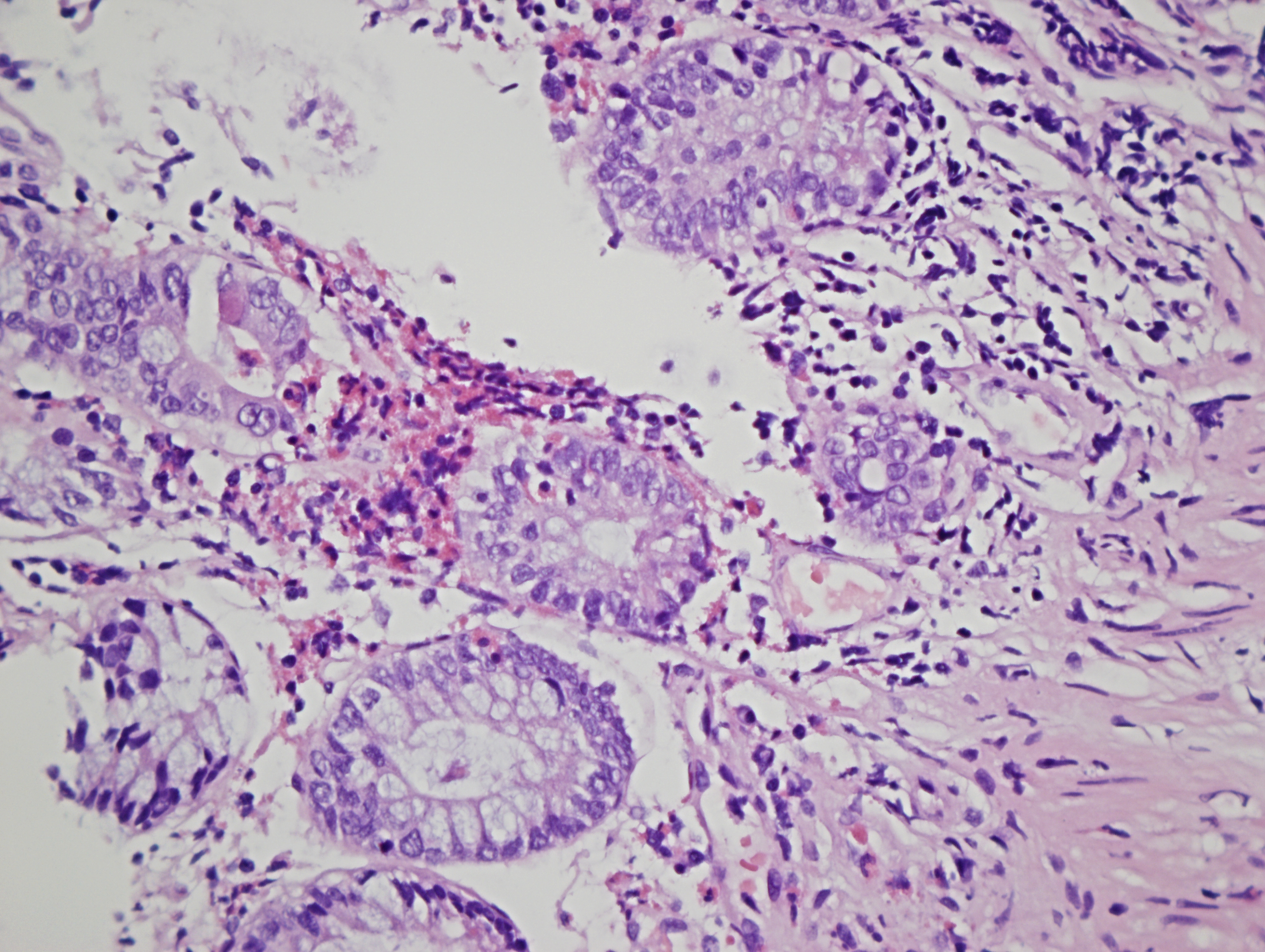
Se realiza estudio con analítica en la que destaca leve ferropenia (IST 12%) sin anemia (Hb 12.4 g/dl) y análisis de heces con coprocultivo, estudio de parásitos y Cl. Difficile negativo, y calprotectina elevada (303 µg/g). Posteriormente se realiza colonoscopia en la que se evidencian múltiples aftas en colon derecho (figura 1) que se biopsian, objetivando una colitis crónica activa de etiología infecciosa con presencia de microorganismos filamentosos compatible con espiroquetosis intestinal (figura 2 y 3).
La paciente no había presentado lesiones cutáneas ni mucosas previamente. Serología con Ac Treponema Pallidum, VIH, HBsAg y antiVHC negativas. Se solicita coprocultivo con incubación lenta que resulta positivo para la especie Brachyspira por lo que se trata con metronidazol 500mg cada 8h durante 10 días consiguiendo remisión sintomática.
Discusión
La EI se define como una colonización de la mucosa colónica por espiroquetas con una prevalencia de 0.7% en nuestro medio, siendo más elevada en hombres que practican sexo con hombres, pacientes portadores del VIH e infección gonocócica, países subdesarrollados y pacientes con fallo multiorgánico. Las especies Brachyspira aalborgi y Brachyspira pilosiloci se han identificado como los agentes patogénicos más frecuentemente asociados a colonización intestinal.
La EI puede afectar a la totalidad del colon, al apéndice e incluso íleon terminal. Puede ser asintomática o presentar clínica de dolor abdominal (46%), diarrea (51%), alternancia de hábito intestinal (13%) y rectorragia.
El diagnóstico se realiza mediante identificación del microrganismo en el examen histológico. Se debe realizar diagnóstico diferencial con la infección por Treponema Pallidum, agente etiológico de la sífilis, ya que las técnicas de inmunohistoquímica no diferencian entre ambos tipos de espiroquetas al existir reacción cruzada.
Se recomienda reservar el tratamiento antibiótico para aquellos pacientes con síntomas persistentes sin otra patología demostrable y tomar biopsia posteriormente para confirmar la erradicación.
Este caso ilustra una causa extraordinariamente rara de diarrea crónica, que debe ser considerada entre el diagnóstico diferencial de esta entidad, especialmente en pacientes con factores de riesgo predisponentes.
CP-138. DIVERTICULITIS DE INTESTINO DELGADO COMO CAUSA INFRECUENTE DE DOLOR ABDOMINAL.
Sánchez Arenas R, Cadena Herrera ML, Maldonado Pérez MB
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: diverticulitis, duodeno, dolor abdominal..
Introducción
Los divertículos pueden estar presentes en cualquier localización del tracto gastrointestinal, si bien la localización más frecuente es la colónica. La diverticulosis de intestino delgado (ID) es menos frecuente, se estima su presencia en el 2-4% de la población general. La localización en duodeno, en segunda y tercera porción, es cinco veces más frecuente que en el resto de tramos de ID, diagnosticándose entre la 3º y la 7º década de vida. Son frecuentemente asintomáticos y descubiertos incidentalmente, aunque pueden presentarse en forma de dolor abdominal, hemorragia, perforación, obstrucción intestinal o malabsorción, siendo la diverticulitis una complicación infrecuente debido al tamaño de los divertículos, el mejor flujo intraluminal y contenido relativamente estéril de duodeno.
Caso clínico
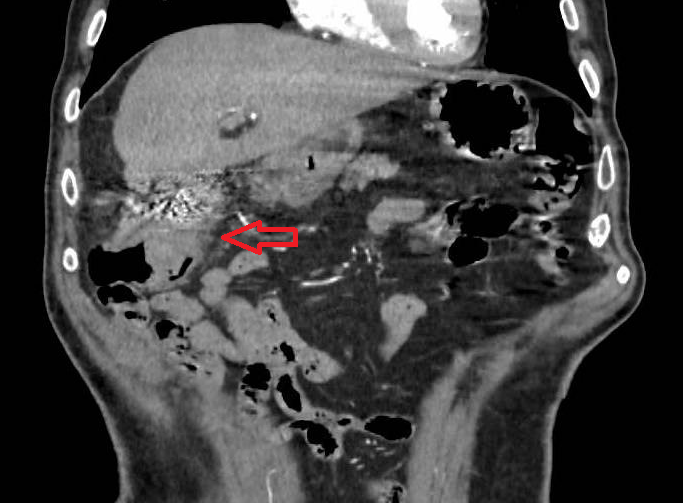
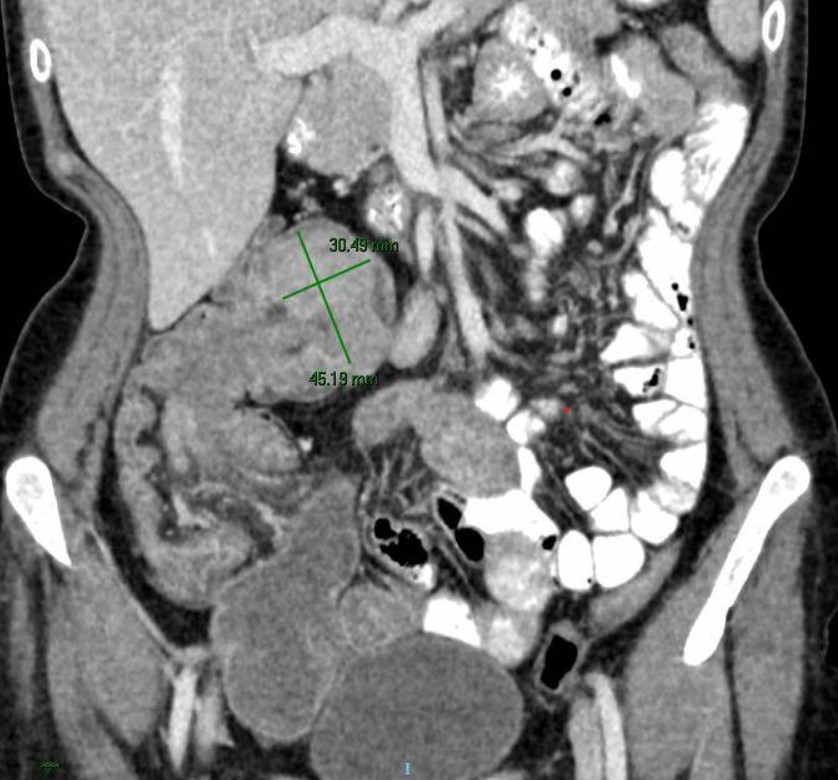
Mujer de 54 años con Diabetes Mellitus tipo 2, Miocardiopatía dilatada no isquémica y portadora de Enfermedad de Steinert. Acude a Urgencias por cuadro de dos meses de evolución de dolor abdominal generalizado tipo cólico asociado a vómitos esporádicos. Analíticamente destaca leucocitosis con neutrofilia. Se realiza TC de abdomen urgente con contraste que visualiza un divertículo entre 2 y 3 porción duodenal moderadamente dilatado, con engrosamiento parietal y cambios inflamatorios periverticulares. Otra imagen similar en la unión duodeno-yeyunal, engrosamiento de asas de yeyuno proximal y algún divertículo aislado en asas de íleon distal. Se solicita enterorresonancia reglada que confirma finalmente el diagnóstico de diverticulitis de intestino delgado, sin complicaciones asociadas. Se inicia antibioterapia con amoxicilina/clavulánico con evolución favorable, controlándose el dolor y normalizándose los reactantes de fase aguda. Se deriva al alta con antibioterapia oral, pendiente de nueva enterorresonancia de control.
Figura 1
TC abdomen y pelvis coronal con contraste dónde se observa gran divertículo duodenal el cual presenta un engrosamiento e hiperrealce mural.
Discusión
La diverticulitis de intestino delgado es una causa infrecuente de dolor abdominal, rara vez sospechada, cuyo diagnóstico se basa en las pruebas de imagen. Su tratamiento inicial se basa en antibioterapia, siendo necesario el drenaje percutáneo o la intervención quirúrgica en los casos de diverticulitis complicada con absceso, perforación, sangrado o fístula.
CP-139. DIVERTÍCULO DE MECKEL: MÁS ALLÁ DE UNA GAMMAGRAFÍA
Calderón Chamizo M, Ternero Fonseca J, Quirós Rivero P, Naranjo Pérez A, Correia Varela Almeida A, Casado Monje PG
Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Juan Ramón Jiménez, Huelva.
Palabras clave: hemorragia, divertículo, cápsula..
Introducción
El divertículo de Meckel es la anomalía congénita más común del tracto gastrointestinal. Es infrecuente detectar su presencia ya que a menudo son asintomáticos, sobre todo en el adulto. Cuando es sintomático, puede presentarse en forma de dolor abdominal, de características inespecíficas, o en forma de hemorragia digestiva baja, cursando de forma crónica e insidiosa o aguda y masiva, siendo las transfusiones poco frecuentes.
Caso clínico
Varón de 16 años, sin ningún antecedente de interés, que acude por deposiciones con sangre roja de 4 días de evolución. No fiebre ni ninguna otra sintomatología acompañante; no lo relaciona con la ingesta, con viajes, ni tiene contactos con la misma clínica. Se solicita analítica y radiografía de abdomen destacando una hemoglobina de 5.8 en hemograma como único dato significativo. A la exploración, el tacto rectal muestra hematoquecia, no se palpan hemorroides. Se transfunden 4 concentrados de hematíes y se decide ingreso.
Durante su estancia hospitalaria precisó transfusión de 5 concentrados de hematíes más por anemia severa sintomática, presentando nuevo episodio de hematoquecia con repercusión hemodinámica que se autolimitó.
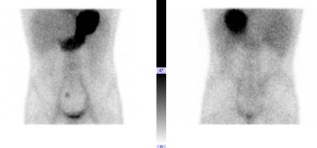
No se objetivaron lesiones potencialmente sangrantes en pruebas endoscópicas convencionales y angioTC abdominal. Se administró la cápsula endoscópica para evaluar lesiones en intestino delgado, objetivándose un divertículo de Meckel en íleon proximal sin datos de hemostasia ni sangrado actual y sangre digerida en colon. Se confirmó dicho diagnóstico mediante gammagrafía con Tc99m pertecnetato (foco de captación con mucosa gástrica ectópica en divertículo de Meckel).
Ante el diagnóstico de hemorragia digestiva baja manifestada como hematoquecia en probable relación con divertículo de Meckel con repercusión hematimétrica y hemodinámica y alto requerimiento transfusional, fue valorado por cirugía para intervención quirúrgica programada.
Discusión
El divertículo de Meckel suele ser clínicamente asintomático o presentar una variedad de manifestaciones clínicas: aquellos que contienen mucosa gástrica ectópica generalmente se asocian con sangrado. No es la mucosa o tejido ectópico del divertículo la que sangra sino la secreción de ácido por parte de esta mucosa gástrica ectópica dentro del divertículo la que causa ulceración y sangrado de la mucosa de intestino delgado adyacente al mismo.
En cuanto al diagnóstico, si la sospecha es muy alta, se debe realizar una gammagrafía con Tc99m pertecnetato. Sin embargo, la cápsula endoscópica para el diagnóstico de hemorragia gastrointestinal de origen incierto puede describir la presencia de divertículos de Meckel normales, ulcerados o sangrantes.
CP-140. ENTEROPATÍA INDUCIDA POR OLMESARTÁN
Sánchez Moreno S1, López González J1, Pinochet Almonacid S2
1Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería. 2Servicio Anatomía Patológica. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: diarrea crónica, enteropatía, olmesartán.
Introducción
Olmesartán es un inhibidor del receptor de la angiotensina II empleado como antihipertensivo que se ha relacionado con la aparición de enteropatía y diarrea. Por ello, y aunque es un factor etiológico infrecuente, debemos tenerlo presente para realizar un adecuado diagnóstico diferencial ante un paciente con diarrea crónica de origen no establecido.
Caso clínico
Varón de 43 años con antecedente de hipertensión y enfermedad renal crónica, en tratamiento con Olmesartán/amlodipino y bisoprolol, que ingresa en Digestivo por síndrome diarreico de hasta 20 deposiciones diarias líquidas sin productos patológicos, de dos meses de evolución, asociado a pérdida ponderal.
Analíticamente, destacaba reagudización de fallo renal crónico, ausencia de reactantes de fase aguda y calprotectina fecal en torno a 1200µg/g. Se realizaron cultivos de bacterias, parásitos y toxina de C. difficile, resultando negativos.
Se solicitó colonoscopia con toma de biopsias, siendo el colon macroscópicamente normal y sin alteraciones histológicas. Se realizaron así mismo TAC abdominal y enteroRM, que no evidenciaron causa etiológica.
Ante la ausencia de hallazgos se decidió retirada de Olmesartán y realización de endoscopia digestiva alta con toma de biopsias duodenales, mostrando la histología presencia de linfocitosis intraepitelial con hiperplasia de criptas y atrofia vellositaria con depósito de colágeno subepitelial, lo cual en el contexto clínico del paciente sugería enteropatía farmacológica. 72 horas tras la suspensión del olmesartán el paciente presentó gran mejoría clínica, siendo revisado a los 3 meses en consulta, encontrándose totalmente asintomático.
Figura 1
Biopsia duodenal con atrofia vellositaria variable e hiperplasia de criptas. (Hematoxilina-eosina; 10x).
Figura 2
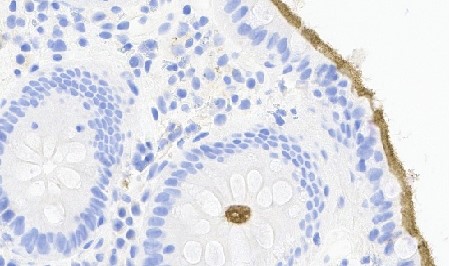
Tinción inmunohistoquímica CD3 que muestra linfocitosis intraepitelial de más de 30 linfocitos por 100 enterocitos (CD3; 20x).
Discusión
La enteropatía por olmesartán es infrecuente y puede ser difícil reconocerla dado que sus manifestaciones clínicas e histológicas son similares a otras entidades clínicas como son la enfermedad celíaca y la enteropatía autoinmune.
La mayoría de pacientes que sufren enteropatía por olmesartán cursan con un cuadro clínico consistente en diarrea crónica acuosa sin productos patológicos con pérdida de peso asociada, aunque también puede aparecer astenia, náuseas, vómitos y dolor abdominal.
Los hallazgos endoscópicos típicos suelen ser la edematización y ulceración de la mucosa del intestino delgado con patrón nodular y atrofia vellositaria. No obstante, no es infrecuente la ausencia de alteraciones endoscópicas en esta enfermedad, lo que puede dificultar el diagnóstico diferencial del síndrome diarreico en cuestión y pone de manifiesto la importancia de la toma de biopsias para esclarecer el diagnóstico.
CP-141. EVOLUCION E INCREMENTO DEL NUMERO DE CASOS NUEVOS DE CANCER COLORECTAL EN EL AREA SANITARIA BAHIA LA JANDA. PERIODO 2013-2021.
Rivas Rivas M1, Carnerero Rodriguez JA1, Camacho Montaño L1, De La Vega Olias C2
1UGC Aparato Digestivo. Hospital de Alta Resolución Especializada La Janda, Vejer de la Frontera. 2UGC Cirugía General. Hospital de Especialidades de Puerto Real, Puerto Real.
Palabras clave: cáncer colon, cáncer recto, incidencia, .
Introducción
Andalucía es la comunidad autónoma que registra la mayor incidencia en cáncer de colon de España. La incidencia de cáncer es mayor en Huelva, Sevilla y Cádiz, tanto en hombres como en mujeres. El objetivo de este estudio ha sido conocer el número de casos nuevos por año diagnosticados de cáncer colorectal desde el periodo de inicio de la consulta de cáncer de colon que asiste al área sanitaria que abarca el Hospital Universitario de Puerto Real y Hospital alta Resolución La Janda (Puerto de Santa María, Rota, Puerto Real, Chiclana, Conil, Vejer, Barbate, Medina Sidonia, Benalup, Alcalá de los gazules y Paterna de Rivera), periodo 2013-2021 y realizar comparativa con la incidencia nacional y regional.
Material y métodos
Estudio descriptivo, retrospectivo, de los casos de cáncer colorectal diagnosticados en el Hospital Universitario de Puerto Real- La Janda en el periodo tiempo de enero de 2013 y diciembre de 2021. Todos los casos tenían un diagnóstico histológico y todos los casos habían sido registrados en el proceso asistencial integrado de cáncer de colon y recto.
Hemos evaluado el número de sucesos y lo hemos dividido por la población en riesgo de experimentar tal evento durante el periodo estudiado, censo poblacional de nuestra área sanitaria que abarca aproximadamente 329.0000 habitantes. Posteriormente lo comparamos con las estimaciones publicadas a nivel nacional y regional.
Resultados
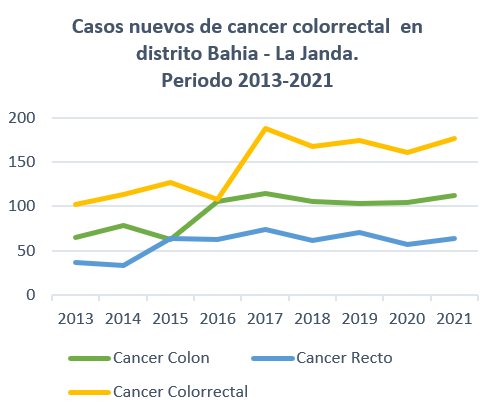
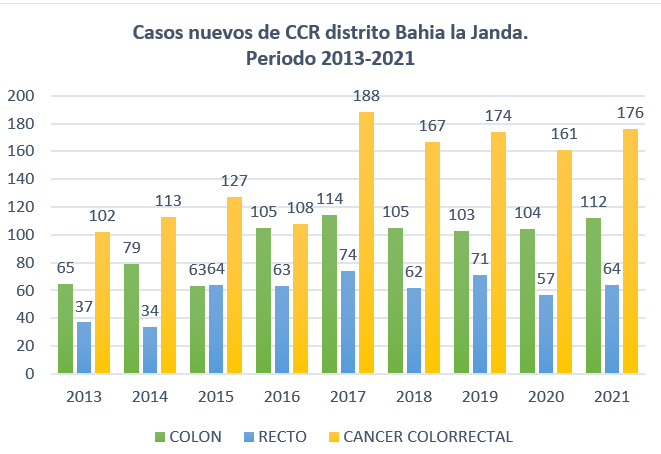
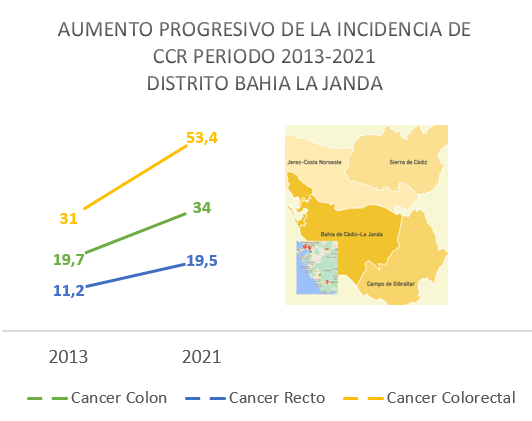
En el periodo de tiempo 2013-2021 se diagnosticaron un total de 1.316 pacientes 64.5% (850) cáncer de colon (65+79+63+105+114+105+103+104+112) y 35,5% (466) cáncer de recto (37+34+64+63+74+62+71+57+64). Lo que supone una incidencia para el cáncer de colon de 19.7/105 , 24.1/105, 19.4/105 , 31.9/105 , 34.6/105, 31.9/105, 31.3/105 , 30.6/105 y 34/105 habitantes respectivamente y una incidencia para el cáncer de recto de 11.24/105 , 10.32/105 , 19.45/105, 19.14/105 , 22.4/105 , 20.3/105 , 21.5/105 , 17.3/105 y 19.45/105 respectivamente.
Conclusiones
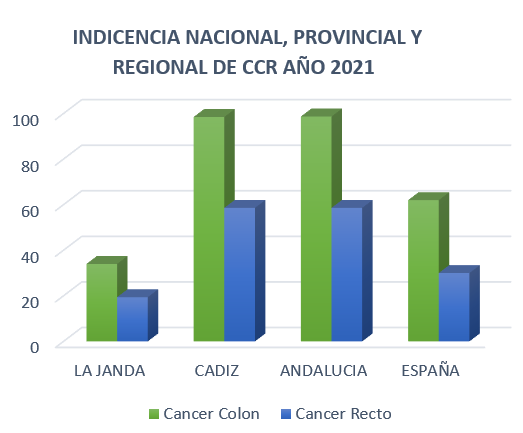
La incidencia del CCR en Andalucía y Cádiz es alta, el hospital de Puerto Real- La Janda incrementa cada año el número de casos nuevos de cáncer colorrectal registrados. En el periodo de tiempo 2013-2021 existe un 72% más de tumores diagnosticados. La incidencia en la provincia de Cádiz es mayor que en área bahía La Janda, tenemos que tener en cuenta algunos factores para interpretar de manera crítica y correcta los resultados obtenidos tales como la alta actividad de medicina privada en la provincia de Cádiz, los centros concertados que trabajan en colaboración con el sistema sanitario andaluz, la creación irregular de unidades de alto riesgo de cáncer colorrectal y la población con cáncer de colon que no se diagnostica.
Es fundamental que seamos conscientes de la necesidad de una atención coordinada y multidisciplinaria en la población andaluza con riesgo de desarrollar cáncer colorrectal.
CP-142. FASCITIS NECROTIZANTE COMO COMPLICACIÓN INFRECUENTE DE NEOPLASIA DE COLON
Alía Verdejo T, Viejo Almanzor A, Sotomayor Orellana MA, Manrique Gil MJ, Macías Rodriguez MA
Servicio Aparato Digestivo. Hospital Puerta del Mar, Cádiz.
Palabras clave: fascitis, neoplasia, colon.
Introducción
La fascitis necrotizante es una destrucción progresiva de la fascia muscular y del tejido circundante. Como principales factores de riesgo están descritos la cirugía reciente, traumatismos, neoplasias intra-abdominales y la obesidad.
Las neoplasias colorrectales constituyen en torno al 30% de las perforaciones intestinales, pudiendo producirse por penetración directa del tumor o por obstrucción intestinal completa que produzca isquemia y necrosis.
Caso clínico
Mujer de 68 años diagnosticada de adenocarcinoma de ciego pobremente diferenciado, pendiente de hemicolectomía derecha, que acude a Urgencias por dolor intenso en glúteo izquierdo. Además, refería dolor abdominal de predominio en hipogastrio y fosa iliaca derecha (FID) asociado a rectorragia y fiebre de 38ºC de 3 días de evolución.
A la inspección destacaba mal estado general, deshidratación moderada, hipoperfusión periférica, sudoración y palidez mucocutánea. Hipotensión (80/55 mmHg) y taquicardia de 110 lpm.
A la exploración abdominal presentaba dolor difuso a la palpación con mayor intensidad en FID e hipogastrio. Además, a nivel de cabeza femoral izquierda se apreciaba un pequeño hematoma con crepitación e importante dolor a la palpación.
Se realizó radiografía de abdomen (FIGURA 1) objetivándose zona enfisematosa a nivel de glúteo izquierdo.
Ante la sospecha clínica de complicación intra-abdominal y posible fascitis necrotizante en MII se realizó TAC abdominal evidenciándose neumoperitoneo en la grasa pélvica perivesical, cistitis enfisematosa y extenso enfisema en musculatura glútea izquierda y de muslo izquierdo secundarios a perforación de la neoplasia cecal ya conocida (FIGURAS 2 a 5).
La paciente fue intervenida de urgencia, evidenciándose peritonitis fecaloidea en cuadrante inferior derecho, y realizándose hemicolectomía derecha con ileostomía junto con fasciotomía y desbridamiento de MII.
Durante el postoperatorio inmediato la paciente presentó un empeoramiento progresivo con desarrollo de fracaso multiorgánico refractario que produjo su éxitus.
Figura 2
Corte axial de TC de abdomen en el que se aprecia perforación colónica (asterisco amarillo) y enfisema en glúteo izquierdo (flecha blanca).
Figura 3
Corte axial de TC de abdomen en el que se aprecia presencia de aire en pared vesical (asterisco amarillo) y continuación de enfisema en glúteo izquierdo (flecha blanca).
Discusión
La fascitis necrotizante secundaria a neoplasia colorrectal es rara, siendo más frecuente tras cirugías o traumatismos. La mortalidad asociada a la fascitis necrotizante es muy elevada, en torno al 75%, depende en gran medida del tiempo transcurrido hasta el diagnóstico y de la extensión de la infección, y asciende >90% si no se atiende a la causa subyacente.
En el caso de perforación de origen neoplásico, se valorará en el mismo acto la posibilidad de resecar de la lesión y la creación de un estoma.
CP-143. FÍSTULA COLECISTOCÓLICA: CAUSA POCO COMÚN DE HEMORRAGIA DIGESTIVA BAJA
Campos Serrano N, Sánchez García O, Pérez Campos E
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: hemorragia digestiva baja, fístula colecistocólica.
Introducción
La hemorragia digestiva baja (HDB) es un motivo de consulta habitual en urgencias probablemente debido al aumento de la población de edad avanzada y al gran uso de anticoagulantes. En general, la HDB suele ceder de forma espontánea, aunque puede llevar asociado una gran morbilidad y mortalidad. Las causas más comunes de HDB son el sangrado diverticular, la colitis isquémica, las hemorroides, los pólipos, los tumores y las lesiones vasculares. Sin embargo, existen otras causas menos comunes como la secundaria a una fístula colecistocólica, para lo que será fundamental una anamnesis dirigida.
Caso clínico
Varón de 82 años con antecedente de ingreso hace 4 meses por colecistitis aguda evolucionada con absceso hepático drenado percutáneamente y complicada con pseudoaneurisma de la arteria cística que precisó embolización que se manejó de forma conservadora, pendiente de programar colecistectomía. Acude a urgencias por episodios intermitentes de rectorragia asociado a astenia de un mes de evolución sin repercusión hemodinámica. En analítica destaca anemización de 4 puntos (hemoglobina de 11.9 a 7.8 mg/dL). Se le transfunden 2 concentrados de hematíes e ingresa para continuar estudio y evolución.
Tras su ingreso en planta el paciente comienza con dolor abdominal intenso, inestabilidad hemodinámica (TA 86/56 mmHg, FC 100 lpm) y rectorragia abundante. En analítica presenta hemoglobina de 7.4 mg/dL a pesar de la transfusión. Se inician medidas de soporte y se realiza angioTC urgente en el que se objetiva una fístula entre una litiasis biliar y ángulo hepático del colon, además de una angiectasia en colon ascendente sin observar hemorragia activa. Se realiza colonoscopia en la que se visualiza en ángulo hepático gran coágulo adherido junto a orificio fistuloso sin sangrado en ese momento.
Se contacta con cirugía general que realiza intervención quirúrgica urgente mediante hemicolectomía derecha más colecistectomía con buena evolución.
Discusión
La fístula colecistocólica es una complicación rara de la colecistitis biliar. Clínicamente suele cursar de forma asintomática, objetivándose como hallazgo incidental en pruebas de imagen. Cuando presenta síntomas, éstos suelen ser diarrea, dolor abdominal, fiebre, ictericia y muy inusualmente en forma de obstrucción intestinal o hemorragia. El tratamiento de elección es la colecistectomía con reparación del orificio fistuloso. En los casos en los que no sea posible o no esté indicada la intervención quirúrgica se puede optar por actitud conservadora o drenaje biliar mediante CPRE.
Consideramos este caso de interés por la forma atípica de presentación, destacando que la colonoscopia permitió identificar el origen exacto del sangrado.
CP-144. FÍSTULA GASTROCÓLICA COMO PRIMER HALLAZGO DE CÁNCER COLORRECTAL COMPLICADO
Díaz Alcázar MM, Martín-Lagos Maldonado A
UGC Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: cáncer colorrectal, fístula gastrocólica, complicación.
Introducción
La fístula gastrocólica es una complicación rara de tumores gastrointestinales malignos. Fundamentalmente se relaciona con neoplasias de colon transverso (en Occidente) y tumores de estómago (en Japón).
Caso clínico
Mujer de 48 años sin antecedentes de interés que consulta por vómitos fecaloideos e intolerancia oral. Analíticamente presenta anemia normocítica, leucocitosis y trombocitosis. Se realiza tomografía computarizada toracoabdominal con contraste con hallazgo de engrosamiento parietal en ángulo esplénico del colon y sospecha de fístula gastrocólica.
Se realiza endoscopia digestiva alta que objetiva en curvatura mayor un orificio fistuloso con bordes eritematosos, sobreelevados e indurados a través del cual refluye material fecaloideo. Se toman biopsias, que son compatibles con infiltración por adenocarcinoma de probable origen colónico.
Se realiza resección oncológica en bloque, incluyendo resección segmentaria de ángulo esplénico, gastrectomía parcial tubulizada, esplenectomía y pancreatectomía distal. Posteriormente recibe quimioterapia adyuvante.
Discusión
La fístula gastrocólica es una complicación rara cuya principal causa actualmente son tumores gastrointestinales, fundamentalmente colon y estómago, aunque también duodeno, vía biliar y páncreas. Histológicamente los tumores suelen ser adenocarcinomas, aunque también se ha descrito con carcinoides y linfomas. Menos frecuentemente, la fístula gastrocólica se debe a enfermedades benignas como úlcera péptica, pancreatitis crónica, absceso pancreático y enfermedad de Crohn. Esta complicación afecta fundamentalmente a mujeres de 50-60 años.
Se han propuesto dos teorías etiopatogénicas: formación de la fístula por extensión directa del tumor a través del omento gastrocólico dada la proximidad entre la curvatura mayor gástrica y el colon transverso; e inflamación peritoneal por ulceración del tumor que causa adherencias y fistulización.
Los síntomas de la fístula son inespecíficos, pero la triada clínica clásica es diarrea, pérdida de peso y vómitos fecaloideos en ausencia de obstrucción intestinal. El diagnóstico se basa en hallazgos clínicos y radiológicos. La endoscopia permite visualización directa, aunque no siempre se encuentra el orificio fistuloso; y la toma de biopsias. La mejor opción terapéutica es la resección en bloque con quimioterapia adyuvante.
CP-145. FRECUENCIA DE TRASTORNOS METABÓLICOS EN EL CÁNCER COLORRECTAL DE DEBUT PRECOZ
Agulleiro Beraza I1, Chica Cid T1, Reyes Díaz ML2, Rico Gutierrez MC1, Pizarro Moreno A1, Gómez Izquierdo L3, Garzón Benavides M1, Giráldez Jiménez MD1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 2UGC Cirugía General y Digestiva. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 3UGC Anatomía Patológica. Complejo Hospitalario Regional Virgen del Rocío, Sevilla.
Palabras clave: cáncer colorrectal de debut precoz, obesidad, patologías metabólicas.
Introducción
La incidencia y mortalidad del cáncer colorrectal (CCR) diagnosticado antes de los 50 años (CCR de debut precoz) ha aumentado en la mayoría de los países occidentales en los últimos años. A pesar de que el CCR de debut precoz es sugestivo de predisposición hereditaria, en la mayoría de pacientes no se identifica ninguna causa genética responsable. En estos casos, factores como la dieta y los trastornos metabólicos podrían tener un papel destacado. Los objetivos fueron analizar las características clínicas de los pacientes diagnosticados de CCR de debut precoz en nuestro medio y determinar la frecuencia de patologías metabólicas en esta población.
Material y métodos
Estudio retrospectivo que incluye los pacientes diagnosticados de CCR a una edad <50 años, tratados quirúrgicamente por la Unidad de Coloproctología del Hospital Universitario Virgen del Rocío, entre enero de 2011 y diciembre de 2021. Se recogieron variables clínicas incluyendo patologías metabólicas de interés (sobrepeso/obesidad, hipertensión, diabetes y dislipemia), demográficas, y relacionadas con el tumor. Para el análisis estadístico se utilizó SPSS v26.0 (Figura 1).
Resultados
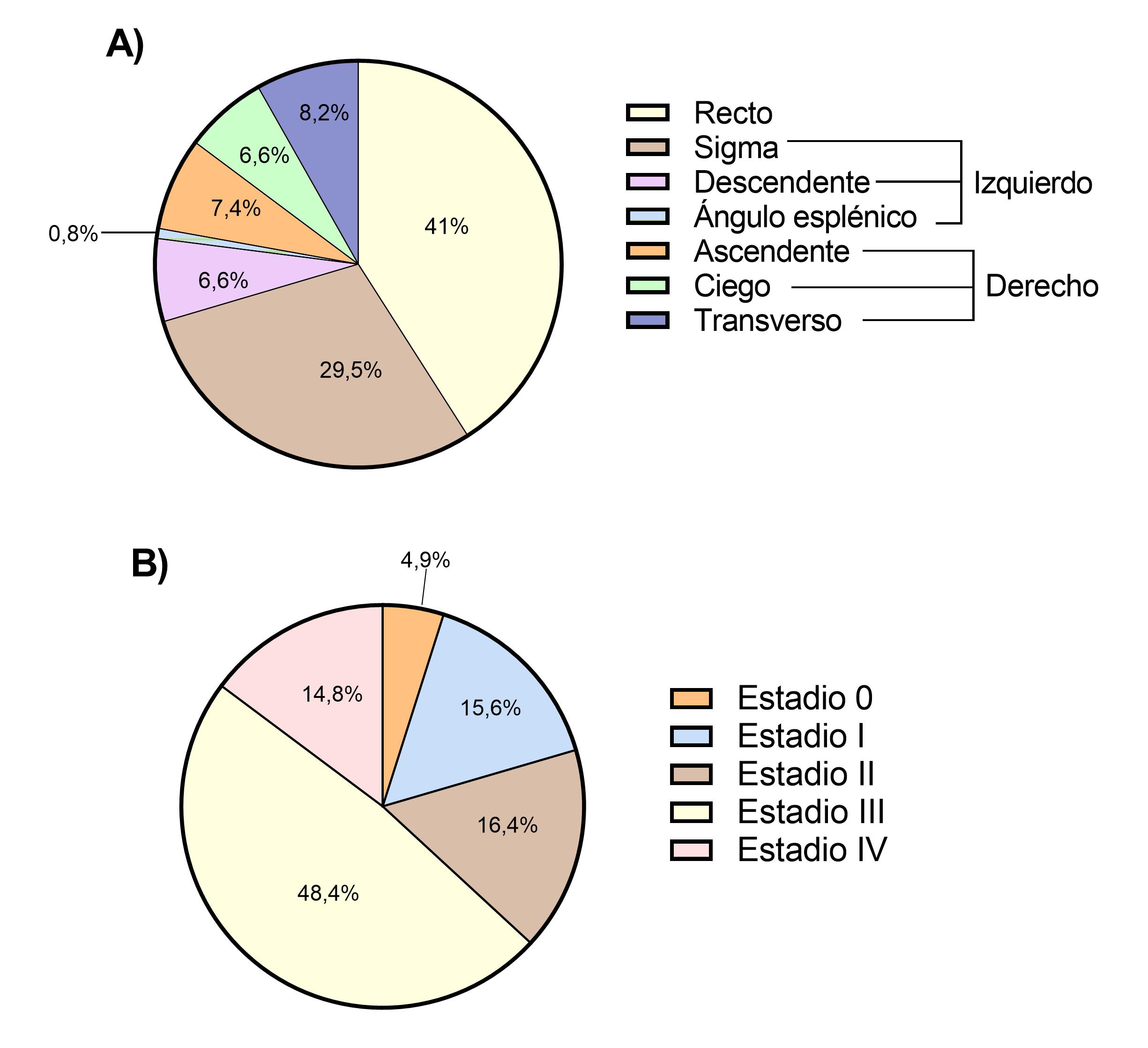
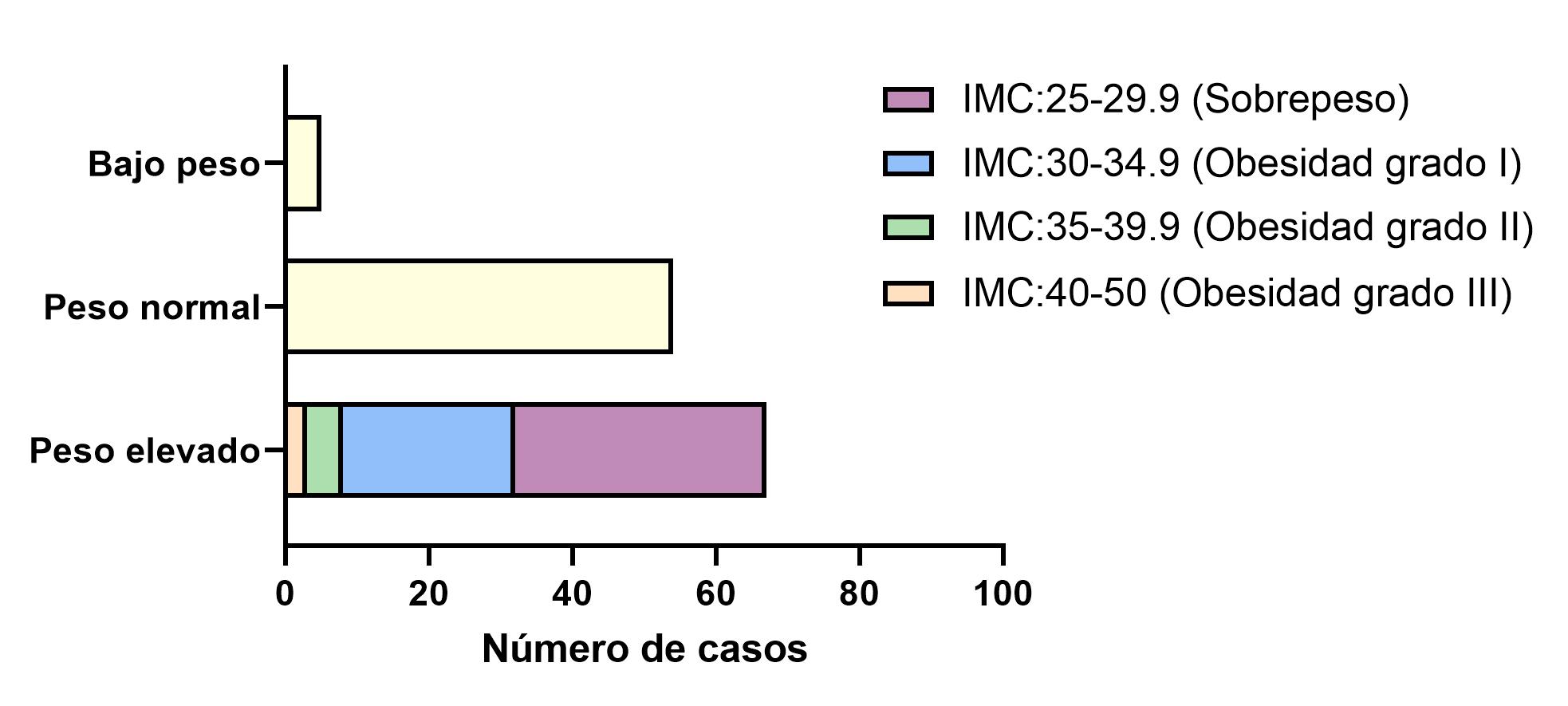
Se incluyeron un total de 124 pacientes. La edad media fue de 42 años (rango 15-49); siendo el 51,6% hombres. Los resultados del análisis descriptivo se muestran en la Tabla 1. La localización más frecuente del tumor fue recto (41%) seguido de sigma (29,5%) y el 63,2% fueron diagnosticados en estadio avanzado (III y IV) (Figura 2). El 20.2% de los casos presentaron antecedentes familiares de primer grado de CCR. En el 17,8% de los tumores se identificó deficiencia del sistema de reparación MMR por inmunohistoquímica. Con respecto a las patologías metabólicas, el 53,2% de los pacientes presentaba al menos una de las alteraciones metabólicas recogidas y el 15,9% dos o más. La alteración metabólica más frecuente fue la existencia de un índice de masa corporal elevado (IMC≥25), presente en el 50,8% de los pacientes (sobrepeso 28,9% y 23,2% obesidad) (Figura 3). En el subánalisis de los pacientes con sistema reparador normal, el porcentaje de alteraciones metabólicas fue similar (53,4% presentaban al menos una alteración metabólica siendo la más frecuente el sobrepeso/obesidad en el 50% de los casos).
CP-146. GASTROENTERITIS EOSINOFÍLICA: UNA CAUSA POCO FRECUENTE DE ILEITIS
González Sánchez MH1, Garcia Calonge M1, Muiño Dominguez D1, Celada Sendino M1, Martin Sanz J1, Villela Ramírez JE1, Campos Martín JM1, Argüelles Estrada P1, Lopez Mourelle A1, Lamas Álvarez S1, Fuente Díaz C2, Cedeño Caballero N2, González Parra MC3, Pérez Martínez I1, Barbeito Castro E1
1Servicio Aparato Digestivo. Hospital Universitario Central de Asturias, Oviedo. 2Servicio Anatomía Patológica. Hospital Universitario Central de Asturias, Oviedo. 3Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: eosinofilica, gastroenteritis, ileitis.
Introducción
La gastroenteritis eosinofílica (GE) es un trastorno raro caracterizado por la infiltración de eosinófilos en el aparato digestivo. Este trastorno suele aparecer más frecuentemente en el estómago, pero puede afectar a todos los tramos y capas del aparato digestivo.
Caso clínico
Presentamos el caso de una mujer de 70 años que consulta por dolor abdominal, diarrea y fiebre. Se realizan ecografía, TC y enteroRM con hallazgo de ileitis inespecífica. En coprocultivo inicial crece Yersinia enterocolítica por lo que se completa antibiótico y se decide alta. Reingresa posteriormente por cuadros similares pero con coprocultivos y parásitos negativos. Como hallazgo analítico, destaca eosinofilia en sangre (Eo >20%) desde el inicio del cuadro.
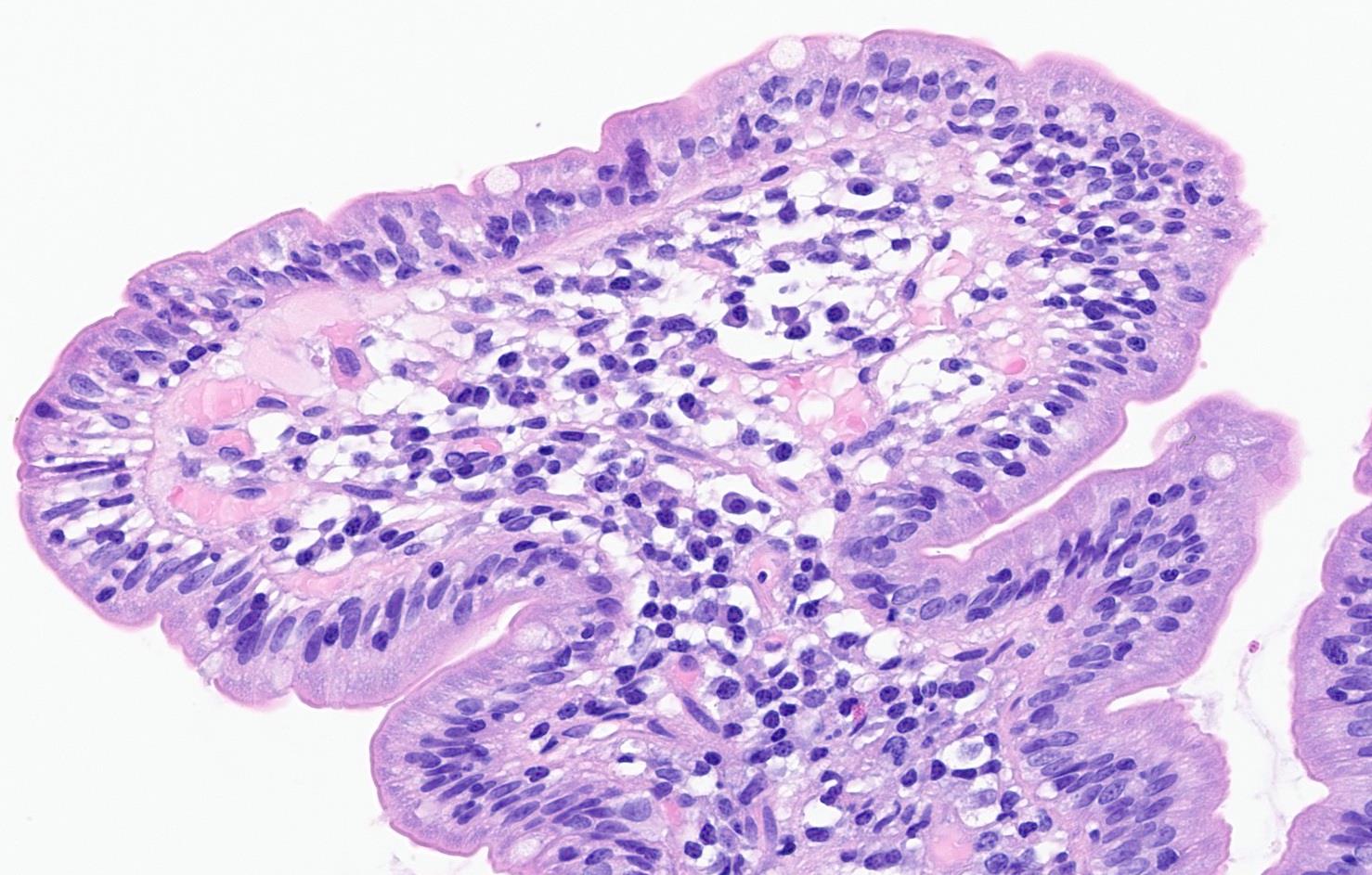
Se realiza ileocolonoscopia en la que se observa eritema y ulceración de 5 mm en íleon terminal (se biopsia) y mucosa colónica normal (se biopsia por segmentos). La anatomía patológica informa de infiltrado eosinofílico con > 56 eosinófilos/campo en la muestra ileal y normalidad de las muestras colónicas, confirmando el diagnóstico de enteritis eosinofílica. Se inicia budesonida 9 mg durante 2 meses con desescalada hasta su suspensión, encontrándose la paciente asintomática en este momento.
Discusión
La GE es una entidad extraña aunque con una incidencia creciente. Su diagnóstico exige un alto grado de sospecha y la exclusión activa de otras posibles etiologías.
La exploración del ileon terminal durante la colonoscopia indicada por diarrea crónica es fundamental, así como la toma de biopsias seriadas del ileon y del resto del colon para descartar enfermedades microscópicas, como las enteritis eosinofílicas.
CP-147. HEMORRAGIA DIGESTIVA BAJA DE ORIGEN GINECOLÓGICO, UNA PRESENTACIÓN INUSUAL.
Soler Góngora M1, Moreno Barrueco M1, Villar Ortega P2, Barrientos Delgado A1
1Servicio Aparato Digestivo. Hospital San Cecilio, Granada. 2Servicio Radiodiagnóstico. Hospital San Cecilio, Granada.
Palabras clave: tumor ovárico, hemorragia digestiva baja, hematoquecia.
Introducción
Presentamos un caso clínico de una paciente con carcinoma seroso de ovario que condicionó una hemorragia digestiva baja (HDB) por fistulización a colon sigmoide, caso que nos parece de interés dado lo inusual de la presentación.
Caso clínico
Mujer de 83 años con antecedentes de DM tipo 2, FA anticoagulada con acenocumarol y carcinoma seroso de ovario de bajo grado estadio III irresecable, en tratamiento hormonal con tamoxifeno. Es derivada al servicio de urgencias de nuestro hospital por presentar durante la noche anterior abundantes deposiciones oscuras, no claramente compatibles con melenas por antecedente de consumo de hierro oral y, una deposición hematoquécica en la mañana, sin otra sintomatología asociada. Se constata un INR de 7 que se corrige hasta 1,7 con complejo protrombínico y fitometadiona. Analíticamente, destaca un aumento de reactantes de fase aguda con PCR 181.1 mg/dL, leucocitosis de 18230 con 90.9% de PMN, leve anemización de Hb 11.3 a Hb 9.4 respecto a control 3 meses antes. La exploración abdominal revela un abdomen blando ligeramente doloroso a la palpación en fosa iliaca izquierda sin peritonismo.
Ante la sospecha de hemorragia digestiva baja y dado el antecedente oncológico se solicita TAC abdominal, que detecta una imagen sugerente de fistulización a colon sigmoide desde lesión anexial izquierda (Figura 1), como origen de la hematoquecia.
Tras control evolutivo la paciente pudo ser dada de alta al autolimitarse el cuadro.
Discusión
Las principales causas de HDB pueden agruparse en diferentes categorías: anatómicas (diverticulosis), vasculares (angiodisplasias, isquemia, rectitis actínica), inflamatorias (infecciosa, enfermedad inflamatoria intestinal) y neoplásicas (como el caso que nos corresponde).
Dentro de las causas neoplásicas destaca el cáncer colorrectal, aunque se han descrito hemorragias secundarias a metástasis a nivel intestinal, así como de otros tumores ginecológicos como el coriocarcinoma.
El caso de nuestra paciente resulta inusual dado que se produjo por una afectación locorregional tumoral en lugar de por implantes metastásicos a distancia.
CP-148. HIPERTROFIA VASCULAR COLÓNICA: VARIANTE DE LA NORMALIDAD DETECTADA DURANTE LA COLONOSCOPIA
García Martínez A, Fernández Olvera D, Hernani Álvarez JA
UGC Aparato Digestivo. Hospital de Especialidades de Jerez de la Frontera, Jerez de la Frontera.
Palabras clave: colonoscopia, hipertrofia vascular, variante.
Introducción
En gastroenterología la colonoscopia es un instrumento esencial en el diagnóstico de numerosas enfermedades digestivas. No obstante, su amplio uso ha permitido la detección no sólo de estas patologías, sino de otras numerosas variantes clínicas que la anatomía intestinal puede presentar.
Caso clínico
Presentamos el caso de un varón de 47 años sin antecedentes de interés que es remitido desde atención primaria para estudio de anemia ferropénica, sin síntomas gastrointestinales. Desde la consulta de Digestivo se realizó colonoscopia resaltando a nivel de colon izquierdo (colon descendente y sigmoide) así como en recto, múltiples engrosamientos longitudinales de coloración blanquecina de la mucosa colónica que recorrían el axis del colon (Figura 1, 2 y 3), sugiriendo origen vascular. Se completó estudio del paciente mediante ecografía con función Doppler y angioTAC de abdomen que, si bien descartaron hipertensión portal, destacaba en esta última una hipertrofia de la vasculatura portal pericolónica en colon izquierdo, sin evidencia de estenosis ni otras anomalías vasculares. En la endoscopia oral se detectaron lesiones que justificaban las alteraciones analíticas del paciente por lo que los hallazgos colónicos se consideraron incidentales.
Discusión
Las variantes de la normalidad de características vasculares y localización colónica son infrecuentes y en ocasiones se pueden confundir con patología clínicamente relevante, si bien la literatura es muy escasa al respecto. En nuestro caso y dada la confusión que generó con varices colónicas se completó el estudio mediante ecografía con función Doppler y angioTAC de abdomen para descartar su relación con la hipertensión portal u anomalías vasculares de carácter patológico. Tras el tratamiento de las lesiones halladas en el tracto digestivo superior el paciente ha recuperado las cifras normales de hemoglobina y permanece asintomático.
CP-149. INVAGINACIÓN INTESTINAL COMO FORMA DE PRESENTACIÓN ATÍPICA DEL LINFOMA INTESTINAL
Bernal Torres A, Manrique Gil MJ, Ramírez Raposo R, Macías Rodríguez MA
UGC Aparato Digestivo. Hospital Puerta del Mar, Cádiz.
Palabras clave: linfoma intestinal no hodgkin, invaginación intestinal. .
Introducción
El tracto gastrointestinal es el sitio extraganglionar más afectado en el linfoma no Hodgkin (LNH), sin embargo, es poco frecuente, representando el 4% de las neoplasias gastrointestinales. El órgano más afectado es el estómago (60-75%), seguido del intestino delgado y la válvula ileocecal.
Sus manifestaciones clínicas varían según la localización de la enfermedad siendo los síntomas más frecuentes el dolor abdominal, vómitos y la diarrea. Las manifestaciones más graves como la perforación, obstrucción intestinal o hemorragia son poco frecuentes (10%).
Caso clínico
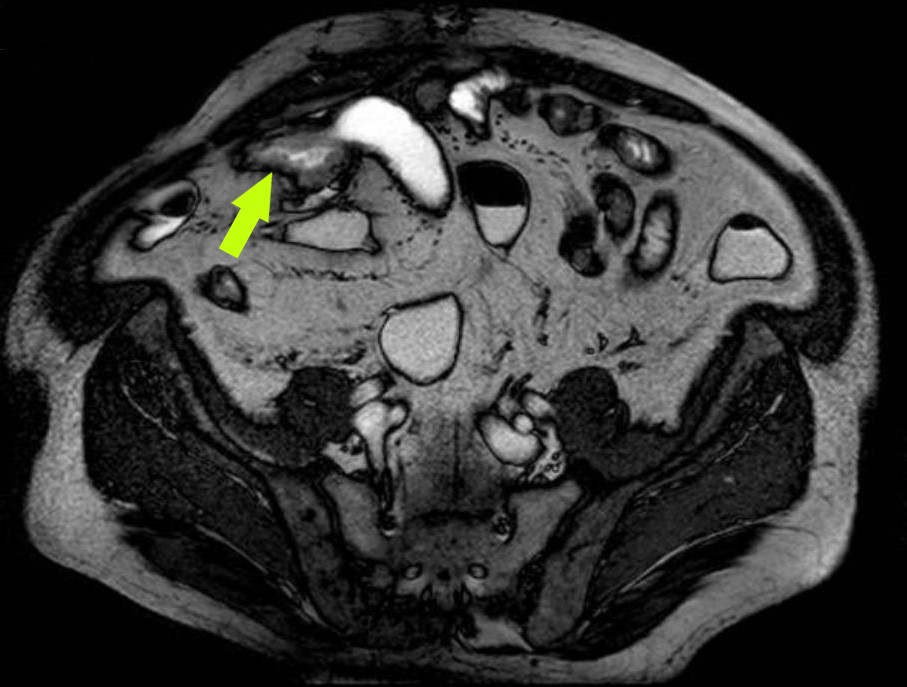
Paciente de 44 años sin enfermedades de interés que presenta dolor abdominal difuso intermitente acompañado de vómitos y síndrome constitucional. Se realiza ecografía abdominal donde se visualiza imagen hipoecoica en hipocondrio derecho dependiente de colon derecho con dilatación de asas intestinales.
Ante dichos hallazgos se completa estudio mediante TAC y colonoscopia. En TAC se aprecia imagen compatible con invaginación intestinal ileocólica en región ileocecal, con presencia de imagen de masa redondeada y densidad de partes blandas, localizada en el interior de la invaginación pudiendo ser la causa de la invaginación (Figuras 1 y 2). En colonoscopia se visualiza en ciego una gran lesión excrecente de 4 cm, polilobulada, irregular y ulcerada, que prolapsa desde válvula ileocecal y parece depender del intestino delgado. Se accede a válvula que está deformada por lesión, pero presenta mucosa normal (Figura 3). Se toman biopsias con hallazgos de proceso linfoproliferativo B de alto grado compatible con linfoma difuso de células grandes B (Figura 4).
Durante el estudio, la paciente presenta cuadro de obstrucción intestinal precisando cirugía urgente con resección ileal y anastomosis ileo-cólica. Actualmente la paciente se encuentra en tratamiento con quimioterapia con ciclofosfamida, doxorrubicina y vincristina con buena respuesta.
Figura 1
Invaginación intestinal ileocólica secundaria a la presencia de una masa de morfología redondeada y densidad de partes blandas, con medidas aproximadas de 3,5 x 3,7 cm, localizada en el interior de la invaginación.
Figura 2
Invaginación intestinal ileocólica secundaria a la presencia de una masa de morfología redondeada y densidad de partes blandas, con medidas aproximadas de 3,5 x 3,7 cm, localizada en el interior de la invaginación.
Discusión
A pesar del desarrollo de nuevas técnicas radiológicas, la endoscopia sigue siendo actualmente una herramienta diagnóstica fundamental en el diagnóstico de los linfomas intestinales. Puede revelar una amplia variedad de diferentes formas como hiperplasia de folículos linfoides, pólipos de diferente morfología, lesiones infiltrantes o de aspecto necrótico. Si bien el desarrollo de complicaciones tipo invaginación u obstrucción intestinal son poco frecuentes, suelen aparecer más comúnmente en los linfomas que asientan sobre la válvula ileocecal. El tratamiento de estas lesiones hematológicas se basa fundamentalmente en quimioterapia, reservando la cirugía para las complicaciones derivadas de éstos como la obstrucción intestinal.
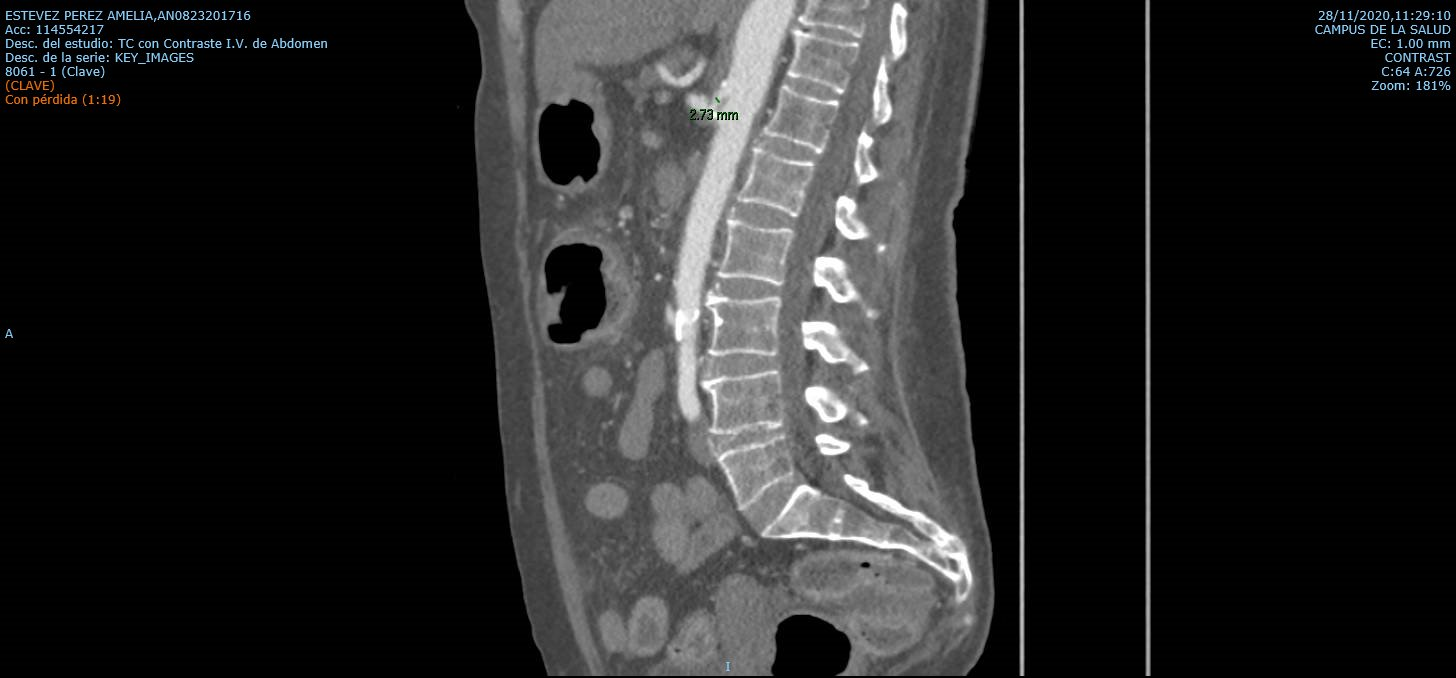
CP-150. ISQUEMIA INTESTINAL POR ESTENOSIS DEL TRONCO CELIACO DIAGNOSTICADA MEDIANTE ECOENDOSCOPIA (USE)
GARCÍA ARAGÓN F, ROSA SÁNCHEZ C, RODRÍGUEZ GÓMEZ VM, REDONDO CEREZO E, SÁNCHEZ CAPILLA AD
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: isquemia intestinal, ecoendoscopia.
Introducción
La isquemia mesentérica crónica es una entidad poco frecuente, cuyo diagnóstico requiere una alta sospecha clínica y al que en muchas ocasiones tan solo llegamos tras la exclusión de patologías más comunes, lo que conlleva un importante retraso terapéutico.
La sintomatología típica engloba un cuadro de dolor abdominal crónico, típicamente postprandial, acompañado de cibofobia y la consiguiente pérdida de peso, generalmente en pacientes ya afectos de patologías de riesgo cardiovascular.
Caso clínico
Varón de 67 años, con numerosos factores de riesgo cardiovascular. Intervenido de colecistectomía ante clínica de meses de evolución de epigastralgia postprandial, náuseas y vómitos, junto con pérdida de peso progresiva asociada a disminución de la ingesta. Fue diagnosticado de cólicos biliares de repetición tras haber descartado otras causas potenciales de la sintomatología.
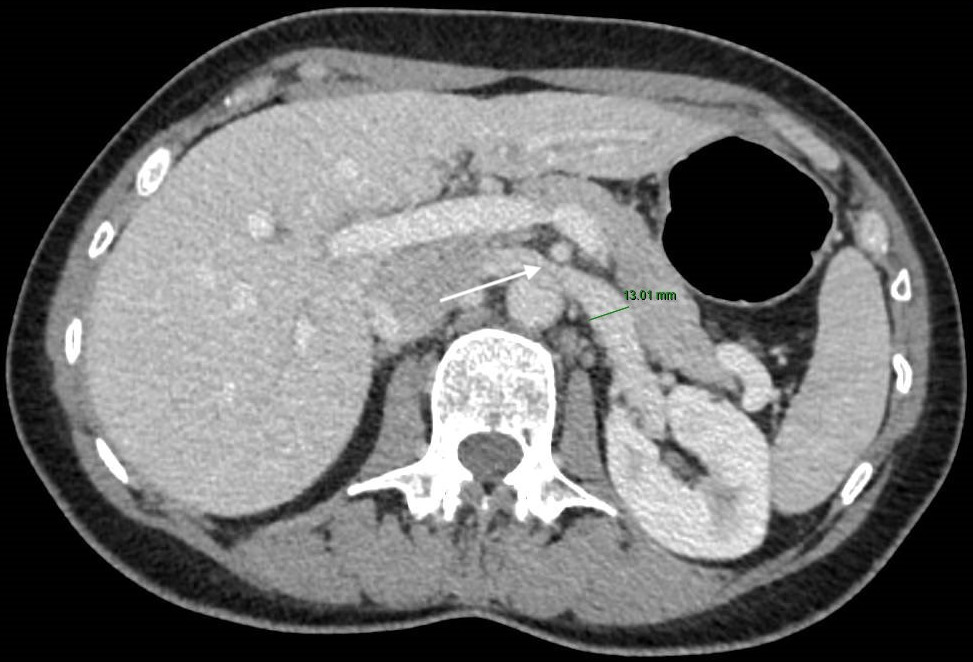
Tras la intervención quirúrgica, no obstante, persiste el cuadro clínico. Se repiten pruebas diagnósticas (endoscopia digestiva alta y baja, ecografía abdominal, TC abdómino-pélvico sin contraste intravenoso, colangiorresonancia magnética) sin hallazgos significativos. Finalmente se solicita ecoendoscopia digestiva (USE), describiéndose marcada ateromatosis que condiciona estenosis a nivel de la salida del tronco celiaco y arteria esplénica en toda su totalidad.
Ante hallazgos que podrían correlacionar la clínica del paciente con un cuadro de isquemia intestinal crónica se solicita angio-TC abdominal, que confirma la presencia de importante estenosis a nivel de los vasos mesentéricos, por lo que fue derivado a cirugía vascular para intervención terapéutica.
Discusión
La isquemia mesentérica crónica, también conocida como angina intestinal, constituye una patología poco frecuente dentro de las entidades de la isquemia intestinal. Se manifiesta en pacientes con ateroesclerosis mesentérica, en forma de episodios de hipoperfusión intestinal en relación a la ingesta, debido al aumento postprandial del riego vascular gastrointestinal.
Dichos episodios de dolor suelen ceder a las dos horas de la ingesta, y pueden terminar provocando en el paciente conductas de aversión a la comida o “cibofobia” al relacionar el dolor con la toma de alimentos, así como pérdida de peso progresiva en relación a esto último.
Más allá de la fuerte sospecha clínica necesaria, la prueba de imagen gold standard para el diagnóstico de esta patología es el angio-TC abdominal. No obstante, como describimos en este caso, los avances cada vez mayores en las técnicas y equipos de ecoendoscopia hacen que esta prueba también sea efectiva a la hora de hallar imágenes compatibles y orientar su diagnóstico, con el fin de evitar el retraso terapéutico y el desarrollo de complicaciones.
CP-151. LINFOMA DE BURKITT DUODENAL: UNA ENTIDAD INFRECUENTE.
Ortiz Sánchez A, Barrientos Delgado A, Berdugo Hurtado F, Soler Góngora M, Gutiérrez Holanda C
Servicio Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: linfoma burkitt, gen myc. .
Introducción
El Linfoma de Burkitt es un tipo de linfoma no Hodgkin muy agresivo cuya localización extranodal más frecuente es el tracto gastrointestinal. Sin embargo, la afectación duodenal es extremadamente infrecuente y presenta un abordaje diagnóstico y terapéutico muy complejo. Presentamos el caso de una paciente con un linfoma de Burkitt duodenal diagnosticada de manera incidental.
Caso clínico
Presentamos el caso de una mujer de 20 años valorada en varias ocasiones por epigastralgia de 6 meses de evolución, junto con distensión abdominal con la ingesta de alimentos y pérdida ponderal. Sin alteración del hábito intestinal ni otra sintomatología, asociando discreta anemia ferropénica ya conocida como única alteración analítica. En la ecografía abdominal se objetiva una masa abdominal mesogástrica hipoecoica de unos 8 cm de diámetro mayor y bordes irregulares. Se completó estudio con TC abdominal (Fig.1) evidenciando una gran lesión circunferencial dependiente de segunda y tercera porción duodenal con infiltración de vasos mesentéricos. Fue preciso abordaje mediante laparoscopia exploradora para el diagnóstico histológico ante la imposibilidad de obtener una adecuada muestra mediante USE-PAAF, obteniendo muestra compatible con linfoma B difuso de célula intermedia con morfología e inmunofenotipo tipo Burkitt. Tras el diagnóstico se inició quimioterapia según esquema Burkimab-14, alcanzando remisión parcial tras estudio de extensión intermedio.
Discusión
El Linfoma de Burkitt es un linfoma no Hodgkin de células B muy agresivo caracterizado por la translocación y desregulación del gen MYC en el cromosoma 8. El tracto gastrointestinal es la localización extranodal más frecuente de los linfomas malignos, siendo el estómago el área más común en casos esporádicos, seguida de íleon distal y ciego. Sin embargo, la afectación duodenal del linfoma de Burkitt es extremadamente inusual en población adulta inmunocompetente, representando menos del 1% del total de los casos y siendo diagnosticada de manera incidental, especialmente tras estudio de complicaciones como hemorragia digestiva o síntomas abdominales crónicos como en el caso de nuestra paciente. En la actualidad existen varias líneas terapéuticas basadas en combinación de quimioterapia sistémica e intratecal, sin existir a día de hoy un estándar de tratamiento, basándose en una evaluación previa de cada paciente para individualizar la terapia a seguir.
CP-152. LOCALIZACIÓN INFRECUENTE DEL ADENOCARCINOMA DUODENAL
Vías Parrado C1, Machuca Aguado J2, Maldonado Pérez MB1, Caunedo Álvarez A1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla. 2UGC Anatomía Patológica. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: adenocarcinoma, bulbo duodenal.
Introducción
El adenocarcinoma duodenal constituye una entidad infrecuente que generalmente asienta en la región ampular, siendo excepcional su presentación a nivel del bulbo, con muy pocos casos publicados en la literatura. Esta baja incidencia parece estar relacionada con las características anatómicas, fisiológicas e histológicas de esta porción duodenal, que parecen proporcionarle una vía de escape a la transformación oncogénica.
Caso clínico
Varón de 77 años, exconsumidor de tabaco y afecto de diabetes mellitus tipo 2. Valorado en consultas de Medicina Interna por astenia y epigastralgia de reciente aparición. Se solicita una endoscopia digestiva alta donde se evidencia una lesión de aspecto neoplásico que asienta en la cara posterior del bulbo duodenal que se extiende hacia rodilla (figura 1), con segunda porción duodenal normal (figura 2), sin otras lesiones. Colonoscopia reciente realizada por sangre oculta en heces sin hallazgos patológicos. Las biopsias de la lesión revelan un adeconarcinoma poco diferenciado (figura 3) con inmunohistoquímica: CK7 positivo, p63 negativo, sinaptofisina negativo, elevado índice de proliferación ki67 > 70. En la analítica, destacan datos de anemia ferropénica (Hb 10,2 g/dl) y CEA elevado (42,5 ng/ml). El estudio de extensión (TC de tórax y abdomen) y la RMN de abdomen revelaron una lesión tumoral dependiente de bulbo duodenal localmente avanzada sin evidencia de lesiones en páncreas (figura 4) y sin otra afectación a distancia. El caso es comentado en el comité de tumores hepatobiliares decidiéndose iniciar tratamiento quimioterápico neoadyuvante (capecitabina y oxaliplatino), con el que se encuentra actualmente el paciente, pendiente de plantear posteriormente tratamiento de rescate.
Figura 1
Imagen endoscópica donde se observa en la cara posterior de bulbo duodenal una lesión de crecimiento endoluminal, mamelonada, ulcerada y friable que ocupa el 75% de la luz y se extiende hasta la primera rodilla.
Imagen 2
Imagen endoscópica que demuestra que la lesión descrita es franqueable, sin evidencia de lesiones en segunda porción duodenal.
Discusión
El diagnóstico de adenocarcinoma duodenal suele hacerse en estadios avanzados por su baja sospecha en relación con su baja prevalencia y presentación clínica inespecífica. La cirugía seguida de quimioterapia constituye la modalidad de elección en los casos de adenocarcinoma duodenal con afectación locorregional. En casos más avanzados, la quimioterapia neoadyuvante debe contemplarse para reducir el estadio tumoral y conseguir una mayor tasa de resección radical posterior. La literatura disponible sobre el adenocarcinoma de bulbo duodenal es escasa, existiendo un caso publicado en el que se observa respuesta completa con quimioterapia neoadyuvante. En espera de la evolución del paciente, consideramos de interés la comunicación de este caso con la intención de optimizar las estrategias de diagnóstico y tratamiento y mejorar su pronóstico.
CP-153. MALROTACIÓN INTESTINAL EN EL ADULTO, EL GRAN OLVIDADO
Pérez Campos E, Plaza Fernández A, Moreno Moraleda I
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: malrotación intestinal, malformación congénita.
Introducción
La malrotación intestinal se trata de la interrupción de la formación del intestino medio durante el desarrollo embriológico, en su proceso de regreso a la cavidad intraabdominal. Resulta un hallazgo altamente infrecuente en la población adulta, diagnosticándose de forma accidental por pruebas de imagen, o por síntomas abdominales inespecíficos.
Caso clínico
Varón de 25 años, sin antecedentes conocidos. Acude a urgencias por presentar vómitos y epigastralgia desde hace dos semanas. Sin alteraciones del hábito intestinal, pérdida ponderal ni fiebre. A la exploración, presenta dolor epigástrico, sin masas ni megalias palpables ni peritonismo. Presenta también deterioro de la función renal (creatinina de 3 mg/dl) e hiponatremia, rápidamente corregidas con sueroterapia. Tras una ecografía abdominal informada como normal, ingresa para estudio de síndrome emético.
La gastroscopia muestra lesiones en tercio distal esofágico sugestivas de esofagitis severa secundarias a hiperémesis. También se realiza TC, que describe giro de la unión duodeno-yeyunal alrededor de los vasos mesentéricos, con predominio de asas en hemiabdomen derecho, además de ángulo hepático en línea media y localización izquierda de colon ascendente y ciego. Posteriormente, el tránsito esofagogastroduodenal confirma el arremolinamiento del primer asa yeyunal y los vasos mesentéricos, con la vena mesentérica superior situada anterior y a la izquierda de la arteria e imagen de pseudovolvulación. Además, describe localización izquierda de ciego, válvula ileocecal, apéndice y colon ascendente, así como venas mesentéricas dilatadas, probablemente secundarias a estasis venoso por el arremolinamiento de los vasos, confirmando todos estos hallazgos radiológicos el diagnóstico de malrotación intestinal.
Discusión
Existen diferentes variantes según el momento de embriogénesis afectado. En nuestro paciente se produjo una primera rotación antihoraria de 90º, sin originarse una segunda (tipo Ia), posicionándose de esta forma el intestino delgado en el hemiabdomen derecho y el grueso en el izquierdo.
La aparición de dolor brusco secundario a volvulación resulta más característica de la edad pediátrica. En cambio, la mayoría de los diagnósticos realizados durante la edad adulta son incidentales, por medio de hallazgos típicos en pruebas de imagen realizadas por otros motivos, o por estudio de sintomatología abdominal crónica e inespecífica. Por ello, resulta lógico pensar que la incidencia real en esta población resulta mayor de lo que se piensa, y la importancia de su diagnóstico radica en la prevención, mediante cirugía, de complicaciones potencialmente graves secundarias a la malrotación, como el compromiso de la vascularización o el tránsito intestinal.
CP-154. METÁSTASIS COLÓNICA 13 AÑOS DESPUÉS DE UN ADENOCARCINOMA GÁSTRICO
SALDAÑA GARCIA L1, TORRES DOMÍNGUEZ A1, SORIA LÓPEZ E1, ABITEI C2, MÉNDEZ SÁNCHEZ IM1
1Departamento Aparato Digestivo. Complejo Hospital Costa del Sol, Marbella. 2Departamento Anatomía Patológica. Complejo Hospital Costa del Sol, Marbella.
Palabras clave: cáncer gástrico, metástasis colónica, células en anillo de sello.
Introducción
Los sitios más comunes de diseminación a distancia del adenocarcinoma gástrico son el hígado 48%, peritoneo 32%, pulmón 15% y hueso 12%, siendo infrecuente la diseminación hacia el colon, con pocos casos descritos en la literatura. Los tumores con células en anillo de sello tienen peor pronóstico, pudiendo conllevar riesgo de metástasis a largo plazo. Se presenta el caso de un paciente intervenido de adenocarcinoma gástrico, el cual debuta con metástasis en colon transverso 13 años más tarde.
Caso clínico
Varón de 59 años con dislipemia mixta y síndrome depresivo, con un hermano diagnosticado de cáncer de colon a los 48 años. En 2007, con 44 años, por epigastralgia de años de evolución se diagnosticó de un adenocarcinoma gástrico pobremente diferenciado difuso infiltrante, sin signos de extensión en el TC toracoabdominal. Se le realizó Gastrectomia subtotal con reconstrucción en Y de Roux con estadiaje final pT2aN1M0 (estadio II), por lo que recibió quimioradioterapia adyuvante con seguimiento posterior en Digestivo y Oncología. En 2020, tras cambios en el hábito intestinal, ingresó por suboclusión intestinal, observándose en TC dilatación de colon derecho y delgado medio-distal (ciego de 7.5cm) hasta colon transverso donde había un cambio brusco de calibre con engrosamiento de paredes y realce de la mucosa de unos 12cm de longitud, que sugería proceso inflamatorio (imágenes 1-2) Inicialmente se trató de forma conservadora y 3 días después, ante la ausencia de mejoría clínica se le realizó laparotomía apreciando masa tumoral que englobaba colon transverso y asa alimentaria, realizándose hemicolectomía derecha ampliada con resección de asa alimentaria, siendo informado en la anatomía patológica como infiltración por adenocarcinoma pobremente diferenciado con células en anillo de sello, compatible con recidiva de neoplasia gástrica a nivel del colon transverso, con afectación de asa de intestino delgado y metástasis en dos ganglios linfáticos regionales, con estudio de inestabilidad de microsatélites negativo. Recibió quimioterapia adyuvante y a los 17 meses, ante el comienzo de clínica obstructiva intestinal se realizó laparotomía exploradora donde se confirmaron implantes peritoneales con histología con células en anillo de sello y se inició quimioterapia paliativa con mala evolución posterior y finalmente éxitus.
Oclusión intestinal secundaria a estenosis.
Imagen de TC donde se aprecia dilatación de colon derecho y delgado medio-distal (el ciego mide 7,5 cm) hasta colon transverso donde existe un cambio brusco de calibre con engrosamiento de las paredes y realce importante de la mucosa de unos 12 cm de longitud que sugiere proceso inflamatorio.
Oclusión intestinal secundaria a estenosis.
Imagen de TC donde se aprecia dilatación de colon derecho y delgado medio-distal (el ciego mide 7,5 cm) hasta colon transverso donde existe un cambio brusco de calibre con engrosamiento de las paredes y realce importante de la mucosa de unos 12 cm de longitud que sugiere proceso inflamatorio.
Oclusión intestinal secundaria a estenosis.
Imagen de TC donde se aprecia dilatación de colon derecho y delgado medio-distal (el ciego mide 7,5 cm) hasta colon transverso donde existe un cambio brusco de calibre con engrosamiento de las paredes y realce importante de la mucosa de unos 12 cm de longitud que sugiere proceso inflamatorio.
CP-155. NEOFORMACIÓN DE COLON COMO DEBUT DE NEOPLASIAS LINFOPROLIFERATIVAS: A PROPÓSITO DE DOS CASOS
Campos Serrano N, Estévez Escobar M, Anguita Montes F, Rodríguez Mateu A
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: neoformación de colon, linfoma.
Introducción
Los linfomas son neoplasias hematológicas con una amplia variedad de subtipos y distintas formas de presentación. La manifestación extraganglionar más frecuente es a nivel del tracto gastrointestinal, siendo poco común que afecte a colon. Los linfomas primarios de colon son raros y suponen entre el 0,2-1% de las neoplasias malignas de colon. El tipo histológico que se presenta con mayor prevalencia es el linfoma difuso B de células grandes.
A continuación, se exponen dos casos de linfomas diagnosticados tras estudio endoscópico.
Caso clínico
Caso 1
Varón de 72 años trasplantado renal en tratamiento con tacrolimus y micofenolato en seguimiento en consultas de digestivo por resección de pólipos tras colonoscopia de cribado. En última endoscopia presenta frente a válvula ileocecal una lesión sobreelevada de 3 cm con mucosa irregular en su centro, ulcerada (Figura 1A), no presente en colonoscopia de hace 1 año, de la que se toman biopsias con anatomía patológica de linfoma difuso B de célula grande.
Caso 2
Mujer de 58 años sin antecedentes personales de interés que se realiza estudio endoscópico por antecedentes familiares de CCR además de rectorragia. Al tacto rectal se palpa masa indurada que en visión con el endoscopio se presenta como una masa mamelonada con zonas de necrosis que ocupa el 75% de la circunferencia (Figura 1B). La anatomía patológica es compatible con un linfoma difuso B de célula grande. La paciente es derivada a Hematología iniciando terapia con R-CHOP.
Figura 1
A: lesión sobreelevada de unos 3 cm de tamaño localizada en ciego frente a válvula ileocecal con mucosa irregular en su centro, con amplia ulceración y coágulo adherido. B: lesión mamelonada, próxima a plexo hemorroidal, que ocupa aproximadamente el 75% de la luz intestinal con presencia de necrosis
Discusión
La mucosa gastrointestinal es rica en tejido linfoide que bajo determinadas circunstancias (estimulación antigénica repetida, procesos inflamatorios) puede llevar a la proliferación monoclonal de este tejido y desarrollo de linfomas.
Los linfomas colorrectales representan entre el 5-15% de los linfomas gastrointestinales. La afectación más común es en ciego, suele presentarse entre los 50 y 70 años con predominancia masculina. El dolor abdominal, la pérdida de peso, presencia de masa abdominal, hematoquecia o incluso síntomas de obstrucción son las formas de manifestación más frecuentes. El diagnóstico es histológico mediante ileocolonoscopia con toma de biopsias. El manejo es similar al del resto de neoplasias linfoproliferativas (regímenes de poliquimioterapia combinados en ocasiones con cirugía), dado que no existen protocolos específicos.
El linfoma colorrectal es una entidad rara que debemos tener en cuenta en el diagnóstico diferencial de la lesiones de colon, aunque su presentación clínica es inespecífica. Su tratamiento se basa en quimioterapia combinada o no con cirugía, si bien no existen protocolos específicos de manejo y seguimiento.
CP-156. OBSTRUCCIÓN DE INTESTINO DELGADO SECUNDARIA A BEZOAR
GARCÍA ARAGÓN F, ROSA SÁNCHEZ C, FERNÁNDEZ GARCÍA R, REDONDO CEREZO E, MARTÍN RODRÍGUEZ MM
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: obstrucción, bezoar.
Introducción
El bezoar es una masa compacta, de volumen variable, formada por el acúmulo de sustancias ingeridas no digeribles (desde pelo y material vegetal de difícil degradación, hasta plásticos, piedras o arena), que puede quedar retenida en el estómago o intestino de animales y humanos al no poder progresar a través del tracto digestivo.
Las molestias abdominales, náuseas y vómitos forman parte de los posibles síntomas, pudiendo en raras ocasiones ser los causantes de auténticos cuadros obstructivos gastrointestinales.
Caso clínico
Varón de 70 años con antecedentes familiares de cáncer gástrico y antecedentes quirúrgicos de hernioplastia inguinal. Acude a urgencias por aparición de intolerancia oral progresiva en la última semana junto con vómitos en las últimas 48 horas que impiden la ingesta. Asocia epigastralgia de larga data y pérdida de peso reciente no cuantificada.
Se realiza ecografía abdominal con hallazgos compatibles con estómago de retención, y endoscopia digestiva alta observando inflamación de la mucosa a nivel de la segunda porción duodenal. Hiperbilirrubinemia leve en pruebas analíticas, de carácter mixto. Ante el cuadro clínico sugerente de obstrucción intestinal se procede al ingreso hospitalario, con sospecha de neoplasia abdominal estenosante como primera opción diagnóstica. Se realiza TAC toraco-abdominal que describe cuadro suboclusivo intestinal con cambio de calibre a nivel de íleon proximal en probable relación a bridas o adherencias pos-quirúrgicas.
Finalmente el paciente fue operado de urgencia ante empeoramiento del estado general, extrayéndose fitobezoar a nivel de la transición yeyuno-ileal, causante del cuadro obstructivo.
Discusión
La formación de bezoares gastrointestinales es un problema poco común, que puede ocurrir a cualquier edad. Su aparición es más frecuente en pacientes con ciertos factores predisponentes: Trastornos de la conducta, cirugía gástrica, patologías relacionadas con retraso en el vaciamiento gástrico (diabetes mellitus, enfermedad mixta del tejido conectivo…), deshidratación, hipoclorhidria o masticación incompleta (ancianos, problemas dentales, patología neurológica…).
Generalmente son asintomáticos, si bien pueden cursar con molestias abdominales inespecíficas y vómitos, o causar patología de mayor gravedad como cuadros obstructivos y perforación intestinal.
El diagnóstico se lleva a cabo por pruebas de imagen o endoscopia, y pueden ser tratados mediante técnicas de disolución química, extracción endosópica o quirúrgica, debiendo individualizarse en cada caso la mejor intervención terapéutica.
Si bien el bezoar, dentro de la etiología de la obstrucción intestinal, representa una causa mucho menos frecuente que las adherencias posquirúrgicas, la patología herniaria o las neoplasias (<5% de los casos), es necesaria su inclusión dentro del diagnóstico diferencial cuando nos encontremos ante un cuadro sub-oclusivo.
CP-157. PRESENTACIÓN ATIPICA DE NECROSIS GRASA MESENTÉRICA ENCAPSULADA
Manrique Gil MJ1, Alía Verdejo T1, Carrasco Fernández D2, Cárdenas Cárdenas JF1, Hidalgo Blanco A1
1Servicio Aparato Digestivo. Hospital Puerta del Mar, Cádiz. 2Servicio Anatomía Patológica. Hospital Puerta del Mar, Cádiz.
Palabras clave: necrosis grasa encapsulada, infarto omental.
Introducción
Los procesos que cursan con necrosis grasa intraabdominal se manifiestan frecuentemente por dolor abdominal agudo/subagudo, hallazgos clínicos que pueden ser originados por afecciones tan variadas como la apendicitis epiplóica, el infarto omental, la necrosis grasa encapsulada, la paniculitis mesentérica, entre otras.
Caso clínico
Mujer de 29 años, obesa, sin antecedentes de traumatismos o cirugías abdominales, que ingresa por dolor abdominal agudo, intenso, de 48 horas de evolución, localizado en epigastrio e hipocondrio derecho, asociado a náuseas y pico febril único de 38.5ºC. Al examen físico, abdomen blando, doloroso en hemiabdomen derecho, sin signos de irritación peritoneal y sin afectación sistémica. Analíticamente destaca leucocitosis con neutrofilia y PCR: 222. Se realiza TC abdominal con contraste urgente, identificándose lesión quística de contenido hipodenso, de 67x71 mm, con mayor densidad en su porción declive y mayor grosor y realce de la pared posteroinferior, cierta trabeculación de la grasa y con datos de complicación (material hemorrágico vs infeccioso) sin poder establecer su organodependencia (Intestinal vs mesentérico) (Figura 1-2). Ante la ausencia de complicaciones que requirieran de intervención quirúrgica, se trata con antibioticoterapia endovenosa y analgesia del 3º escalón de la OMS. Se lleva a cabo ecografía con contraste, visualizándose lesión no captante de contraste, paredes finas y sin septos vascularizados (Figura 3); se realiza PAAF, obteniéndose líquido de aspecto quiloso (Figura 4), que se analiza para bioquímica con neutrofilia y alto contenido en colesterol y triglicéridos, y citología hipocelular con linfocitos sugestiva de linfagioma quístico. Se amplió estudio con EnteroRM que describe lesión quística compleja encapsulada, con contenido formando niveles con grasa macroscópica y material proteináceo/hemorrágico, espectro de necrosis grasa complicada (infarto omental) y descarta lesión lipomatosa maligna por ausencia de componente sólido de partes blandas (Figura 5-6). Ante la mejoría clínica y analítica se da de alta con cirugía programa a las 6 semanas, con excéresis de la lesión y estudio anatomopatológico compatible con necrosis grasa encapsulada de origen mesentérico (Figura 7-8).
Figura 1
Axial TC con contraste en fase portal: lesión de aspecto quístico unilocular en flanco derecho, con contenido heterogéneo avascular en su interior formando niveles y cápsula periférica captante, discretamente engrosada.
Figura 2
Coronal TC con contraste en fase portal: misma lesión hipodensa avascular con capsula discretamente engrosada y trabeculación de la grasa mesentérica adyacente por probables cambios inflamatorios
Figura 3
Ecografía Digestiva con contraste observándose como la lesión no muestra captación de contraste durante todo el estudio, presenta pared fina, sin septos vascularizados.
Figura 4
PAAF de la lesión con extracción de 8cc de líquido blanquecino de aspecto macroscópico quiloso.
Figura 5
Axial T2: Lesión encapsulada, heterogénea, con niveles aparentemente líquidos en su interior con señal isointensa a la grasa en región antideclive y señal hiperintensa en nivel declive.
Figura 6
Axial T1 con supresión grasa tras la administración de gadolinio IV: La lesión no muestra componente sólido en su interior y mínimo realce periférico en la cápsula, persistiendo contenido que forma nivel por componente de grasa macroscópica y nivel hiperintenso por material proteináceo/hemorrágico.
Discusión
La necrosis grasa encapsulada (NGE), es un proceso degenerativo de los tejidos adiposos maduros, más frecuente en el tejido celular subcutáneo de los miembros inferiores y mamas, pero puede localizarse en cualquier otra zona. Es de etiología incierta, siendo posibles factores causales el traumatismo, cirugías intrabdominales y la isquemia. La mayoría de los casos de infarto intraperitoneal focal de la grasa corresponden a torsión y/o infarto del omento mayor o apéndice epiplóico, existiendo muy pocos casos de NGE mesentérica descritos en la literatura.
CP-158. SÍNDROME DE SECRECIÓN ECTÓPICA DE ACTH EN PACIENTE CON ENFERMEDAD DE CROHN
Pérez Ramírez A1, Moreno Loro A1, Mohigefer Barrera J2, Herrera Justiniano JM1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 2UGC Anatomía Patológica. Complejo Hospitalario Regional Virgen del Rocío, Sevilla.
Palabras clave: tumor neuroendocrino, síndrome de cushing, enfermedad de crohn.
Introducción
La enfermedad inflamatoria intestinal (EII) asocia un riesgo aumentado de desarrollo de neoplasias gastrointestinales. El subtipo más frecuente es el adenocarcinoma. El desarrollo de tumores neuroendocrinos (TNE), aunque mucho menos frecuente, también presenta una mayor incidencia en pacientes con EII respecto a la población general.
Caso clínico
Varón de 62 años con enfermedad de Crohn (EC) ileal en tratamiento con azatioprina desde 2018, aún con datos de actividad en 2020 pero sin seguimiento posterior.
Consulta por dolor abdominal y edema en miembros inferiores (MMII). Analíticamente destaca hipopotasemia moderada (2,5 mEq/L) e hiperbilirrubinemia leve (1,33 mg/dl). La ecografía abdominal mostró múltiples lesiones hepáticas sugestivas de metástasis y datos de ileitis, con dos colecciones adyacentes al íleon, hallazgos confirmados por por TC.
Se inició corticoterapia y antibioterapia, mejorando la clínica abdominal y los reactantes de fase aguda. Sin embargo, el paciente presentaba hipernatremia, hipopotasemia, e hiperglucemia junto con HTA y edema en MMII.
Una RM de abdomen mostró un engrosamiento asimétrico en íleon, sospechoso de tumor primario y lesiones hepáticas sugestivas de metástasis. La ileocolonoscopia evidenció alteraciones propias de EC. Se decidió realizar biopsia hepática que demostró infiltración por TNE de células grandes.
Se solicitaron niveles de corticotropina (ACTH) en sangre y, ante cifras >1500 pg/mL, se sospechó síndrome de Cushing (SC) ectópico iniciándose tratamiento con ketoconazol.
Poco después el paciente sufrió una hemorragia digestiva baja inestabilizante con necesidad politransfusional asumiéndose, como origen, la tumoración ileal. Por ello, se realizó resección quirúrgica urgente y estudio histopatológico, que confirmó la presencia de TNE grado 3. Tras múltiples complicaciones postoperatorias, el paciente falleció.
Discusión
Los TNEs son un grupo heterogéneo de tumores cuya localización más frecuente es el tracto gastrointestinal (TGI) y páncreas, seguido de la pulmonar. Algunos TNE diferenciados pueden proliferar rápidamente y producir metástasis a distancia. Por su baja incidencia, heterogeneidad y bajo índice de sospecha, siguen siendo una entidad de diagnóstico tardío en muchos casos.
El SC paraneoplásico es causado por producción tumoral ectópica de ACTH o su hormona liberadora (CRH) y supone un 10% de los casos. Es más común en TNEs y carcinoma microcítico pulmonares, y extremadamente infrecuente en TNEs del TGI.
Los TNEs digestivos de yeyuno e íleon metastásicos tienen una baja tasa de supervivencia, pero la resección del tumor primario aporta beneficios significativos. Sin embargo, el SC paraneoplásico precipita peores resultados por mayor tasa de complicaciones.
CP-159. SÍNDROME DEL CASCANUECES, UNA ENTIDAD INFRECUENTE CAUSANTE DE DOLOR ABDOMINAL
Bracho González M, Bravo Aranda AM, Morales Bermúdez AI, Jiménez Pérez M
UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: dolor abdominal, síndrome del cascanueces, congestión pélvica.
Introducción
El dolor abdominal es uno de los principales motivos de consulta a urgencias. Existe una amplia variedad de patologías que pueden causarlo. Presentamos dos casos clínicos con diagnóstico de síndrome del cascanueces, una entidad infrecuente que cursa con dolor abdominal.
Caso clínico
En el primero de ellos se trata de un hallazgo incidental en TC abdominal con contraste realizado en una mujer de 45 años, fumadora, con antecedentes quirúrgicos de apendicectomía y resección ileocecal por obstrucción intestinal en 2012, con diagnóstico posterior de enfermedad de Crohn ileal en tratamiento de mantenimiento con infliximab. La TC se realizó por dolor abdominal y describía varices pélvicas de predominio izquierdo y disminución de calibre de la vena renal izquierda a su paso entre la aorta y la AMS, con diagnóstico de síndrome del cascanueces, además de inflamación de ileon terminal. En este caso se decidió actitud expectante del síndrome, con manejo de su enfermedad inflamatoria intestinal asociando budesonida oral, con buena respuesta y control del dolor.
El segundo caso trata de una mujer de 47 años, con dolor hipogástrico y en flanco izquierdo de meses de evolución y refractario a analgesia domiciliaria, con necesidad de ingreso hospitalario para control sintomático y estudio. Se realiza esofagogastroduodenoscopia y colonoscopia sin hallazgos que justifiquen el dolor, serología de celiaquía y estudio de heces negativos, calprotectina fecal normal, enteroRM sin alteraciones y valoración ginecológica que descarta patología ginecológica. Continúa estudio ambulatorio por Cirugía Digestiva planteando laparoscopia exploradora, pero solicitan TC abdominal previo, que describe atrapamiento de la vena renal izquierda en la pinza aortomesentérica con formación retrógrada de varices retroperitoneales y pélvicas, compatible con síndrome del cascanueces. Finalmente, se realiza flebografía y posterior embolización de vena ovárica izquierda, tras lo cual la paciente refiere mejoría franca del dolor abdominal.
Figura 1
Corte axial de TC de abdomen, donde se evidencia atrapamiento de la vena renal izquierda en la pinza aortomesentérica (flecha blanca), con dilatación posterior de la vena renal izquierda (línea verde)
Discusión
El síndrome del cascanueces es una entidad infrecuente, más habitual en mujeres que rondan la 4ª década de vida. Se manifiesta habitualmente por dolor en flanco izquierdo, pudiendo acompañarse de hematuria macro o microscópica y sintomatología de congestión pélvica. Su manejo puede variar desde vigilancia hasta procedimientos quirúrgicos (transposición de la vena renal izquierda o autotrasplante de riñón izquierdo), angioplastia con balón o colocación de stents intra o extravasculares. Nuestro caso enfatiza la necesidad de estar alerta al reconocimiento radiológico de esta entidad, y muestra dos opciones terapéuticas opuestas según los casos y su severidad.
CP-160. SÍNDROME DEL LIGAMENTO ARCUATO. THE ARCUATE LIGAMENT SYNDROME.
Bailón Gaona MC, Berdugo Hurtado F, Moreno Barrueco M, Barrientos Delgado A
Servicio Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: ligamento arcuato, síndrome dunbar, dolor abdominal.
Introducción
El síndrome del ligamento arcuato medio (SLAM) o síndrome de Dunbar es una afección infrecuente causada por la compresión extrínseca del tronco celíaco por parte del ligamento arcuato medio. Este ligamento, que une ambos pilares del diafragma a ambos lados del hiato aórtico, frecuentemente presenta una localización craneal al tronco celíaco. Sin embargo, en algunas ocasiones el origen del ligamento es más bajo o el origen del tronco celíaco es más alto, causando una angulación y estrechez de este último en su porción proximal, que se hace más evidente durante la espiración.
Caso clínico
Mujer de 70 años sin antecedentes de interés ni consumo de tóxicos ni fármacos, que consulta por cuadro de epigastralgia de predominio postprandial de larga data que en los últimos días no cede con analgesia y se acompaña de sensación nauseosa e hiporexia.
Se le realiza una analítica sin alteraciones destacables y una TC de abdomen con contraste donde se evidencia una estenosis en el origen del tronco celiaco en una extensión de 13 mm con calibre posterior ligeramente dilatado (Figuras 1 y 2), en relación con síndrome de compresión por ligamento arcuato medio, que provoca una estenosis en el límite de la significación (57 %).
Dada la respuesta clínica a la analgesia y la ausencia de gravedad en las pruebas complementarias realizadas, se decide proseguir con una actitud conservadora.
Discusión
El SLAM es una patología poco frecuente que en algunos individuos puede comprometer el flujo sanguíneo, siendo la gravedad de la estenosis lo que justificaría la condición de isquemia intestinal y los síntomas gastrointestinales.
La mayor parte de los casos han sido descritos en mujeres jóvenes y delgadas, aunque este diagnóstico no debe descartarse en pacientes que no cumplan estas condiciones, como en nuestro caso. Este diagnóstico ha de tenerse en cuenta ante un dolor abdominal que empeora con las comidas y el ejercicio y presenta mejoría con la dorsoflexión. No obstante, este debe hacerse siempre por exclusión, después de haber descartado otras causas de dolor abdominal.
La angio-TAC y RM son las técnicas diagnósticas de elección, ya que permiten determinar la gravedad del caso en función del diámetro el tronco celíaco y la existencia de colaterales y/o aneurismas. La edad y la gravedad del paciente condicionan la necesidad de tratamiento conservador mediante analgesia, como en el caso expuesto, o la necesidad de cirugía, en casos recurrentes o que no presenten mejoría con tratamiento médico.
CP-161. SÍNDROME FEMOROCUTÁNEO: UNA CAUSA INFRECUENTE DE DOLOR ABDOMINAL
Rodríguez Mateu A, Plaza Fernandez A, Moreno Moraleda I
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: meralgia parestésica, síndrome femorocutáneo, trombosis vena epigástrica.
Introducción
El síndrome femorocutáneo, también llamado meralgia parestésica, se caracteriza por la presencia de dolor y alteraciones de la sensibilidad (tales como hipoestesia o disestesias) en la cara anterolateral del muslo por afectación del nervio femorocutáneo lateral. La etiología suele ser compresiva pudiendo ocurrir en cualquier punto desde su salida del plexo lumbar, en su trayecto por la cavidad abdominal y ligamento inguinal o, incluso, a nivel del muslo.
Caso clínico
Se presenta el caso de una mujer de 74 años con antecedente de hemocromatosis que ingresa para estudio de dolor en fosa iliaca derecha irradiado a región inguinal y fiebre de 38 ºC de una semana de evolución.
En la analítica al ingreso únicamente destaca una PCR de 14 mg/dl. Inicialmente, se solicitó un TC abdominal con contraste que informó de diverticulosis en sigma ya conocida, sin signos de diverticulitis. Para descartar otros orígenes del dolor se realizó tanto una gastroscopia como una colonoscopia, siendo ambas normales.
Y, finalmente, para completar el estudio se decidió realizar una ecografía de pared abdominal, la cual evidenció un incremento del calibre de los vasos epigástricos inferiores alrededor del nervio femorocutáneo lateral derecho, sin evidenciar señal doppler a este nivel. El cuadro era compatible con un síndrome femorocutáneo secundario a trombosis de la vena epigástrica inferior derecha (Figuras 1 y 2).
Tras comentar el caso con el servicio de Hematología, se inicia tratamiento anticoagulante y se controla la sintomatología con analgesia convencional, por lo que se decide alta hospitalaria y seguimiento en consultas externas.
Discusión
La importancia de este caso radica, en primer lugar, en la poca evidencia que existe en la bibliografía acerca de la etiología vascular en el síndrome femorocutáneo. En segundo lugar, en incluir esta entidad en el diagnóstico diferencial de las distintas causas de dolor abdominal, especialmente si existen factores de riesgo (en nuestro caso, la hemocromatosis).
Su diagnóstico suele demorarse ya que es fundamentalmente clínico y muchas veces puede solaparse con síntomas propios de otras enfermedades. En algunas ocasiones, como en nuestro caso, pueden ser necesarias distintas pruebas complementarias para alcanzar un diagnóstico.
Su tratamiento consiste fundamentalmente en medidas conservadoras que eviten la compresión del nervio, así como control del dolor. Al ser este de tipo neuropático, el papel de fármacos antiepilépticos como terapia aditiva a la analgesia convencional será fundamental.
CP-162. ÚLCERAS RECTALES EN PACIENTE CON ENFERMEDAD DE BEHÇET
Palomino Luque P1, Flores Moreno H1, Bracho González M2
1Servicio Aparato Digestivo. Hospital Comarcal de la Axarquía, Vélez-Málaga. 2UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: behçet, rectorragia, úlcera.
Introducción
La Enfermedad de Behçet es una vasculitis sistémica autoinflamatoria de curso remitente-recurrente y etiología desconocida que puede afectar a distintos órganos en diferentes momentos de su historia natural. El patrón clásico de presentación consiste en úlceras genitales, afectación ocular y lesiones cutáneas; sin embargo, la frecuencia de manifestaciones articulares, gastrointestinales y del sistema nervioso central han ido aumentando progresivamente.
Caso clínico
Mujer de 73 años con antecedentes personales de Enfermedad de Behçet HLA-B51-negativo diagnosticada por aftas orales a la que se le realizó una endoscopia digestiva baja por clínica de rectorragia, atribuida a patología hemorroidal, despeños diarreicos aislados, y aumento de actividad metabólica en sigma y recto en PET-TC solicitado por neumología dentro del estudio de un nódulo pulmonar solitario. En la colonoscopia se evidenciaron úlceras rectales profundas y serpiginosas (Figura 1). Las biopsias fueron informadas como “inflamación aguda y tejido de granulación de fondo de úlcera” pautándose enemas de budesonida con mejoría sintomática. Al mes de finalizar al tratamiento consultó en el servicio de urgencias por clínica de proctalgia y pujos, pautándose corticoterapia oral con resolución del cuadro y mejoría de las úlceras en la endoscopia de control (Figura 2).
Discusión
La incidencia de afectación gastrointestinal no es baja y se encuentra infradiagnosticada debido a que hasta el 60% puede ser asintomática. La presentación clínica más frecuente es el dolor abdominal, con o sin diarrea, la odinofagia o el dolor retroesternal. Un 30% presentan complicaciones como hemorragia o perforación. Puede presentarse a lo largo de todo el tubo digestivo siendo más prevalente a nivel ileocecal, y menos en el tracto digestivo superior. En pacientes asintomáticos ha de sospecharse cuando exista PCR elevada y fiebre, siendo menos frecuente en pacientes con uveítis. En su diagnóstico diferencial se encuentran la enfermedad de Crohn, la tuberculosis intestinal y las úlceras por AINEs. Las úlceras se caracterizan por ser ovales, profundas y en número menor a 6. La histología es inespecífica, siendo frecuente el infiltrado neutrofílico, y el tratamiento consiste en corticoesteroides, aminosalicilatos, inmunomoduladores y fármacos biológicos.
CP-163. VÓLVULO DE SIGMA SECUNDARIO A GLOBO VESICAL, UNA ETIOLOGÍA INFRECUENTE.
Soler Góngora M, López Peña C, Ortiz Sánchez A, García Verdejo FJ
Servicio Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: vólvulo, sigma, globo vesical.
Introducción
Presentamos el caso de un paciente con un vólvulo de sigma incompleto secundario a compresión por globo vesical, caso que nos parece de interés por lo infrecuente de la etiología.
Caso clínico
Varón de 74 años con antecedentes personales de hipertensión arterial, diabetes mellitus tipo 2, adenocarcinoma de sigma estadio IIIc tratado mediante sigmoidectomía y quimioterapia adyuvante en 2005 (actualmente en remisión) y en seguimiento en Neurología por degeneración frontotemporal con Parkinsonismo en tratamiento con levodopa/carbidopa.
Acude a Urgencias por diarrea de casi un mes de evolución, sin productos patológicos, sin vómitos, con hiporexia y con fiebre de hasta 38º los primeros días. A su vez, asociaba recorte de diuresis en las últimas 48h y disminución de ventoseo.
En la exploración abdominal destaca distensión abdominal junto con defensa voluntaria generalizada y analíticamente no se hallaron datos de interés salvo un leve incremento de reactantes de fase aguda.
Se realiza radiografía abdominal que muestra dilatación de asas a nivel de sigma/colon descendente (Imagen 1).
A continuación, se solicita TC abdominal (Imágenes 2 y 3) que muestra distensión marcada del sigma, que alcanza los 9 cm de diámetro aproximado junto con hiperdistensión vesical (600 cc de contenido) que contacta lateralmente con el segmento de sigma alargado. Distorsión sigmoidea que podría estar causada por compresión del globo vesical o en relación con vólvulo de sigma incompleto.
Se instaura manejo conservador con sondaje rectal y vesical siendo efectivos con resolución espontánea del cuadro.
Discusión
El vólvulo de sigma ocurre debido a una torsión del colon sigmoide sobre su mesenterio, pudiendo generar un cuadro de obstrucción intestinal e isquemia a dicho nivel.
Aunque no está claramente establecida la etiología del cuadro, se cree que factores anatómicos (como un sigma largo y redundante con un corto anclaje mesentérico), junto con factores relacionados con la dismotilidad del colon (estreñimiento, largo tránsito, enfermedad de Hirschprung…) pueden estar relacionados.
Sin embargo, apenas existen casos documentados de volvulación secundaria a compresión extrínseca vesical.
En cuanto las medidas terapéuticas iniciales está la colocación de sondaje rectal, pudiendo optar posteriormente por la colonoscopia descompresiva o en última instancia a la cirugía, sobre todo si se sospechan complicaciones sobreañadidas como isquemia intestinal, necrosis o perforación.
El desencadenante en nuestro paciente fue una retención urinaria en probable relación con su patología neurológica de base, que pudo ser resuelta de forma conservadora al no condicionar una volvulación completa.
CP-164. VÓLVULO SIMULTÁNEO DE CIEGO Y SIGMA COMO CAUSA RARA DE OBSTRUCCIÓN INTESTINAL
Calderón Chamizo M, Naranjo Pérez A, Ternero Fonseca J, Quirós Rivero P, Gómez Delgado E, Maraver Zamora M
Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Juan Ramón Jiménez, Huelva.
Palabras clave: vólvulo, ciego, sigma..
Introducción
El vólvulo es la torsión axial de un segmento móvil del colon alrededor de su mesenterio, siendo las localizaciones más frecuentes en sigma (75%) y en ciego (22%). Son entidades independientes describiéndose el vólvulo simultáneo de sigma y colon como una causa rara de obstrucción intestinal (alrededor de 10 casos publicados hasta la fecha).
Caso clínico
Varón de 66 años sin antecedentes de interés salvo episodio 6 meses antes de obstrucción colónica secundaria a vólvulo de sigma no complicado que se resolvió endoscópicamente, perdiendo seguimiento posterior. Acude a Urgencias por dolor abdominal de 3 días de evolución acompañado de estreñimiento y distensión abdominal progresiva. No fiebre, no nauseas, no vómitos ni ninguna otra sintomatología. Analíticamente, ningún hallazgo a destacar. En cuanto a las pruebas de imagen, se solicita radiografía de abdomen en la cual se aprecian niveles hidroaéreos sugestivos de obstrucción intestinal. Posteriormente, se realiza TAC de Abdomen urgente confirmándose el diagnóstico de obstrucción intestinal secundaria a vólvulo de sigma (dolicosigma) tipo mesentérico axial, apreciándose el signo del remolino, y dispuesto por encima del colon transverso, sin datos de hipoperfusión ni isquemia.
Se procede a la desvolvulación endoscópica, encontrándose a unos 20 cm del margen anal frunce de mucosa colónica de aspecto normal, sin datos de isquemia, que se sobrepasa sin dificultad, pasando a gran cavidad repleta de heces semisólidas que se intentan aspirar sin éxito, con empeoramiento progresivo de la distensión abdominal. Se avanza y parece observarse otro frunce más arriba que no se logra sobrepasar. El paciente comienza a vomitar y, ante el riesgo de broncoaspiración, se procede a colocación de SNG y se realiza tratamiento quirúrgico urgente. Intraoperatoriamente, se confirma la presencia simultánea de un vólvulo de ciego y sigma y una llamativa dilatación colónica sin signos de complicación (no isquemia ni perforación), llevándose a cabo una colectomía total más ileostomía, con buena evolución clínica postoperatoria.
Discusión
El vólvulo de sigma es una entidad con características clínicas y radiológicas fáciles de reconocer; sin embargo, hay casos en los que el signo radiográfico del "grano de café", enmascara la aparición simultánea del vólvulo de ciego siendo el diagnóstico preoperatorio muy difícil, requiriendo un alto índice de sospecha (probablemente no fue inicialmente evidente en el TAC debido al efecto masa ejercido por el sigma agrandado). Es importante diferenciar ambos frunces pues la descompresión endoscópica del proximal puede ser peligrosa pudiendo provocar complicaciones como la perforación.

 Descargar número completo
Descargar número completo Download full issue
Download full issue