CITA ESTE TRABAJO
García García MD, Gómez Rodríguez BJ. Tratamiento erradicador en la infección por Helicobacter Pylori. 2023;46(1):16-25.
Introducción
Recientemente se han publicado hasta siete consensos o guías de actuación sobre el tratamiento de la infección por H. pylori con recomendaciones distintas[1]-[8].
Sin embargo, en general coinciden en determinadas recomendaciones generales como son el uso de cuatro fármacos y el hecho de que, a mayor inhibición del ácido, mayor eficacia del tratamiento. Esta revisión pretende hacer unas recomendaciones razonables y prácticas a partir de los distintos consensos, basándonos principalmente en las desarrolladas en el consenso del 2021.
Recomendaciones generales de tratamiento
Al considerarse la gastritis crónica asociada a H. pylori una enfermedad infecciosa en los últimos consensos a nivel nacional e internacional, se considera que debe tratarse a todos los pacientes diagnosticados de la infección, independientemente de su clínica. Las estrategias actuales óptimas deben alcanzar un éxito erradicador como mínimo del 90% de los casos tratados.
La evidencia acumulada en los últimos años sugiere que las terapias triples utilizando un IBP y dos antibióticos obtienen generalmente resultados subóptimos[9],[10]. Por este motivo la mayoría de los tratamientos actualmente recomendados en series amplias en práctica clínica incluyen cuatro fármacos, añadiendo un tercer antibiótico o bismuto[11],[12].
También durante los últimos años se ha acumulado una notable evidencia que demuestra que cuanto más intensa es la inhibición ácida, más efectivo es el tratamiento de la infección por H. pylori. Esomeprazol 40 mg cada 12 horas ofrece la inhibición ácida más potente con un número mínimo de comprimidos[13]. Sin embargo, el coste relativamente elevado frente al omeprazol, hace que no quede claro que esta pauta sea coste-efectiva y que, por tanto, se pueda recomendar de forma generalizada.
Los tratamientos de rescate no deben incluir aquellos antibióticos que se hayan utilizado en primera línea y a los que H. pylori desarrolla resistencia con facilidad[14]. En concreto, no debemos repetir claritromicina ni ciprofloxacino. En cambio, en un tratamiento de rescate podemos utilizar de nuevo amoxicilina o tetraciclinas porque la probabilidad de que H. pylori desarrolle resistencia es prácticamente nula. Aunque generalmente aparecen resistencias secundarias tras un primer tratamiento, puede repetirse metronidazol si se usa a dosis altas y durante más de 10 días, ya que en este caso pueden superarse estas resistencias y se obtienen tasas razonables de curación[15].
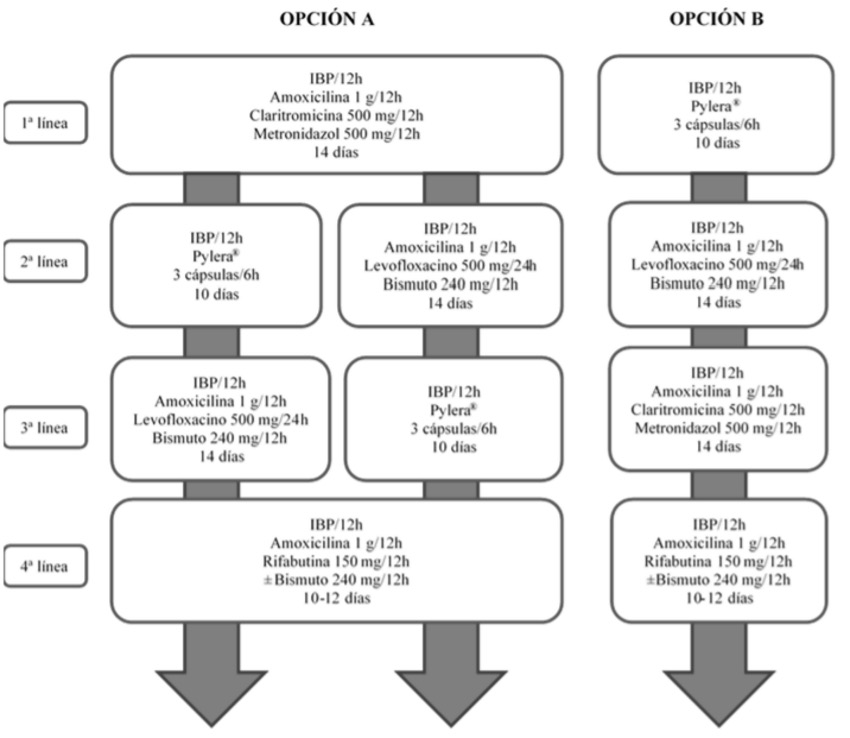
En la tabla 1 y figura 1 se resumen las terapias erradicadoras, sus posologías y los esquemas de tratamiento actuales.
Tabla 1
Terapias erradicadoras y sus posologías.
Tratamiento de primera línea
Actualmente, no se recomienda el tratamiento triple clásico con un inhibidor de la bomba de protones (IBP), claritromicina y amoxicilina (OCA), dada la variabilidad de su eficacia, que, en la mayoría de las series recientes, no llega al 80%; ni utilizando terapias clásicas optimizadas (con duración de 14 días y con dosis doble de IBP) (Tabla 2) [16],[17].Los dos tratamientos que se recomiendan como de elección son la terapia cuádruple concomitante durante 14 días o laterapia cuádruple clásica con bismuto durante 10 días (BMT tres-en-uno)[2],[3],[11],[18]. Otra opción eficaz podría ser añadir bismuto a la triple terapia clásica[19].
Tabla 2
Estudios que han evaluado la eficacia de la terapia triple con un inhibidor de la bomba de protones (IBP), amoxicilina y claritromicina en España desde 2007 a 2012.
| Autores | Tipo de publicación | Año de publicación | Ciudad | N | Eficacia PP | Eficacia IT | IBP y dosis |
| Artaza Varasa et al.[9] | Artículo | 2008 | Toledo | 27 | 81% | 81%a | R 20 mg/12h |
| Molina Infante et al.[10] | Artículo | 2010 | Cáceres | 115 | 66% | 64%a | O 20 mg/12h |
| Cuadrado Lavín et al.[11] | Artículo | 2012 | Laredo | 128 | 78% | 78%a | O 20 mg/12h |
| Molina Infante et al.[12] | Artículo | 2012 | Cáceres | 33 | 74% | 70%a | O 20 mg/12h |
| Cosme et al.[13] | Artículo | 2013 | San Sebastián | 104 | 49%a | O 20 mg/12h | |
| García Fernández et al.[14] | Resumen | 2008 | Sevilla | 248 | 63,3% b 67,7% a | O, ne | |
| Pérez Pastor et al.[15] | Resumen | 2008 | Sevilla | 333 | 62,9% b 69,9% a | O, ne | |
| Irisarri Garde et al.[16] | Resumen | 2009 | Pamplona | 521 | 81,5% b 80% a | O, ne | |
| Guardiola Arévalo et al.[17] | Resumen | 2010 | Toledo | 46 | 73,9% a | R 20 mg/12h | |
| Irisarri Garde et al.[18]> | Resumen | 2011 | Pamplona | 463 | 72,7% b 72,4% a | O, ne | |
| Guardiola Arévalo et al.[19] | Resumen | 2011 | Toledo | 50 | 78% a | R 20 mg/12h | |
| Ibáñez et al.[20] | Resumen | 2011 | Oviedo, Avilés | 375 | 69,1% a | O, ne | |
| Campillo Arregui et al.[21] | Resumen | 2012 | Tudela | 353 | 61,5%b 70,7%a | O, ne | |
| Romero Ordóñez et al.[22] | Resumen | 2012 | Marbella | 351 | 71,4%b 80,7%a | O, ne |
Ambos tratamientos han demostrado eficacias iguales o superiores al 90% en estudios bien diseñados y un reciente metaanálisis[20]. Las ventajas de la terapia cuádruple clásica es que requiere sólo dos fármacos, el IBP y BMT tres-en-uno (un fármaco que incluye metronidazol, tetraciclina y bismuto en una sola cápsula) y es por tanto más fácil de prescribir y explicar. Sus inconvenientes son a) que la evidencia de su eficacia en nuestro medio es más limitada que la de la cuádruple sin bismuto, b) el precio es moderadamente más caro que la cuádruple concomitante y c) el hecho de que BMT tres-en-uno debe administrarse cuatro veces al día según ficha técnica.
No obstante, algunos de estos inconvenientes ya no lo son con los datos de estudios publicados recientemente sobre práctica clínica en España. En éstos, la eficacia (alrededor del 95%) y la adherencia al tratamiento (98%) han sido muy satisfactorios[21]-[24]. Otros estudios recientes administrando BMT tres-en-uno tres veces al día, obtienen unas tasas de efectividad del 95%, con el mismo cumplimiento y tolerancia que el esquema de cuatro veces al día[25],[26].
La terapia cuádruple concomitante, por su parte, se administra dos veces al día. En nuestro entorno la eficacia parece similar a la de la terapia cuádruple clásica con bismuto durante 10 días (BMT tres-en-uno). Además, ha demostrado su eficacia en situación de práctica clínica en un estudio multicéntrico. La eficacia de la terapia cuádruple concomitante en este estudio fue del 93%[27]. Sus inconvenientes son a) la duración más larga y b) el hecho de que se tenga que prescribir cada uno de sus componentes por separado lo que la hace más difícil de prescribir y explicar. En la tabla 3 se encuentran los estudios que han demostrado la eficacia de la terapia cuádruple sin bismuto en España[2].
Tabla 3
Estudios españoles que han evaluado la eficacia de la terapia cuádruple sin bismuto concomitante de primera línea en España.
Los efectos adversos son moderados y parecen similares con ambos tratamientos. Son parecidos a los de la terapia triple y pueden incluir mal sabor de boca, náuseas y vómitos y raramente síndrome diarreico. Además, se debe advertir al paciente específicamente de que cuando se toma bismuto, las heces pueden ser de color oscuro.
Tratamiento de segunda línea
En la actualidad se recomienda una pauta cuádruple con IBP a dosis altas, levofloxacino, amoxicilina y bismuto como tratamiento de rescate cuando falla el tratamiento inicial, sea una pauta concomitante o BMT tres-en-uno[2],[3].
La terapia triple con un IBP, amoxicilina y levofloxacino durante 10 días obtiene tasas de curación insuficientes, con un 74% de media[1],[7]. Por ello, aunque el número de estudios es limitado, es razonable recomendar una pauta cuádruple con IBP a dosis altas, levofloxacino, amoxicilina y bismuto como tratamiento de rescate cuando el tratamiento inicial que ha fallado es una pauta concomitante o la terapia cuádruple clásica con bismuto durante 10 días (BMT tres-en-uno). Un estudio observacional bien diseñado demostró tasas de curación superiores al 90%. Aunque se trata de un único estudio, los resultados son congruentes con la clara evidencia de que, al añadir bismuto a los tratamientos triples con levofloxacino se mejora su tasa de curación en aproximadamente un 10%. En la tabla 4 y 5 se muestran los estudios que avalan la eficacia de esta pauta erradicadora[3],[28].
Tabla 4
Estudios que evalúan la eficacia de la combinación de IBP, amoxicilina, levofloxacino y bismuto para la erradicación de la infección por Helicobacter Pylori.
Tabla 5
Eficacia de la combinación amoxicilina, levofloxacino y bismuto como segunda línea de tratamiento erradicador para H. pylori.
| Eficacia | Número de pacientes | Porcentaje (95% intervalo de confianza) |
| Intention-to-treat | 180/200 | 90 (86-94) |
| Pre-protocol | 175/192 | 91.1 (87-95) |
Otras alternativas actuales igualmente eficaces tras el fracaso de la terapia concomitante, sería la terapia cuádruple con BMT tres-en-uno[22],[24]; y si el fallo fue con este último, terapias triples con IBP a dosis altas, amoxicilina y quinolonas (levofloxacino/moxifloxacino) durante 14 días[12].
Tratamiento de rescate tras dos fracasos de tratamiento
Dada la alta eficacia de los tratamientos previos, el tratamiento de rescate debería ser administrado de manera excepcional. Se debe replantear la indicación del tratamiento erradicador y evaluar a fondo la adherencia al tratamiento. Si finalmente se acuerda con el paciente, indicar un tercer tratamiento, hay una serie de normas, ya comentadas previamente, que se deben tener en cuenta:
a) No se pueden utilizar ni levofloxacino ni claritromicina si se han utilizado en tratamientos previos ya que las cepas que sobreviven habrán adquirido resistencia a estos antibióticos y el tratamiento de rescate no sería eficaz. En cambio, se puede utilizar metronidazol dado que se ha observado que un porcentaje alto de pacientes con resistencia in vitro curan la infección siempre que se administren tratamientos de más de 10 días y dosis altas de estos antibióticos o amoxicilina, antibiótico al que pylori desarrolla resistencias solo excepcionalmente.
b) En caso de que la terapia inicial fuera la cuádruple concomitante y la segunda la cuádruple con levofloxacino y bismuto, se recomienda utilizar rescate con BMT tres-en-uno 10 días; o cuádruple clásica con bismuto con tetraciclina o doxiciclina 14 días (con una eficacia de erradicación del 81%)[29].
c) En el caso de que se haya utilizado terapia concomitante de primera línea y BMT tres-en-uno de segunda, se recomienda utilizar una cuádruple con levofloxacino y bismuto (que alcanza una tasa de curación del 80%). Finalmente, tras el fracaso de BMT tres-en-uno y una segunda pauta con levofloxacino se puede utilizar cuádruple concomitante o una combinación de IBP a dosis altas, amoxicilina, metronidazol y bismuto[30].
Tratamiento de cuarta línea
Tras tres fracasos de tratamiento se recomienda persistir en el tratamiento de la infección sólo en pacientes con indicación muy clara - úlcera, especialmente con hemorragia, o linfoma MALT, por ejemplo- o en pacientes que realmente estén altamente motivados para hacer un cuarto tratamiento después de una información adecuada. Se debe evaluar muy cuidadosamente tanto la adherencia a tratamientos previos como la adherencia esperada a un nuevo tratamiento. Muchos de los pacientes con tres fracasos (y más con las terapias altamente efectivas que se recomiendan actualmente) presentarán problemas de adherencia al tratamiento.
Si finalmente se acuerda con el paciente un cuarto tratamiento y consideramos que la probabilidad de una buena adherencia es alta, la pauta recomendada incluye IBP, amoxicilina, rifabutina y bismuto. Rifabutina es un análogo de la rifampicina, con baja tasa de resistencias y cuyo principal efecto adverso es la mielotoxicidad, que suele ser autolimitada tras la finalización del tratamiento. En la tabla 6 se presentan los estudios en los que se ha usado rifabutina como terapia de rescate[31].
Tabla 6
Terapias erradicadoras para H. pylori que contienen rifabutina en pacientes en los que se han realizado al menos tres tratamientos erradicadores fallidos.
En caso de que el clínico tenga dudas o no se encuentre cómodo con el tratamiento de rescate, debe plantearse enviar estos pacientes para evaluación a un centro especializado.
Tratamientos en alergia a penicilina
En los pacientes alérgicos a la penicilina, se desaconseja emplear como primera línea una combinación triple con IBP, claritromicina y metronidazol. El tratamiento de elección es cuádruple con bismuto (clásica o BMT tres-en-uno) con efectividad de hasta el 91% (Tabla 7).
Tabla 7
Primera línea de tratamiento para la erradicación de H. pylori en pacientes alérgicos a la penicilina en el “Registro europeo de manejo de H. pylori”.
Como tratamiento de rescate, se podrían usar dos terapias que muestran una eficacia similar: tras el fracaso de una terapia triple se puede usar la terapia cuádruple con bismuto (78%); mientras que si ha fracasado un primer tratamiento con terapia cuádruple con bismuto la alternativa de rescate sería una terapia cuádruple con IBP, levofloxacino, claritromicina y bismuto[2].
Otros aspectos del tratamiento
a) En este momento el cultivo no tiene un papel relevante en el manejo de la infección en la práctica clínica. No se ha demostrado que sea superior a la asociación de terapias empíricas altamente eficaces como las actualmente recomendadas. Además, recientemente se ha comunicado que las resistencias en adultos naïve mantiene una tendencia lineal estable para todos los antibióticos usados habitualmente[32].
b) Existen pocos estudios controlados que hayan evaluado la utilidad de los probióticos como coadyuvantes a los efectos secundarios de las terapias cuádruples, por tanto, en la actualidad no se recomienda su utilización sistemática en la práctica clínica[33].
c) Se debe advertir al paciente de los posibles efectos secundarios del tratamiento, ya que son frecuentes con todos los regímenes erradicadores, oscilando entre el 15% y el 35% en series amplias. Habitualmente son leves y de duración limitada, por lo que no suelen ser relevantes en el cumplimiento[34].

 Descargar número completo
Descargar número completo Download full issue
Download full issue