CITA ESTE TRABAJO
Pereira Martinez J, Ruiz Sánchez A, Herrería Fernández I, Sousa Martín JM. Una oportunidad al Ritumab en el síndrome de solapamiento de colangitis biliar primaria y hepatitis autoinmune. RAPD 2026;49(1):33-35. DOI: 10.37352/2026491.5
Introducción
La hepatitis autoinmune (HAI) y la colangitis biliar primaria (CBP) son enfermedades de origen autoinmune poco frecuentes[1]. En los casos en que ambas entidades coinciden en un mismo paciente se denomina síndrome de solapamiento HAI-CBP[2]. Su presentación clínica es variable, siendo en ocasiones el diagnóstico difícil, usándose habitualmente los criterios de París[2][3]. El tratamiento se basa en inmunosupresores en el caso de HAI y ácido ursodesoxicólico para CBP[4]. Generalmente la inmensa mayoría de los pacientes con síndrome de solapamiento HAI-CBP suelen responder adecuadamente al tratamiento con inmunosupresores y ácido ursodeoxicólico[5]. No obstante, no es despreciable el porcentaje de pacientes en los que el tratamiento estándar puede ser infausto, de hasta 40% en pacientes con cirrosis y un 27% en pacientes que no la tienen[6]-[7]. Hay diversos fármacos utilizados en los casos de fallo terapéutico, entre los que destaca micofenolato de mofetilo, inhibidores de la calcineurina y fármacos biológicos (como rituximab o infliximab).
Caso clínico
Varón de 57 años diagnosticado en 1992 de CBP por biopsia hepática tras estudio por alteración colestásica persistente con anticuerpos antimitocondriales negativos, iniciándose tratamiento con ácido ursodesoxicólico con adecuada respuesta inicial.
En 1998 presentó una crisis hepatocelular severa con elevación marcada de transaminasas y positividad para anticuerpos anti-LKM, estableciéndose el diagnóstico de síndrome de solapamiento HAI-CBP. En el año 2000 se inició tratamiento con azatioprina, que fue suspendido de forma inmediata por reacción de hipersensibilidad.
La evolución posterior estuvo marcada por actividad inflamatoria persistente, progresando a cirrosis hepática en 2011. Se inició entonces micofenolato mofetilo como alternativa inmunosupresora, alcanzando una respuesta parcial pero sin normalización completa de transaminasas, desarrollando corticodependencia.
Desde 2020 el paciente presentó múltiples reagudizaciones hepatocelulares que requirieron incrementos repetidos de la dosis de prednisona. Entre finales de 2022 y principios de 2023 persistía actividad inflamatoria significativa a pesar de mantener 15 mg diarios de prednisona.
Ante el fracaso de la inmunosupresión convencional y la corticodependencia mantenida, en marzo de 2023 se administraron dos dosis de Rituximab como tratamiento alternativo al habitual. En los meses posteriores se objetivó normalización progresiva de los parámetros bioquímicos hepáticos, manteniéndose la respuesta a medio plazo y permitiendo la reducción de la dosis de corticoides.
Discusión
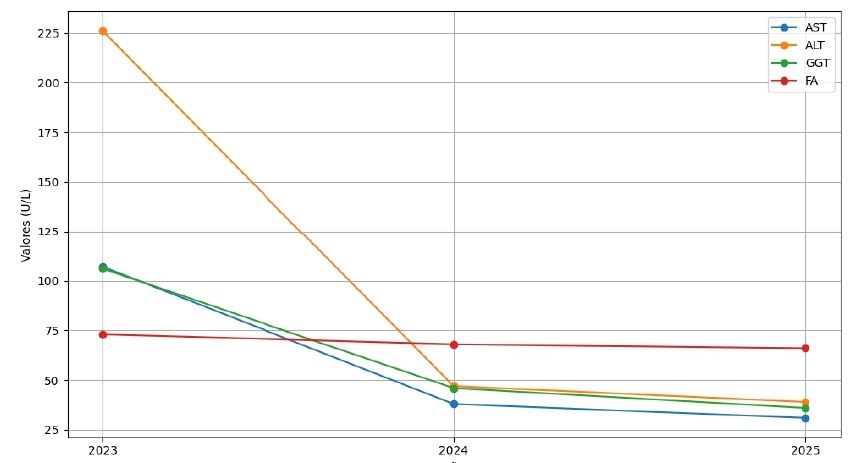
Hay escasa evidencia publicada sobre el uso de rituximab en el síndrome de solapamiento HAICBP, aunque algunos estudios sugieren su utilidad en enfermedad refractaria a terapia inmunosupresora convencional[8]-[9]. Su principal mecanismo consiste en la depleción de linfocitos B CD20+, lo que conduce a reducción de células productoras de autoanticuerpos y a una modulación de la activación inmunitaria dependiente de células B[9]. En el contexto de enfermedades inmunomediadas como el síndrome de solapamiento HAI-CBP, los linfocitos B desempeñan un papel relevante no solo como productores de autoanticuerpos (anti-LKM, AMA), sino también como células presentadoras de antígeno y moduladoras de la respuesta T autorreactiva[10]-[11]. En nuestro paciente el uso de rituximab consiguió reducir el número de crisis hepatocelulares así como la dosis de corticoides (Tabla 1, Figura 1).
Tabla 1
Evolución de bioquímica hepática y biliar, pre y post administración de rituximab. A la izquierda, dosis de corticoides en el momento de la medición analítica.
| Dosis de prednisona | Fecha | AST (U/L) | ALT (U/L) | GGT (U/L) | FA (U/L) |
| 15 mg | 2023 | 107 | 226 | 106 | 73 |
| 7.5 mg | 2024 | 38 | 47 | 46 | 68 |
| 5 mg | 2025 | 31 | 39 | 36 | 66 |
Una forma de monitorizar la eficacia del rituximab es mediante la cuantificación de linfocitos CD19. El marcador CD19 es una proteína de membrana presente en prácticamente todos los linfocitos B desde el estadio pre-B hasta el maduro (excepto células plasmáticas terminales)[12]. La depleción de linfocitos CD19+ refleja la actividad biológica del fármaco y su reaparición puede preceder a la recaída clínica[13]. En el caso de nuestro paciente se monitorizaron los niveles de linfocitos CD19 varios meses tras la administración de rituximab, siendo estos indetectables.
En conclusión, a pesar de que la evidencia es limitada, el uso del rituximab puede ser una alternativa eficaz en pacientes con síndrome de solapamiento HAI-CBP refractario a tratamiento estándar, al actuar mediante la depleción de linfocitos B y la modulación de la respuesta autoinmune. En el caso de nuestro paciente, su uso permitió reducir las crisis hepatocelulares y la dosis de corticoides, con adecuada respuesta clínico- analítica así como biológica, objetivada por la depleción mantenida de linfocitos CD19+.

 Descargar número completo
Descargar número completo Download full issue
Download full issue