Introducción
El concepto de trasplante intestinal nació de los progresos realizados en el terreno de la nutrición parenteral total, que facilitó el mantenimiento o el advenimiento de una población de "insuficientes intestinales crónicos", en los que el trasplante del "aparato de absorción" aparecía como la alternativa ideal a las complicaciones, en ocasiones mortales, de la nutrición parenteral[1], [2].
Los primeros trasplantes de intestino se realizaron a mediados de la década de los 60 del siglo pasado. A diferencia del resto de trasplantes, el trasplante intestinal se desarrolló de forma mucho más lenta, debido a complicaciones y malos resultados. Las razones de estos fracasos pudieron ser técnicos, si bien, hoy día se acepta que parece que en buena medida pudieran haber estado ligados, también, a la ineficacia de la inmunosupresión "convencional" basada en corticoides a dosis altas y azatioprina que, sin embargo, demostraba su utilidad en aquella época en el trasplante renal[2], [3].
La complejidad de las interacciones inmunológicas entre el injerto intestinal y el receptor se caracteriza porque el injerto intestinal además de inducir una reacción clásica de rechazo del aloinjerto por el huésped, genera una reacción de destrucción de los órganos del huésped por las células inmunocompetentes del donante localizadas en los ganglios mesentéricos del injerto. Es la enfermedad del injerto contra el huésped (graft versus host disease)[4].
La aparición de la ciclosporina, junto a la azatioprina demostró que estos trasplantes no solamente son viables sino que además son capaces de garantizar la digestión y la absorción de los alimentos, así como el desarrollo morfológico normal de los receptores[2], [5].
Más recientemente, el advenimiento de nuevos inmunosupresores, en particular del FK 506 y micofenolato, han permitido mejorar aún más los resultados en este tipo de trasplantes.
Por otro lado, debido al papel de protección que tiene el injerto hepático sobre el injerto intestinal, la realización de trasplantes multiviscerales en los que junto al intestino se trasplanta el hígado, han mejorado también la supervivencia de los injertos intestinales y de los enfermos trasplantados, incluso utilizando una inmunosupresión "convencional"[6], [7].
La mejora de resultados se ha acompañado de un incremento en el número de trasplantes intestinales y multiviscerales y de centros trasplantadores. Se ha pasado de una tasa de indicación de 0,1 pmp a 0,6 pmp en Estados Unidos, 0,4 pmp en Europa, siendo en España de 0,2 pmp. La menos tasa de indicaciones en nuestro pais puede estar justificada por el menor número de centros de referencia para estos trasplantes. Así, mientras que en Estados Unidos existe 1 centro por cada 17 millones de habitantes y en el resto de Europa, 1 centro por cada 20 millones, en España sólo existe 1 centro para adultos y uno para infantil (1/45 millones de habitantes).
Indicaciones
El trasplante intestinal tiene su indicación primaria en el concepto del fallo o insuficiencia intestinal.
Se considera Fallo o Indsuficiencia Intestinal cuando se produce la pérdida real o inminente de la autonomía nutricional debido a la disfunción intestinal[6], [8] (Figura 1). El tratamiento de elección inical en esta situación es la nutrición parenteral.
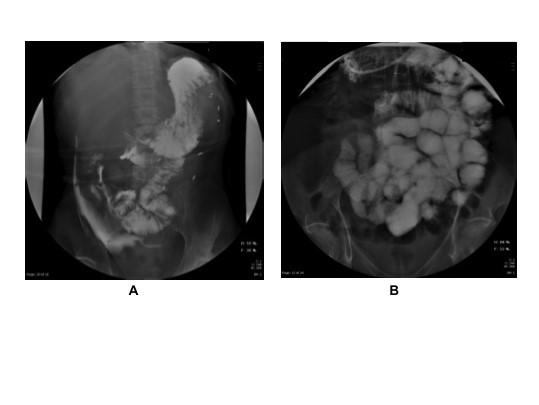
Figura 1
A.- Intestino corto en paciente multioperado por enfermedad de Chron. B.- Evaluación post-trasplante intestinal.
Muchos pacientes, particularmente aquellos con el síndrome de intestino corto, sólo requieren un soporte parenteral temporal mientras el intestino lesionado tiene un tiempo de adaptación. Sin embargo, este proceso es impredecible. En algunos pacientes, la adaptación es rápida, mientras que en otros, se necesitan años o nunca se logra[6], [8], [9], [10].
La Asociación Americana de Gastroenterología (AGA)[11] definió "fallo de la NPT" en relación al desarrollo de una o más de las siguientes complicaciones:
Fallo hepático secundario a NPT (bilirrubina sérica y/o enzimas hepáticas elevadas, esplenomegalia, trombocitopenia, varices gastroesofágicas, coagulopatía, fibrosis hepática o cirrosis.
Pérdida de al menos dos de los grandes vasos venosos centrales (subclavia, yugular, o venas femorales). Puede producirse por trombosis o por sepsis de repetición.
Sepsis recurrentes frecuentes relacionadas con las vías centrales: 2 episodios de sepsis sistémica relacionada a infección del catéter por año, un episodio de fungemia relacionado con la vía, shock séptico, o síndrome de distress respiratorio del adulto.
Requerimientos nutricionales de por vida , entendiendo por tal, a partir del segundo año de inicio de la NPT.
Mala calidad de vida secundaria al fallo intestinal. Las hospitalizaciones frecuentes por complicaciones sépticas, metabólicas o quirúrgicas, deshidrataciones severas, etc., producen una mala calidad de vida y deben ser considerados para trasplante intestinal aún en ausencia de complicacio - nes derivadas de la NTP.
Un paciente debe ser considerado para el trasplante de intestino si tiene un alto riesgo de mortalidad a pesar de la terapia de nutrición parenteral. Las situaciones que seterminan la indicación del trasplante intestinal son[12]-[15]:
La insuficiencia hepática inminente o manifiesta inducida por la NPT.
La trombosis de las dos principales sitios de acceso vascular (subclavia, venas yugulares o femorales)
Dos o más episodios de sepsis por año, secundaria a la infección del catéter venoso central (que requiere hospitalización); o, un solo episodio de fungemia relacionada con catéter venoso central, el shock séptico y / o síndrome de distrés respiratorio agudo.
Los episodios frecuentes de deshidratación severa a pesar de la reposición de líquidos por vía intravenosa
Otras indicaciones menos comunes de trasplante intestinal / multivisceral son[12]-[15]:
trombosis difusa del sistema porto-mesentérica e insuficiencia hepática, incluso en ausencia de insuficiencia intestinal. La causa más frecuente de trombosis venosa son los estados de hipercoagulabilidad y los traumatismos. Los pacientes con trombosis del eje mesentérico portal por déficits de proteína S y C deberían ser referidos a un centro de trasplante intestinal para evaluar el trasplante hepato-intestinal.
catástrofes abdominales tales como extensa traumatismo abdominal, la enteritis por radiación, re-trasplante
tumores malignos de grado benigna o baja, tumores neuroendocrinos primarios .
mala calidad de la vida en la nutrición parenteral total, comentada anteriormente.
Según el Registro Internacional de Trasplante Intestinal las indicaciones más frecuentes de trasplante intestinal en el adulto son[16]:
Las vasculopatías mesentéricas (22%), los traumatismos (12%), la enfermedad de Crohn (13%), los tumores desmoides (10%), trastornos de motilidad (9%), los vólvulos intestinales (7%), otras causas de intestino corto (no vólvulos) (7%), la enfermedad de Gardner y las poliposis familiares (3%).
Contraindicaciones del trasplante intestinal
Aunque las contraindicaciones para el trasplante de intestino son similares a las de otros órganos sólidos (tumores malignos, enfermedades sistémicas etc), la morbilidad y la mortalidad del mismo hace preciso asegurarse de que el trasplante está realizado con la esperanza de una buena calidad de la vida al largo plazo.
Así se consideran contraindicaciones para el trasplante intestinal y multivisceral[6]-[10]:
Las enfermedades autoinmunes sistémicas y las deficiencias inmunes graves también representan contraindicaciones al trasplante intestinal.
Bebedor activo de alcohol o consumidor de tabaco.
Enfermedad cardiopulmonar irreversible.
Inadecuado soporte social o incapacidad para el autocuidado.
Los pacientes con BMI >35 deben evaluarse de forma individualizada por el alto riesgo de complicaciones.
Modalidades de trasplante
El componente esencial que define cualquier modalidad de trasplante intestinal-multivisceral es el intestino delgado; yeyuno e ileon.
Sin embargo, existen varias modalidades (6,14, 17) (Figura 2):
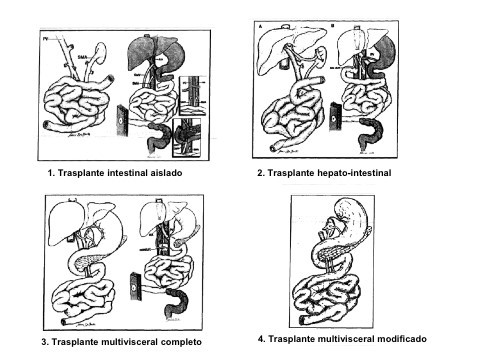
Figura 2
Modalidades de trasplante intestinal y multivisceral. Tomado de: "Tzakis A, Todo S, Starzl TE. Orthotopic liver transplantation with preservation of inferior vena cava. Ann Surg. 1989; 210(5):649-52".
Trasplante intestinal aislado: Cuando esta parte del intestino se trasplanta solo
Trasplante hepatointestinal: o Combinado "en bloque" en el que se trasplanta simultáneamente el hígado y el intestino delgado en bloque. Lleva asociado el duodeno y páncreas.
Trasplante Multivisceral: - Completo: que incluye hígado, estómago, duodeno, páncreas, intestino delgado, con o sin colon.
Modificado: multivisceral sin el hígado.
Complicaciones
Complicaciones precoces
Las especiales características de este trasplante condicionan que las complicaciones postoperatorias sean variadas[18]-[22].
Complicaciones quirúrgicas:
Son frecuentes (aproximadamente en 50% de los casos).
Hemorragia postoperatoria:
Atribuidas a la compleja disección quirúrgica requerida en enfermos con cierto grado de coagulopatía e hipertensión portal, múltiples adherencias intra-abdominales por cirugías previas.
Síndrome compartimental abdominal:
Para evitarlo no se recomienda el cierre primario de la laparotomía.
Complicaciones vasculares:
El diagnóstico se realiza por Eco doppler que confirme el estado de anastomosis vasculares.
La trombosis arterial conduce a la pérdida del injerto y es obligada la enterectomía si es un trasplante intestinal aislado; si es combinado la solución es el retrasplante. La revascularización de los injertos tras trombectomía y reconstrucción arterial, no es posible dada la alta sensibilidad a la isquemia del intestino.
La trombosis venosa manifiesta clínicamente con la presencia de ascitis masiva, congestión del estoma y más tardíamente isquemia y necrosis del mismo.
Fístulas anastomóticas:
Su aparición suele ser precoz (primera semana del trasplante). Los síntomas suelen ser dolor, distensión abdominal y fiebre y obligan a tratamiento quirúrgico inmediato.
Disfunción primaria del injerto:
Se manifiesta por coagulopatía grave, acidosis metabólica láctica progresiva y necrosis intestinal en las primeras 24 horas postrasplante.
Complicaciones gastrointestinales:
Hemorragia del tracto gastrointestinal: Es frecuente y suele ser manifestación de una complicación séptica o inmunológica del injerto. Una ileoscopia y panendoscopia oral con biopsia y cultivos determina la causa de la hemorragia.
Alteraciones de la motilidad: Son frecuentes. Se trata de un injerto denervado que recupera en un plazo de unos 15 días una motilidad normal.
Complicaciones inmunológicas:
Rechazo agudo:
Es la principal complicación de este tipo de trasplante, siendo su frecuencia superior a la de otro tipo de trasplantes de órganos sólidos (30-40%).
El primer episodio suele aparecer en las dos primeras semanas tras el trasplante.
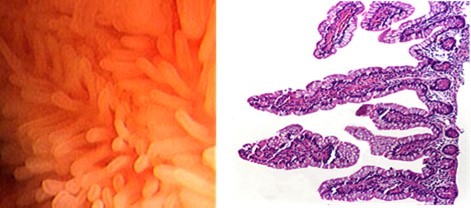
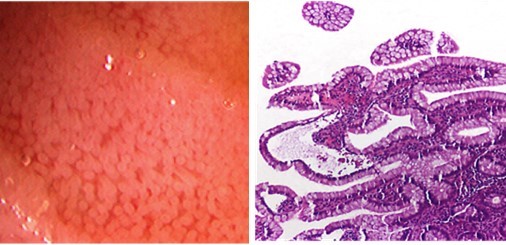
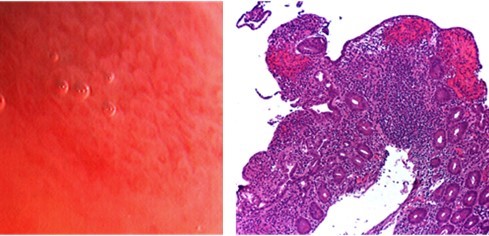
Para detectarlo precozmente es fundamental la monitorización endoscópica del injerto y la toma de biopsia para determinar el grado de rechazo (Figura 3).
Según el grado se trata con bolos de esteroides, OKT3 o nueva dosis de alemtuzumab.
Complicaciones infecciosas:
La infección es la mayor causa de morbilidad y mortalidad. Las infecciones que aparecen en el primer mes tras el trasplante suelen ser consecuencia del propio procedimiento quirúrgico. Entre los factores que influyen encontramos:
Prolongada necesidad pre y postoperatoria de vías centrales para soporte nutricional.
Frecuente administración de tratamientos antibióticos antes del trasplante para control de las infecciones existentes.
Necesidad de administrar una "inmunosupresión agresiva".
Las infecciones diagnosticadas en los siguientes cinco meses con respecto al trasplante, suelen ser consecuencias de la colateralidad del tratamiento inmunosupresor.
Las infecciones bacterianas son las más frecuentes, con una incidencia alrededor del 80%; su localización es generalmente abdominal. Las formas de presentación más frecuentes son infección de herida quirúrgica, abscesos abdominales, peritonitis y neumonías, confirmándose en las mismas la presencia de gérmenes entéricos.
Un aspecto importante es el fenómeno de la translocación bacteriana. La barrera de la mucosa se ve claramente afectada como resultado de la lesión de preservación, episodios de rechazo o sobrecrecimiento bacteriano. Por ello la presencia de una bacteriemia de causa no claramente conocida, obliga a la realización de una ileoscopia diagnóstica con el objetivo de descartar la presencia de un episodio de rechazo.
Las infecciones fúngicas suelen ser consecuencia del fenómeno de la translocación bacteriana. El tratamiento con antifúngicos suele ser eficaz cuando se trata de una especia de cándida, pero si se debe a aspegilus suele ir asociada a una elevada mortalidad.
Entre las infecciones virales la más frecuente es la infección por CMV (34%). En el período más tardío, el virus de Epstein-Barr (VEB) y la enfermedad linfoproliferativa toman mayor protagonismo.
Otras infecciones menos frecuentes son las derivadas de virus de origen respiratorio.
Resultados
Supervivencia del injerto y del paciente.
Como se ha referido anteriormente, se han producido mejoras significativas en la supervivencia de injertos y pacientes en los últimos años, pasando de un 52% de supervivencia al año a finales de los 90, al 75% en el 2005 y de aquí al 85-90% que presentan las series actuales[6], [16], [23](Figura 4).
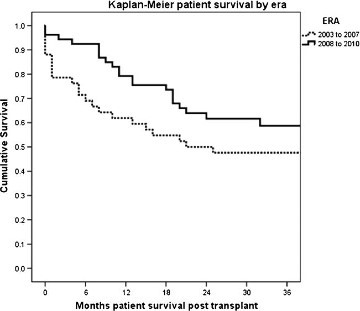
Figura 4
Supervivencia de pacientes por eras. Tomado de "Mangus RS, Tector AJ, Kubal CA, Fridell JA, Vianna RM. Multivisceral transplantation: expanding indications and improving outcomes. J Gastrointest Surg. 2013 ;17:179-86".
Las causas principales de mortalidad del paciente o de pérdida del injerto son los rechazos, las infecciones fúngicas, bacterianas y por CMV, los linfomas y las causas técnicas[24], [25].
En cuanto a la función intestinal, el 70% de los pacientes que superan los seis meses de vida están totalmente libres de nutrición parenteral total[6].
Los mejores resultados se han obtenido en receptores jóvenes que son trasplantados estando en el domicilio y no están hospitalizados; cuando reciben el primer trasplante y los que reciben la terapia de inducción de anticuerpos[26], [27].
Estos resultados enfatizan la importancia de la remisión precoz de los pacientes que están lo suficientemente bien como para recibir un trasplantes y tolerar la agresiva inmunosupresión
Calidad de vida
Varios estudios confirman que el estado de fracaso intestinal se asocia con discapacidad psico-social importante, disminución de la calidad de vida, y un aumento la dependencia de narcóticos, los cuales mejoran después de la realización de un trasplante con éxito[28]-[31].
Más del 80% de los receptores de trasplante que sobreviven se liberan de la nutrición parenteral y pueden reanudar sus actividades regulares, con una alta puntuación en el Indice de Karnofsky[16], [24], [29]. Sin embargo, es necesario realizar una rehabilitación intestinal, debido a cierto grado de disfunción inicial por ser un órgano denervado sometido a isquemia-reperfusión y por los posibles rechazos. Cuando el injerto empieza a funcionar, se inicia dieta enteral oligomérica o polimérica, administrándose los lípidos lentamente, a partir de la semana cuarta[25]. Todo ello se traduce de una mejora en la calidad de vida percibida por el paciente.
Coste-efectividad
Se estima que el mantenimiento de la nutrición parenteral domililiaria conlleva un coste en torno a los 1000€ mensuales. Aunque no existen estudios amplios que analicen este aspecto, se estima que el trasplante intestinal, al igual que el renal, se hace coste-efectivo a partir del segundo año[28].
Pero, junto a la evaluación de los costes, sin duda relevante a la hora de analizar cualquier proceso, es importante evaluar la relevancia clinica del procedimiento. En una revisión reciente, Fishbein[6] considera que cada año, miles de personas que presentan infarto intestinal completo debido a isquemia mesentérica, enterocolitis necrotizante vólvulos u otras patologías, fallecen por sepsis porque no se lleva a cabo una resección masiva. Gracias al incremento de centros que realizan trasplante intestinal e incorporan programas de rehabilitación intestinal, esta práctica de abortar una resección masiva está empezando a cambiar. De esta forma se le da la oportunidad a los enfermos de tener una supervivencia y calidad de vida aceptable con la nutrición parenteral y posteriormente tener la posibilidad del trasplante intestinal o multivisceral. De aquí la importancia de aproximar la tasa indicaciones a los estandares internacionales y generar centros de referencia que permitan abordar estos enfermos complejos.
En resumen, aunque aún quedan por evaluar grandes series de seguimiento a largo plazo, el papel del trasplante intestinal en el tratamiento de pacientes con insuficiencia intestinal se considera en la actualidad una terapéutica consolidada, en las indicaciones específicas establecidas.