CP-146. ABORDAJE DE LA ENFERMEDAD PERIANAL EN LA ENFERMEDAD DE CROHN EN TRATAMIENTO CON USTEKINUMAB
Práxedes González E, Lázaro Sáez M, Delgado Maroto A, Hernández Martínez Á
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: enfermedad de crohn, enfermedad perianal, ustekinumab.
Introducción
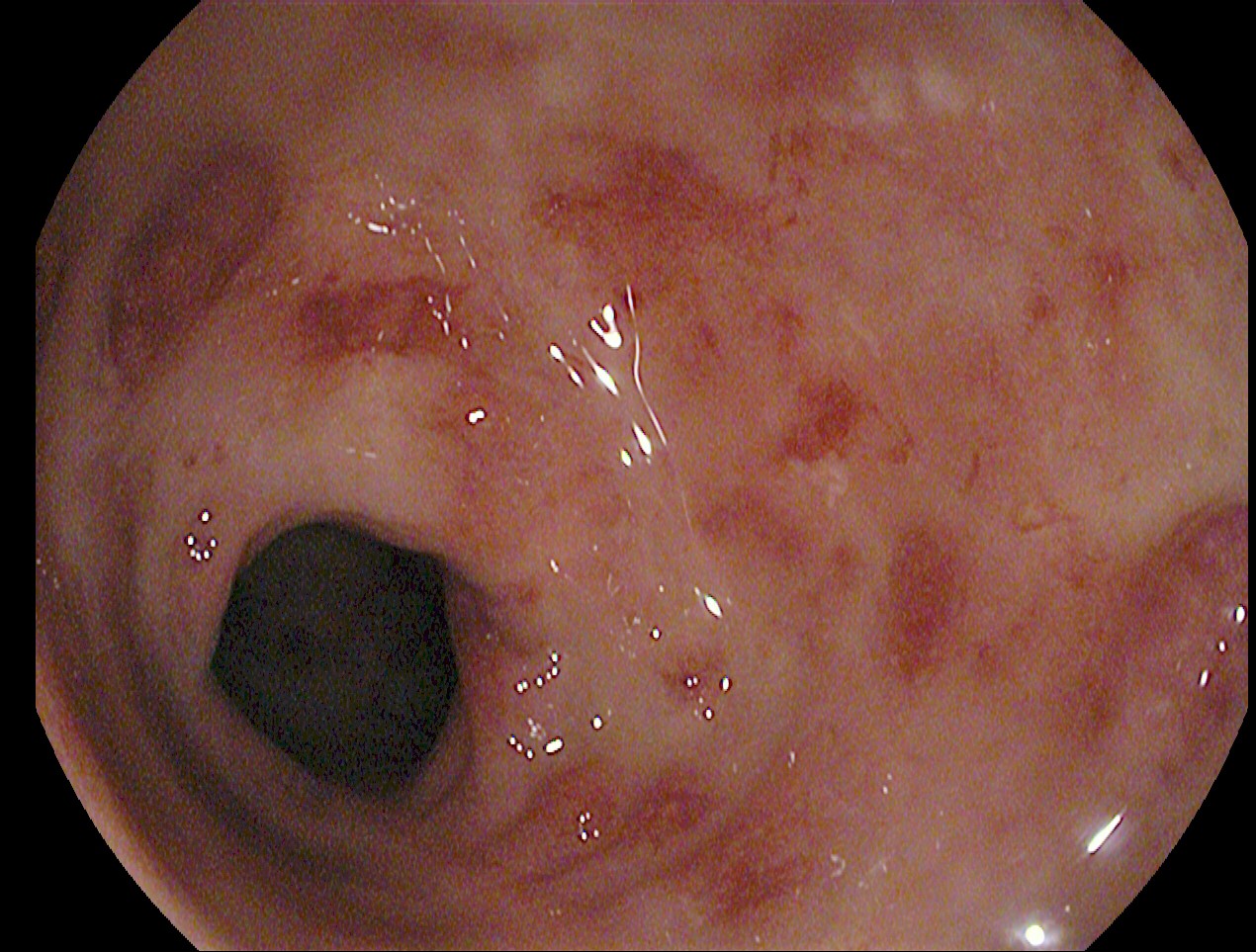
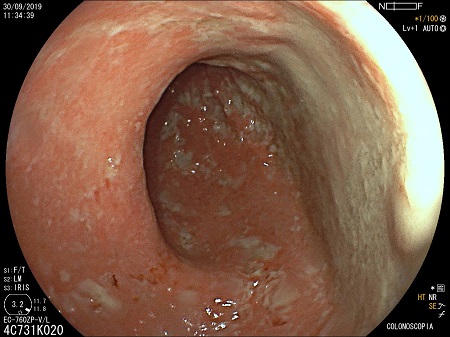
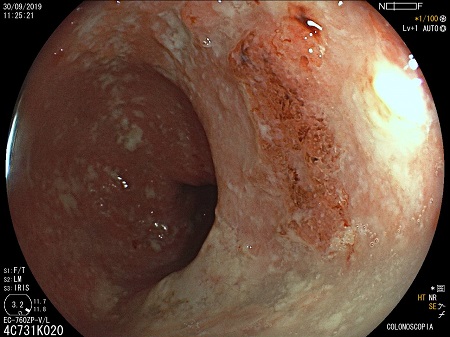
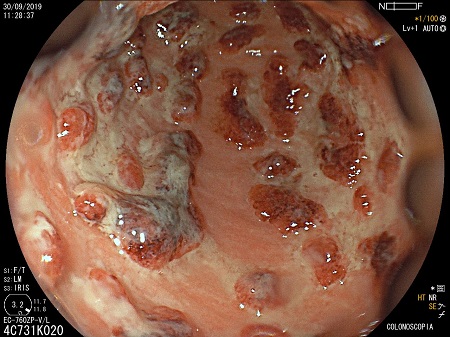
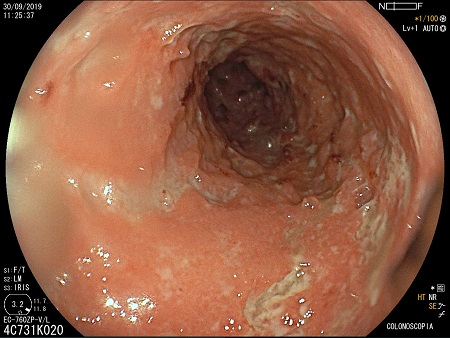
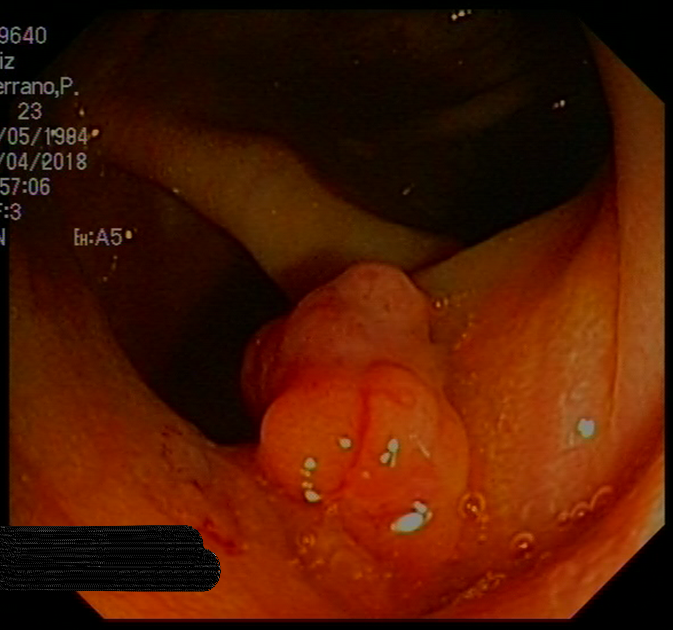
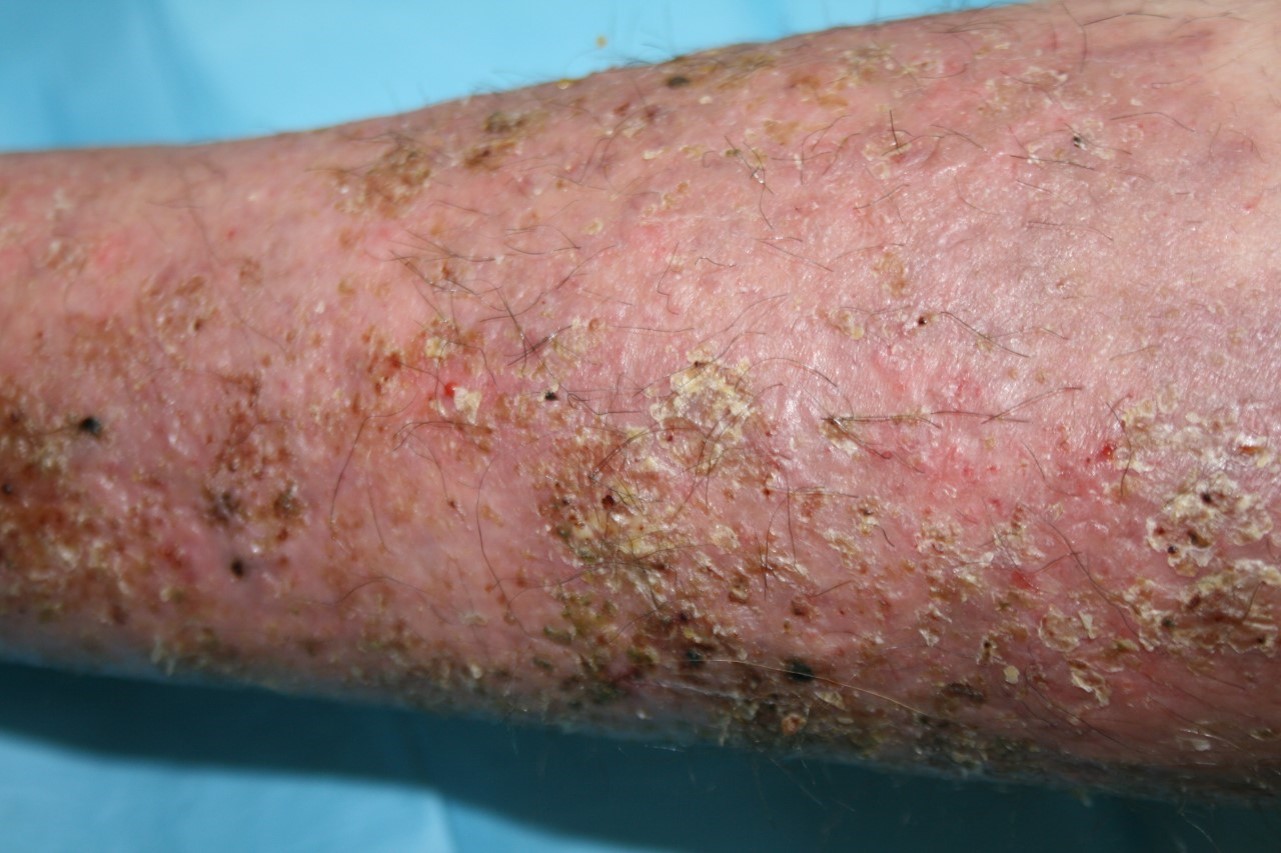
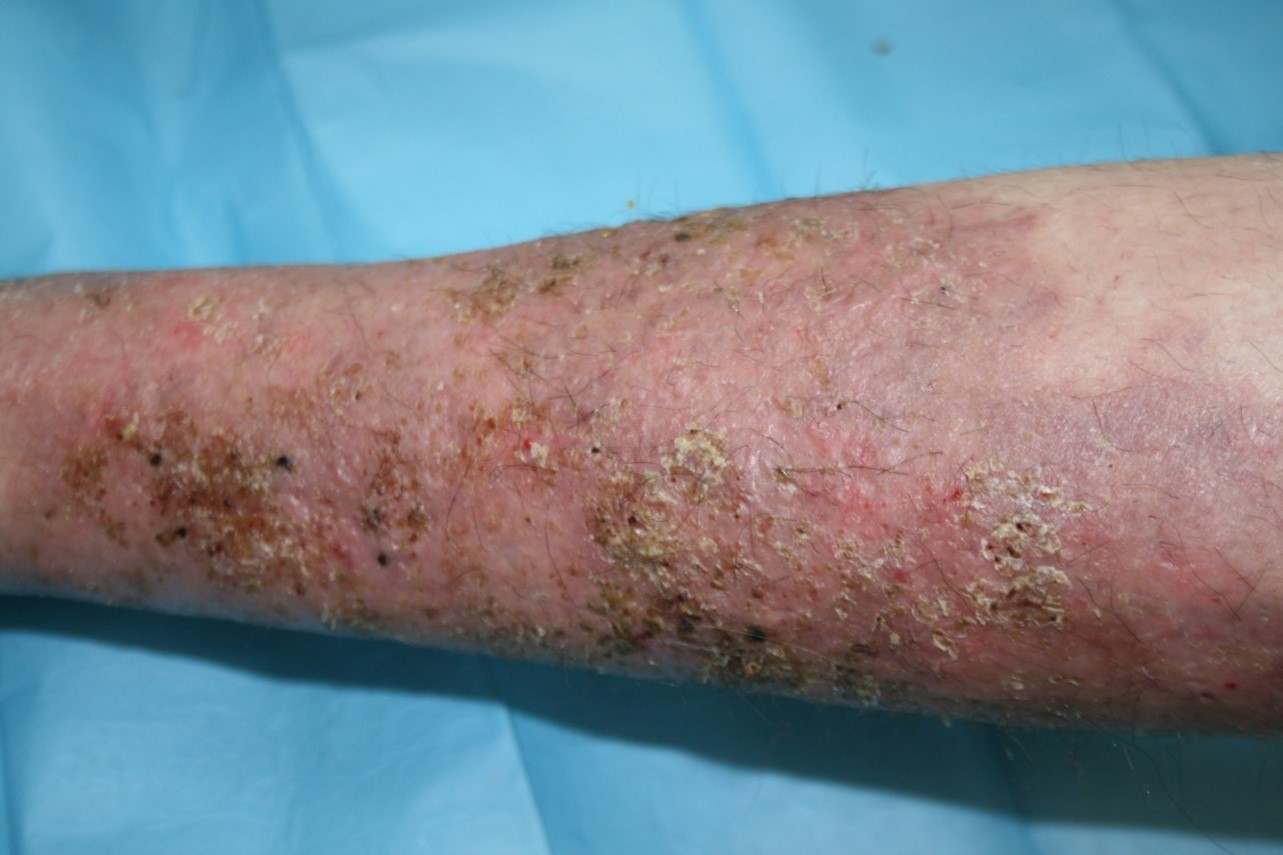
Bajo la denominación de enfermedad perianal (EPA) se incluyen las anomalías anorrectales (fisura, fístula o absceso, los repliegues cutáneos y la maceración perianal) presentes en pacientes con enfermedad de Crohn (EC), asociando elevada morbilidad y una disminución significativa en la calidad de vida de los mismos. Ustekinumab, anticuerpo monoclonal IgG1k anti interleucina (IL)-12/23, constituye un escalón terapéutico en el manejo de la enfermedad de Crohn; sin embargo su relevancia en el control de la enfermedad perianal es más desconocido. El objetivo de nuestro estudio ha sido evaluar el efecto del Ustekinumab sobre la enfermedad perianal, la importancia del abordaje invasivo de la misma y su correlación con la actividad inflamatoria intestinal.
Material y métodos
Se han evaluado pacientes con Enfermedad de Crohn que presentan enfermedad perianal asociada, tratados con Ustekinumab en el Hospital Universitario Torrecárdenas en un periodo comprendido desde julio de 2017 hasta junio de 2019.
Resultados
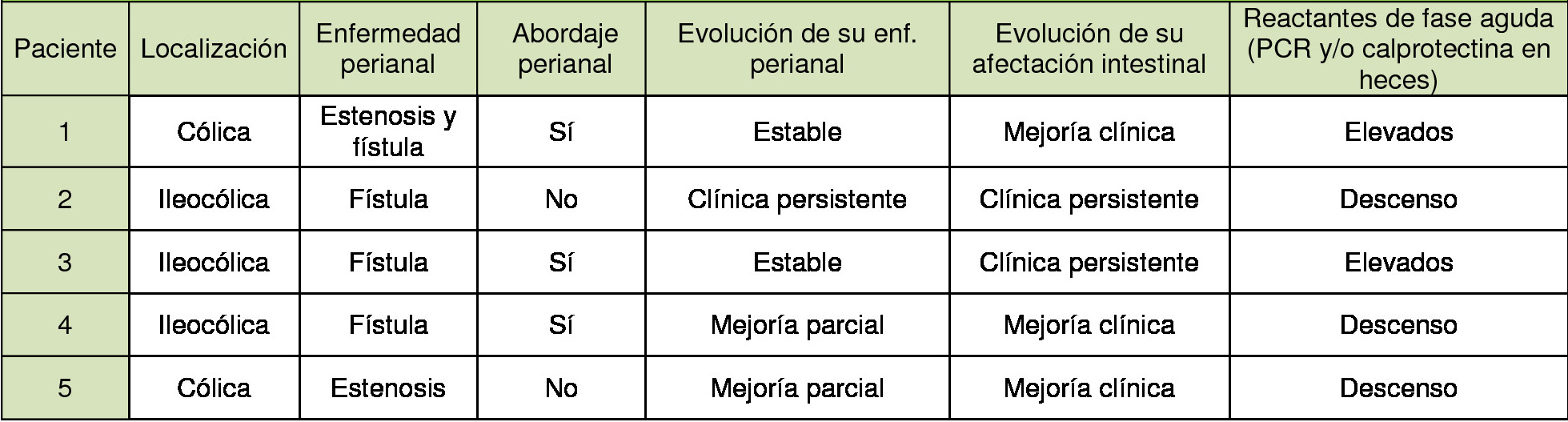
Se analizó un total de 5 pacientes, 3 mujeres y 2 hombres, con una mediana de edad de 35 años, y afectación ilecólica en tres de ellos y cólica en dos. Atendiendo a las lesiones perianales que manifestaron, 3 de los pacientes presentaron fístulas perianales, uno estenosis anal y un quinto presentó de forma concomitante fístula y estenosis anal (Tabla 1). Tres de los pacientes precisaron abordaje quirúrgico de la lesión asociado al tratamiento con Ustekinumab de su enfermedad, presentando una evolución estable o favorable de su enfermedad perianal y una mejoría clínica en dos de ellos. Respecto a los dos pacientes que no recibieron cirugía, uno de ellos progreso favorablemente de su enfermedad perianal y su afectación intestinal con tratamiento con Ustekinumab; el segundo si bien presentó descenso de reactantes de fase aguda con tratamiento médico mantiene clínica intestinal y enfermedad perianal activa y limitante.
Conclusiones
La prevalencia de la enfermedad perianal en la EC varía significativamente según las series publicadas (21-54%) y su historia natural es aún muy desconocida. El impacto de la EPA sobre la calidad de vida de los pacientes ha llevado a constituir un reto terapéutico, y por ello la necesidad de un abordaje médico, endoscópico y quirúrgico según la naturaleza y evolución de las lesiones. La aparición de nuevos fármacos biológicos como el Ustekinumab supone una herramienta más al arsenal terapéutico de esta entidad; y si bien el reducido tamaño muestral no nos permite sacar conclusiones generalizadas, es probable que la optimización del tratamiento resida en un abordaje integral, sistémico y local, sobre la enfermedad.
CP-147. ABORDAJE DE LAS MANIFESTACIONES EXTRAINTESTINALES DE LA ENFERMEDAD DE CROHN EN TRATAMIENTO CON USTEKINUMAB
Práxedes González E, Lázaro Sáez M, Delgado Maroto A, Hernández Martínez Á
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: enfermedad de crohn, manifestaciones extraintestinales, ustekinumab.
Introducción
El desarrollo de manifestaciones extraintestinales es frecuente en los pacientes con enfermedad inflamatoria intestinal (EII) con una prevalencia variable del 21-36%; en especial estructuras como las articulaciones, piel, ojos y vías biliares entre otros. Como anticuerpo monoclonal IgG1k anti interleucina (IL)-12/23, Ustekinumab constituye un escalón terapéutico en el manejo de esta entidad; sin embargo su efecto sobre dichas manifestaciones resulta más controvertido. El objetivo de nuestro estudio ha sido evaluar el efecto del Ustekinumab sobre las manifestaciones extraintestinales y su correlación con la actividad inflamatoria intestinal.
Material y métodos
Se han evaluado pacientes con Enfermedad de Crohn que presentan manifestaciones extraintestinales asociadas, tratados con Ustekinumab en el Hospital Universitario Torrecárdenas en un periodo comprendido desde julio de 2017 hasta junio de 2019.
Resultados
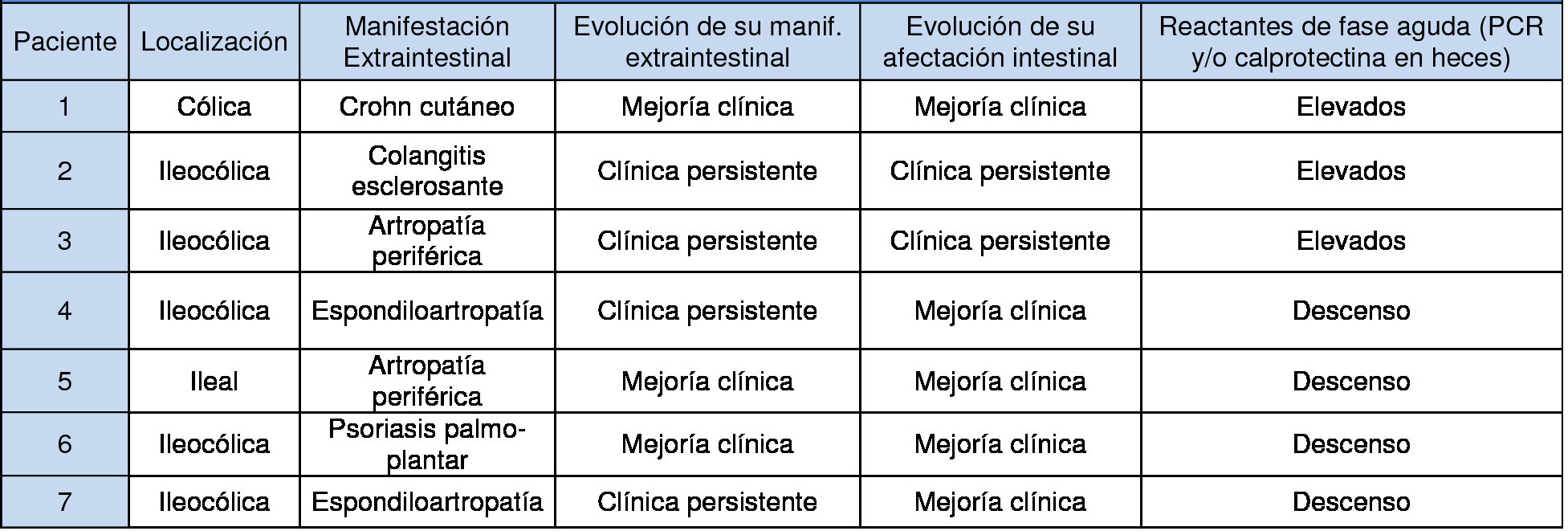
Se analizó un total de 7 pacientes, 6 mujeres y 1 hombre, con una mediana de edad de 49 años, y afectación ileocólica en cinco de ellos, cólica en uno, e ileal en otro. Las manifestaciones extraintestinales desarrolladas fueron articulares (artropatía periférica en dos pacientes y espondiloartropatía en otros dos), cutáneas (Crohn cutáneo en un paciente y psoriasis palmo-plantar en otro), y biliares (colangitis esclerosante en un paciente) (Tabla 1). Los pacientes afectos de manifestaciones cutáneas y uno de los pacientes con artropatía periférica presentaron mejoría clínica de su cuadro extraintestinal tras tratamiento con Ustekinumab, así como de su afectación intestinal, con descenso de reactantes de fase aguda. Por el contrario, los pacientes afectos de espondiloartropatía no refirieron mejoría de dicho trastorno, si bien desde el punto de vista intestinal se hallaron asintomáticos. Por último, nuestra paciente con colangitis esclerosante mantuvo cifras similares de GGT previas al tratamiento con Ustekinumab, así como cuadros suboclusivos persistentes y reactantes de fase aguda elevados.
Tabla 1
Pacientes con enfermedad de Crohn y manifestaciones extraintestinales en tratamiento con Ustekinumab
Conclusiones
Las manifestaciones extraintestinales de la EII presentan mecanismos de acción diferentes y clínica dependiente (artritis periférica, eritema nodoso, estomatitis aftosa, epiescleritis) o independiente (Espondiloartropatía, pioderma gangrenoso, colangitis esclerosante primaria, uveítis) del curso de la enfermedad intestinal. La aparición de nuevos fármacos biológicos como el Ustekinumab, tienen también como caballo de batalla el manejo de dichas manifestaciones. El reducido tamaño muestral no permite sacar conclusiones generalizadas, pero obliga a la necesidad de más estudios para optimizar el abordaje de manifestaciones extraintestinales con curso dependiente y también independiente de su enfermedad intestinal.
CP-148. ALOPECIA COMO MANIFESTACIÓN TRAS TRATAMIENTO CON USTEKINUMAB EN PACIENTE CON ENFERMEDAD DE CROHN
Amado Villanueva PP, López González J, Lázaro Saez M
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: alopecia, enfermedad de crohn, inhibidor interleuquina 12-23.
Introducción
La enfermedad de crohn es una enfermedad inflamatoria intestinal progresiva, incapacitante que requiere un manejo específico y multidisciplinar para su control. Ustekinumab (Stelera®) es un anticuerpo monoclonal humano que se une a la subunidad p40 de la interleuquina-12 (IL-12) y de la IL-23 y se usa como segunda línea de tratamiento en enfermedad de Crohn desde su aprobación en el 2016. La alopecia areata es una enfermedad inmunológica, crónica, inmuno mediada que afecta la fase anágena del folículo piloso produciendo pérdida de pelo no cicatricial. La relación entre esta enfermedad y otras enfermedades inmunológicas está bien documentada. Por ello presentamos el caso clínico donde se ve esta manifestación en paciente con enfermedad de Crohn de larga data e inicio de tratamiento con Ustekinumab.
Caso clínico
Paciente mujer de 43 años con antecedentes de enfermedad de crohn ileal de larga data con múltiples intervenciones quirúrgicas con resección intestinal (actualmente síndrome de intestino corto) y que ha precisado varias opciones terapéuticas a lo largo de los años (Tratamiento con azatioprina, infliximab, adalimumab siendo suspendidas por diferentes efectos secundarios) sin un control total de los signos y síntomas. No refiere hábitos tóxicos. No otras enfermedades dermatológicas. Por lo que ante la persistencia de sintomatología de dolor abdominal, cuadros suboclusivos y deposiciones diarreicas sin tener ningún tratamiento de mantenimiento, se le inicia tratamiento con Stelera cada 8 semanas y posteriormente intensificado cada 6 semanas y en espera de la remisión clínica. Tres semanas después de la segunda dosis de Stelera la paciente presenta pérdida de pelo no cicatricial en diferentes zonas del cuero cabelludo sin que se precisara causa aparente y sin antecedentes previos que tras tratamiento corticoideo tópico tuvo cierta mejoría.
Discusión
Se ha documentado ampliamente en la literatura sobre la aparición de alopecia areata en enfermedades inmunomediadas y el tratamiento con fármacos anti-TNF, existe pocos casos reportados de esta misma relación con el uso de Ustekinumab en pacientes con psoriasis más no en pacientes con enfermedad de crohn. La paciente del caso clínico en todos los años de su enfermedad y tras los diferentes tratamientos biológicos no había mostrado este tipo de manifestación cutánea. Es debido que tras la administración de la segunda dosis de Ustekinumab es donde presenta la alopecia habiendo una posible relación que en estudios posteriores se debe confirmar.
CP-149. ANEMIA EN PACIENTE CON ENFERMEDAD DE CROHN DESENCADENADA POR ADALIMUMAB
Belvis Jiménez M, Maldonado Pérez B, Castro Laria L, Caunedo Álvarez A
Departamento Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: adalimumab, anemia, enfermedad de crohn.
Introducción
El uso de la terapia biológica ha revolucionado la evolución y el pronóstico de los pacientes con Enfermedad Inflamatoria Intestinal (EII), pero estas terapias no están exentas de efectos adversos (EA). Presentamos el caso de un chico con enfermedad de Crohn (EC) que presentó anemia inducida por adalimumab.
Caso clínico
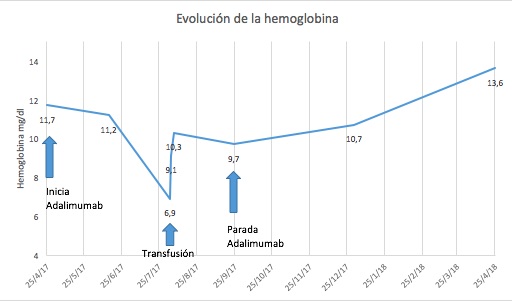
Varón de 17 años en tratamiento con Adalimumab debido a una EC ileal con una pobre respuesta clínica. En junio de 2017 comenzó con Adalimumab a dosis de inducción (160-80 mg) y posteriormente con dosis de mantenimiento (40 mg cada 2 semanas). Inicialmente presentó buena respuesta clínica, con descenso en los reactantes de fase aguda, pero en Agosto consultó por astenia, detectándose anemia severa que precisó la transfusión de tres concentrados de hematíes, sin evidencia de sangrado digestivo. Se realizó analítica con perfil férrico, vitamina B12 y ácido fólico normales. El test de Coombs y el frotis de sangre periférica también resultaron normales. En septiembre, debido a la normalidad de las pruebas y a la posibilidad de anemia hemolítica y aplasia medular secundaria al fármaco descrito en algunos artículos, decidimos suspenderlo comprobando posteriormente la estabilización de los niveles de hemoglobina.
Figura 1
Evolución de la Hemoglobina. Obsérvese el aumento de la Hemoglobina desde la retirada del fármaco
Discusión
En los últimos años, la estrategia terapéutica de la EII ha cambiado considerablemente. Los antagonistas del factor de necrosis tumoral-alpha (TNFα), como el adalimumab, actúan previniendo la unión del TNF a su receptor, neutralizando su actividad y disminuyendo así la inflamación mucosa; siendo eficaces para la inducción y el mantenimiento de la remisión y la mejora del pronóstico a largo plazo en la EII. Los EA más importantes del adalimumab son las infecciones, seguido en frecuencia por las neoplasias. Los estudios iniciales post-comercialización no mostraron un aumento significativo en las complicaciones hematológicas, siendo las citopenias medicamentosas clínicamente significativas un EA raro, y entre los cuales no se ha detectado una relación causal clara. La aplasia medular, aunque infrecuente, se ha reportado en algunos estudios como EA de los fármacos anti-NFα4. Encontramos solo un caso en la literatura que relaciona el adalimumab con anemia de tipo autoinmune. En nuestro caso, no encontramos ninguna causa que indujera la anemia, pero la retirada del adalimumab consiguió la estabilización de la misma. La anemia puede ser un EA del tratamiento con adalimumab, por lo que se debe tener en cuenta la posibilidad de retirada de éste fármaco en pacientes con anemia severa que se perpetúa a pesar del tratamiento.
CP-150. COLITIS HERPÉTICA COMO DEBUT DE UNA COLITIS ULCEROSA
del Pino Bellido P, Morales Barroso ML, Maldonado Perez B, Mouhtar el Halabi SA, Hergueta Delgado P, Caunedo Alvarez A
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: colitis ulcerosa, virus herpes simple, enfermedad inflamatoria intestinal.
Introducción
La colitis por virus herpes simple (VHS) es una causa poco frecuente de colitis, incluso en paciente inmunosuprimidos. Se han descrito pocos casos, manifestándose como diarrea sanguinolenta, dolor abdominal y síntomas sistémicos. Endoscópicamente se suelen identificar eritema, friabilidad y úlceras confluentes, hallazgos fácilmente confundibles con colitis ulcerosa. La detección de PCR positiva para VHS en biopsias, es la prueba más sensible y específica para su diagnóstico.
Caso clínico
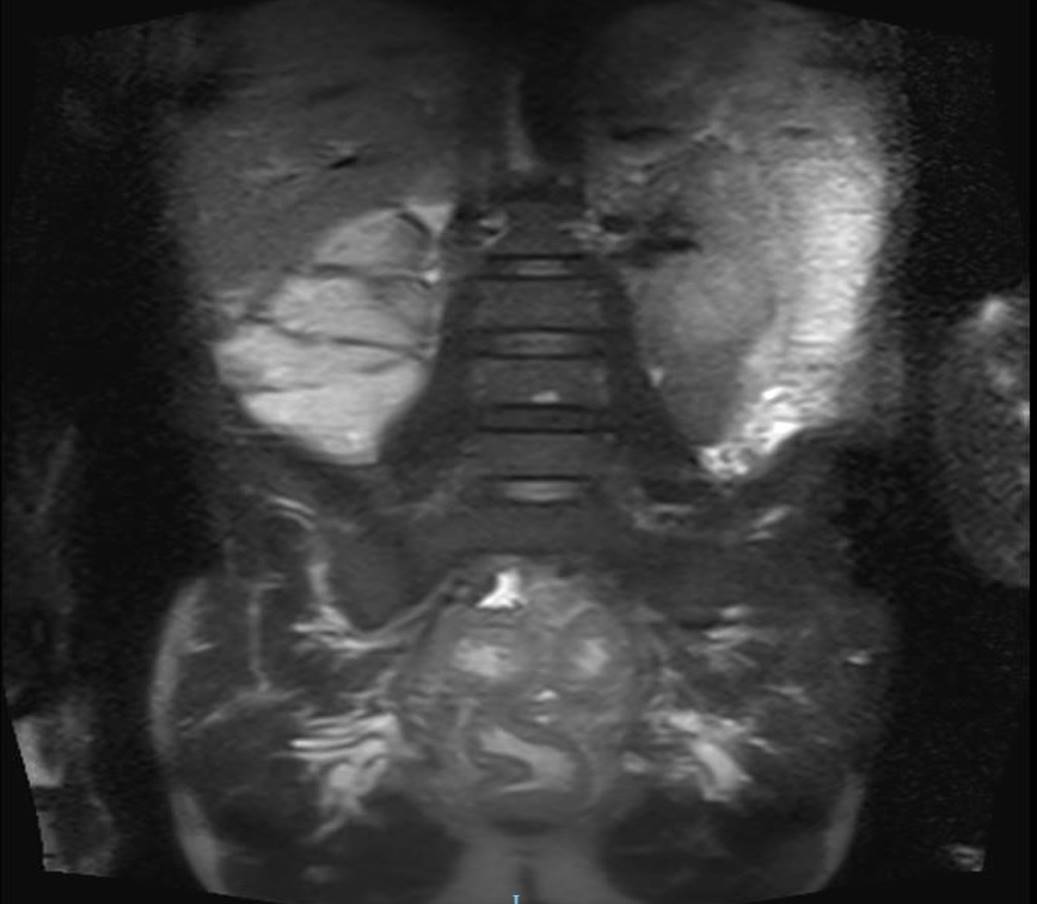
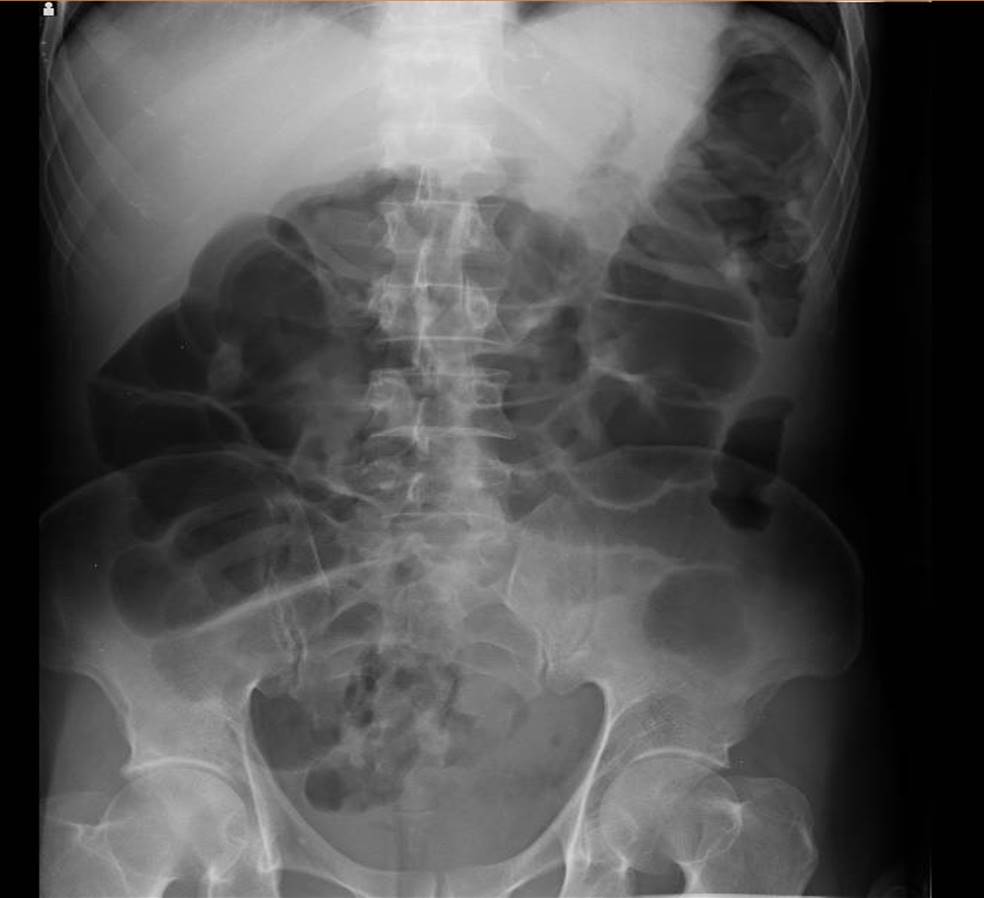
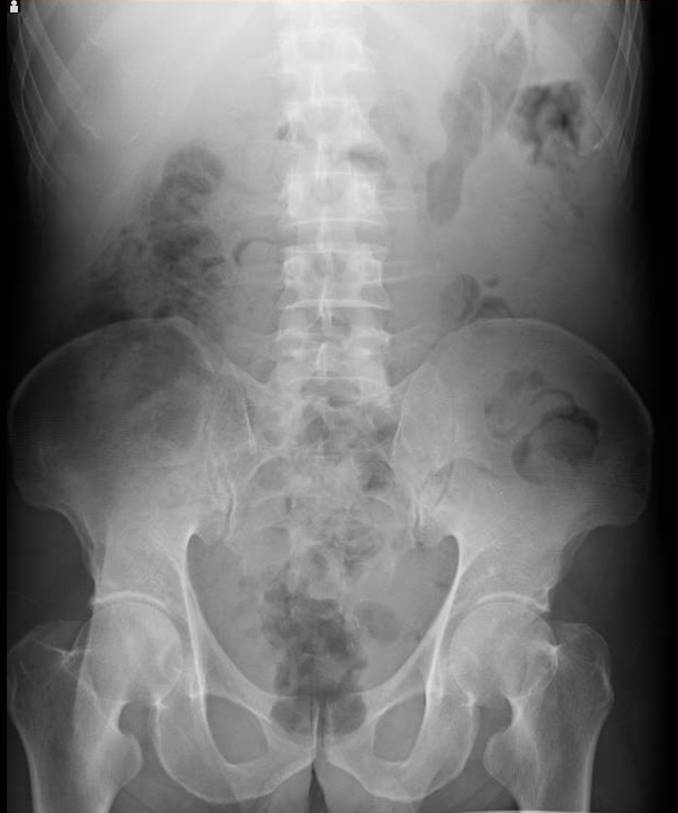
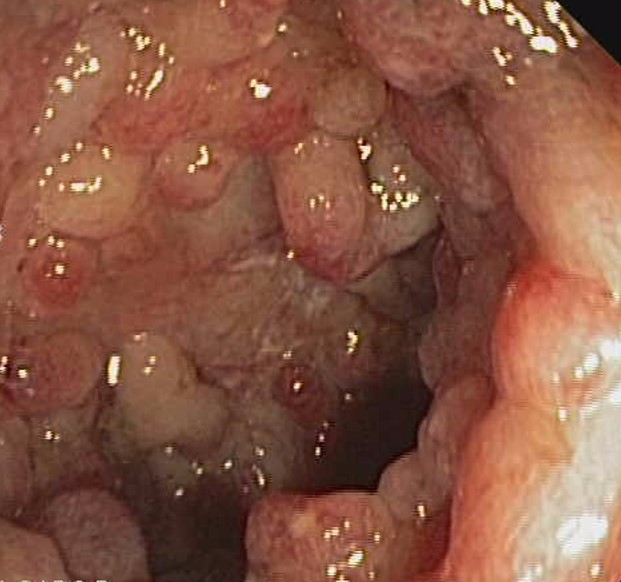
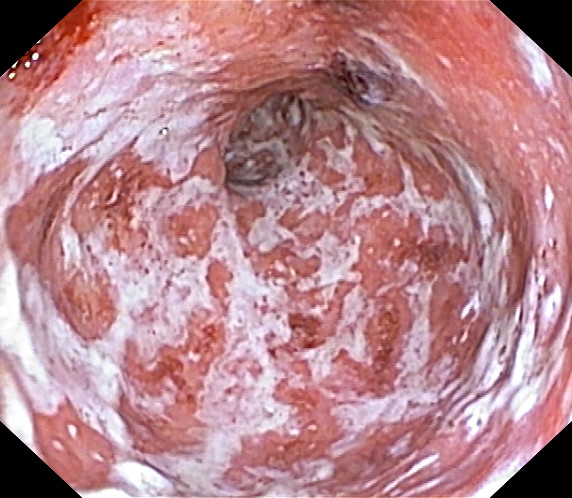
Varón de 53 años que ingresa por rectorragia, dolor, distensión abdominal y pérdida ponderal no cuantificada de un mes de evolución. Inicialmente, descartamos proceso infeccioso (PCR de clostridium y coprocultivos negativos). En rectoscopia se visualiza mucosa desestructurada con ulceraciones, compatible con colitis ulcerosa (biopsia compatible) y en entero-RNM proceso inflamatorio a nivel colónico (Figura 1). Coincidiendo con la preparación para la enteroRNM el paciente presenta dolor y distensión abdominal, con dilatación de todo el marco cólico (Figura 2), sin fiebre ni síntomas sistémicos. Se inicia estudio prebiológico y tratamiento con corticoides intravenosos a dosis plenas sin respuesta completa. Previo a iniciar tratamiento biológico se toman muestras colónicas que descartan infección por CMV, por lo que pautamos primera dosis de Infliximab. A los dos días avisan de microbiología por cultivo de biopsia colónica positivo para VHS con PCR positiva. Tras iniciar tratamiento con aciclovir el paciente presenta mejoría clínica y desaparición del megacolon (Figura 3). 3 meses tras haber completado tratamiento con Aciclovir, se realiza rectoscopia de control con persistencia de actividad inflamatoria y pseudopólipos (Figura 4). En biopsia, hallazgos compatibles con colitis ulcerosa y PCR VHS y CMV negativos con buena respuesta al tratamiento con corticoides vía oral.
Figura 1.
Entero- RNM. Se aprecia engrosamiento irregular de recto y sigma y dilatación moderada del resto del colon
Discusión
La infección por VHS se ha relacionado con fracaso al tratamiento en pacientes con enfermedad inflamatoria intestinal. Los casos descritos en estos pacientes se han relacionado con el tratamiento inmunosupresor. Sin embargo, la presencia de inflamación activa también se ha considerado un factor predisponente para la infección por VHS, siendo posible en pacientes sanos. En nuestro paciente, dada la mejoría tras aciclovir, a pesar de su proximidad a la primera dosis de infliximab, nos planteamos el diagnóstico diferencial entre colitis aguda por VHS sobre colon sano o sobreinfección de colitis ulcerosa aún no diagnosticada. La negativización de la PCR de VHS en las muestras colónicas, tras completar el tratamiento con Aciclovir, y la persistencia de los hallazgos inflamatorios en la colonoscopia, nos hace decantarnos hacia el diagnóstico de colitis herpética como debut de una colitis ulcerosa.
CP-151. COLITIS ULCEROSA REFRACTARIA A TRATAMIENTO HABITUAL: RESCATE CON USTEKINUMAB INTENSIFICADO
Camacho Montaño LM, Viejo Almanzor A, Mata Perdigón FJ, Correro Aguilar FJ
Servicio Aparato Digestivo. Hospital Puerta del Mar, Cádiz.
Palabras clave: colitis ulcerosa.
Introducción
Ustekinumab es un antagonista de la subunidad p40 de interleucina-12 e interleucina-23. Está aprobado su uso en psoriasis, artritis psoriásica, y enfermedad de Crohn moderada a grave. Su uso en colitis ulcerosa se encuentra bajo investigación, con resultados preliminares favorables.
Caso clínico
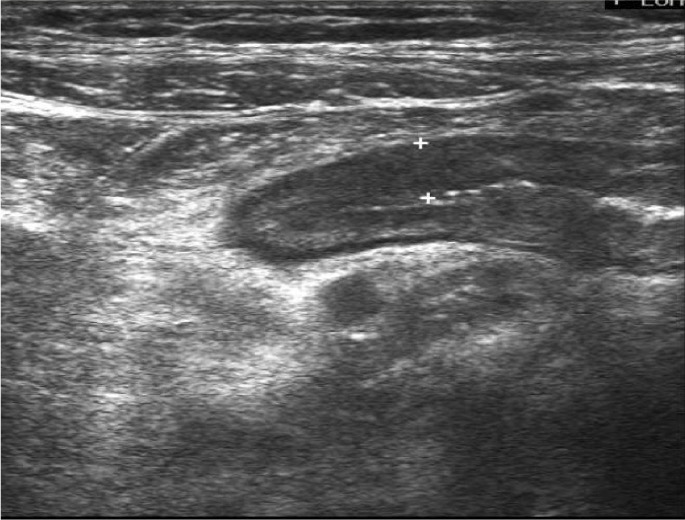
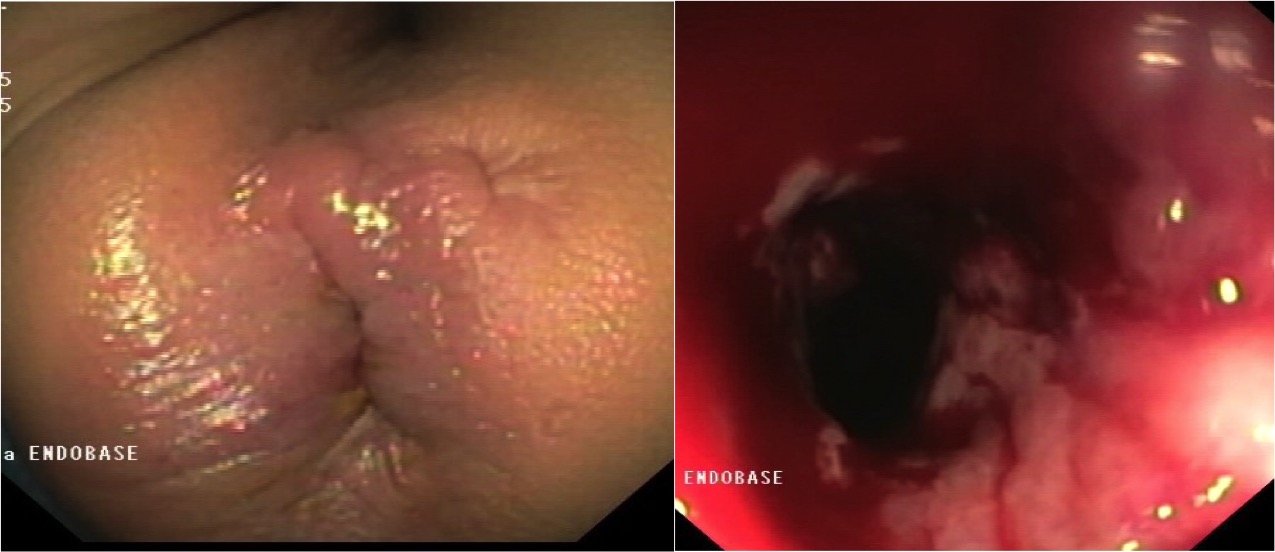
Mujer de 45 años diagnosticada desde la juventud de colitis inflamatoria con enfermedad perianal atípica, sin diagnóstico definitivo de Colitis Ulcerosa (CU) ni Enfermedad de Crohn(EC). En 2004 inició azatioprina por corticodependencia y tras mala evolución inició infliximab(IFX) en 2005, con mejoría clínica. Desde 2014, brotes intermitentes manejados con corticoides tópicos, orales e intensificación de IFX a cada 6 semanas. En 2017 se planteó nueva intensificación pero presentaba niveles de IFX altos sin anticuerpos, por lo que se decidió cambiar de diana. En colonoscopia de 2018 presentaba una proctitis grave (Figura 1) y tras descartar CMV, se inició tacrólimus tópico rectal como puente a vedolizumab(VDZ), sin respuesta. Antes de comenzar con VDZ, empeoró el brote y apareció clínica perianal en forma de tumefacción perineal. Se realizó resonancia magnética(RM) pélvica que no identificó colecciones ni trayectos fistulosos, y una ecografía endoanal que evidenció una fístula cercana a horquilla vulvar. Se inició antibioterapia oral con escasa respuesta, que se completó con antibioterapia intravenosa, produciéndose drenaje espontáneo. Se realizó entero-RM con cambios inflamatorios en mesosigma-mesorrecto, sin otra afectación. Asumimos por la enfermedad perianal que se trataba de una EC, iniciando ustekinumab en pauta de inducción habitual con mantenimiento sc cada 8 semanas, asociado a un ciclo de corticoides orales, con respuesta parcial, sin conseguir la retirada completa de corticoides hasta pasados 6 meses. Realizamos recotsigmoidoscopia donde presentaba mejoría en la mucosa rectal con cambios cicatriciales (Figura 2), y mucosa muy eritematosa de forma difusa en sigma, con biopsias compatibles con CU activa. Tras una mejoría inicial comenzó nuevamente con clínica al mes de suspender los corticoides. Indicamos un nuevo ciclo y se propuso intensificar ustekinumab a 4 semanas con el consentimiento de la paciente. Tras dos dosis, la paciente mantiene remisión clínica, libre de corticoides y en remisión endoscópica (colitis extensa inactiva en colonoscopia de control).
Figura 2
Colonoscopia de control tras 6 meses de tratamiento, donde se observa mejoría de la afectación inflamatoria
Discusión
Se están realizado ensayos clínicos en pacientes con CU moderada-grave, donde ustekinumab es más eficaz que placebo para lograr inducción y mantenimiento de remisión clínica. En nuestro caso, el tratamiento ha sido eficaz y seguro. Hemos precisado dosis más altas de las habituales probablemente por haberlo utilizado tras varias líneas de tratamiento.
CP-152. DEBUT DE ENFERMEDAD INFLAMATORIA INTESTINAL SECUNDARIA A INMUNOFÁRMACO: UN NUEVO RETO EN GASTROENTEROLOGÍA
Llamas Bellido I1, Miras Lucas L1, Pérez González Á1, Vázquez Rodríguez JA1, Cózar Granja T2, Viciana Martínez-Lage MJ2, Gallego Rojo FJ1
1UGC Aparato Digestivo. Complejo Hospitalario de Poniente, Ejido, El. 2Departamento Anatomía Patológica. Complejo Hospitalario de Poniente, Ejido, El.
Palabras clave: colitis, pembrolizumab, eii.
Introducción
Las nuevas terapias biológicas para tratamiento del cáncer no están exentas de efectos secundarios gastrointestinales. Entre ellos destacar la colitis inducida por pembrolizumab, anticuerpo monoclonal humanizado frente al receptor de la muerte celular programada-1 (PD-1) que potencia la respuesta de los linfocitos T.
Caso clínico
Hombre de 61 años con melanoma metastásico tratado con pembrolizumab 2 mg/kg/ciclo suspendido tras 5 ciclos por toxicidad dermatológica (varias lesiones de eritema multiforme con necrolisis epidérmica y un carcinoma espinocelular diferenciado con bordes libres) y sospecha de digestiva por diarrea con rectorragia y moco. Analíticamente calprotectina fecal de 1600 microgramos/g con PCR normal, ASCA positivos con colonoscopia sin ileoscopia que informa de afectación continua desde margen anal hasta 60 cm con úlceras fibrinadas con biopsias de criptitis e inflamación aguda difusa en lámina propia además de eneroRM normal. Ante la ausencia de mejoría con mesalazina oral, tópica y prednisona oral a dosis plenas, suspendida temporalmente por drenaje quirúrgico de absceso perianal, y ante empeoramiento clínico-analítico (dolor abdominal, aumento de deposiciones con rectorragia y anemia, sin fiebre) ingresa en hospital. Tras descartar causas infecciosas se inicia corticoterapia intravenosa a dosis plenas sin mejoría y se realiza rectosigmoidoscopia que objetiva afectación mucosa continua desde margen anal hasta 35 cm con pérdida de patrón vascular, eritema y exudado fibrinoide con friabilidad a la toma de biopsias (Figuras 1 y 2) así como numerosas lesiones pseudopolipoideas eritematosas con sangrado espontáneo y exudado con mucosa sana interlesional desde unión recto-sigmoidea hasta 35 cm (Figuras 3 y 4). Ante la corticorrefractariedad se realiza estudio prebiológico e investiga sobreinfección por CMV. A la espera de las biopsias y ante ausencia de contraindicaciones, se decide inducción con infliximab (5mg/kg), tras lo cual informan las biospias de presencia de CMV (Figuras 5 y 6) e inflamación mucosa aguda, crónica y abscesos crípticos compatible con enfermedad inflamatoria intestinal de actividad moderada (Figura 7). Se pauta ganciclovir y segunda dosis de infliximab con mejoría clínico-analítica.
Discusión
La dificultad del caso reside en su diagnóstico diferencial ya que, descartada etiología infecciosa, podría tratarse tanto de una colitis aguda (farmacotoxicidad) o del debut de una EII inducida por inmunofármaco. El diagnóstico finalmente lo otorga la anatomía patológica que evidencia signos de EII, además de sobreinfección por CMV (paciente inmunodeprimido por corticoterapia de larga duración). Por ello, tras inducción con infliximab (inicialmente indicada para tratamiento de sospecha de colitis aguda inmunomediada), y ante antecedente neoplásico, se decide completar inducción con antiTNF y posteriormente tratamiento de mantenimiento con vedolizumab.
CP-153. DIAGNÓSTICO DIFERENCIAL DE COLECCIÓN ABDOMINAL EN PACIENTE CON ENFERMEDAD DE CROHN ILEOCÓLICA DE PATRÓN PERFORANTE
Bravo Aranda AM, Romero Cara P, Ocaña Ledesma A, Jiménez Pérez M
UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: colección abdominal, enfermedad de crohn, perforante.
Introducción
Alrededor de un 25% de los pacientes con enfermedad de Crohn presentará un absceso intraabdominal como complicación evolutiva a lo largo de su vida. No obstante, no todas las colecciones intraabdominales resultan abscesos, siendo recomendable realizar un diagnóstico diferencial con otras entidades.
Caso clínico
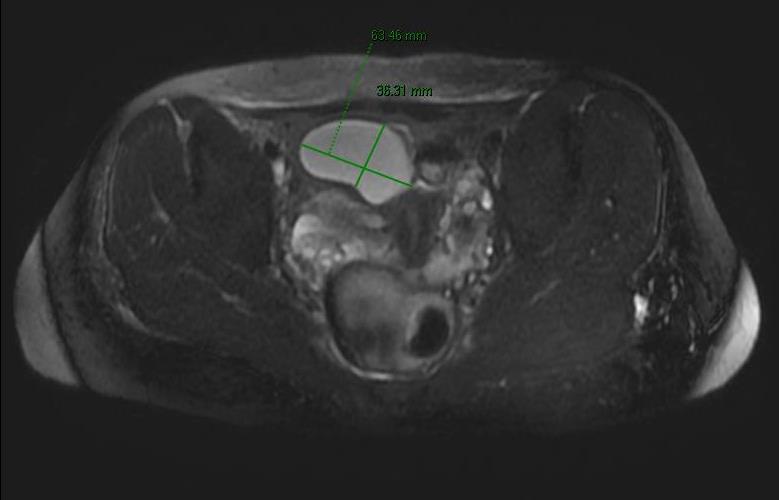
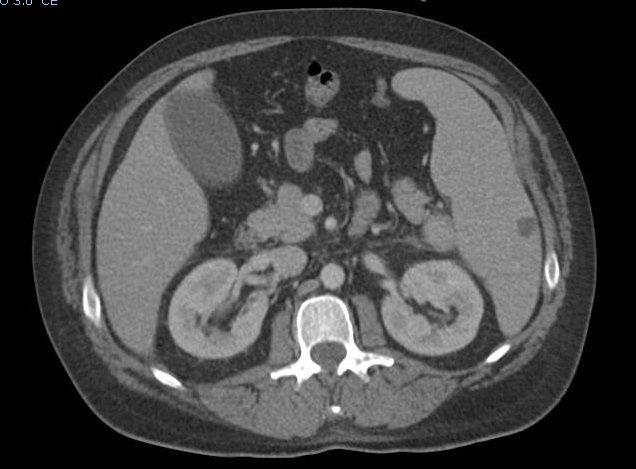
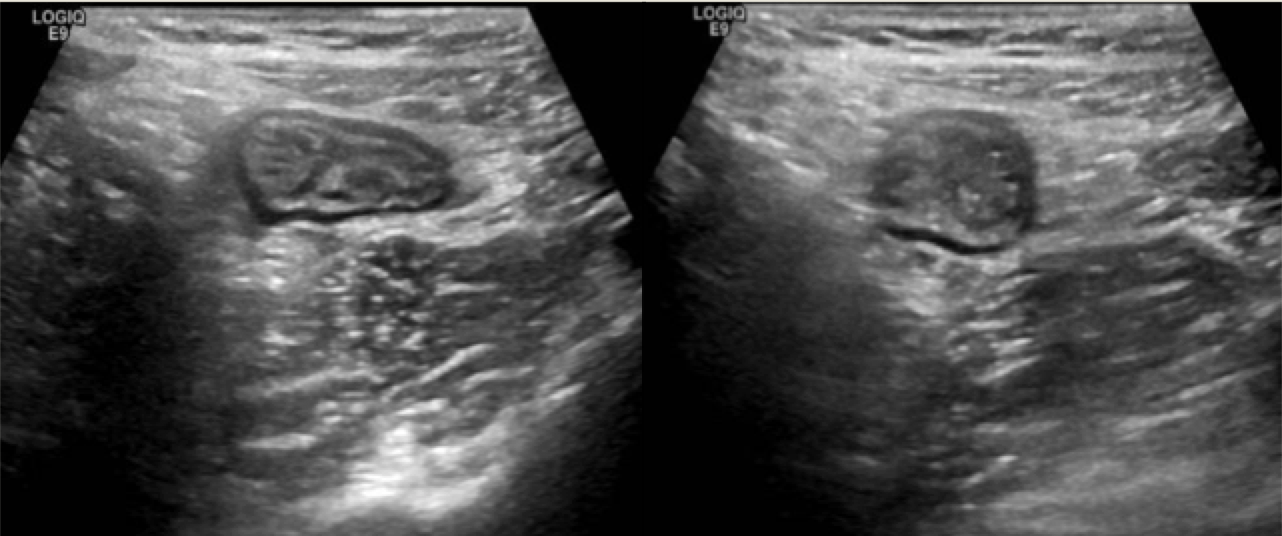
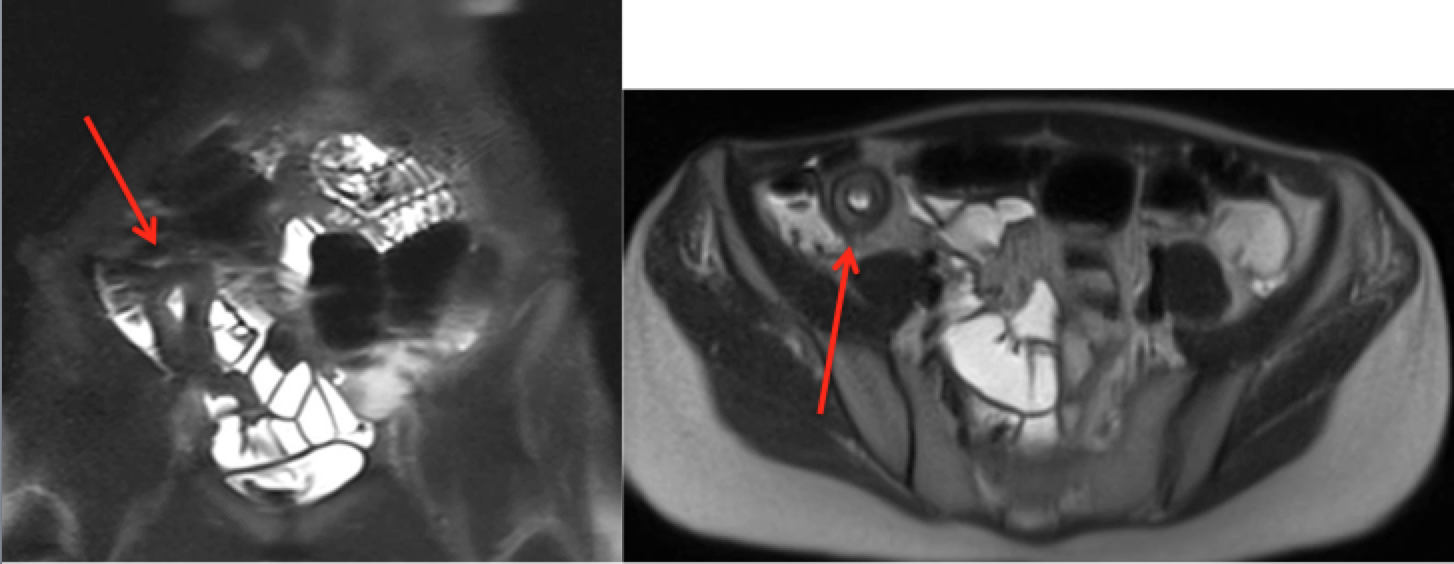
Mujer de 26 años con enfermedad de Crohn (EC) ileocólica (A2L3B3) de patrón perforante. Ingresa por dolor en hipogastrio de dos semanas de evolución asociado a sensación distérmica, diarrea y síndrome miccional. En analítica sanguínea destaca anemia, trombocitosis y leucocitosis con neutrofilia. En ecografía abdominal urgente se objetiva engrosamiento parietal de ciego e íleon terminal, con aumento de la ecogenicidad de la grasa adyacente, acompañado de una colección de 6.5x4 cm sugestivo con absceso supravesical decidiéndose ingreso hospitalario. La enteroRMN programada muestra un trayecto fistuloso entre ciego y asa de íleon terminal con marcados cambios inflamatorios locales y una colección supravesical de contenido homogéneo no fistulizada a vejiga sugestiva de quiste de inclusión peritoneal (QIP) . Se comprobó ausencia de fistula a vejiga mediante cistoTC y se realizó drenaje percutáneo de la misma obteniéndose un líquido claro ambarino no purulento cuyo cultivo fue negativo confirmando que la colección no era un absceso como complicación de EC perforante.
Figura 1
EnteroRM. Colección intraabdominal localizada caudal a ciego y supravesical compatible con quiste de inclusión peritoneal.
Discusión
El QIP es una lesión extremadamente rara producida por una proliferación mesotelial anómala reactiva secundaria a un daño en el peritoneo. Se postula que tiene su origen en una colección de líquido producido por un ovario activo, cuyas paredes están formadas por adhesiones peritoneales. Por lo tanto, ocurre predominantemente en mujeres en edad fértil. No obstante, el hecho de haber hallado esta entidad en varones y mujeres post-menopáusicas, y en abdomen superior, lejos de los anejos, sugiere que la secreción de líquido también puede provenir de la serosa peritoneal inflamada. Esto explicaría la incidencia de QIP en pacientes con antecedentes de cirugía abdominal y en pacientes con enfermedad de Crohn. El tratamiento de elección, en caso de pacientes sintomáticos, es el drenaje percutáneo. En casos recurrentes habría que considerar un tratamiento más invasivo, como la extracción laparoscópica del quiste y la lisis de adherencias abdominales. En conclusión, ante la presencia de una masa quística abdominal perianexal en pacientes con enfermedad inflamatoria intestinal, más allá de que se trate de un absceso, debería siempre incluirse en el diagnóstico diferencial la presencia de un quiste de inclusión intraperitoneal.
CP-154. ERITEMA NODOSO EN PACIENTE INMUNODEPRIMIDO
Valdés Delgado T, Maldonado Pérez B, Castro Laria L, Fernández Álvarez P, Caunedo Álvarez A
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: eritema nodoso, enfermedad inflamatoria intestinal, enfermedades oportunistas.
Introducción
El eritema nodoso (EN) es la forma de paniculitis más frecuente. Es un tipo de reacción cutánea inmunomediada que se asocia a una gran variedad de procesos patológicos.
Caso clínico
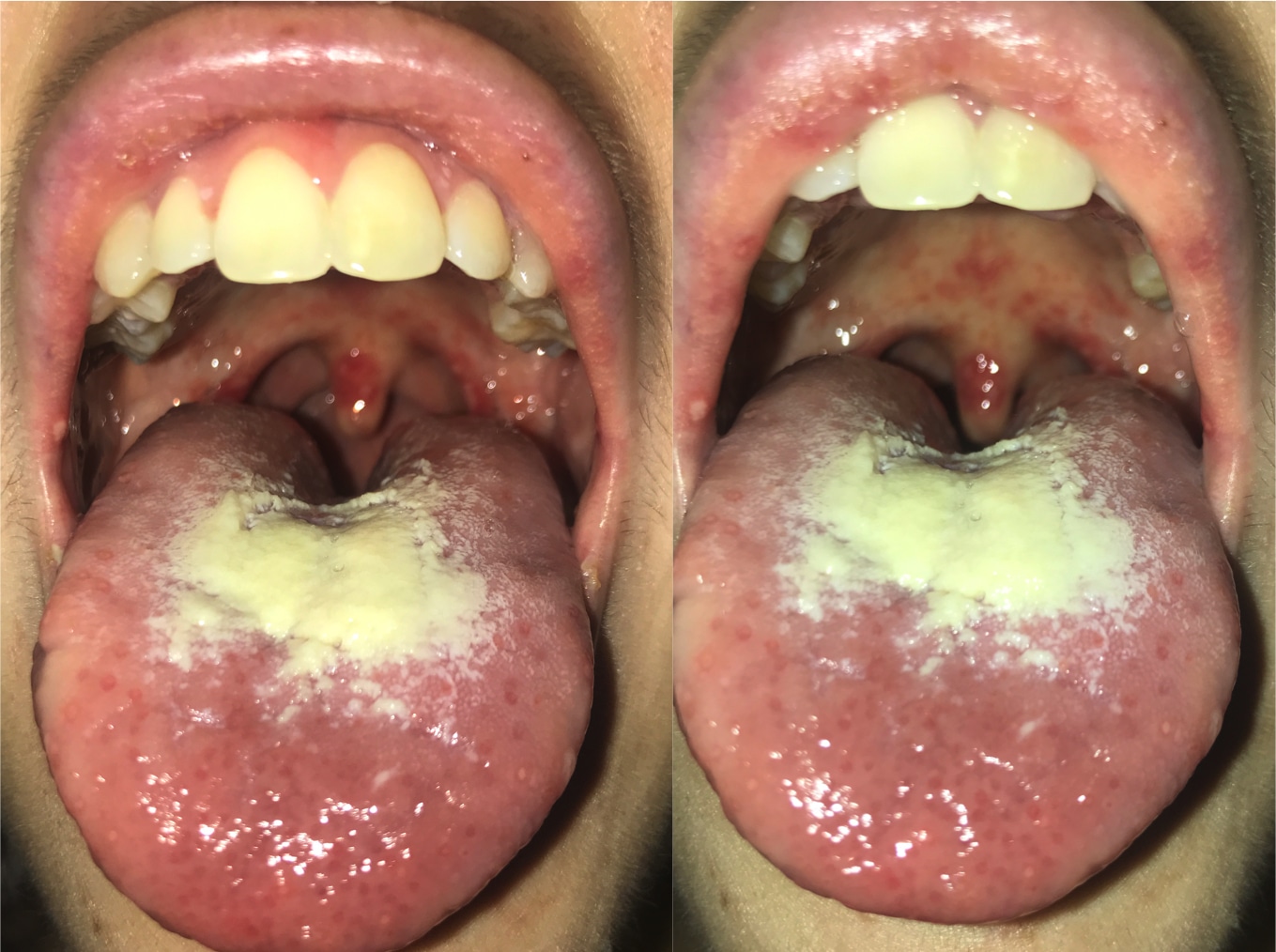
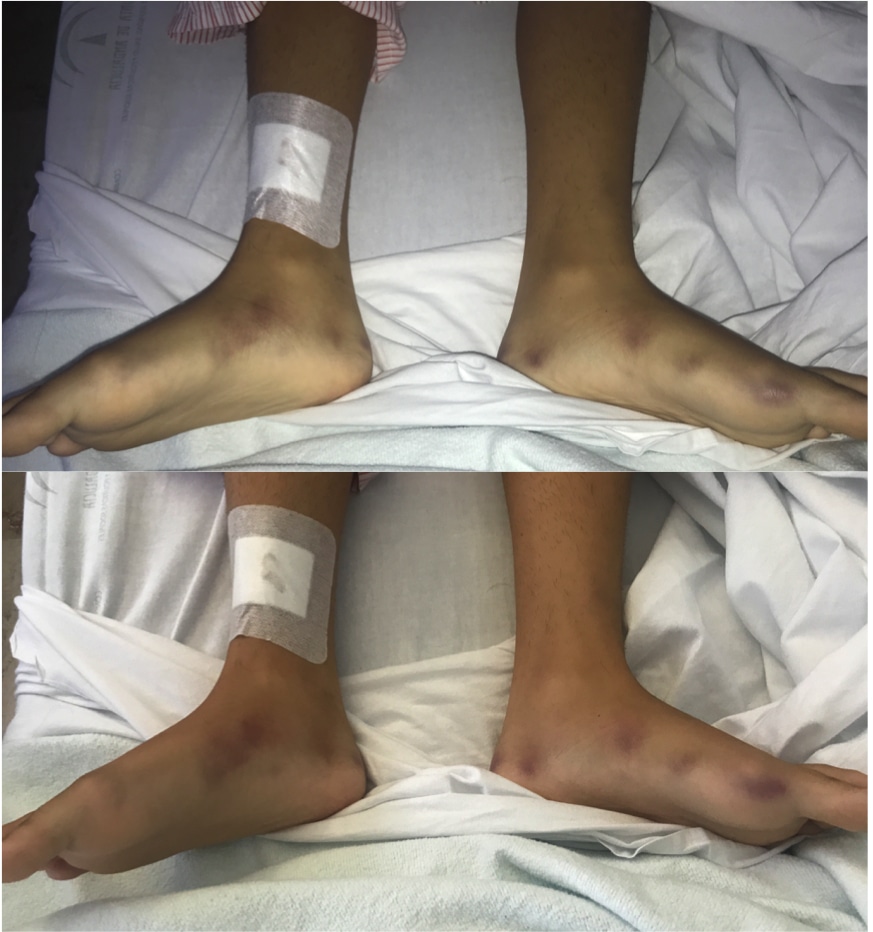
Mujer de 24 años con diagnostico de Colitis Ulcerosa (CU) izquierda en tratamiento con infliximab 5 mg/kg iv cada 6 semanas. Remitida desde consultas de Inflamatorias por cuadro febril de 15 días de evolución junto con odiofagia y dolor en ambos tobillos. A la exploración física destacó en mucosa oral placa blanquecina en lengua y pequeñas lesiones ulcerosas y dolorosas en paladar blando (Foto 1). En cuanto a las articulaciones no se objetivó edema, si dolor y tumefacción en ambos tobillos con lesiones violáceas, eritematosas, calientes y dolorosas en ambas caras internas de unos 5 cm de diamétro (Foto 2). Abdomen y resto de la exploración física normal. Analitica destacó: Hb 10.8 mg/dl, leucocitosis de 1490 con neutrofilia, PCR 163 y VSG 110. Serologías: IgG e IgM del VHS tipo I y II positivos (en 2 determinaciones), resto negativo. Autoinmunidad completa: negativa. Colonoscopia: Sin signos de actividad inflamatoria. PCR de CMV negativa. Biopsia lesiones dérmicas: Paniculitis septal sin vasculitis compatible con EN. Dado la clínica de la paciente junto con el resultados de las complementarias se inició tratamiento con Aciclovir 200 mg cada 6 h presentando una clara mejoría clínica dándose de alta con diagnóstico de Eritema Nodoso secundario a gingivoestomatitis Herpética.
Discusión
La revisión de la literatura demuestra que existen múltiples y variadas causas que pueden provocar brotes de EN. La presencia de este trastorno debe conducir siempre a la búsqueda de la posible etiología subyacente, aunque se estima el 30% son idiopáticos. Entre los factores etiológicos que pueden dar lugar a la aparición de EN se incluyen: infecciones, fármacos, enfermedades sistémicas, autoinmunes, EII y neoplasias. Especial mención a la EII, se asocia con más frecuencia a la EC (6-15%) que a la CU (1-9%) y es habitual que se correlacione el EN con la actividad de la enfermedad, coincidiendo la aparición de las lesiones con los brotes y remitir cuando se resuelve el brote. Destacar de nuestro caso la importancia que tiene el despitaje de enfermedades infecciosas en estos pacientes inmunodeprimidos (tanto por su patología de base como por la terapia biólogica). En este caso la aparición del EN se asoció a la CU (colonoscopia sin actividad inflamatoria) sino que fue desencadenado por una reactivación del VHS en nuestra paciente inmunodeprimida.
CP-155. FIEBRE SIN FOCO EN PACIENTE EN TRATAMIENTO INMUNOSUPRESOR
Barranco Castro D, Maldonado Pérez MB, Lorenzo González L, Castro Laria L, del Pino Bellido MP, Caunedo Álvarez Á
UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: enfermedad de crohn, tratamiento inmunosupresor, leishmaniasis.
Introducción
El manejo terapéutico de la enfermedad de Crohn (EC) incluye el uso de fármacos inmunosupresores y biológicos, que inducen una inmunodepresión celular, favoreciendo la aparición de infecciones oportunistas.
Caso clínico
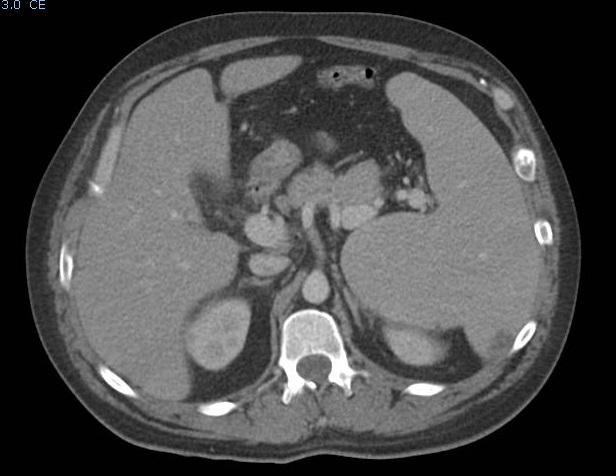
Varón de 44 años diagnosticado de EC hace 3 años (A3L2B1), en tratamiento con mesalazina, metotrexato e infliximab por enfermedad perianal desde hace 2 años, con buen control de su enfermedad. En seguimiento en consulta de oftalmología por queratouveítis herpética en ojo derecho. Acude a urgencias por malestar general, fiebre de 40ºC y vómitos de 48 horas de evolución. No signos de actividad de su enfermedad inflamatoria ni otra clínica asociada. No antecedentes epidemiológicos de interés. Exploración física sin hallazgos patológicos. Analíticamente destacan pancitopenia y elevación de lactato deshidrogenasa. Radiografía de tórax normal. En ecografía abdominal urgente se evidencia hepatoesplenomegalia. Inicialmente se sospechó posible infección oportunista, por lo que se suspendió su tratamiento inmunosupresor y se extrajeron hemocultivo, urocultivo, quantiferon y serología frente a diferentes agentes infecciosos. Dada la persistencia de la fiebre, se inició antibioterapia empírica con piperacilina-tazobactam y aciclovir intravenoso (ante posible infección herpética diseminada). Se realizó TAC de abdomen, confirmando hepatoesplenomegalia y descartando signos de afectación inflamatoria intestinal. La serología fue positiva para leishmania, por lo que comenzó tratamiento dirigido con anfotericina B liposomal como primera línea frente a leishmaniasis visceral, que fue sustituido por antimoniato de meglumina debido a efectos adversos (episodio de dolor lumbar, sudoración y palidez). El paciente presentó una mejoría clínica progresiva, permaneciendo afebril a partir del octavo día de tratamiento y con normalización del hemograma. Sin embargo, dada la ausencia de tratamiento para su EC, comenzó con aumento del número de deposiciones, algunas con restos de sangre y moco. Por ello se prescribió ciclo de corticoides en pauta descendente y como mantenimiento, se inició tratamiento con ustekinumab, por su buen perfil de seguridad y no requerir tratamiento inmunosupresor concomitante. De este modo se logró controlar el brote, y tras tres dosis de ustekinumab el paciente continua en remisión clínica.
Discusión
Este caso demuestra la importancia de descartar infecciones oportunistas en pacientes en tratamiento inmunosupresor. La presencia de fiebre, pancitopenia y hepatoesplenomegalia en un paciente con inmunodepresión celular en un área endémica, obliga a descartar leishmaniasis. Actualmente no hay recomendaciones en la profilaxis de leishmania para este tipo de pacientes. Por otro lado, destacar el buen perfil de seguridad de ustekinumab, especialmente frente a infecciones oportunistas, que son más frecuentes en el uso de fármacos anti-TNF.
CP-156. MANEJO DE COLITIS ULCEROSA GRAVE CORTICORREFRACTARIA. EXPERIENCIA EN NUESTRO CENTRO: ANTICALCINEURÍNICOS Y VEDOLIZUMAB.
Moreno Moraleda I, López Gon´zalez J, Lazaro Saéz M, Dieguez Castillo C
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: colitis ulcerosa grave, anticalcineurínicos, vedolizumab.
Introducción
El objetivo de esta revisión es describir la experiencia en nuestro centro en cuanto al manejo del brote grave de colitis ulcerosa, centrándonos fundamentalmente en el papel del tratamiento combinado con ciclosporina y vedolizumab.
Material y métodos
Revisión de carácter retrosprectivo en la que incluimos tres casos clínicos con diagnóstico de colitis ulcerosa grave corticorrefractaria en nuestro centro (C.H. Torrecárdenas), en un periodo comprendido entre enero de 2015 y junio de 2019, obteniendo los datos de nuestra base informática Diraya Clínico.
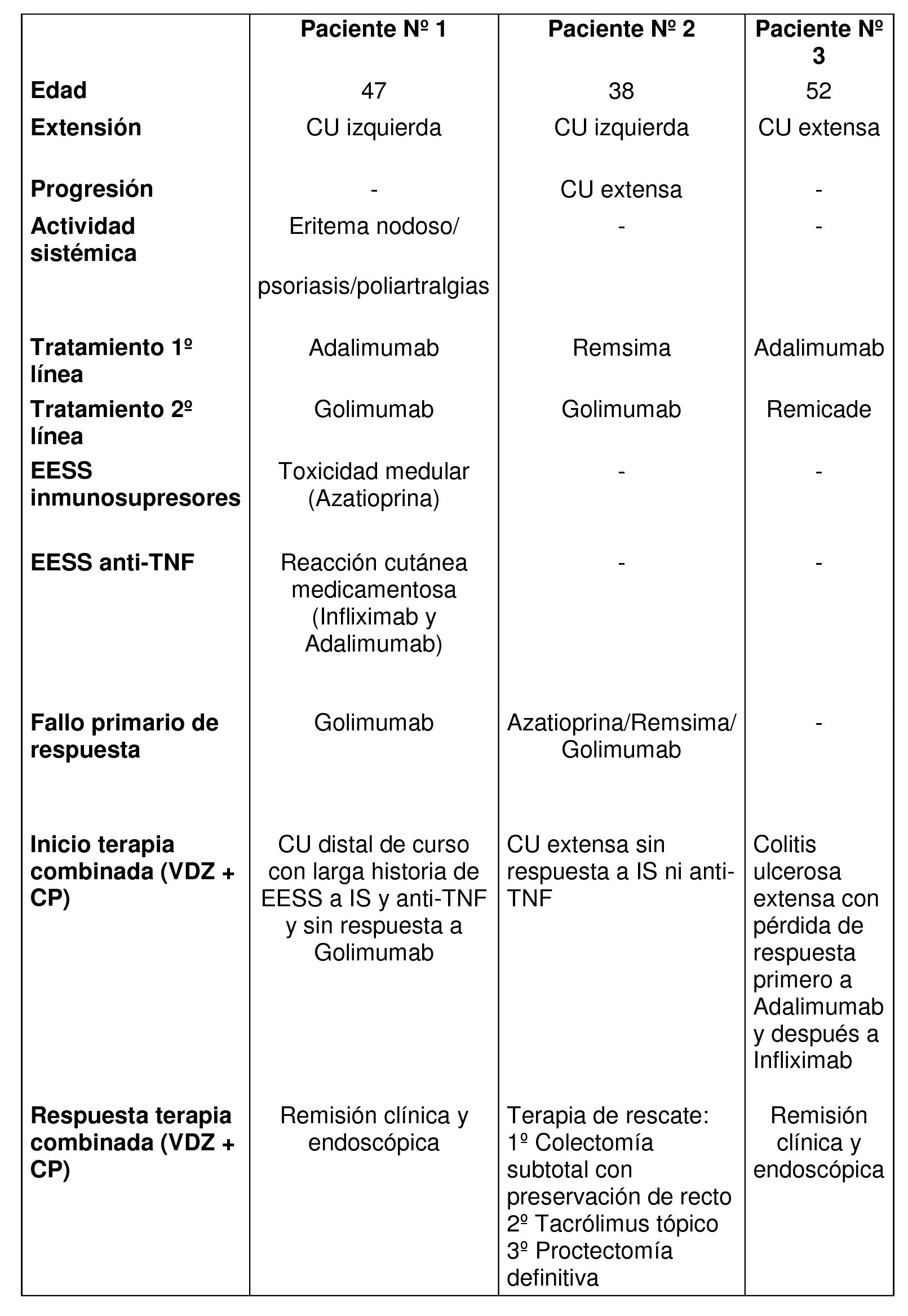
Resultados
En los tres pacientes se inició tratamiento con vedolizumab tras ausencia de respuesta a tratamiento con inmunosupresores y al menos dos anti-TNF. En uno de ellos, tras diagnóstico inicial de colitis ulcerosa distal, se confirmó tras meses de evolución progresión de la enfermedad a colitis extensa. Uno de ellos cursó desde el inicio con actividad sistémica severa, describiéndose en el curso de la misma una larga historia de efectos adversos a inmunosupresores (toxicidad medular) y a anti-TNF (reacciones cutáneas con adalimumab e infliximab). Primera línea de tratamiento. El primer tratamiento biológico empleado en dos de los casos fue adalimumab (uno de ellos tras brote grave que precisó ciclosporina IV), ambos en combinación con azatioprina. El segundo caso comenzó tratamiento con infliximab, en un primer momento con el biosimilar (REMSIMA), aunque tras comprobar mejoría parcial de la sintomatología se decide cambio por otro anti-TNF (golimumab). Segunda línea de tratamiento. En los casos en los que se empleó adalimumab, como segunda opción de tratamiento se emplea en uno de ellos remicade y en el otro golimumab. En los dos casos en los que se emplea golimumab como 2º línea de tratamiento se comprueba un fallo de respuesta primario. Terapia combinada (vedolizumab y ciclosporina). Uno de los casos precisó terapia quirúrgica de rescate por ausencia de respuesta a todas las modalidades de tratamiento.
Conclusiones
La colitis ulcerosa es una enfermedad inflamatoria crónica que presenta un curso recurrente y una gran variabilidad clínica en cuanto a la forma de presentación, a la gravedad del brote y a la respuesta a los diferentes tratamientos disponibles. Los principales dilemas que nos encontramos en la práctica clínica son cómo identificar en un estadio precoz qué pacientes precisarán cirugía y cuándo empezar una terapia de rescate. La terapia combinada con ciclosporina y vedolizumab podría ser una opción en pacientes con brote grave de colitis ulcerosa refractarios a otras terapias.
CP-157. NEUMONITIS POR MESALAZINA EN PACIENTE CON COLITIS ULCEROSA
Morcillo Jimenez E, Rico Cano A, Garcia Sanchez AB
Unidad Aparato Digestivo. Clínica Parque San Antonio, Málaga.
Palabras clave: neumonitis, mesalazina.
Introducción
La mesalazina es ampliamente utilizada en el tratamiento de la colitis ulcerosa. Los efectos secundarios descritos son raros o muy raros. Las enfermedades pulmonares intersticiales difusas (EPID) constituyen un grupo de afecciones con manifestaciones clínicas, radiológicas y funcionales respiratorias similares; la etiología de las EPID es muy variada. Las manifestaciones clínicas más frecuentes son disnea progresiva y tos. Habitualmente, la sospecha de que sea un fármaco el que puede estar provocando la situación clínica de neumonitis intersticial se produce cuando se descartan otras causas más frecuentes y otros procesos, como los neoplásicos.
Caso clínico
Paciente de 71 años, cartero jubilado y sin hábitos tóxicos, con hipertensión arterial en tratamiento con enalapril. Diagnosticado de colitis ulcerosa extensa moderada en Julio de 2017 iniciándose corticoterapia, mesalazina oral a dosis altas (4 g/dia) y mesalazina tópica. Al mes y medio de haber iniciado este tratamiento y tras llevar 6 días sin corticoides, acude a urgencias por rash cutáneo generalizado pruriginoso, fiebre vespertina, tos seca, disnea y molestia centrotorácica. Se realiza analítica al ingreso con linfomonocitosis relativa y PCR elevada. Durante su hospitalización se realiza serología de CMV, VEB, clamydia, coxiella, mycoplasma pneumoniae, rickettsia y parvovirus B19 siendo negativas. ANA, factor reumatoide y C3, C4 y C50 negativos. Ag de legionella y pneumococo en orina negativos. Hemocultivo negativo. Tc de tórax con infiltrado intersticial reticular con infiltrados periféricos. Inicialmente se trata con levofloxacino sin clara mejoría clínica persistiendo tos y disnea. Ante estos datos, se suspende mesalazina oral y tópica y ya que el paciente se encuentra muy sintomático, se inicia corticoterapia desapareciendo rápidamente los síntomas respiratorios.
Discusión
Las alteraciones pulmonares, como la neumonitis, solo están recogidas como reacciones muy raras en la ficha técnica de la mesalazina, complicando la identificación de los posibles casos. En este paciente inicialmente nos planteamos el diagnóstico diferencial entre neumonitis por hipersensibilidad a mesalazina, neumonía viral y atípica. Dado que las serologías virales y atípicas fueron negativas, y existía una secuencia temporal entre el inicio del tratamiento y entre el comienzo de los síntomas (aunque quizás levemente alargada por la toma concomitante de corticoides), se planteó como principal diagnóstico neumonitis por hipersensibilidad a mesalazina, aunque en este caso no se pudo realizar broncoscopia por el estado clínico del paciente, para su confirmación. Al mes del alta hospitalaria, el paciente se encontraba asintomático desde el punto de vista respiratorio y digestivo, realizándose tc de torax de control con mejoría del infiltrado intersticial.
CP-158. OPTIMIZACIÓN TERAPÉUTICA CON USTEKINUMAB BASADA EN REINDUCCIONES EN PACIENTE GRAVE: ¿LOS NIVELES IMPORTAN?
Fernández Alvarez P, Belvis Jimenez M, Maldonado Pérez B, Castro Laria L, Caunedo Alvarez A, Argüelles Arias F
UGC Aparato Digestivo. Hospitales Universitarios Virgen Macarena - Virgen del Rocío, Sevilla.
Palabras clave: enfermedad de crohn, niveles farmacológicos, ustekinumab.
Introducción
El tratamiento con Ustekinumab es muy eficaz en pacientes con enfermedad de Crohn (EC) en los que ha fallado la terapia anti-TNF. En determinados casos, la reinducción con Ustekinumab (UST) intravenoso (iv), puede utilizarse de forma segura para inducir respuesta y/o remisión completa en pacientes en los que la fórmula subcutánea (sc) no lo consigue.
Caso clínico
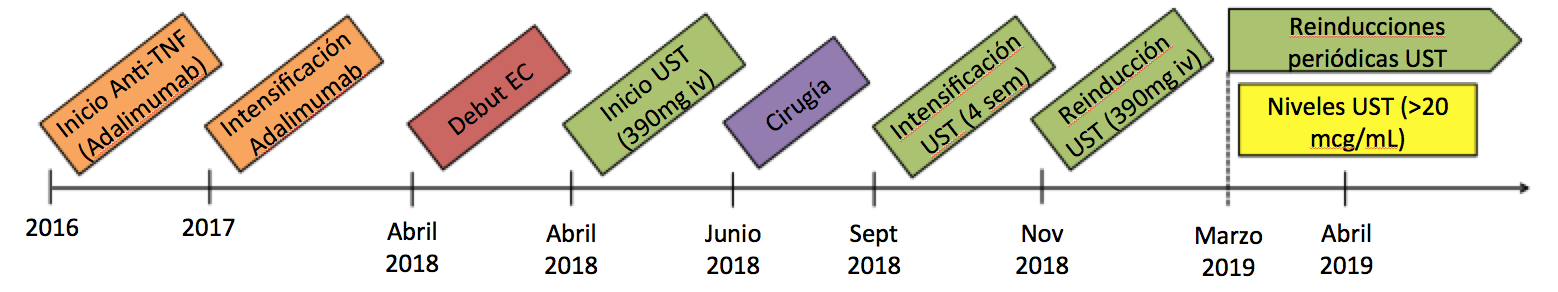
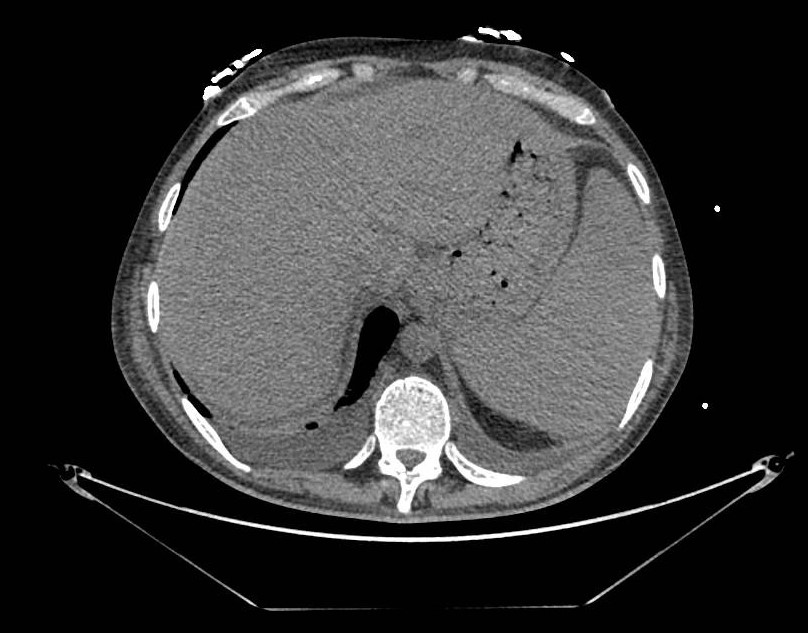
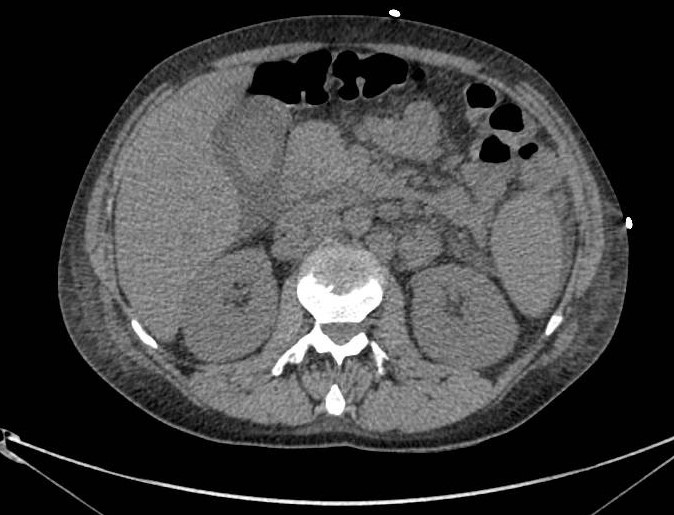
Presentamos el caso de una mujer de 26 años con antecedentes de artritis psoriásica (AP) desde los 4 años, en tratamiento inicial con Metrotexato. En 2016, por mala evolución de la enfermedad se inició tratamiento con anti-TNF (adalimumab). Tras nuevo brote se decidió intensificación del fármaco acortando los intervalos de administración a 40 mg/semana. Posteriormente, tras apendicectomía por clínica compatible con apendicitis aguda se llegó al diagnóstico histológico de EC. A los pocos meses, la paciente fue hospitalizada por un brote moderado-grave de su EC con actividad en pruebas de imagen (Figuras 1 y 2) y endoscópicas (Figura 3). Dados los hallazgos compatibles con EC inflamatoria-estenosante con inadecuada respuesta a anti-TNF y antecedentes de AP, se decidió iniciar tratamiento con UST a dosis de inducción de 390 mg (iv) y 90 mg (sc)/8 sem. En 2018 precisó ileocequectomía laparoscópica, manteniéndose tratamiento con UST. Tras varios brotes de su AS, se intensificó tratamiento, acortando el intervalo de administración a 4 semanas. Posteriormente, tras colonoscopia con datos de recurrencia sobre la anastomosis i2b según Rutgeerts, se propuso reinducción 390 mg (iv) y mantenimiento 90 mg (sc)/4 sem. Finalmente, desde marzo de 2019, dada la dependencia intermitente a corticoterapia se ha optado por reinducciones periódicas, administrándole UST 390 mg (iv) y 90 mg(sc) de forma alternante cada 4 semanas; consiguiendo la remisión clínica y analítica (calprotectina fecal 125 μg/g) y niveles del fármaco >20mcg/mL.
Figura 1
Imagen ecográfica que muestra marcado engrosamiento de la pared de ileon distal con estenosis de la luz y dilatación de asas proximales.
Figura 2
Imágenes de resonancia magnética en el plano sagital y axial que muestran el engrosamiento de la pared del ieón terminal afectando a un segmento de unos 10 cm.
Figura 3
En colonoscopia se objetiva válvula ileocecal estenótica (no canjeable) con úlceras y pseudopólipos sobre sus bordes.
Discusión
En pacientes graves, es importante alcanzar niveles superiores de fármaco, probablemente porque su carga inflamatoria es mayor. Así, en algún estudio, se ha propuesto la necesidad de reinducir para alcanzar dosis superiores de fármaco y conseguir mayores tasas de remisión. Planteamos que, en determinados casos, como el que nos atañe, reinducciones periódicas cada 4 semanas o con dosis iv periódicas, manteniendo concentraciones séricas de UST muy elevadas, pueden ser necesarias para conseguir la remisión clínica, biológica y endoscópica. Revisando la literatura no hemos encontrado el manejo en EC con dosis tan elevadas de UST. De este modo, y siempre teniendo en cuenta que el tratamiento de la EC ha de ser individualizado para cada paciente, proponemos una nueva estrategia de intensificación en pacientes graves y/o con enfermedades reumáticas asociadas, con pérdida de respuesta.
CP-159. SÍNDROME HEMOFAGOCÍTICO Y LINFOMA B DIFUSO DE CÉLULAS GRANDES EN PACIENTE TRATADO CON ADALIMUMAB POR ENFERMEDAD DE CROHN
Herrador Paredes M, Librero Jiménez M, Cabello Tapia MJ, Ortega Suazo EJ, Abellán Alfocea P, Redondo Cerezo E
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: adalimumab, enfermedad de crohn, virus de epstein barr.
Introducción
El Síndrome hemofagocítico (SHF) es una entidad poco frecuente caracterizada por una activación masiva de macrófagos que fagocitan elementos hematopoyéticos y células sanguíneas maduras. Diversas condicionaes llevan a que este proceso se desencadene, entre las destacan infecciones, enfermedades autoinmunes y neoplasias.
Caso clínico
Se trata de un paciente varón de 29 años con antecedentes personales de enfermedad de Cronh ilecólica diagnosticada en 2006 en tratamiento actual con adalimumab. Previamente tratado con mesalazina, azatioprina, suspendida por mala tolerancia, e infliximab, con buena repuesta pero que fue cambiado a adalimumab por preferencia del paciente, con buena respuesta también. Ingresa en la UCI por shock hemodinámico, pancitopenia y disfunción hepática con cuadro previo de un mes de evolución de fiebre asociada a síndrome constituacional. Durante su estancia en UCI se realiza batería de pruebas microbiológicas con único hallazgo de infección aguda por VEB con 86 000 copias de DNA, con IgG VEB previamente positiva. En pruebas de imagen presencia de hallazgos compatibles con proceso proliferativo con afectación de múltiples cadenas ganglionares y hepatoesplenomegalia (Figuras 1 y 2). En biopsia ganglionar axilar hallazgos compatibles con linfoma B difuso de células grandes y biopsia de médula ósea compatible con hemofagocitosis, con diagnóstico final de SHF secundario a linfoma B difuso de células grandes y a infección por VEB. Se produjo mejoría importante tras inicio de tratamiento quimioterápico y pudo irse de alta a domicilio con control ambulatorio. A los pocos meses reingresa por nuevo cuadro febril y pancitopenia severa, en relación con reactivación de SHF. En planta presenta mala evolución, con importante compromiso respiratorio y finalmente fallece en la UCI a consecuencia de una hemorragia intracreaneal masiva.
Discusión
El contexto clínico y la infección de VEB hablan a favor de un proceso linfoproliferativo B asociado a inmunodeficiencia, en este caso terapia biológica con adalimumab, que ha propiciado la reactivación del VEB y este a su vez al desarrollo de linfoma. Ambos acontecimientos han conducido a la reactivación masiva del sistema fagocítico y a sus consecuencias fatales. Tanto el desarrollo del linfoma como el dearrollo del síndrome hemogafocítico son de los efectos adversos más temidos del tratamiento inmunomodulador. Suele producirse más frecuentemente en relación a primoinfección del VEB y sobre todo en relación a tratamiento con tiopurinas. En este caso se trataba de una reactivación del virus, ya que el paciente era previamente IgG positivo, y además en relación con un antiTNF.
CP-160. TRATAMIENTO CON USTEKINUMAB EN PACIENTE CON ENFERMEDAD DE CROHN Y SÍNDROME DE INTESTINO CORTO.
Bernal Torres Á, Viejo Almanzor A, Guerrero Palma E, Correro Aguilar FJ
Servicio Aparato Digestivo. Hospital Puerta del Mar, Cádiz.
Palabras clave: enfermedad de crohn, ustekinumab, síndrome de intestino corto.
Introducción
Hasta un 40% de pacientes con EC no responden de forma primaria a los anti-TNF y hasta un 30% de ellos pueden experimentar una pérdida secundaria de repuesta. En los últimos años se han desarrollado nuevos tratamientos, como ustekinumab (UST), anticuerpo monoclonal que inhibe la acción de la interleucina 12-23 bloqueando la subunidad común p40.
Caso clínico
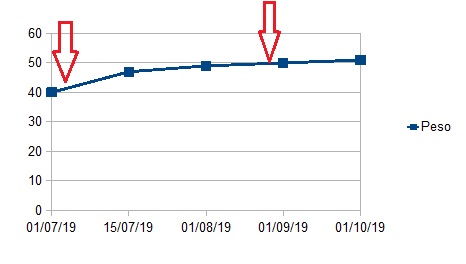
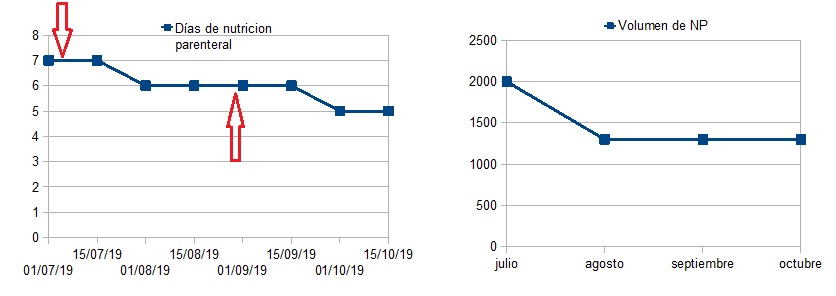
Mujer de 40 años diagnosticada de EC a los 13 años de edad, con afectación estenosante de íleon distal. Patrón agresivo que precisó cuatro resecciones intestinales y finalmente proctocolectomía total con ileostomía definitiva en 2010. Múltiples ingresos por nuevos brotes, fístulas en diferentes localizaciones, complicaciones infecciosas… desarrollando pérdida de respuesta a los inmunosupresores y psoriasis secundaria a anti-TNF, por lo que se mantuvo sin tratamiento en los últimos años. Desarrolló en 2011 un síndrome de intestino corto (SIC) tratado inicialmente mediante sueroterapia pero precisando con el paso del tiempo de alimentación parenteral domiciliaria (NPD). Desde el último año en tratamiento también con tedoglutide, reduciendo necesidad de líquidos pero manteniendo NPD. Último ingreso en Mayo-2019, con nuevo un brote de su EC, actividad inflamatoria ileal, fístula enterocutánea con débito alto y colección abscesificada. Tras dieta absoluta, NP, antibioterapia y drenaje presentó aceptable respuesta. Se planteó nueva cirugía pero dados los antecedentes de SIC, se propuso tratamiento con UST por su perfil de seguridad y rapidez de acción. Tras resolución del cuadro infeccioso, recibió inducción en pauta habitual con rápida respuesta clínica y biológica: cierre completo de la fístula enterocutánea y débito por ileostomía controlado. Reinició tolerancia oral tras 24h de la dosis iv, manteniendo tratamiento con tedoglutide y NPD. Presentó ganancia ponderal progresiva (FIGURA-1) hasta alcanzar normopeso a las 10-12 semanas de haber recibido la primera dosis de UST, lo que le ha permitido reducir por el momento en 2 días la NPD (FIGURA-2). No ha presentado complicaciones infecciosas ni efectos secundarios.
Discusión
A pesar de los tratamientos inmunomodulares, muchos pacientes con EC requerirán intervenciones quirúrgicas que pueden producir SIC. La nutrición parenteral primaria o suplementaria a la nutrición enteral es el tratamiento clásico. Se han desarrollado fármacos específicos que mejoran la absorción intestinal del intestino remanente, como Tedoglutide. En nuestro caso, el tratamiento con UST ha reducido la actividad inflamatoria intestinal, mejorando el débito por la ileostomía y cerrando la fístula enterocutánea, lo que ha permitido mejorar la capacidad funcional intestinal de la paciente posibilitando la reducción de la NPD, sin que se hayan registrados efectos adversos.
CP-161. TRATAMIENTO DE BROTE DE COLITIS ULCEROSA CORTICORREFRACTARIA EN PACIENTE CON ESCLEROSIS MÚLTIPLE
Abellán Alfocea P, Herrador Paredes M, Sánchez Capilla AD, López Vico M, Rosa Sánchez C, Redondo Cerezo E
Unidad Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: colitis ulcerosa, esclerosis múltiple, plasmaféresis.
Introducción
La colitis ulcerosa constituye una de las enfermedades más importantes dentro del marco de la gastroenterología actual, pudiendo ser una enfermedad muy limitante y con importante riesgo de complicaciones y alta morbimortalidad. El uso de biológicos como los antiTNF resulta esencial en el manejo de esta patología. Sin embargo, una de las principales contraindicaciones absolutas para el uso de estos fármacos son las enfermedades desmielinizantes tales como la esclerosis múltiple. En este caso clínico se expone el caso de una paciente con ambas patologías y el uso de una terapia alternativa en estas situaciones: la granulocitoaféresis.
Caso clínico
Mujer de 65 años con antecedentes de colitis ulcerosa izquierda, esclerosis múltiple y psoriasis que ingresa por nuevo brote de intensidad moderada-grave de su EICI (Mayo parcial 7). Durante su ingreso presenta una evolución tórpida y refractaria a corticoides intravenosos (1mg/kg), por lo que se realiza colonoscopia que descarta CMV y confirma afectación grave (Mayo 3) y se inicia ciclosporina intravenosa con respuesta parcial cambiando a azatioprina oral. Dada la situación, se plantea terapia con vedolizumab, para lo cual se realizan dos IGRA, presentando un resultado repetidamente indeterminado, por lo que se inicia tratamiento profiláctico con isonizada y, como terapia puente, se decide realizar plasmaféresis seriadas. Pasado un mes, y tras varias sesiones de plasmaféresis, la paciente, presenta mejoría clínica (Mayo parcial 4), sin anemia y recuperando peso perdido.
Discusión
Aunque en el manejo de la colitis ulcerosa hay numerosas opciones terapéuticas, la gravedad del brote y la presencia de comorbilidades como en este caso pueden reducir enormemente nuestro arsenal terapéutico. Aunque la plasmaféresis se ha usado en casos de Esclerosis Múltiple, son necesarios más estudios que indiquen el papel de la granulocitoaféresis en esta enfermedad. La granulocitoaféresis debe ser una terapia a considerar, ya sea como tratamiento coadyuvante o como puente a otros tratamientos contraindicados de forma temporal, debido a su perfil de seguridad.
CP-162. USO COMPASIVO DE USTEKINUMAB COMO RESCATE EN COLITIS ULCEROSA CON FALLO A CUATRO LÍNEAS TERAPÉUTICAS: A PROPÓSITO DE UN CASO
Pinazo Bandera JM, Cobos Rodriguez J, García García AM, Toro Ortiz JP, Fernandez García F, Gil Ayuso J, Asady Ben G, Martos Van Dussen JV, Camargo Camero R, Alcain Martinez G
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Virgen de la Victoria, Málaga.
Palabras clave: ustekinumab, colitis ulcerosa, corticodependencia.
Introducción
Ustekinumab es un agente biológico que actúa inhibiendo la actividad de IL-12 e IL-23. En los últimos años se ha instaurado en el algoritmo terapéutico de la Enfermedad de Crohn con un uso creciente debido a su eficacia (tanto en pacientes "naive" como en fallos previos a otras líneas terapéuticas) y por su perfil de seguridad debido a su baja tasa de infecciones/tumores. Presentamos un caso de buena respuesta al uso compasivo de Ustekinumab en el seno de un brote grave de pancolitis ulcerosa.
Caso clínico
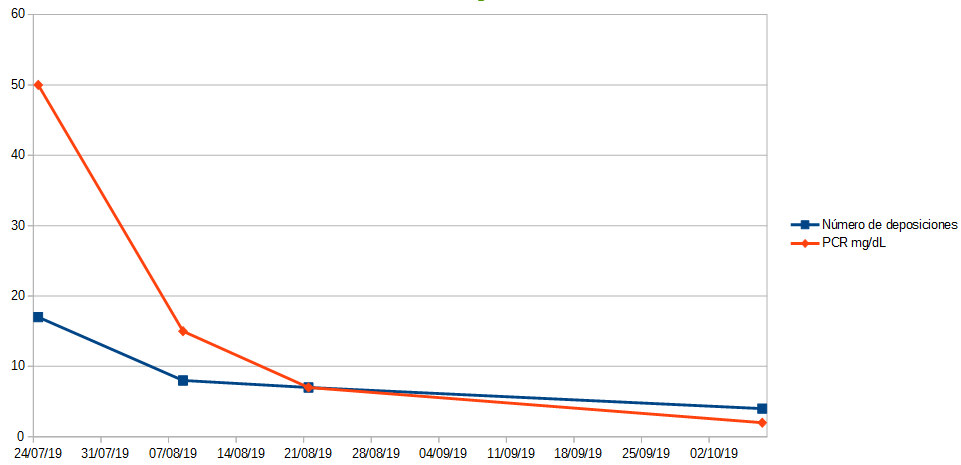
Varón, 40 años, Colitis Ulcerosa E3 de Montreal diagnosticado en 2004. Eritema nodoso y artritis como manifestaciones extraintestinales. En tratamiento con Mesalazina y Azatioprina desde su diagnóstico. A los pocos meses del mismo, inició tratamiento con Infliximab por brote grave que tuvo que suspender en 2015 por fallo secundario. Se realizó switch a Adalimumab que se intensificó por baja respuesta y finalmente se suspendió por fallo primario (2016). Se decidió iniciar Vedolizumab para cambiar de línea terapéutica pero tras dos años de tratamiento, por reaparición de síntomas, se consideró fallo secundario, discontinuando el fármaco (2018). Tras constatar de nuevo actividad endoscópica y clínica, y dado corticodependencia, se suspendió azatioprina y se inició Tofacitinib con muy buena respuesta al inicio. Tras seis meses reaparecieron los síntomas y se interrumpió el tratamiento. Desde el fallo a tercer biológico se le planteó la opción de cirugía curativa pero el paciente declinaba y se abogó por agotar todas las opciones médicas. En julio 2019 el paciente reingresó por brote grave y criterios de corticorresistencia. Se inició, de forma compasiva, Ustekinumab intravenoso a dosis inicial de 390 mg ajustado a peso con buena respuesta inicial que nos permitió ir reduciendo corticoides e incluso desescalar a vía oral. El paciente fue dado de alta por mejoría clínico-analítica evidente (Tabla 1/Figura 1). Ambulatoriamente, se continuó tratamiento con Ustekinumab subcutáneo cada 8 semanas con buen control sintomático y analítico. Actualmente el paciente se encuentra pendiente de la cuarta dosis de dicho biológico y en pauta descendente de corticoterapia (actualmente menos de 10 mg de Prednisona).
Figura 1
Evolución clínico-analítica desde el ingreso en planta hasta la última visita a la consulta (Número de deposiciones/PCR mg/dL)
Tabla 1
Evolución clínico-analítica del paciente desde ingreso del paciente hasta la última visita en consulta
Discusión
Este caso apoya lo percibido en la literatura. Los fármacos biológicos anti-IL12-23 son eficaces en el tratamiento de pacientes con colitis ulcerosa, incluso con fallo a varias líneas terapéuticas, con un buen perfil de seguridad y excelente respuesta clínica; por lo que es muy probable que a corto plazo se apruebe este fármaco para el tratamiento de la Colitis Ulcerosa en la Unión Europea y en España.
CP-163. USTEKINUMAB COMO TRATAMIENTO CURATIVO DE PIODERMA GANGRENOSO
Lopez Gonzalez J, Lázaro Saez M, Calvo Bernal MM, Hernandez Martinez A
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: ustekinumab, pioderma gangrenoso, enfermedad crohn.
Introducción
El pioderma gangrenoso es una dermatosis ulceronecrótica neutrofílica que se manifiesta como un nódulo o pústula estéril que rápidamente progresa a una úlcera purulenta dolorosa, con bordes irregulares, serpinginosos, edematosos, violáceos y socavados. Pueden ocurrir en cualquier localización, siendo las piernas la más frecuente. Su aparición es mas frecuente en pacientes con Colitus Ulcerosa que en aquellos que presentan Enfermedad de Crohn, si bien puede darse en ambas entidades.
Caso clínico
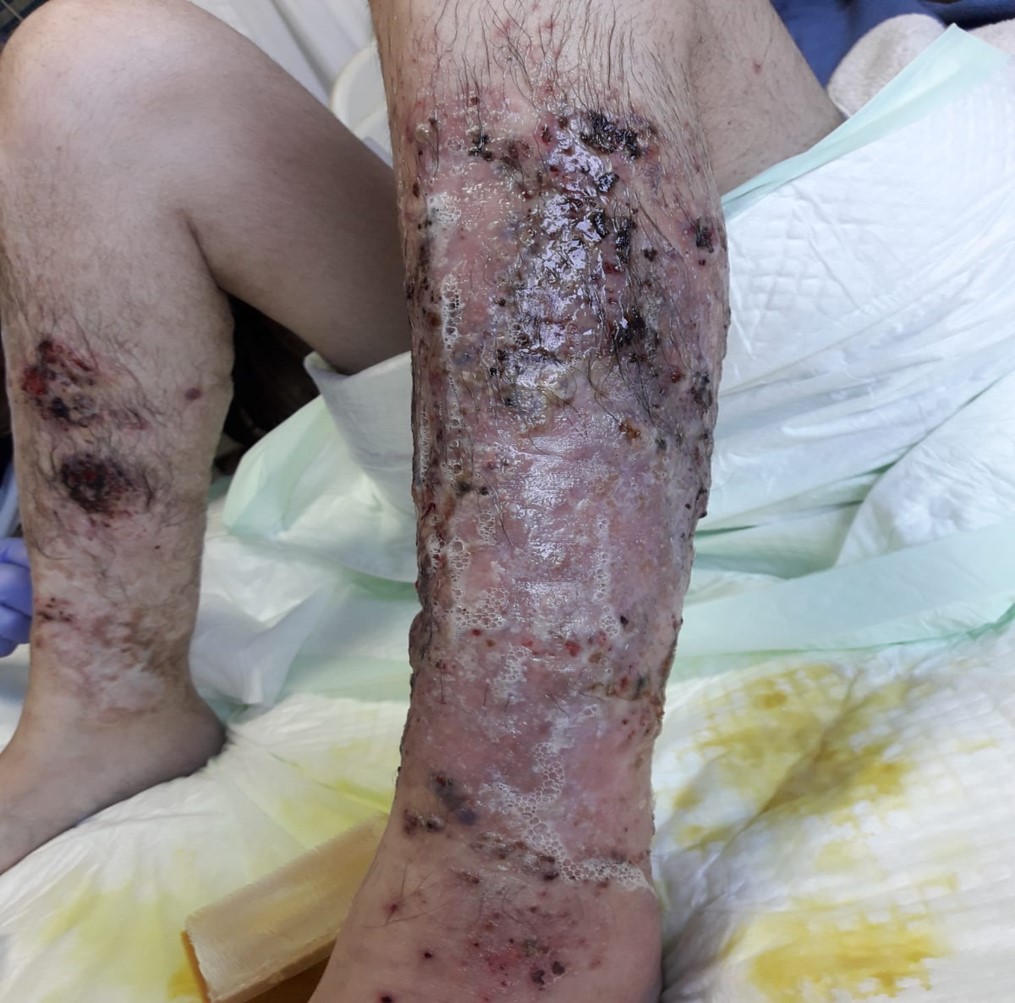
Mujer de 29 años con antecedente personal de Enfermedad de Crohn fistulizante compleja y de Pioderma Gangrenoso resuelto mediante ciclosporina y medidas locales (sulfato de zinc y mupirocina), en tratamiento en esos momentos con Adalimumab intensificado, con buen control de la clinica digestiva, que es derivada desde Atención Primaria por lesiones cutáneas muy dolorosas a nivel pretibial en ambos miembros inferiores de dos meses de evolución, acompañadas de fiebre de hasta 38ºC. Al ingreso, se solicita cultivo del exudado de la úlcera (Figuras 1 y 2), donde se desarrolla una Pseudomona Aeruginosa productora de carbapenemasas, sensible a piperacilina-tazobactam y ciprofloxacino. Se inicia antibioterapia con piperacilina-tazobactam y corticoterapia (además de terapia local con permanganato, clobetasol y mupirocina), y se programan sesiones de curas en quirófano de Dermatología. Al mes del alta hospitalaria, se objetiva nuevo empeoramiento de las lesiones cutáneas , a pesar de encontrarse la paciente asintomática desde el punto de vista digestivo. Con objetivo de control del cuadro dermatológico, se decide la suspensión de Adalimumab y el inicio de tratamiento con Ustekinumab, tras lo cual la paciente mejora de forma muy significativa (Figura 3), sin objetivarse recidiva de la clínica digestiva, manteniendose actualmente asintomática también desde el punto de vista dermatológico.
Discusión
El diagnostico del pioderma gangrenoso se basa en una clínica y hallazgos histológicos compatibles, asi como el descarte de otras posibilidades diagnósticas. Para su tratamiento, clásicamente se ha dispuesto de inmunosupresores como la ciclosporina, la azatioprina o el micofenolato de mofetilo, además de antibióticos como la doxiciclina. En los últimos años, la aparición de los biológicos ha supuesto una revolución en el tratamiento de esta patología. Ustekinumab está apareciendo como alternativa válida para el tratamiento de esta patología. En el caso de nuestro paciente, su uso ha conseguido la mejoría significativa del cuadro de pioderma gangrenoso, refractario previamente a infliximab y adalimumab, lo cual suscita gran interés debido a un posible desarrollo futuro del fármaco en esta patología.
CP-164. USTEKINUMAB EN LA EDAD PEDIÁTRICA. A PROPÓSITO DE UN CASO.
Valdés Delgado T1, Balboa Vega MJ2, Fernández Álvarez P1, Maldonado Pérez B1, Castro Laria L1, Caunedo Álvarez A1, Argüelles Arias F1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla. 2UGC Gastroenterología Pediátrica. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: ustekinumab, pediatria, enfermedad de crohn.
Introducción
Con la nueva incorporación de ustekinumab al algoritmo terapéutico en la Enfermedad Inflamatoria Intestinal (EII), parece ser que se están obteniendo altas tasas de respuesta clínica en paciente adultos con enfermedad de Crohn (EC) moderada/severa que han fracasado a terapias previas con anti-TNF. Sin embargo, todavía no se ha establecido la seguridad y eficacia de Ustekinumab para el tratamiento de la EC en niños menores de 18 años de edad. No hay estudios referente a ello y son muy escasos los casos recogidos en la literatura hasta la fecha.
Caso clínico
Varón de 12 años, diagnosticado de EC (A1, L3, B2p) con 4 años de edad, con comportamiento agresivo y fracaso a tratamiento con Anti-TNFs. Había realizado tratamiento hasta la fecha con:
- Mesalazina 2g/día
- Azatioprina 100 mg/día hasta el 2016, se retira y se intensifica Adalimumab.
- Prednisona 30 mg/día a dosis plenas en brotes.
- Infliximab en 2012 (solo recibió 3 dosis de inducción posteriormente se suspendió por no presentar mejora alguna).
- Adalimumab 40mg cada 2 semanas introducido en 2012. Intensificado a 40 mg/semana en 2016 hasta la fecha actual. (Figura 1)
*Tratamiento actual: Mesalazina 2 g/dia oral, Prednisona 30 mg/24 h oral, Adalimumab 40 mg/semana subcutáneo, Hierro oral y calcio + Vitamina D oral.
*Situación Clínica: Dolor abdominal difuso. 6 deposiciones al día consistencia líquida. Fiebre 38ºC intermitente. Brote Moderado-severo. CDAI 366.
Imagen 1
Ecografia abdominal: muestra un marcado engrosamiento de la pared del sigma de más de 0,4 cm (rojo)
Imagen 2
A la izquierda visualizamos las fístulas perianales. A la derecha visualizamos mucosa colónica con extensas úlceras profundas, friables al endoscopio y distribución discontinua.
Discusión
Para concluir, destacar que se necesitan estudios que avalen la eficacia y sobre todo la seguridad de Ustekinumab en pacientes pediátricos con EC, pero hasta la fecha los casos publicados junto con el expuesto, reflejan resultados que parecen ser prometedores.
CP-165. USTEKINUMAB INTRAVENOSO COMO TERAPIA DE INDUCCIÓN Y MANTENIMIENTO EN PACIENTE CON ENFERMEDAD DE CROHN Y DESNUTRICIÓN
Guerrero Palma E, Viejo Almanzor A, Moreno Garcia AM, Bernal Torres A, Correro Aguilar FJ
Servicio Aparato Digestivo. Hospital Puerta del Mar, Cádiz.
Palabras clave: enfermedad de crohn, ustekinumab, desnutricion.
Introducción
La introducción de fármacos biológicos ha supuesto una revolución en el manejo de la enfermedad de Crohn moderada-grave. Ustekinumab es un anticuerpo monoclonal totalmente humano IgG1, que se une a la subunidad p40 de las citoquinas IL-12 e IL-23 impidiendo que se unan a su receptor (IL-12Rb1) expresado en la superficie de los linfocitos T CD4+ y los linfocitos Natural Killer (NK), con lo que inhibe la respuesta inmune mediada por IL-12 e IL-23.
Caso clínico
Varón de 46 años diagnosticado hace 12 años de enfermedad de Crohn colónica de patrón estenosante (Clasificación de Montreal: A3L2B2p). Entre sus antecedentes destaca enfermedad renal crónica secundaria a glomerulonefritis mesangial por depósitos de lgA que precisó trasplante de cadáver hace 19 años, en tratamiento con Advagraf y prednisona 5mg, en seguimiento por Nefrología.
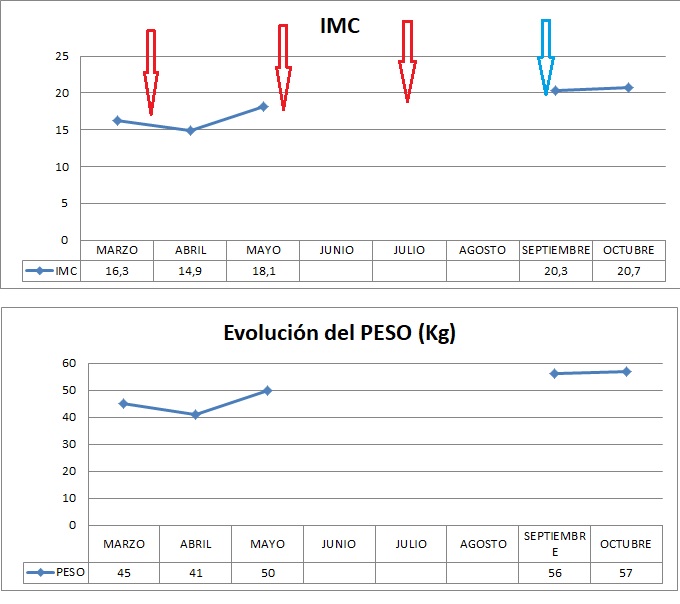
Recibió tratamiento con Infliximab desde 2014 con buen control, hasta final de 2018 cuando presentó pérdida de respuesta secundaria, presentando brotes de la enfermedad intestinal, clínica perianal (fístula perianal con absceso) y empeoramiento de las manifestaciones extraintestinales (artritis enteropática). Los múltiples ingresos, la corticoterapia y la disminución de la ingesta conllevaron el desarrollo de desnutrición proteinocalórica (Peso 41 kg, IMC 14.9).
Se consensuó con el paciente tratamiento con Ustekinumab por vía intravenosa, tanto en inducción (230 mg) como mantenimiento (130 mg cada 8 semanas) dado el escaso tejido celular subcutáneo disponible, hasta mejoría del estado nutricional. Tras 8 semanas de tratamiento presentó mejoría clínica, alcanzando la remisión a las 12 semanas, con ganancia progresiva de peso (hasta 57 kg, IMC 20.7) y mejoría analítica.
Tras 3 dosis iv, y ante la mejoría nutricional, se decidió pasar a terapia de mantenimiento por vía subcutánea (90 mg sc cada 8 semanas), manteniéndose estable y sin haber presentado efectos adversos hasta el momento actual.
Discusión
En el caso presentado, se utiliza la vía intravenosa como terapia de mantenimiento ante un paciente con desnutrición proteinocalórica moderada-severa con escaso tejido celular subcutáneo. Con esta pauta de tratamiento se consiguió una respuesta rápida, con mejoría clínica, analítica y nutricional, sin registrar efectos adversos, permitiendo el uso de la vía subcutánea tras la recuperación ponderal. La terapia intravenosa de mantenimiento podría ser una pauta eficaz en pacientes con desnutrición proteinocalórica, pero se precisa de estudios que confirmen la eficacia y seguridad de esta vía de administración.

 Descargar número completo
Descargar número completo Download full issue
Download full issue