CITA ESTE TRABAJO
Serrano Borrero I, Roldán Aviña JP, Merlo Molina S, Ferrusola Díaz AD, Muñoz Pozo F. Dilatación del estómago por estenosis pilórica en paciente con cirugía gástrica previa. RAPD Online. 2021;44(2):65-68.
Introducción
La inflamación aguda o crónica del duodeno, puede conducir a un síndrome de obstrucción de la salida gástrica de tipo mecánico, conocido en inglés como "gastric outlet obstruction", y que se manifiesta en forma de dolor epigástrico postprandial, retraso del vaciamiento gástrico, anorexia, náuseas y vómitos. Cuando la situación se mantiene durante un periodo prolongado de tiempo, el estómago continúa dilatándose progresivamente, perdiendo rápidamente su tono muscular lo que acentúa aún más la sintomatología[1].
Caso Clínico
Paciente de 89 años de edad. Sus antecedentes más destacados son intervención por patología ulcerosa gástrica (probable piloroplastia - no aporta informes) unos 30 años antes; anticoagulado con Sintrom por trombosis venosa profunda M.I.D. 3 meses antes.
El paciente refiere dolor abdominal generalizado de varios meses de evolución, acentuado en la última semana, con vómitos alimentarios en los últimos días, motivo por el que acudió a Urgencias. Hábito intestinal estreñido con una deposición de características normales esa misma mañana. No hay fiebre.
La exploración está afectada por el dolor, con mal estado general. El abdomen era blando, aunque poco depresible, timpanizado sobre todo en el hemiabdomen derecho. Existía una sensación de ocupación del cuadrante superior izquierdo del abdomen sin bazuqueo gástrico. Cicatriz de laparotomía media sin complicaciones.
Se prescribió tratamiento con Metamizol 2 g IV, Omeprazol 40 mg IV, Metoclopramida 10 mg IV. Tras un nuevo episodio de vómito, se colocó sonda nasogástrica.
En la analítica destacaba una anemia microcítica e hipocroma ya conocida con Hb 6,5 mg/dl y hematocrito 30,3% con recuento y fórmula leucocitaria normales. INR 2,47.
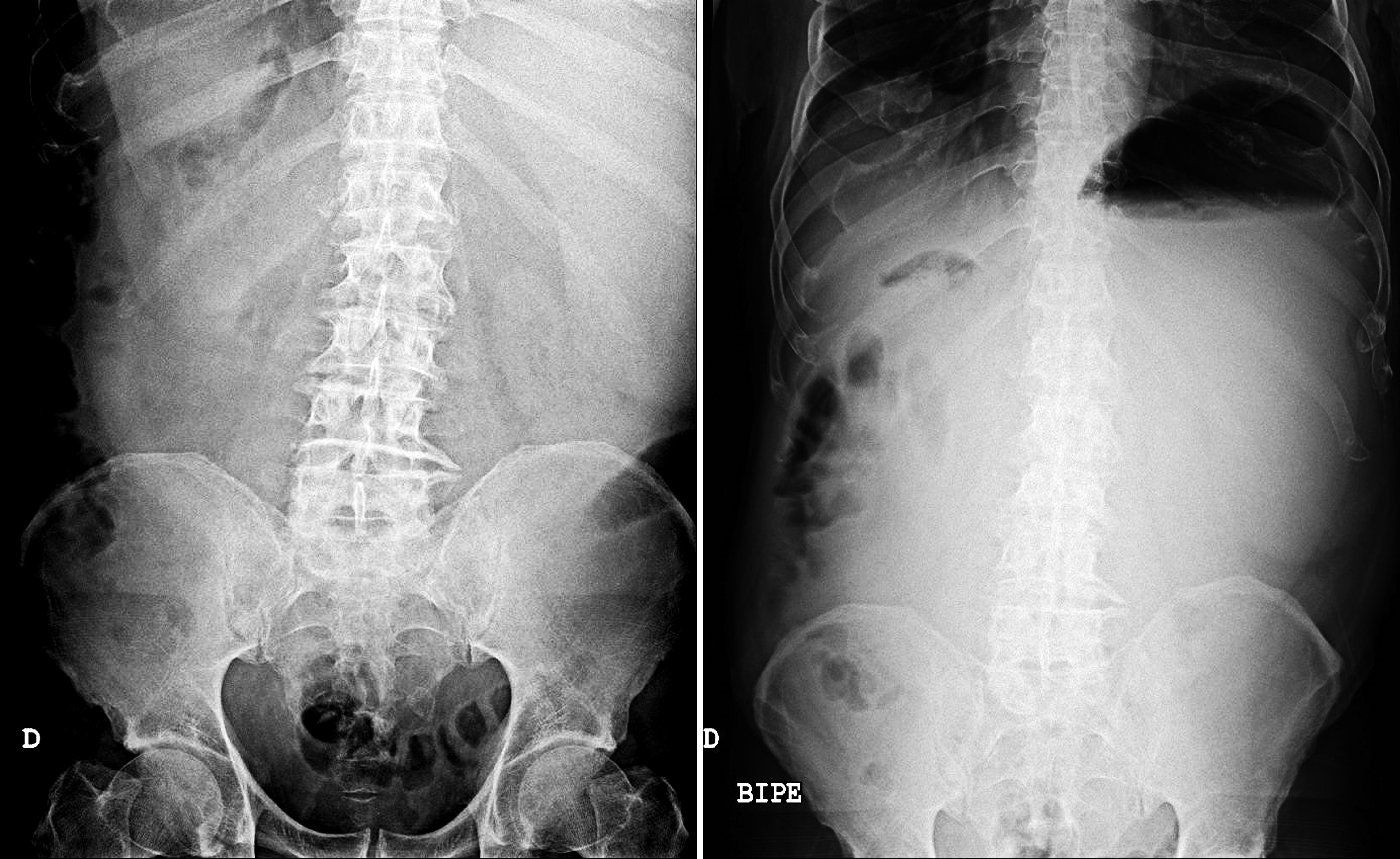
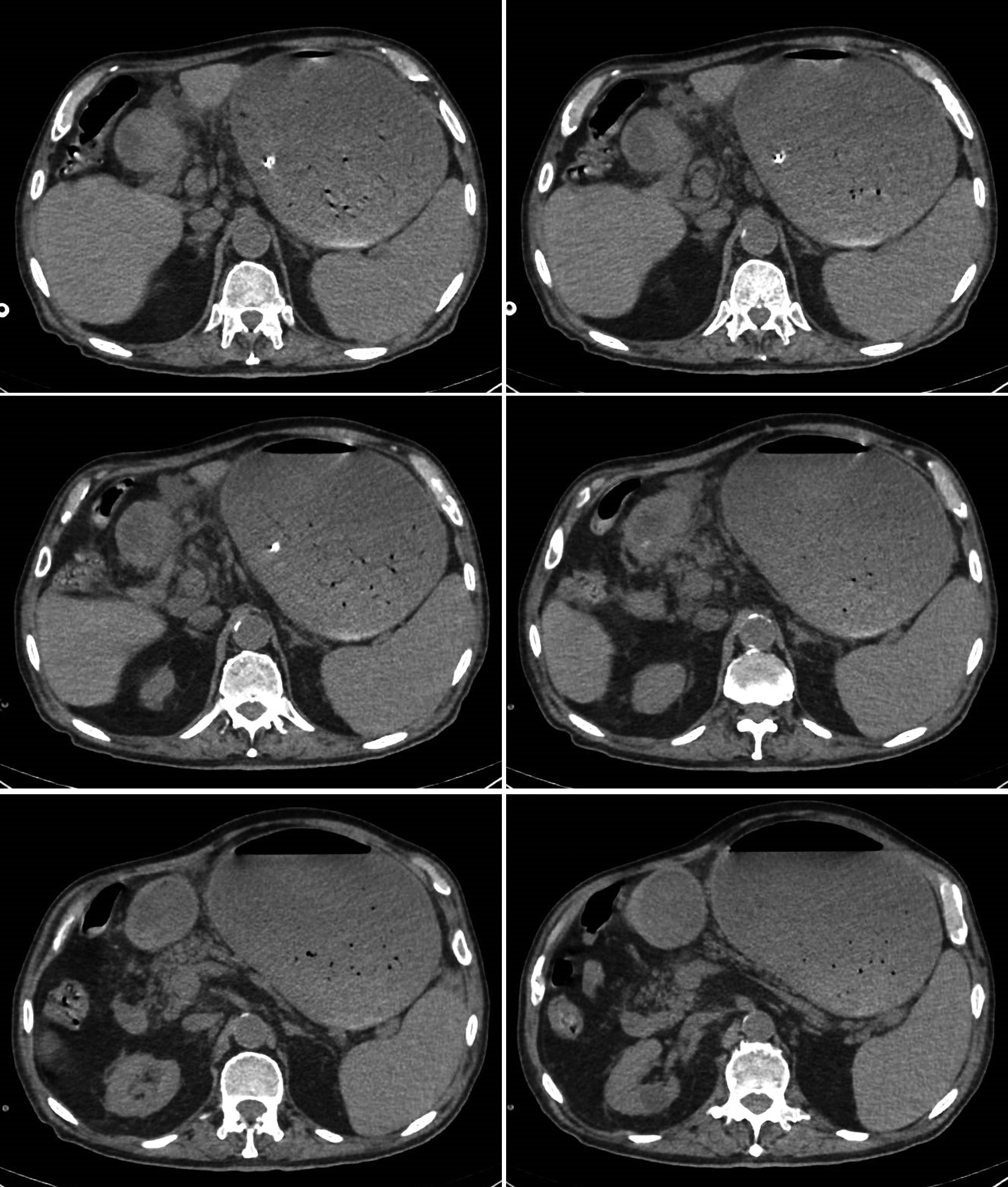
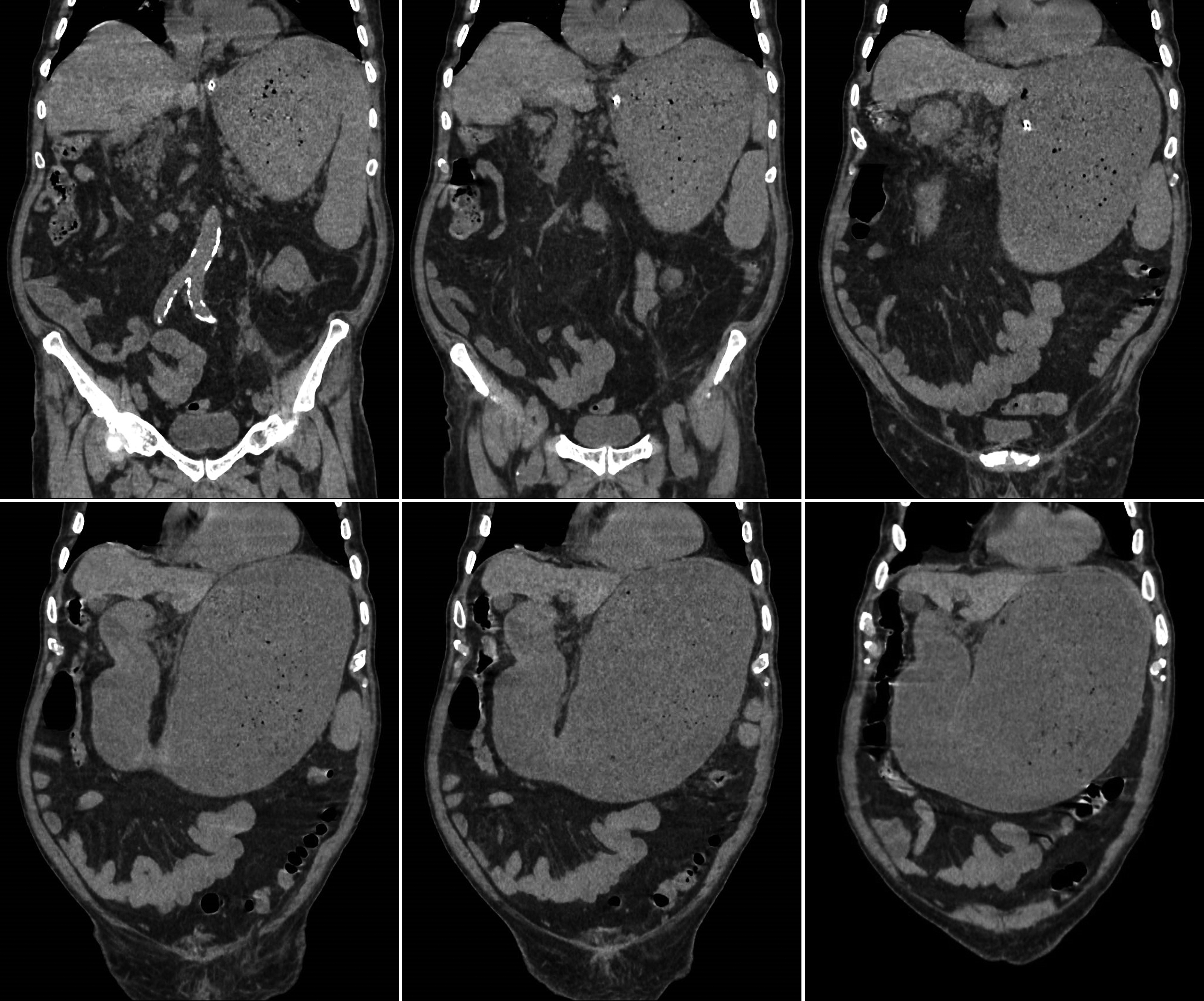
En la radiografía abdominal (Figura 1) llamaba la atención un desplazamiento hacia abajo y hacia los lados del contenido intestinal por una sombra de densidad agua que impresionaba como un estómago retencionista. Se completó el estudio con un TAC de abdomen (Figuras 2 y 3) que informó de una gran dilatación gástrica, con contenido en su interior (sonda en posición correcta) y masa de bordes mamelonados a nivel pilórico, estenosante, con un tamaño 43,7 x 52 mm que provoca obstrucción gástrica, compatible con neoplasia pilórica, junto con adenopatías locorregionales sugestivas de afectación metastásica.
Una vez ingresado, comenzó tratamiento con Nutrición Parenteral y se completaron los estudios con una endoscopia oral en la que el estómago sólo fue valorado en la zona de antro por la existencia de abundante contenido líquido/semisólido, que se intentó aspirar consiguiéndose solo en parte. La zona del píloro estaba desestructurada, con desaparición del orificio pilórico por la existencia de una mucosa protruyente que ocupaba toda la zona impidiendo el paso del endoscopio. El aspecto de la mucosa no era claramente neoplásico, pudiendo presentar ese aspecto por compresión extrínseca neoplásica a nivel de bulbo. Las biopsias tomadas informaban de una mucosa con cambios mínimos, sin identificarse tejido neoplásico.
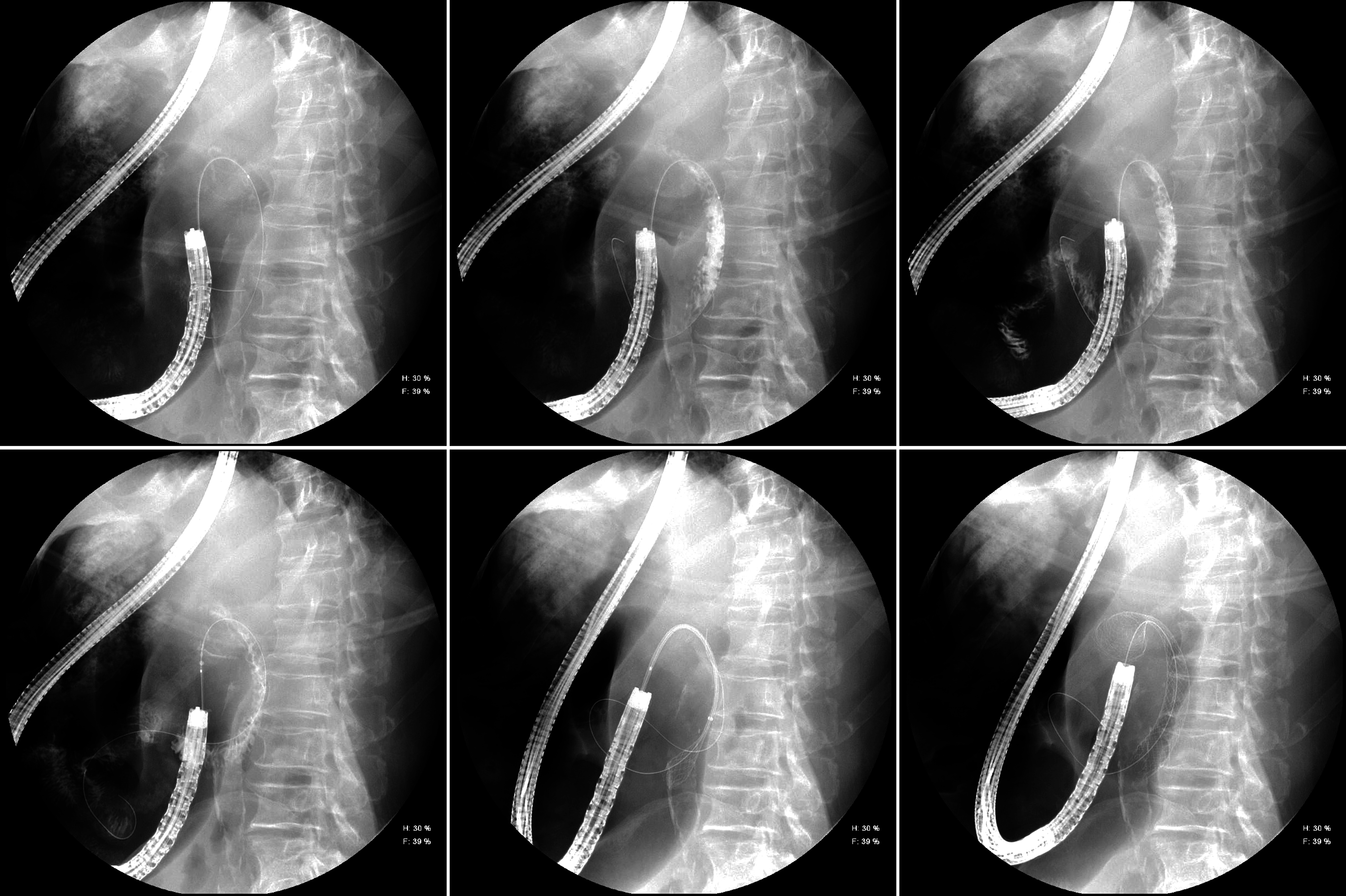
El curso clínico fue favorable, con desaparición de los síntomas que motivaron su ingreso. Finalmente se completó el tratamiento con una endoscopia oral terapéutica en la que se apreciaba una estenosis de píloro, severa, que impedía el paso del endoscopio. Bajo control radiológico se consiguió ver, contrastando la luz, la existencia de una estenosis de unos 10-15 mm de longitud a nivel de bulbo. Bajo control endoscópico y radiológico se procedió a la colocación de una prótesis duodenal no recubierta de 22 x 120 mm (Figura 4) .
El paciente fue dado de alta tolerando dieta oral triturada, con tránsito intestinal normal y tras haber sido valorado por la Unidad de Cuidados Paliativos. Cuatro meses después de alta, el paciente continúa asintomático, con buena calidad de vida.
Discusión
La obstrucción intrínseca o extrínseca del píloro o del duodeno es el mecanismo fisiopatológico del SOSG; la causa final de la obstrucción dependerá de la etiología subyacente. Debido a la gran diversidad de causas que lo pueden producir se desconoce la incidencia real de esta patología[2].
Los pacientes inicialmente presentan síntomas intermitentes que progresan hasta la obstrucción completa de la salida gástrica. Característicamente el vómito es el síntoma cardinal, presentado restos alimentarios ingeridos varios días antes. En la fase aguda o crónica de la obstrucción, los vómitos continuos pueden provocar deshidratación y anomalías electrolíticas. En cuadros de instauración lenta y progresiva es posible incluso que con una obstrucción severa el paciente presente mínimos síntomas sin afectación nutricional[3].
Inicialmente, los pacientes pueden demostrar una mejor tolerancia a los líquidos que a los alimentos sólidos y en una etapa posterior, los pacientes pueden desarrollar una pérdida de peso significativa debido a una ingesta calórica deficiente. La desnutrición es un signo tardío, pero puede ser muy profunda en pacientes con malignidad concomitante.
Cuando la obstrucción persiste, los pacientes terminan presentando una dilatación gástrica significativa, perdiendo el estómago finalmente su contractilidad. Los alimentos no digeridos se acumulan aumentando el riesgo de presentar una neumonía por aspiración.
A finales del siglo XX, las causas benignas constituían el 37% de los casos, y dentro de ellas la enfermedad ulcerosa duodenal complicada suponía el 90. Con el uso de fármacos inhibidores de la bomba de protones (IBP) y los tratamientos de erradicación de la infección por H. Pylori se ha reducido la incidencia de úlcera péptica, y las enfermedades malignas se han convertido en la principal causa del SOSG.
Aunque su incidencia es baja en comparación con otras patologías gástricas, el diagnóstico de dilatación gástrica debe ser tenido siempre en cuenta en pacientes con antecedentes de cirugía del tracto digestivo superior. Un diagnóstico precoz facilitará su correcto tratamiento médico y quirúrgico (si fuese necesario), disminuyendo la morbimortalidad asociada a este cuadro.
La endoscopia es el examen más útil para establecer la localización y la posible causa de la obstrucción de la salida gástrica y sirve para obtener muestras de tejido de las áreas implicadas para confirmar o excluir etiología maligna. Los estudios de contraste con bario o agentes hidrosolubles, así como la radiografía simple de abdomen pueden mostrar un estómago retencionista y aportar pistas sobre la enfermedad subyacente. La ausencia de paso de contraste al intestino delgado sugiere una obstrucción completa. El TAC es útil especialmente para evaluar el grosor de la pared del píloro o del estómago, evaluar la existencia de adenopatías regionales, así como el área pancreática, biliar y el retroperitoneo[5],[6].
En el diagnóstico diferencial[5], una vez realizada la endoscopia oral, contempla dos amplias categorías etiológicas: benignas o malignas, quedando recogidas en la Tabla 1 .
Tabla 1
Causas del Síndrome de Obstrucción de la Salida Gástrica (SOSG).
En cuanto al manejo terapéutico inicial, todos los pacientes deben ser hospitalizados para la inmediata reposición hidroelectrolítica y descompresión nasogástrica. En pacientes con obstrucción por enfermedad ulcerosa se aprecia una mejoría de los síntomas a las 48-72 horas, según las series revisadas, debido a la disminución del edema y espasmo gracias a los IBP y el uso de sondaje nasogástrico[7]. En cambio, en pacientes con síntomas de causa maligna debemos recurrir a métodos endoscópicos, (dilatación con balón o inserción de stents) cuando la única opción es paliativa y a la cirugía cuando se requieren resultados eficaces a largo plazo[2]. En cuanto a técnica quirúrgica se refiere, la resección quirúrgica y derivación (gastroyeyunostomia) es la opción más empleada.
El dilema se presenta ante pacientes con enfermedad avanzada donde se busca una actitud paliativa, debatiéndose entre el uso de stents autoexpansibles y la realización de gastroyeyunostomías. Parece ser que los stents aportan periodos de hospitalización más cortos, menor tiempo para la reintroducción de la ingesta oral y no hay diferencias significativas en cuanto a mortalidad, complicaciones y tasas de supervivencia cuando comparamos con cirugía, En contraposición, a veces se requieren procedimientos endoscópicos repetidos por los fallos de los stents[8],[9].
Como conclusión el SOSG no es una entidad única; es la consecuencia clínica y fisiopatológica de cualquier proceso patológico que produzca un impedimento mecánico al vaciamiento gástrico. Un retraso en la actuación puede comprometer el tejido gástrico ya edematizado y complicar la intervención quirúrgica previa, aumentando la tasa de morbimortalidad, disminuyendo la eficacia de los tratamientos.

 Descargar número completo
Descargar número completo Download full issue
Download full issue