CP-165. ABDOMEN AGUDO POR PSEUDOQUISTE PANCREÁTICO. A PROPÓSITO DE UN CASO.
Lecuona Muñoz M, Ortega Suazo EJ, Fernández García R, Redondo Cerezo E, Heredia Carrasco C
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: pseudoquiste pancreático, drenaje.
Introducción
Los pseudoquistes pancreáticos presentan en la mayor parte de pacientes un curso indolente. Sin embargo, en ocasiones pueden producirse complicaciones derivadas de su presencia como hemorragia, infección, obstrucción de la vía biliar o rotura.
Caso clínico
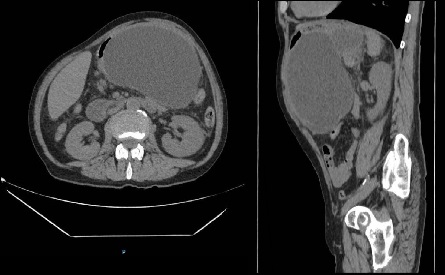
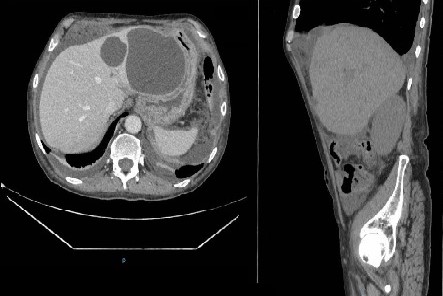
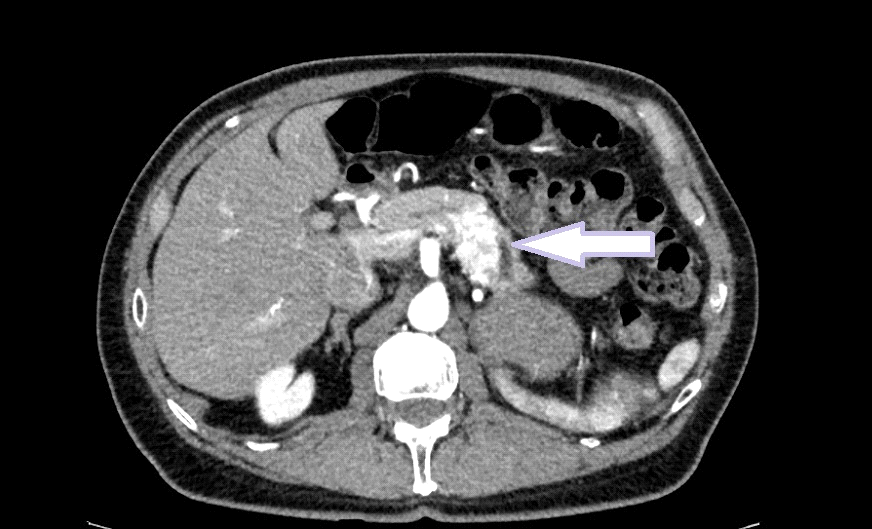
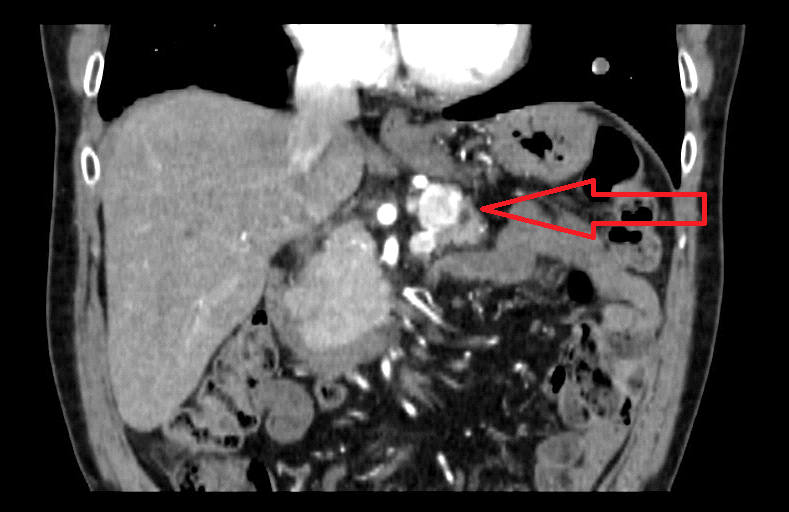
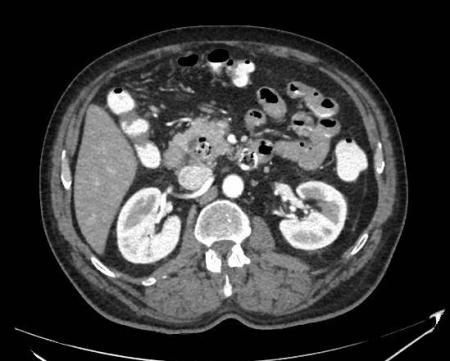
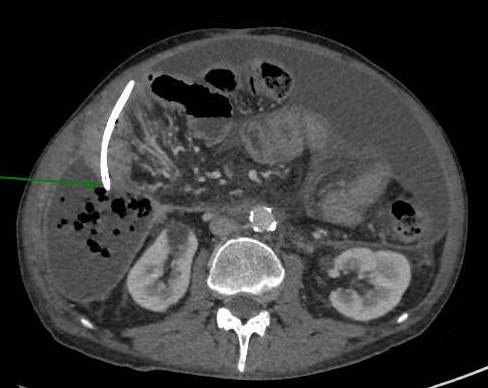
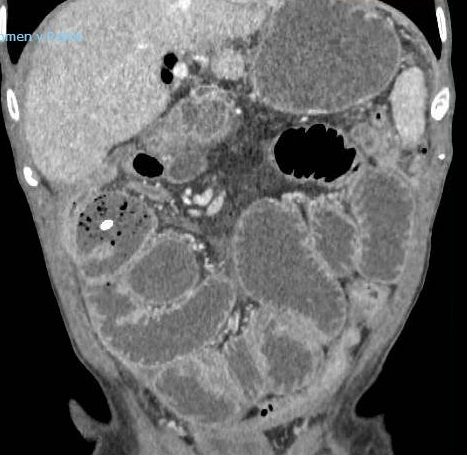
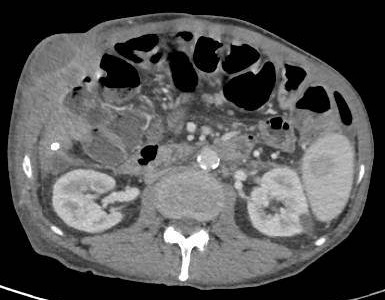
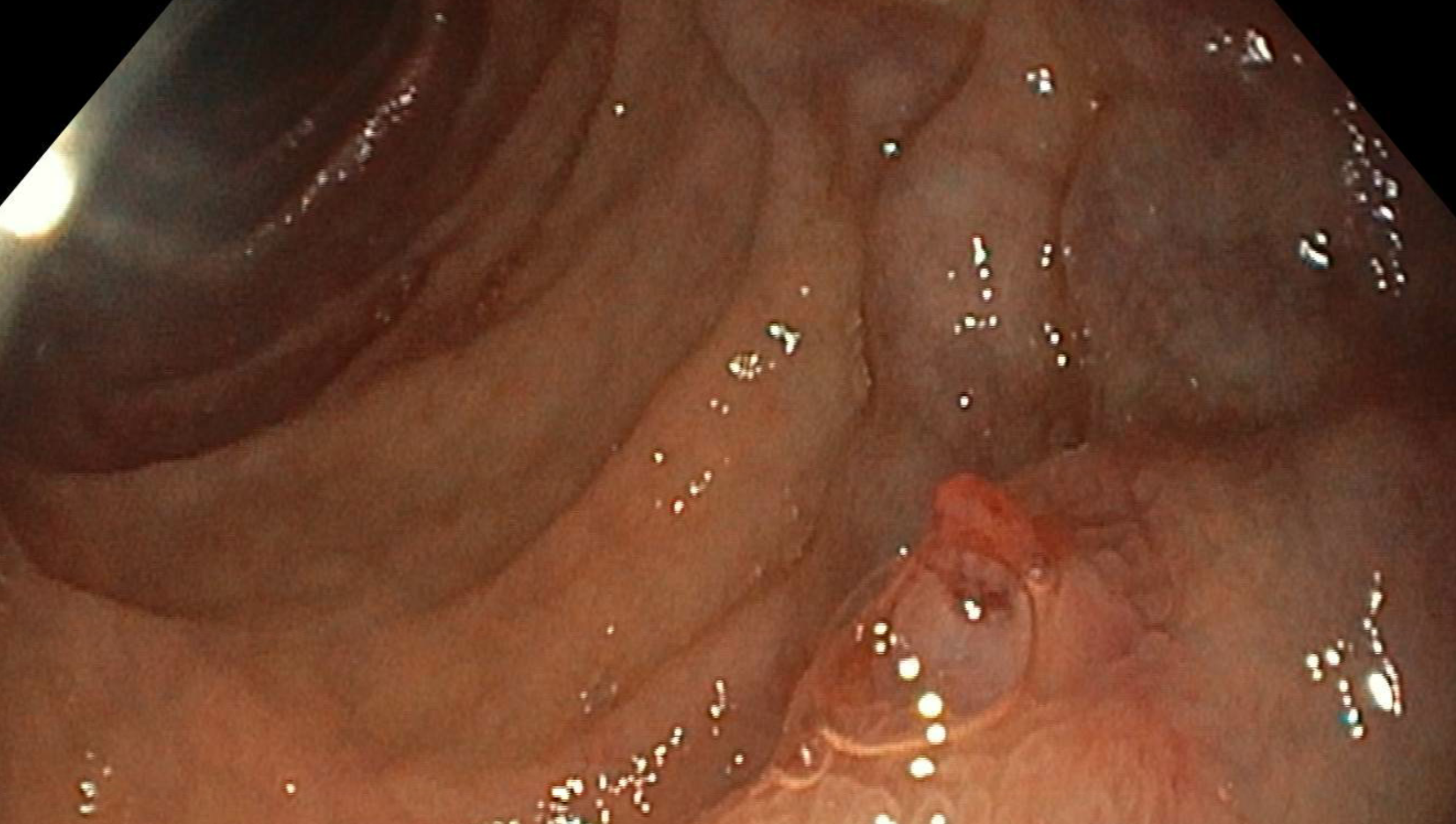
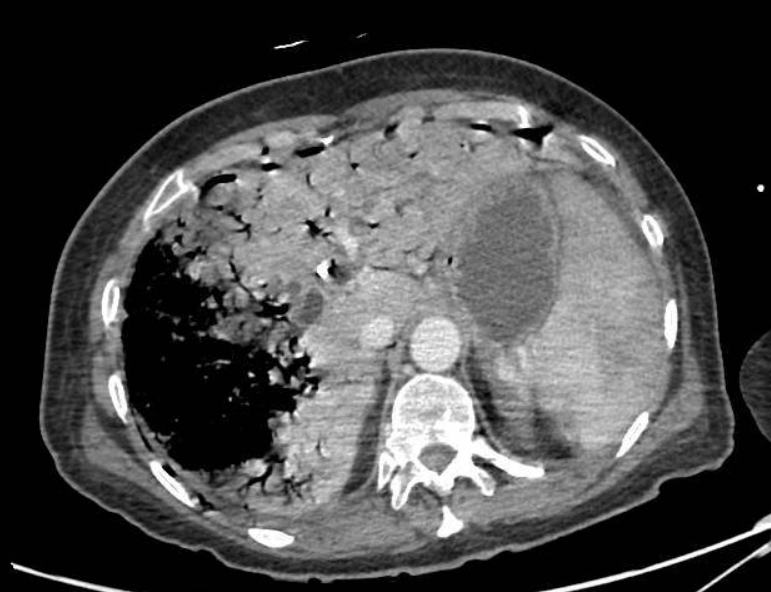
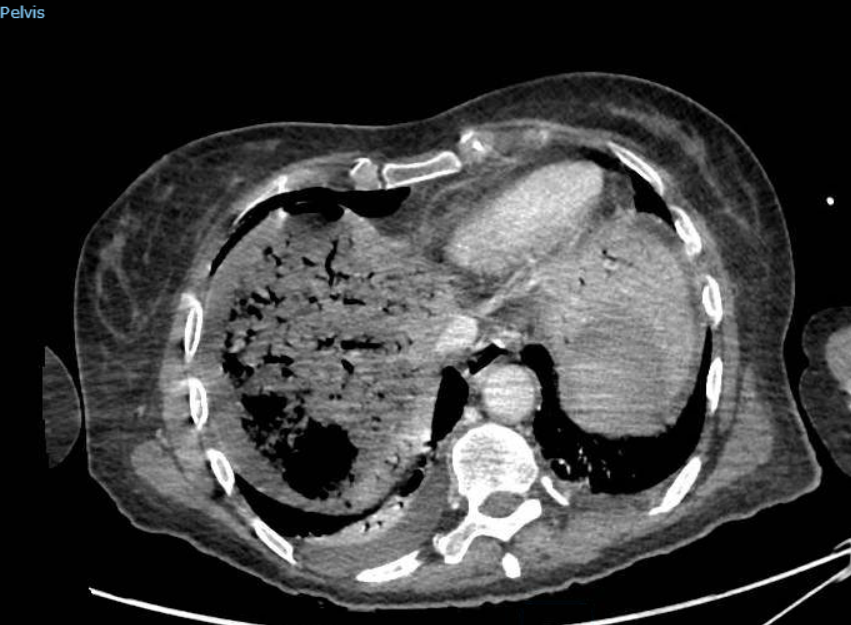
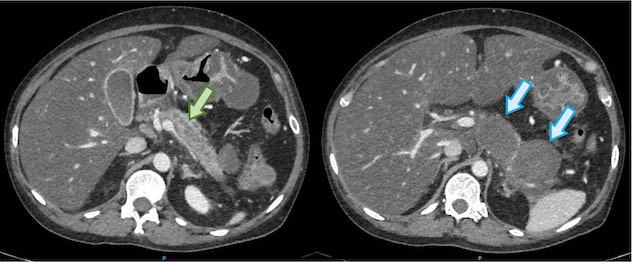
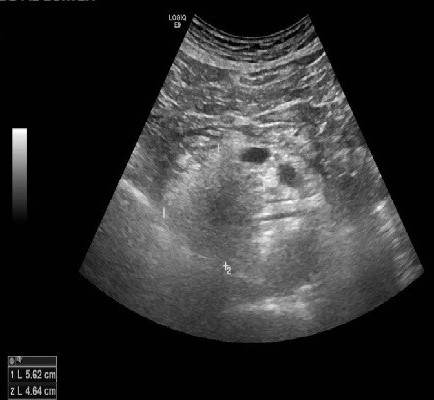
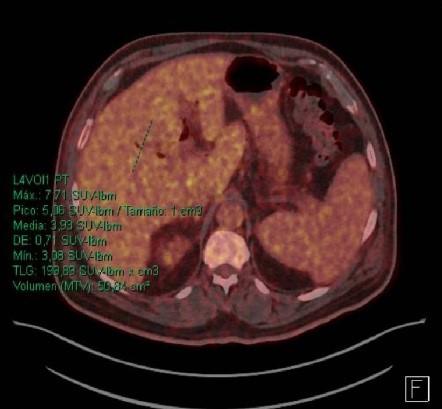
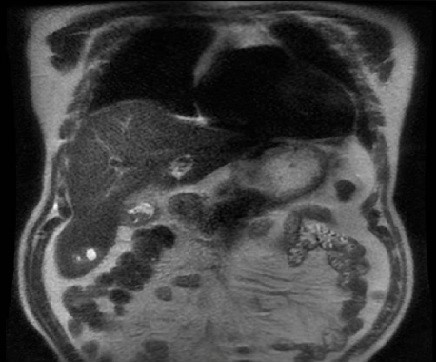
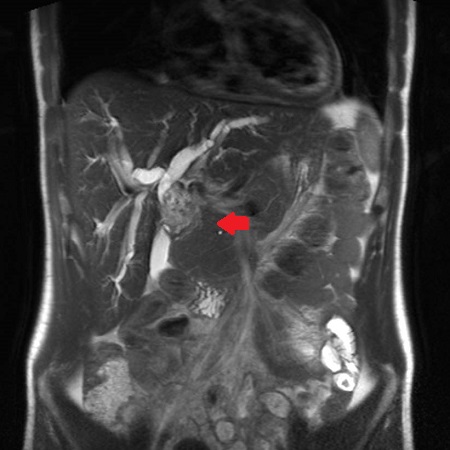
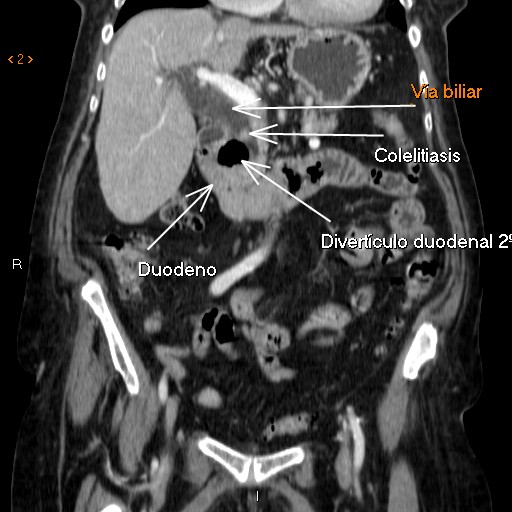
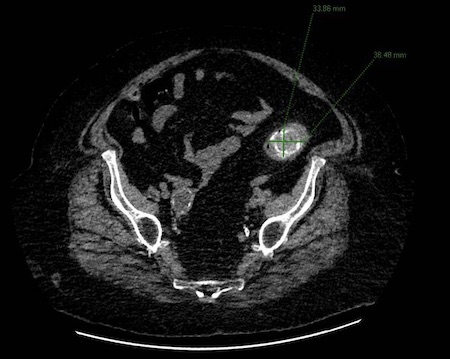
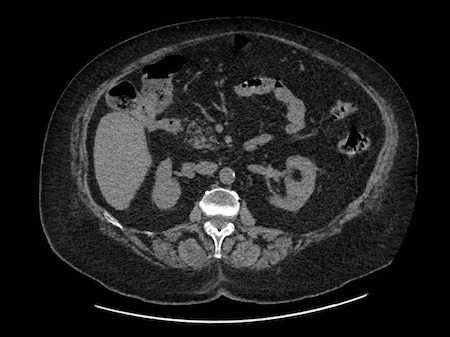
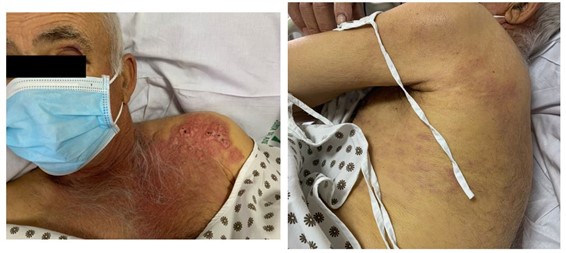
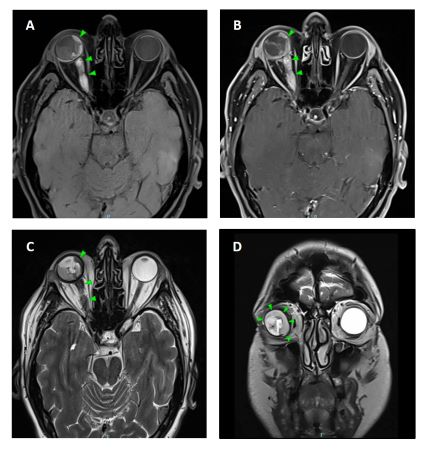
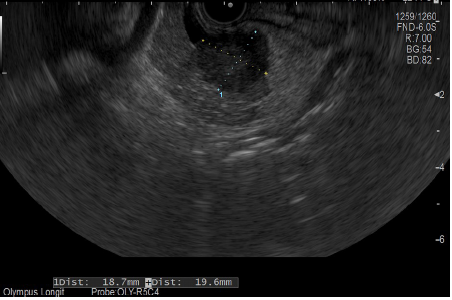
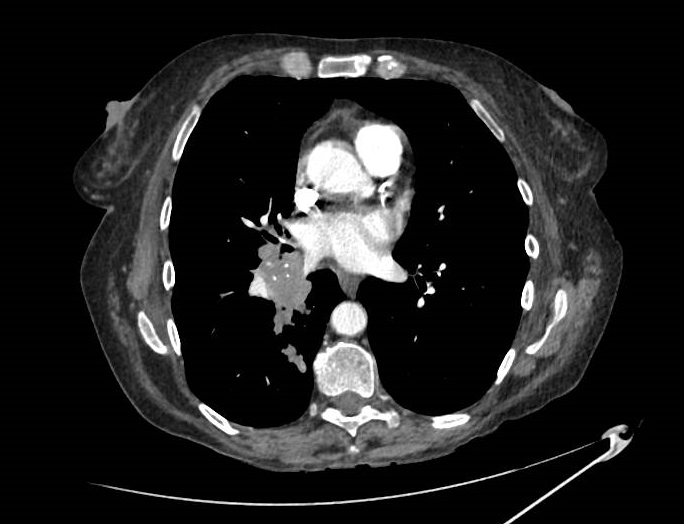
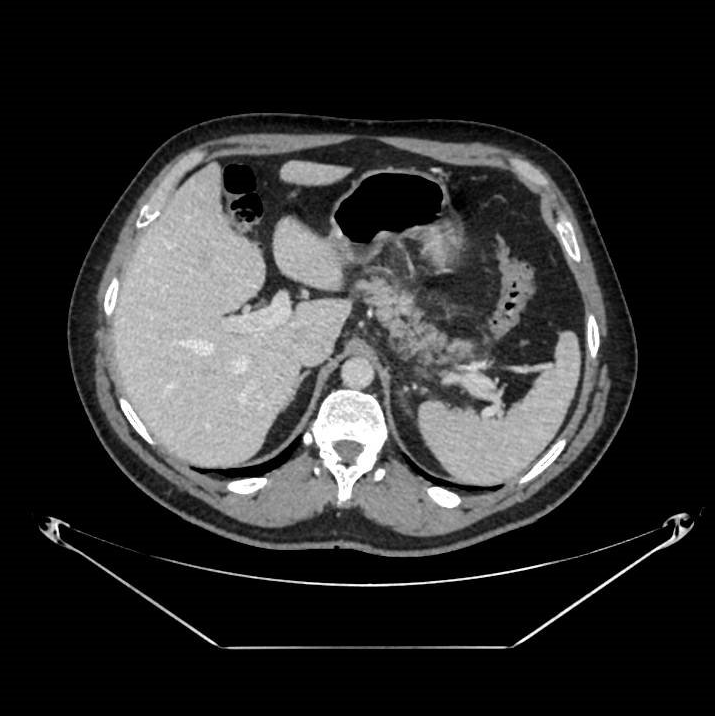
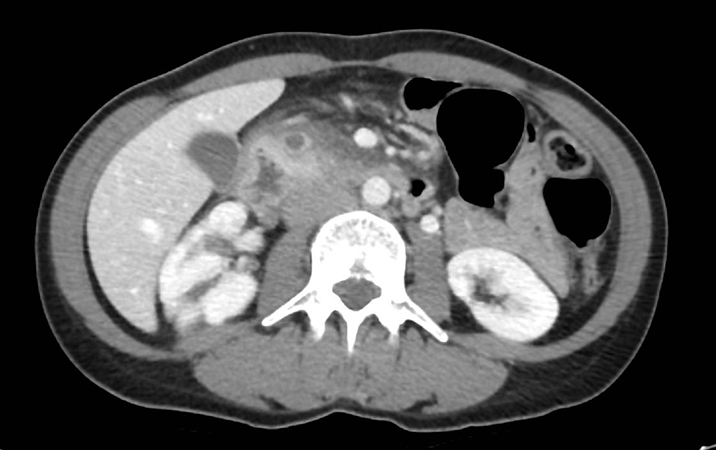
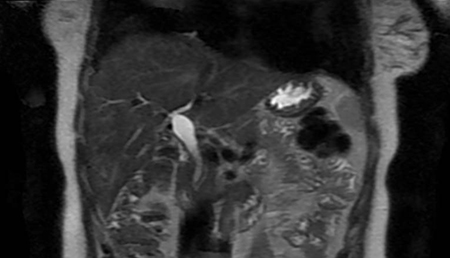
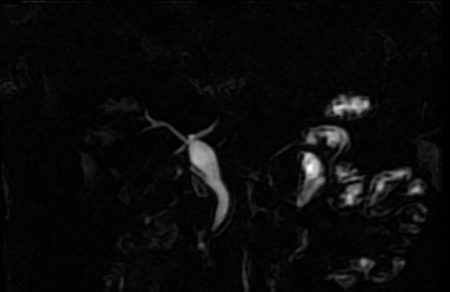
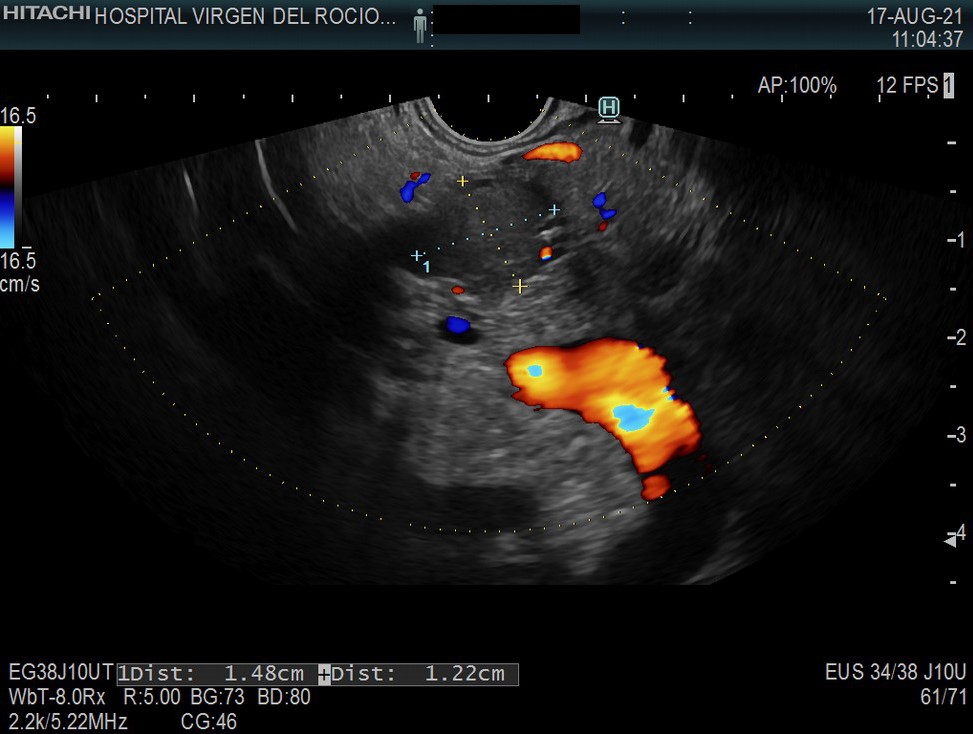
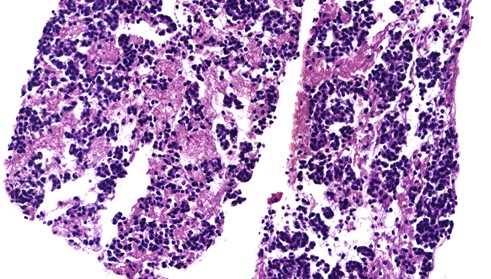
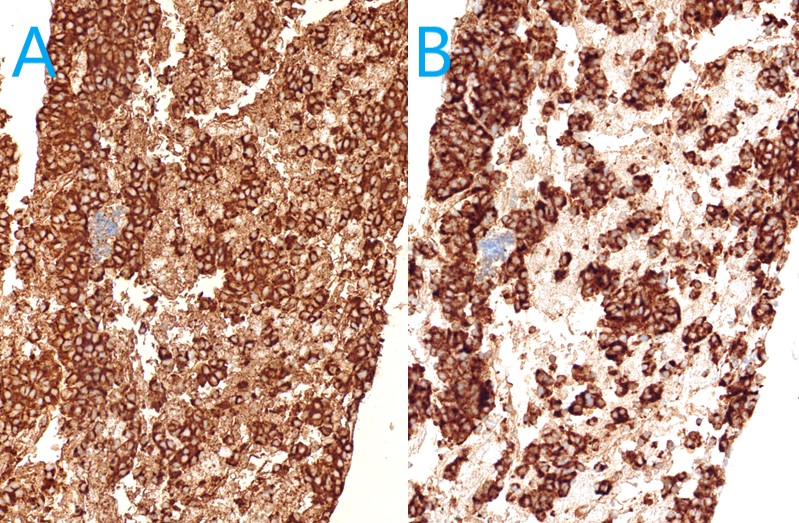
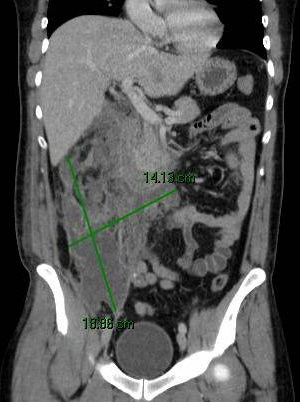
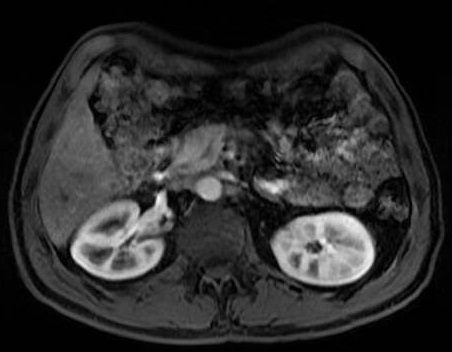
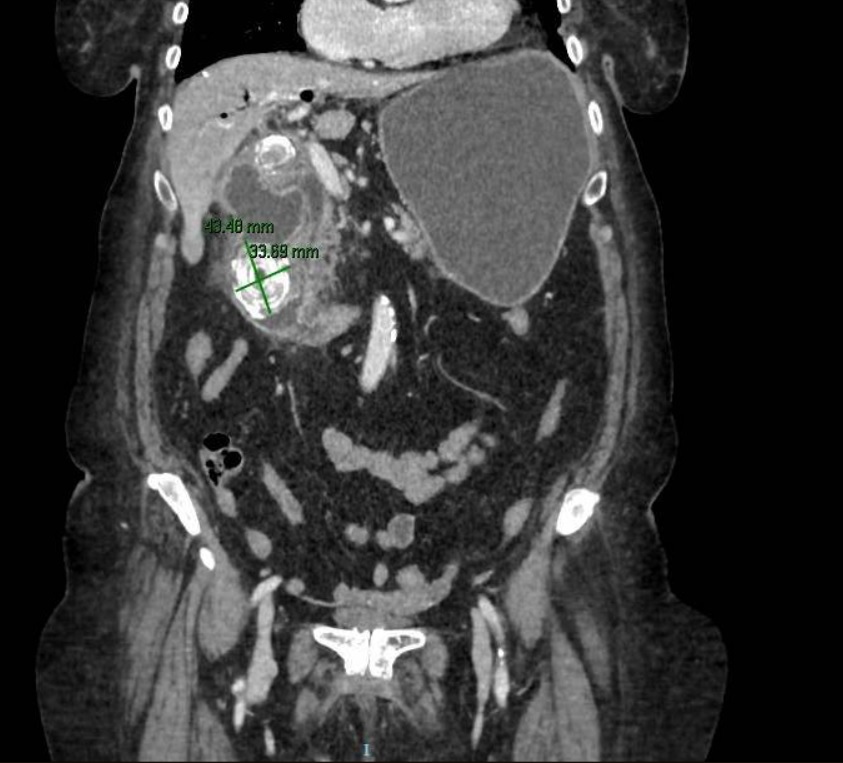
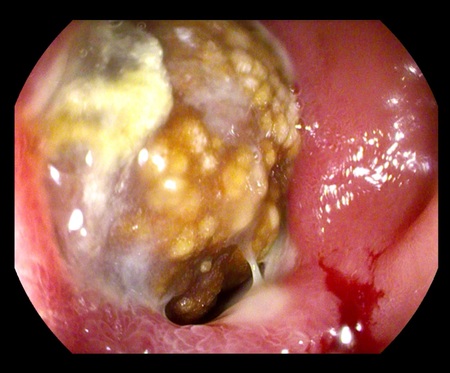
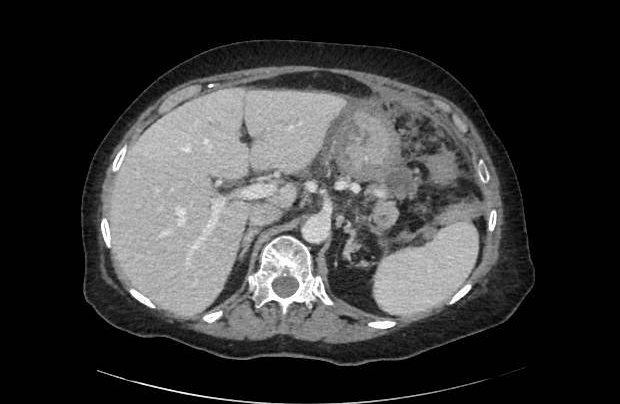
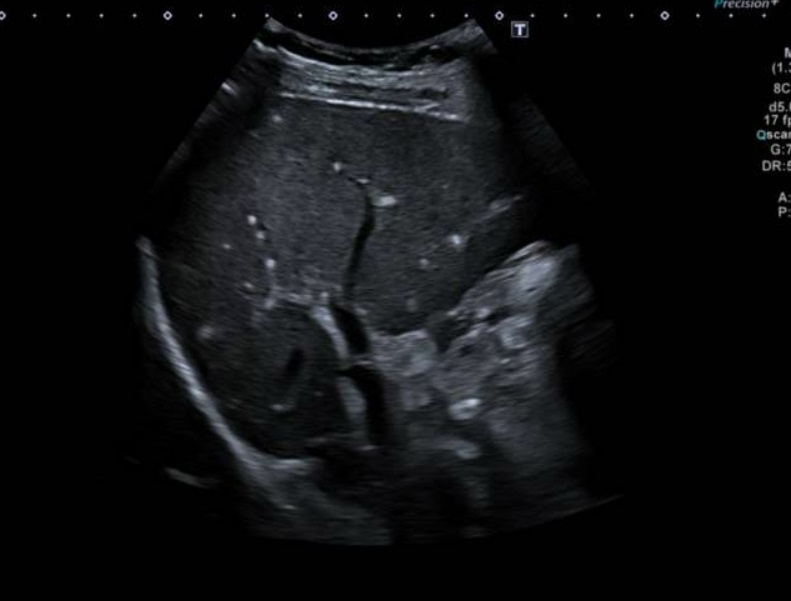
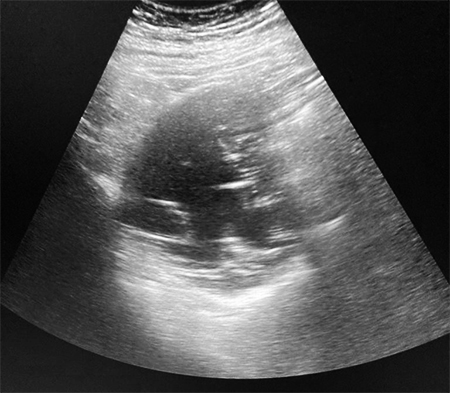
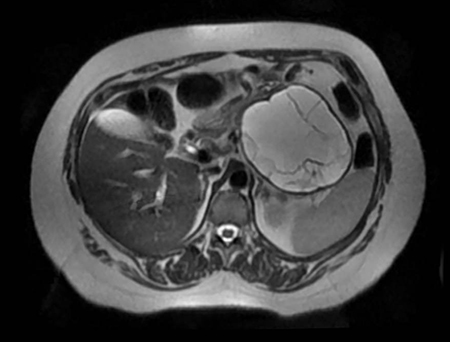
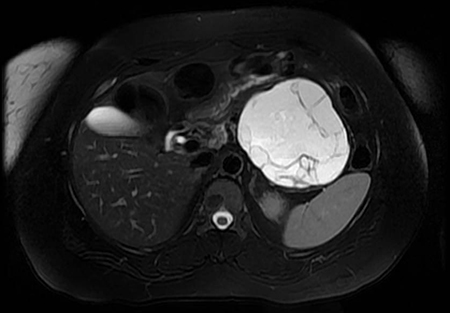
Varón de 64 años con antecedente de pancreatitis crónica enólica, que consulta por fiebre de hasta 38ºC junto con vómitos alimentarios de una semana de evolución, que condicionan intolerancia oral. A la exploración física destaca abdomen muy distendido, doloroso a la palpación en epigastrio. Se realiza analítica evidenciando elevación de reactantes de fase aguda, con Proteína C Reactiva de 330 mg/L, y se solicita TC abdominal (imágenes 1-2). Mediante esta técnica se identifica un pseudoquiste pancreático de gran tamaño que condiciona una marcada compresión extrínseca del estómago. Dados los hallazgos, ingresa a cargo de Aparato digestivo y se inicia antibioterapia de amplio espectro.
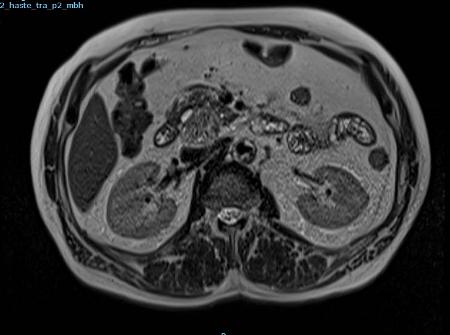
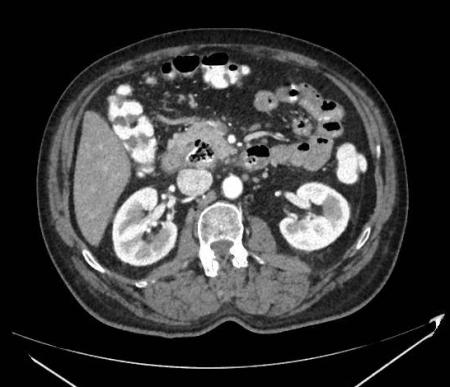
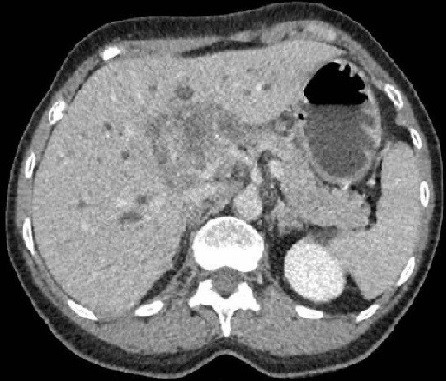
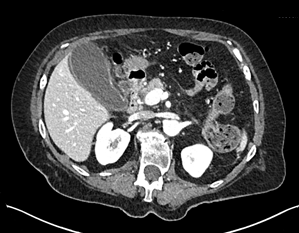
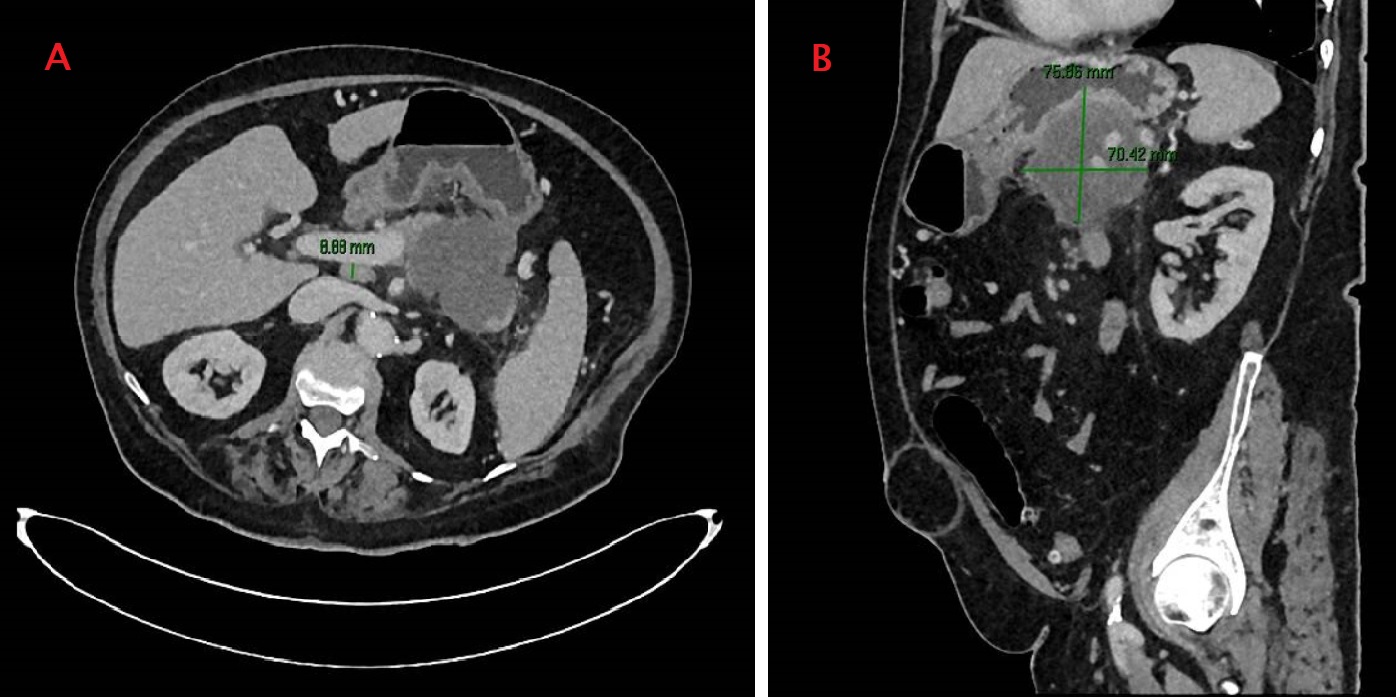
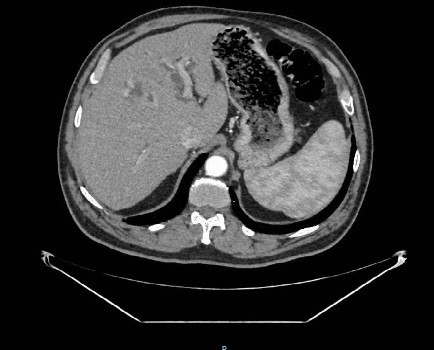
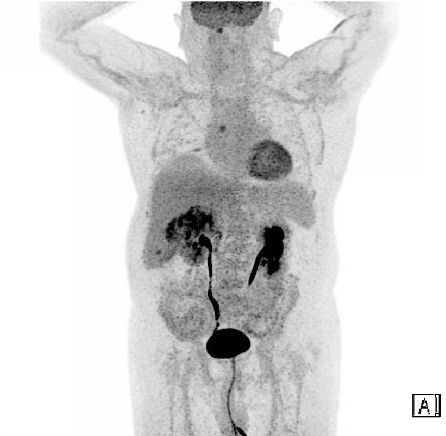
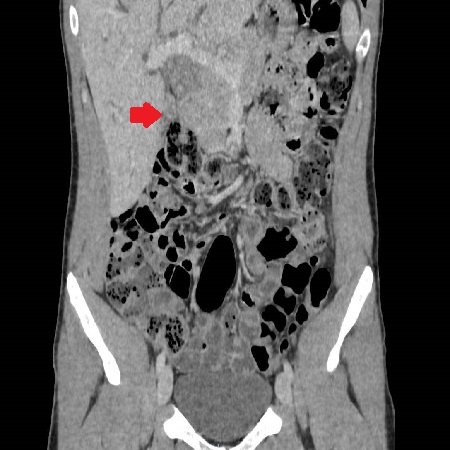
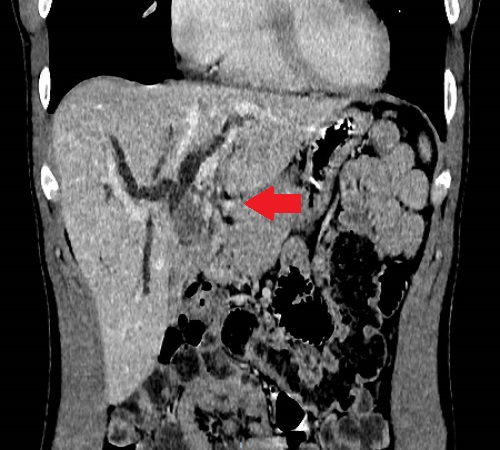
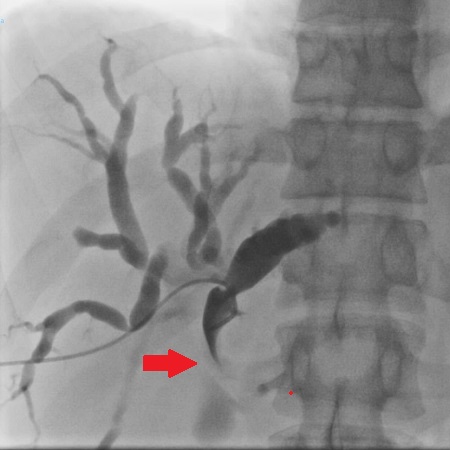
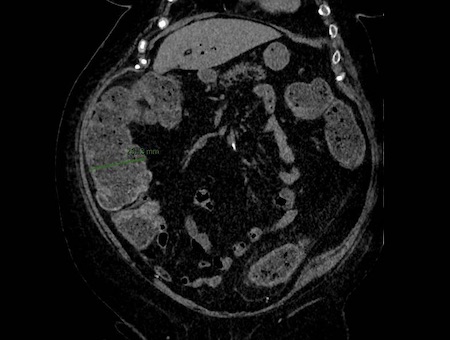
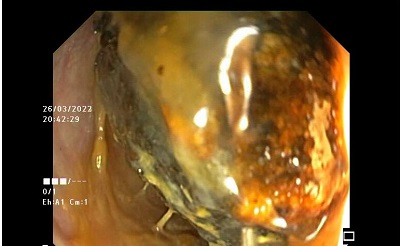
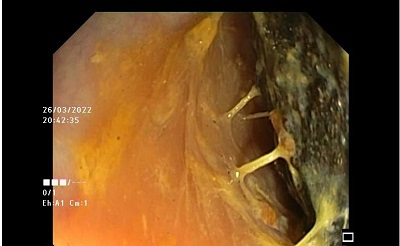
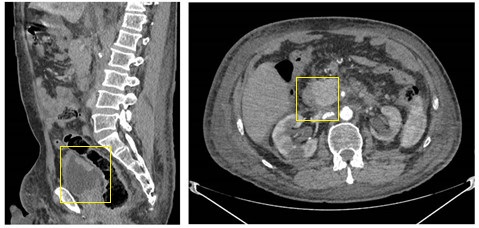
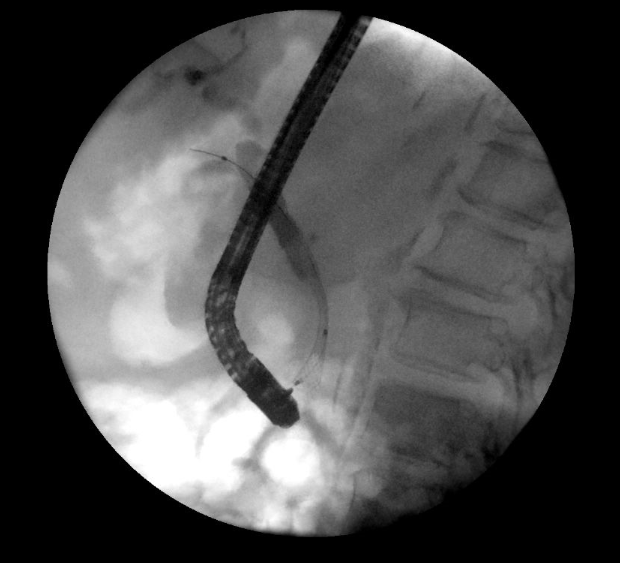
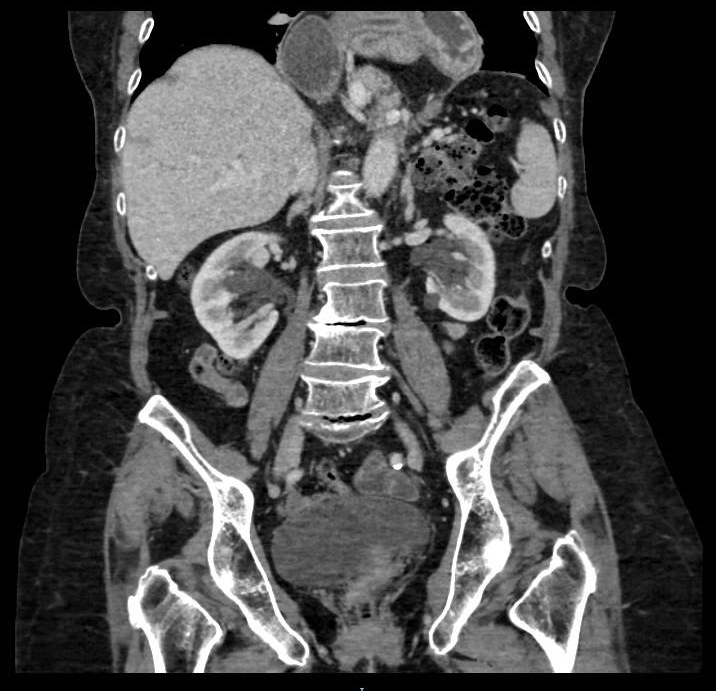
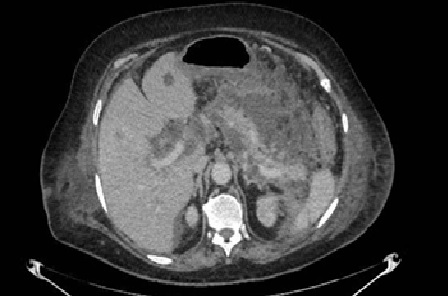
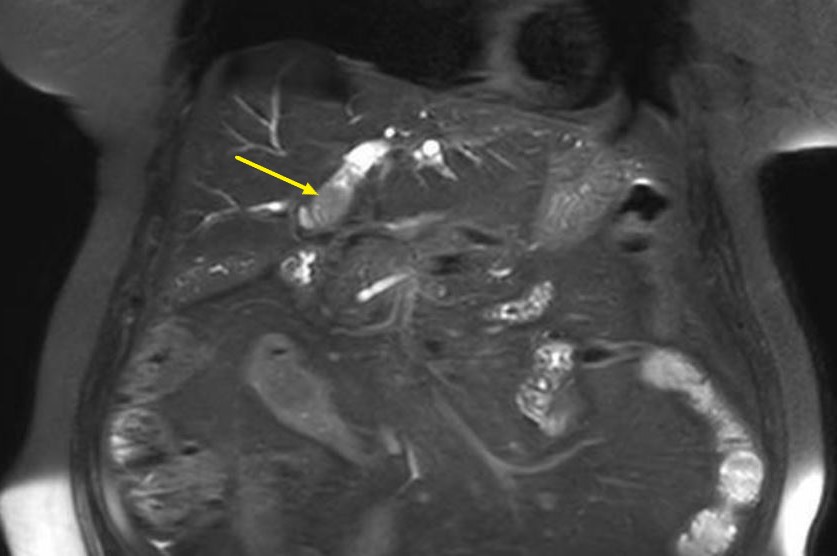
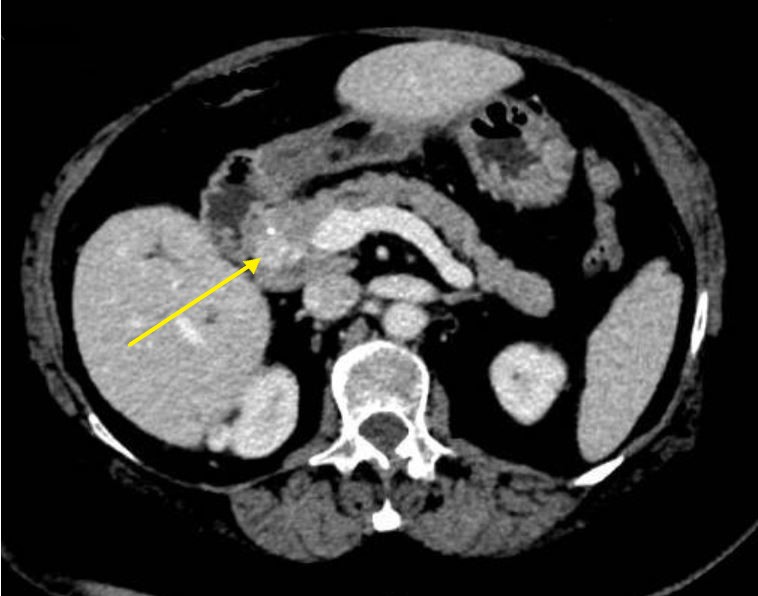
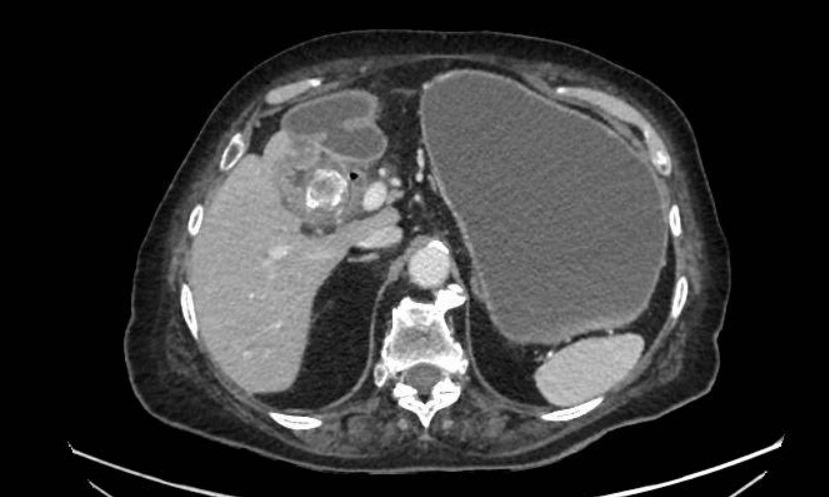
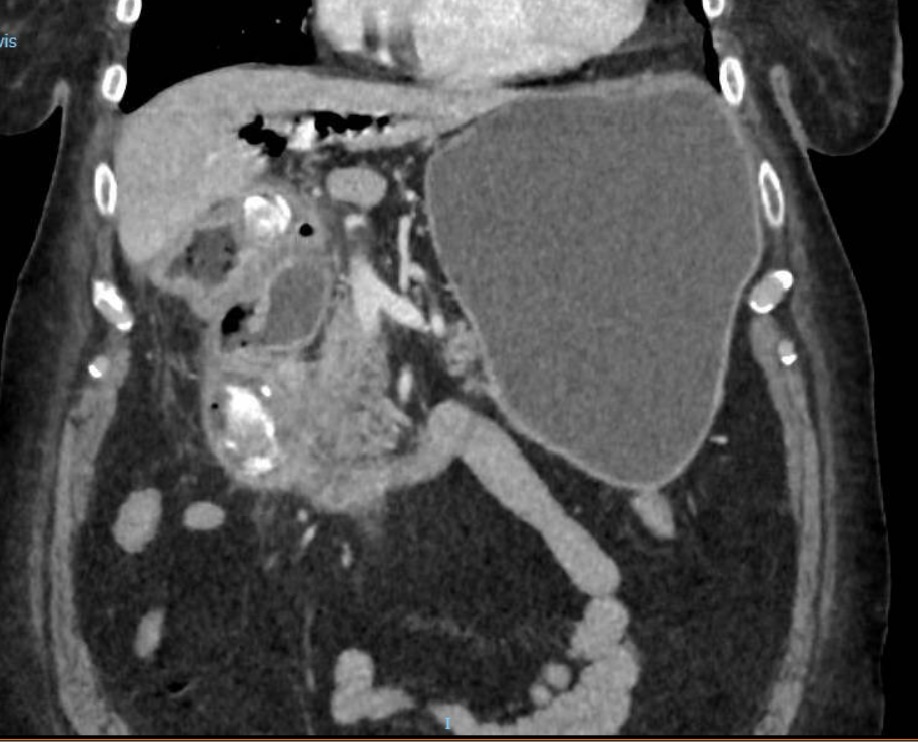
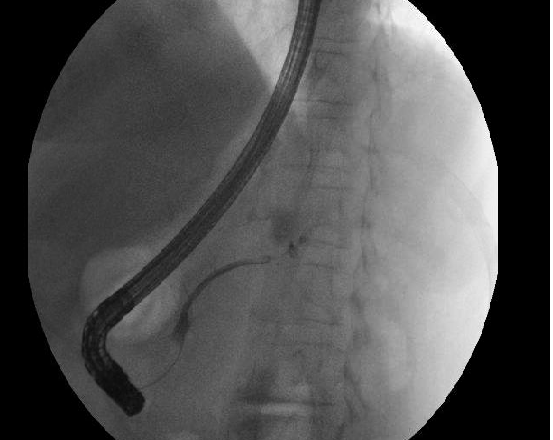
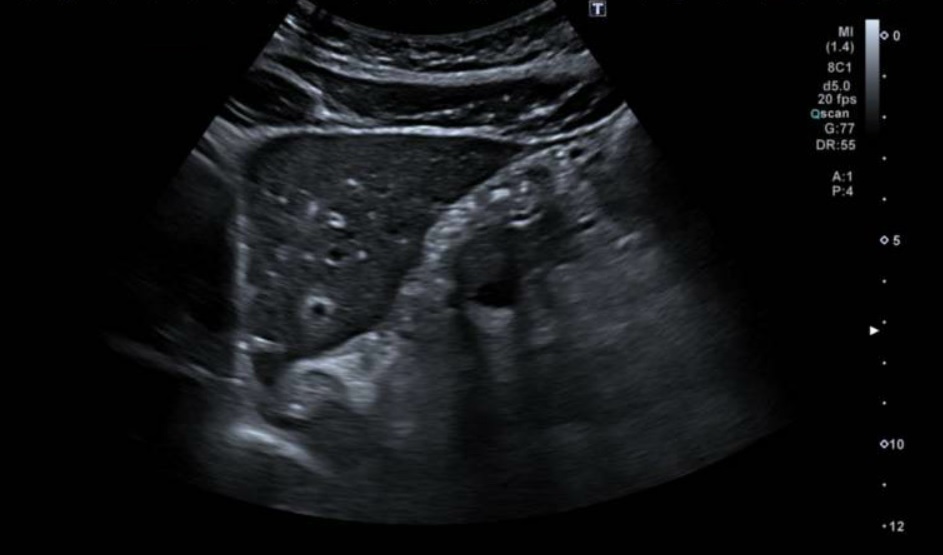
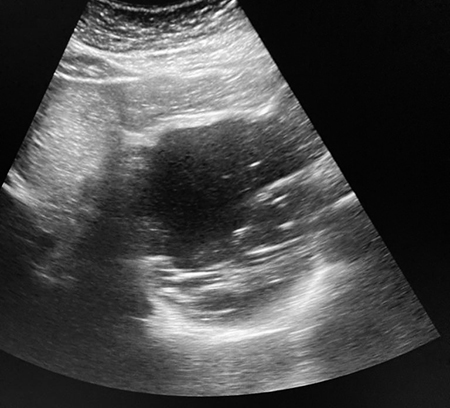
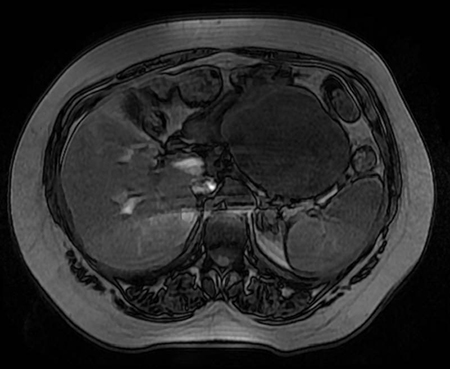
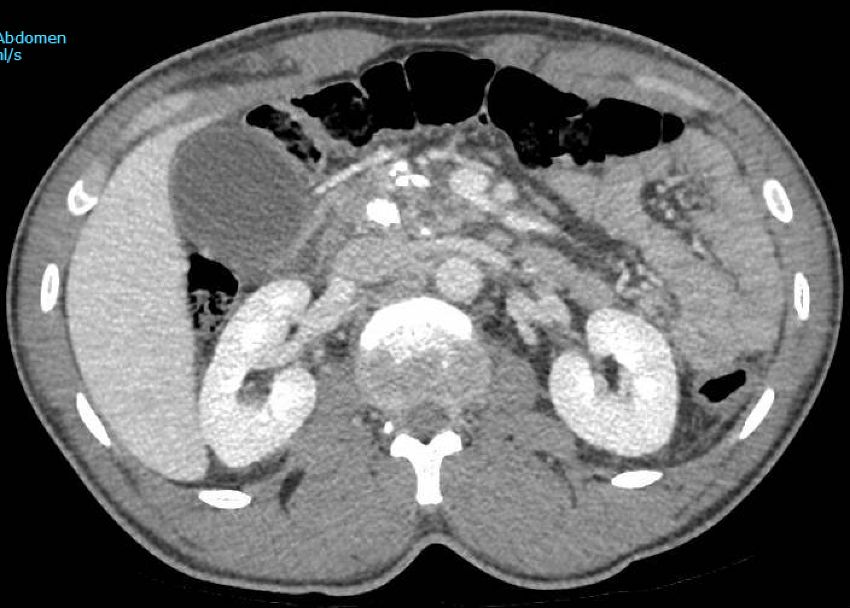
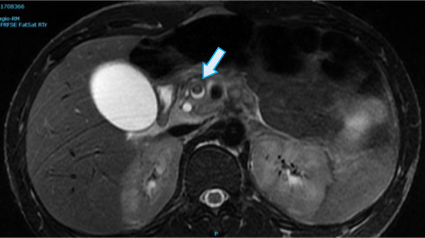
Transcurridas 48h, el paciente refiere mejoría súbita de síndrome emético. Sin embargo, en la exploración se evidencia dolor a la palpación en hemiabdomen inferior y signos de peritonismo que no estaban presentes a su llegada. Se realiza TC abdominal de control (imágenes 3-4) donde se observa una reducción importante del tamaño del pseudoquiste, y se identifica además líquido peritoneal en cuantía abundante que no estaba presente en estudio previo. Ante la sospecha de rotura espontánea del pseudoquiste, se contacta con Radiología Intervencionista para realización de drenaje percutáneo. El paciente evolucionó favorablemente evidenciándose mejoría clínica, analítica y radiológica en los sucesivos controles realizados.
Discusión
Los pseudoquistes pancreáticos aparecen hasta en el 25% de pacientes con pancreatitis crónica, aumentando su prevalencia cuando la etiología es enólica. Habitualmente se produce una resolución espontánea de los mismos siendo infrecuente la aparición de complicaciones asociadas. En concreto, la rotura espontánea se ha descrito en menos del 5% los casos. En aproximadamente la mitad de los pacientes, la rotura se produce hacia una víscera hueca sin causar complicaciones. Por el contrario, en el 50% restante el contenido se localiza en cavidad peritoneal tal y como se reporta en el presente caso clínico, siendo necesario realizar un drenaje percutáneo o una intervención quirúrgica urgente.
CP-166. ABORDAJE ENDOSCÓPICO DEL SÍNDROME DE DUCTO PANCREÁTICO DESCONECTADO
Ortiz Sánchez A, Cervilla Sáez De Tejada E, Zúñiga De Mora Figueroa B, Barrientos Delgado A, Gijón Villanova R
Servicio Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: pancreatitis, ducto pancreático desconectado, prótesis pancreática.
Introducción
El síndrome del conducto pancreático desconectado (SCPD) se debe a una interrupción del conducto pancreático principal o sus ramas secundarias, siendo una complicación presente entre un 30-80% de las pancreatitis agudas necrotizantes. La secreción de enzimas pancreáticas por el tejido pancreático aislado funcionante puede facilitar la recurrencia de colecciones necróticas encapsuladas (CNE), por lo que su abordaje endoscópico sigue siendo un tema controvertido en la práctica diaria.
Caso clínico
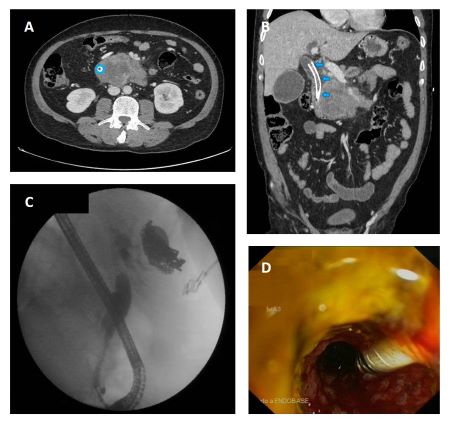
Presentamos el caso de una mujer de 57 años ingresada por pancreatitis aguda necrotizante grave con fracaso multiorgánico y necesidad de ingreso en UCI. Tras corrección de complicaciones sistémicas se objetivó necrosis peripancreática encapsulada con datos de sobreinfección en TC abdominal, por lo que se realizó drenaje transmural endoscópico con prótesis metálica, así como colocación de doble pigtail a su través (Figura 1).
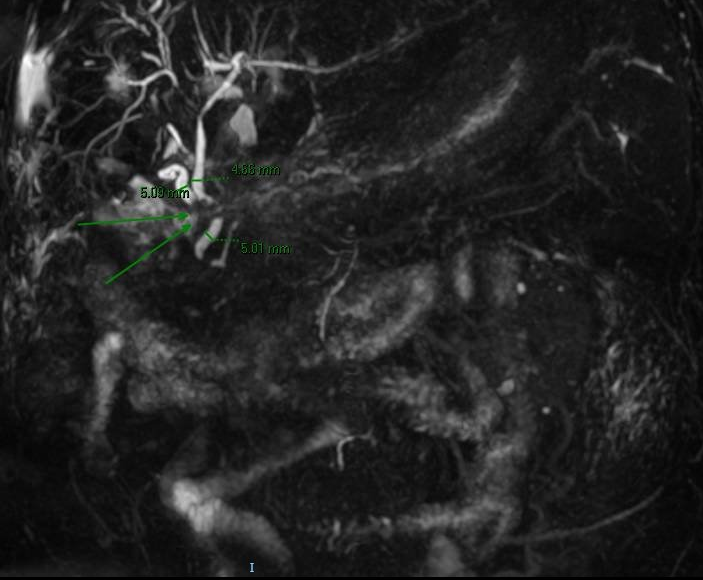
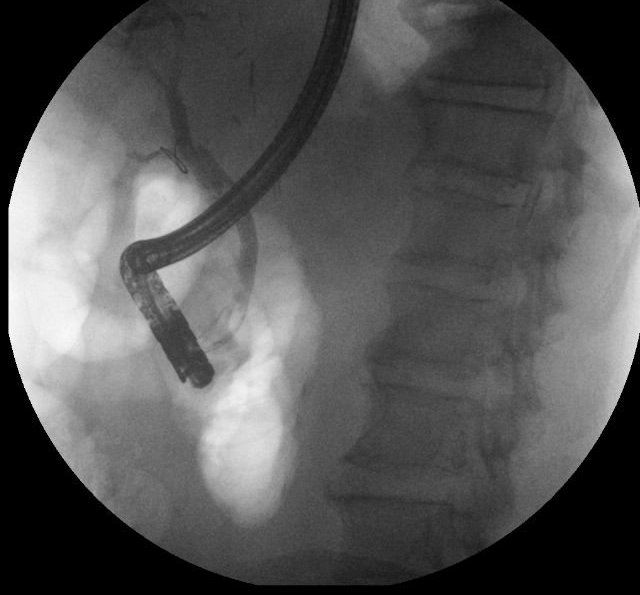
En sucesivos controles, se apreció persistencia de dicha colección necrótica a pesar de drenaje transmural, así como aparición de una nueva colección en cola de páncreas fistulizada a piel, sospechando SCPD. Se realizó CPRE que confirmó el diagnóstico, apreciando extravasación de contraste en conducto pancreático a nivel cuerpo y cola (Figura 2), decidiéndose colocar prótesis plástica pancreática tapizando la ruptura del CP (Figura 3). La paciente presentó buena evolución clínica y radiológica posterior, con desaparición colección necrótica, permitiendo retirada de prótesis transmural a las 8 semanas de su implantación.
Discusión
La ruptura, parcial o completa, del CP se asocia a una mayor tasa de recurrencia de CNE así como a un mayor porcentaje de intervencionismo endoscópico y rescates quirúrgicos para conseguir óptimos resultados.
Las guías de práctica clínica actuales no recomiendan la implantación de prótesis pancreática de forma sistemática en pacientes con SDPD y CNE, con preferencia sobre la colocación de prótesis plástica transmural a largo plazo para favorecer el drenaje pancreático hacia el tracto gastrointestinal.
Sin embargo, en casos con ruptura parcial del CP, la colocación de prótesis pancreática que selle dicha fuga es una alternativa a tener en cuenta, puesto que podría reducir la recurrencia y mejorar los resultados de dichas colecciones, evitando así posibles complicaciones derivadas del mantenimiento de prótesis transmurales a largo plazo.
CP-167. CAPACIDAD DE DETECCIÓN DE MINILITIASIS DE VESÍCULA BILIAR CON COLANGIORESONANCIA VS ECOENDOSCOPIA
Quirós Rivero P, Ternero Fonseca J, Calderón Chamizo M, Naranjo Pérez A, Caballero Fernández A, Elena Gómez E, Maraver Zamora M
Departamento Aparato Digestivo. Complejo Hospitalario de Especialidades Juan Ramón Jiménez, Huelva.
Palabras clave: colelitiasis, endosonografía, dolor abdominal.
Introducción
El término de minilitiasis o microlitiasis corresponde a la presencia de cálculos 3 mm. La ecografía abdominal tiene una sensibilidad (S) del 95% para detectar litiasis, disminuyendo en pacientes obesos, cálculos <5 mm, meteorismo y cálculos en cístico. Cuando el estudio es negativo y hay sospecha de litiasis existen otras opciones como la colangioresonancia (cRNM) o la ecoendoscopia (USE). Existen estudios que demuestran la utilidad de la USE en el dolor abdominal de probable origen biliar tras colecistectomía. Otros estudios sugieren que USE y cRNM deben ser ambas usadas en el diagnóstico de pancreatitis aguda y crónica idiopática
Material y métodos
Se trata de un estudio observacional, y retrospectivo, realizado en el Hospital Juan Ramón Jiménez (Huelva). De 207 pacientes analizados, sólo 37 cumplían criterios de inclusión.
El objetivo es evaluar la capacidad de detección de minilitiasis vesicular con cRNM vs USE en pancreatitis aguda idiopática (PAI), pancreatitis aguda recurrente idiopática (PAR), pancreatitis crónica idiopática (PCI), o por dolor abdominal sin causa (DAsC) en pacientes con probabilidad intermedia (movilización enzimas hepáticas y/o de colestasis) para litiasis vesicular no evidenciadas en ecografía ni TAC, y en los que se ha descartado el consumo de alcohol/tabaco.
Se realizó el análisis estadístico con STATA 12.0 para MAC OS utilizando el Test Mcnemar para muestras apareadas para comparar sensibilidades y especificidades. Se consideró óptimo un valor de p<0,5
Resultados
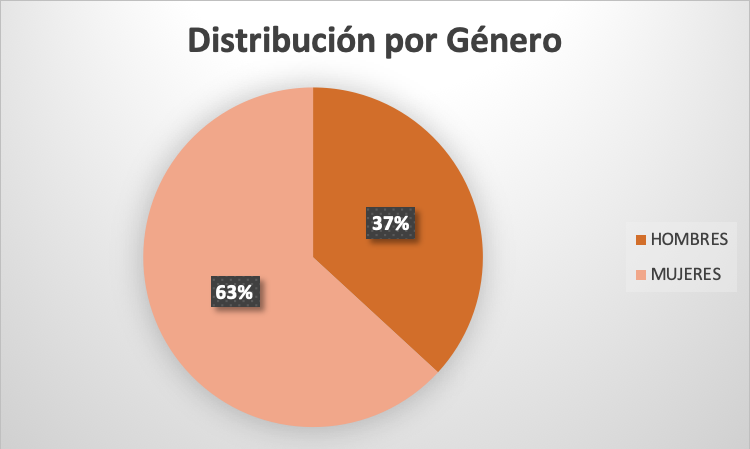
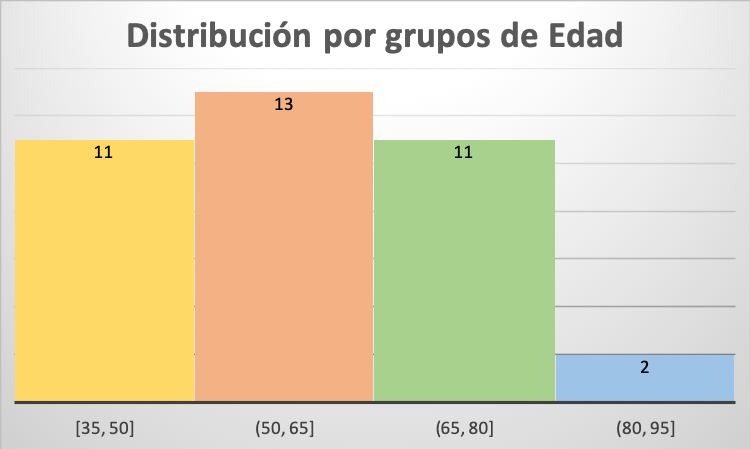
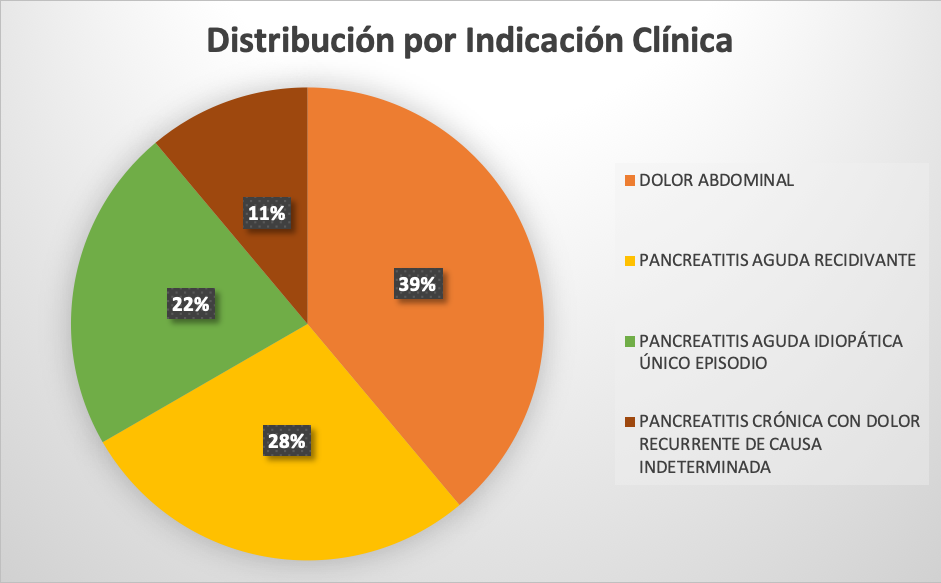
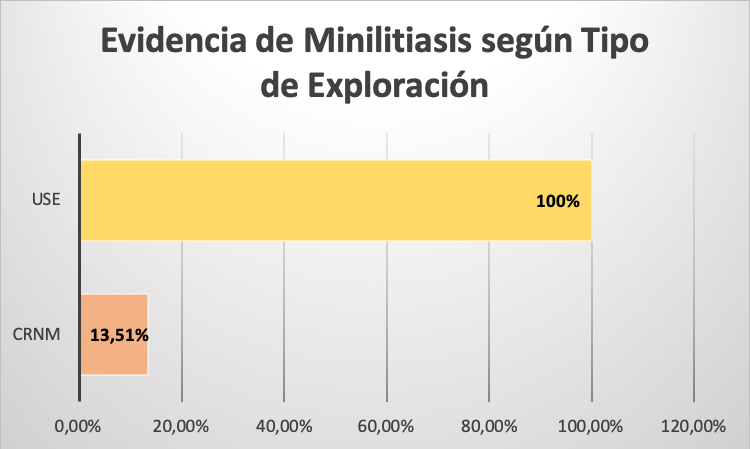
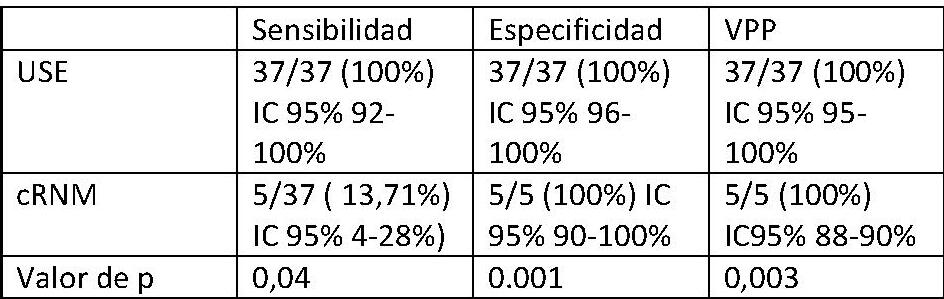
De un total de 37 pacientes, 24 (63%) fueron mujeres y 13 (37%) hombres. En cuanto a la edad, 11 (4%) tenía entre 35 y 50 años, 13 (5%) entre 50 y 65 años, 11 (4%) entre 65 y 80 años y 2 (1%) entre 80 y 95 años. Se realizó cRNM y USE en 14 (39%) de los pacientes con DAsC, en 8 (22%) de las PAI, en 10 (28%) de PAR y en 4 (11%) de las PCI. En relación a los hallazgos según método diagnóstico, comprobamos que la USE detectó en 37 (100%) de los pacientes presencia de minilitiasis como causa del cuadro. En cambio, la cRNM sólo encontró las minilitiasis en 5 (13,8%) de estos pacientes. Teniendo en cuenta que se tomó como gold standard la presencia/ausencia de minilitiasis en la colecistectomía posterior, evidenciamos una sensibilidad y especificidad del 100% para la detección de minilitiasis con USE, respecto una sensibilidad del 13,4% de la cRNM (p<0,05).
Conclusiones
Nuestro estudio sugiere que ante determinadas indicaciones de etiología incierta como son el DAsC, la PAI, PAR o la PCRI, debe plantearse la realización de USE como prueba de elección para el despistaje de minilitiasis vesicular en aquellos pacientes con probabilidad intermedia para un origen biliar en los que la ecografía y los estudios analíticos no encuentran agente etiológico.
CP-168. CASO INFRECUENTE DE METÁSTASIS PANCREÁTICA ÚNICA SECUNDARIA A CARCINOMA RENAL DE CÉLULAS CLARAS.
Guerrero Palma E, Alía Verdejo T, Calderon Ramírez MR, Macías Rodríguez MA
UGC Aparato Digestivo. Hospital Puerta del Mar, Cádiz.
Palabras clave: metástasis, páncreas, carcinoma renal de células claras .
Introducción
La metástasis pancreática aislada es excepcional. Asintomáticas hasta en el 50% de los casos, se suelen diagnosticar en el seguimiento de la neoplasia primaria. La sintomatología dependerá de su localización y puede ser similar a la de un tumor pancreático primario, siendo su diagnóstico diferencial esencial.
Caso clínico
Paciente de 67 años con antecedentes de colitis ulcerosa diagnosticada en 2007, con afectación extensa, en tratamiento con mesalacina y azatioprina, con buen control. En ecografía de control realizada al año, se identifica masa renal no conocida. Se completa estudio con TAC, que confirma el hallazgo de hipernefroma. Se realiza nefrectomía radical con diagnóstico, tras estudio anatomopatológico, de carcinoma de células claras estadio T1B GII.
El paciente permanece asintomático, retirándose la inmunosupresión y realizando controles anuales sin evidencia de recidiva hasta 2022 , que por TAC se identifica lesión hipervascular en cuerpo-cola de páncreas , de 3,8 x 2,6cm, asociándose discreta ectasia retrógrada del conducto pancreático. Se realiza ecoendoscopia con toma de biopsias con anatomía patológica compatible con metástasis de tumor renal de células claras. Se realiza antrectomía gástrica, duodenopancreatectomía total y esplenectomía con postoperatorio sin complicaciones. El informe anatomopatológico confirmó el origen metastásico renal de la lesión, sin afectación vascular ni ganglionar.
Figura 2
Corte axial de tomografía computada abdominal con contraste intravenoso donde se visualiza la lesión renal visualizada previamente en ecografía compatible con hipernefroma.
Discusión
Las metástasis pancreáticas de cáncer renal son infrecuentes. Según estudios basados en autopsias y cirugías, los órganos que más frecuentemente metastatizan en páncreas son pulmón (42%), seguidos por los del tracto gastrointestinal (24,7%) y cáncer renal (4%).
El diagnóstico suele ser un hallazgo casual durante el seguimiento de la neoplasia primaria. Las manifestaciones clínicas dependen de la localización y son similares a las de un tumor pancreático primario. La TC y RMN son las técnicas de elección para su estudio, teniendo un comportamiento hipervascular, característica que comparten con los tumores neuroendocrinos, siendo importante el diagnóstico diferencial con este tipo de lesiones dada las diferencias en el manejo y pronóstico. Cuando el diagnóstico permanece incierto, la biopsia percutánea o endoscópica es el método de elección, permitiéndonos confirmar la estirpe de la lesión con las técnicas inmunohistoquímicas y la positividad para CD10, vimentina y CK AE1-3.
El tratamiento de elección ante una metástasis pancreática solitaria resecable, sin extensión extrapancreática, es la resección quirúrgica, que es lo que ha demostrado aumentar significativamente la supervivencia de estos pacientes. Es la localización la que condiciona la técnica a emplear, con los criterios oncológicos correspondientes, para obtener un margen de seguridad.
CP-169. CAUSA INFRECUENTE DE ICTERICIA OBSTRUCTIVA: SÍNDROME DE LEMMEL
Rico Cano A, Vera García P
UGC Aparato Digestivo. Hospital Comarcal de la Axarquía, Vélez-Málaga.
Palabras clave: síndrome lemmel, .
Introducción
El síndrome de Lemmel es una patología rara definida como ictericia obstructiva por divertículo duodenal periampular en ausencia de coledocolitiasis o neoplasia.
Caso clínico
Varón de 60 años, colecistectomizado por colelitiasis, ingresa por dolor abdominal e ictericia observándose en analítica elevación de Bilirrubina total (2.27) a expensas de Bilirrubina directa (1.5). Se realiza ecografía abdomen que describe colecistectomía y dilatación de vía biliar intra y extrahepática de hasta 1.3 cm, sin identificar causa. Se solicita Colangio-RM ( Figura 1) donde informa de masa en proceso uncinado que comprime y estenosa el colédoco distal provocando dilatación secundaria de la vía biliar(a descartar neoplasia) y se completa estudio con TC abdomen (Figura 2,3) donde evidencia que la masa descrita anteriormente corresponde con un divertículo periampular de 27 mm y Ecoendoscopia donde se aprecia el divertículo duodenal de gran tamaño con papila de difícil acceso intradiverticular, descartándose coledocolitiasis. Dado que el paciente en ese momento se encuentra asintomático con normalización del perfil hepático, siendo este su primer episodio, y el acceso difícil a la vía biliar, se decide no realizar esfinterotomía en este momento por posibles riesgos.
Discusión
Los divertículos duodenales se presentan en el 10-20% de las endoscópicas, localizándose más frecuentemente en la segunda porción duodenal, próximos a la ampolla de Vater (periampulares). La enfermedad biliopancreática puede ser debida a la compresión extrínseca que produce el propio divertículo sobre la vía biliar (Síndrome de Lemmel) o por favorecer el sobrecrecimiento bacteriano y la producción de litiasis biliares e inducir la disfunción del esfinter de Oddi.
La mayoría son asintomáticos, produciendo solo clínica en un 5% de los casos presentándose como obstrucción biliopancrática o duodenal, perforación o hemorragia. Su presentación clínica es variable, desde ictericia obstructiva intermitente, dolor abdominal postprandial o colangitis.
El diagnóstico comienza con la sospecha clínica, confirmándose mediante pruebas de imagen ( TAC, Colangio-RM, CPRE o ecoendoscopia) la compresión extrínseca del conducto biliar por el divertículo.
El tratamiento en asintomáticos no está justificado, puesto que las complicaciones pueden superar a los beneficios. Si existe complicación biliar o pancreática la esfinterotomía biliar es el tratamiento de elección, con/sin colocación de stent, teniendo en cuenta que si la papila se encuentra intradiverticular su canulación puede ser dificultosa. La cirugía se deja para aquellos en los que fracase el tratamiento endoscópico, no existiendo consenso de la técnica quirúrgica a realizar por los pocos casos descritos en la literatura.
CP-170. COLANGIOCARCINOMA METASTÁSICO CON IMPLANTES DE LOCALIZACIÓN ATÍPICA.
Lecuona Muñoz M, Tendero Peinado C, Rosa Sánchez C, Redondo Cerezo E, Rodríguez Sicilia MJ
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: colangiocarcinoma, metástasis.
Introducción
El colangiocarcinoma hiliar o tumor de Klatskin presenta afectación metastásica al diagnóstico hasta en el 30% de pacientes, siendo la localización más frecuente el hígado y resultando excepcional la diseminación extraabdominal.
Caso clínico
Mujer de 55 años sin antecedentes de interés, que consulta por ictericia indolora. Asocia lesión en cara anterior del muslo izquierdo de un mes de evolución, que ha ido aumentando progresivamente de tamaño y condiciona impotencia funcional generando dificultad para la deambulación. Analíticamente destacan bilirrubina total de 18.6 mmol/L (Br directa 13.8 mmol/L), fosfatasa alcalina 1320 UI/L y gamma-glutamil transferasa 2267 UI/L. Se realiza TC abdominopélvico (Figura 1) donde se evidencia una lesión hipovascular en hilio hepático que condiciona dilatación de la vía biliar intra y extrahepática. Se observan además trombosis portal, implantes suprarrenales bilaterales y adenopatías metastásicas paraaórticas. Se realizó PAAF guiada por ecoendoscopia para estudio histológico, confirmando el diagnóstico de colangiocarcinoma.
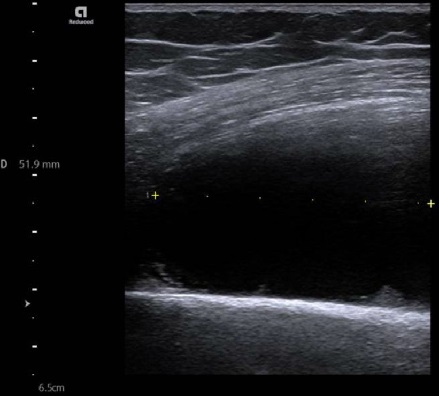
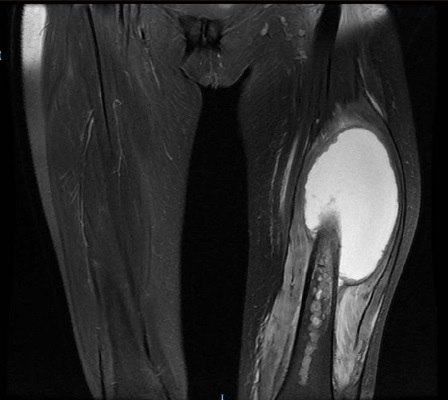
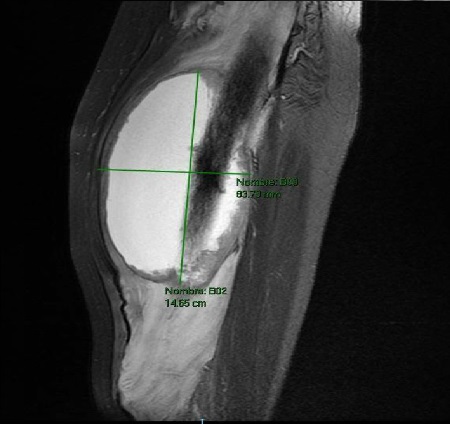
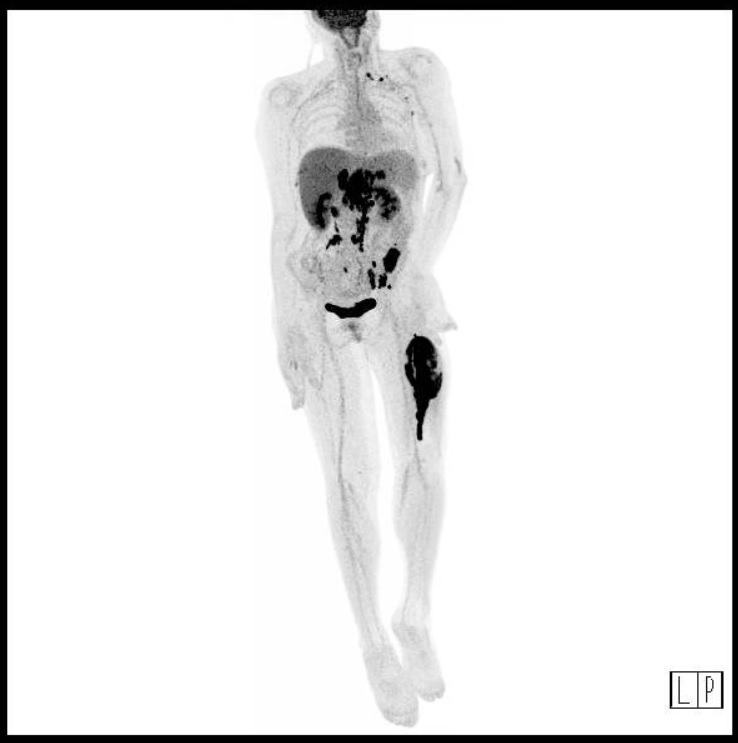
Con el objetivo de caracterizar la lesión localizada en muslo izquierdo, se solicita inicialmente ecografía de partes blandas (Figura 2) identificando una masa hipoecogénica intramuscular de 8,4 x 7,9 x 14,7 cm (AP x T x CC). Se realiza posteriormente resonancia magnética nuclear Figuras 3-4) donde se visualiza tumoración mayoritariamente quística en el espesor del cuádriceps que infiltra diáfisis femoral y que sugiere afectación metastásica, sin poder descartar tumoración de estirpe sarcomatosa. Mediante PET-TAC (Figura 5) se evidencia gran masa irregular hipermetabólica con interior ametabólico sin poder discernir origen. Finalmente se realizó biopsia con aguja gruesa guiada por TC de la diáfisis femoral. El estudio histológico mostró elementos mieloides concordante con metástasis de colangiocarcinoma pobremente diferenciado. La paciente fue derivada a Cuidados Paliativos para soporte sintomático y finalmente falleció transcurrido un mes.
Figura 1
TC abdomino-pélvico con contraste. Lesión sólida hipovascular en hilio hepático de dimensiones 53 x 47 x 42 mm (AP x T x CC) que condiciona marcada dilatación de la vía biliar intra y extrahepática, sugerente de colangiocarcinoma.
Figura 2
Ecografía de partes blandas. Lesión hipoecogénica de aproximadamente 8,4 x 7,9 x 14,7 cm (AP x T x CC). localizada en vasto intermedio. No presenta flujo doppler en su interior
Figura 3
Resonancia magnética nuclear con contraste. Lesión mayoritariamente quística en el compartimento anterior del muslo izquierdo, localizada en el espesor del músculo cuádriceps (predominantemente vasto intermedio).
Discusión
El colangiocarcinoma es un tumor maligno originado en el epitelio de las vías biliares, que genera metástasis por diseminación linfática habitualmente. Las metástasis óseas son frecuentes en pacientes con tumores primarios de próstata, mama o pulmón, pero resultan excepcionales en el colangiocarcinoma. Por otra parte, cuando se producen metástasis óseas en el colangiocarcinoma, se localizan habitualmente a nivel de columna vertebral y no fuera del esqueleto axial tal y como se reporta en el presente caso clínico. Dada su baja prevalencia y su diagnóstico diferencial complejo, que incluye otras lesiones malignas como el osteosarcoma, habitualmente son necesarias técnicas de imagen e histológicas para lograr un diagnóstico definitivo.
CP-171. COMPLICACIONES DE PRÓTESIS BILIAR PLÁSTICA: MIGRACIÓN, PERFORACIÓN, OBSTRUCCIÓN INTESTINAL Y ABSCESO.
Morales Bermúdez AI, Bracho González M, Fernández Cornax A, Pinto García I, Jiménez Pérez M
UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: cpre, prótesis biliar, complicaciones.
Introducción
La migración de prótesis biliares plásticas ocurre en hasta el 14 % de los drenajes biliares endoscópicos. La migración puede derivar en diferentes complicaciones como perforación u obstrucción intestinal.
Caso clínico
Varón de 65 años. CPREs previas por coledocolitiasis. Se realiza limpieza de la vía biliar con balón, con extracción de litiasis y barro biliar y posicionamiento de prótesis biliar plástica de 10F x 5 cm. Tres meses después presenta febrícula y dolor abdominal. Se realiza TC de abdomen: colección a nivel de flanco derecho en contacto con un asa de intestino delgado perforada por prótesis biliar migrada. Se realiza laparotomía exploradora visualizando peritonitis y se procede a adhesiolisis, siendo muy dificultosa y con asas intestinales muy frágiles. Se localiza perforación en duodeno, sin posibilidad de localizar la prótesis, por lo que se sutura la perforación, se colocan drenajes y se desiste en la búsqueda de la prótesis por riesgo de iatrogenia. El paciente presenta evolución lentamente favorable y es dado de alta al mes del ingreso. Un mes más tarde, el paciente presenta dolor abdominal y vómitos, con diagnóstico de obstrucción intestinal secundaria a prótesis biliar migrada. Se opta por manejo conservador con sonda nasogástrica, con buena evolución. Tres meses después presenta clínica de febrícula, empastamiento y dolor en flanco derecho. En TC de abdomen se detecta absceso de pared abdominal con comunicación torácica secundario a prótesis biliar. Se inicia antibioterapia y se realiza drenaje de absceso abdominal. Se decide retirada de prótesis biliar. Radiología Vascular localiza la prótesis mediante ecografía en ángulo hepático del colon con salida parcial de la misma hacia espacio lateroconal derecho. Se realiza marcaje con arpón de la prótesis a modo de guía y posteriormente Cirugía lleva a cabo laparotomía realizando disección guiada por arpón hasta localizar la prótesis y retirarla. Desde entonces el paciente se encuentra asintomático.
Figura 1
Corte transversal TC: prótesis biliar migrada con perforación de asa intestinal que comunica con colección con gas en su interior. Peritonitis secundaria.
Discusión
El drenaje de la vía biliar mediante prótesis posicionadas por CPRE se ha convertido en uno de los tratamientos más importantes de las estenosis de la vía biliar. Las prótesis plásticas tienen mayor probabilidad de migración que las metálicas, aunque la mayoría pueden ser eliminadas espontáneamente a través del ano. En raras ocasiones, la migración de una prótesis biliar produce complicaciones como perforación, obstrucción intestinal o absceso. Sin embargo, debemos estar alerta ante síntomas digestivos en pacientes portadores de prótesis para poder llevar a cabo una rápida detección de estas complicaciones graves que pueden poner en peligro la vida del paciente.
CP-172. EFECTO ADVERSO INUSUAL DE SORAFENIB: COLECISTITIS AGUDA ALITIASICA
Martinez Burgos M1, Angulo McGrath I2, Morales Bermudez AI3, Bracho Gonzalez M3
1UGC Aparato Digestivo. Complejo Hospitalario Universitario de Cartagena, Cartagena. 2UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Virgen de Valme, Sevilla. 3UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: sorafenib; colecistitis aguda; efecto adverso.
Introducción
El sorafenib es un fármaco que se utiliza en el tratamiento de diferentes tumores y que pertenece a la familia de los inhibidores de la quinasa. Actúa enlenteciendo la tasa de crecimiento de las células cancerosas e interrumpiendo el aporte de sangre a las mismas. En los últimos años ha aumentado su uso en aparato digestivo debido a su indicación en el hepatocarcinoma en estadio avanzado. Sus efectos adversos más conocidos son la diarrea, la hipertensión arterial, la hiperqueratosis palmar o el aumento del riesgo de hemorragias y descompensación en los pacientes cirróticos. Sin embargo, existen otros efectos adversos menos frecuentes y que también se han relacionado con este fármaco.
Caso clínico
Mujer de 67 años. Diagnostico reciente de tumor de partes blandas en miembro superior izquierdo con anatomía patológica de hemangioendotelioma epitelial. La paciente acude a urgencias por dolor abdominal en epigastrio e hipocondrio derecho desde hace 5 días que comenzó a las 48 horas de iniciar tratamiento con Sorafenib. La paciente presenta buen estado general TA 190/90 mmHg FC: 70 lpm y 37.2ºC. Murphy negativo y perfil hepático normal por lo que se decide ingreso para estudio y suspender sorafenib. Durante las primeras 24 horas del ingreso la paciente presenta deterioro clínico y analítico, con empeoramiento de la exploración abdominal que ahora presenta irritación peritoneal, por lo que se decide realización de un TC abdominal urgente (Figura 1). TC informa de vesícula distendida con paredes engrosadas y cambios inflamatorios de la grasa perivesicular, datos compatibles con colecistitis aguda. En TC abdominal no se informa de litiasis vesicular. Se inicia tratamiento antibiótico con excelente respuesta. Ecografía abdominal programada descarta litiasis vesicular. Revisamos ficha técnica de sorafenib y comprobamos que la colecistitis aguda alitiásica está descrita como efecto adverso. La paciente se recupera en pocos días normalizando dieta y finalizando pauta de antibioterapia en domicilio. Pendiente de colecistectomía por parte de cirugía.
Discusión
Sorafenib es un fármaco que ha demostrado ser eficaz en frenar la evolución de varios tumores, entre ellos el hepatocarcinoma. Como todos los fármacos y en especial los quimioterápicos debemos estar especialmente atentos a la aparición de complicaciones derivadas de su uso. La mayoría de los efectos adversos más frecuentes son conocidos y vigilados de forma estrecha, pero existen otras complicaciones más inusuales que también es preciso sospechar.
CP-173. ESTUDIO DESCRIPTIVO ADENOCARCINOMA DE PÁNCREAS EN HOSPITAL UNIVERSITARIO REINA SOFÍA DE CÓRDOBA
Gómez Pérez A1, Ortiz Chimbo DS1, Zamora Olaya JM1, Leiva-Cepas F2, Serrano Ruiz FJ1, Hervás Molina AJ1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba. 2UGC Anatomía Patológica. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: adenocarcinoma páncreas, incidencia, supervivencia global..
Introducción
Analizar la incidencia y supervivencia global de los pacientes con adenocarcinoma de páncreas (ADP) que son diagnosticados y/o reciben tratamiento en Hospital Universitario Reina Sofía (HURS).
Objetivos secundarios: conocer las características del tumor, población atendida, así como el tipo de tratamiento recibido.
Material y métodos
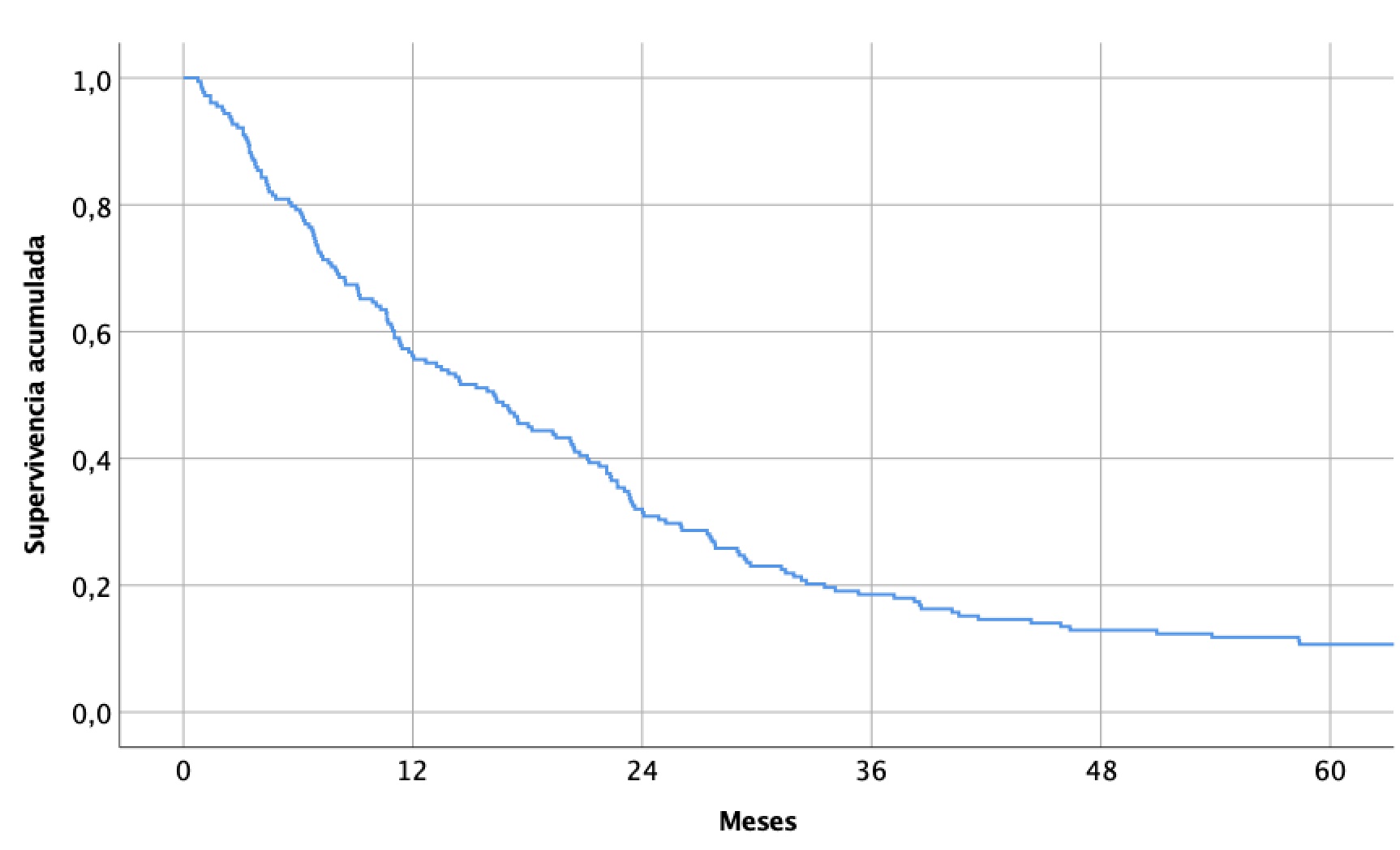
Estudio observacional, retrospectivo y unicéntrico que incluye a pacientes con diagnóstico histológico de ADP que son atendidos en el HURS entre los años 2012 y 2017. El tiempo de seguimiento fue de al menos 5 años. Se recogieron variables demográficas, relacionadas con el tumor y el tipo de tratamiento recibido. Se realizaron curvas de supervivencia mediante el método Kaplan-Meier.
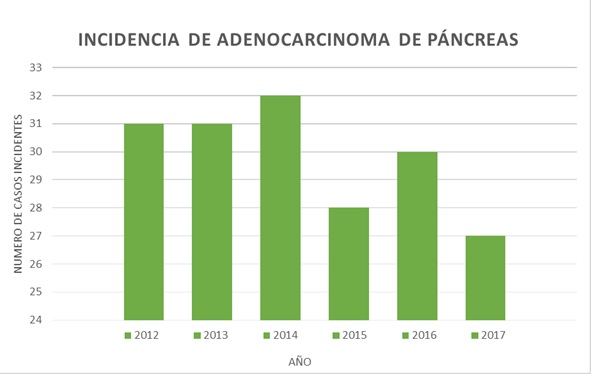
Figura 1
Incidencia anual de ADP atendido en el HURS en el período comprendido entre los años 2012 y 2017.
Resultados
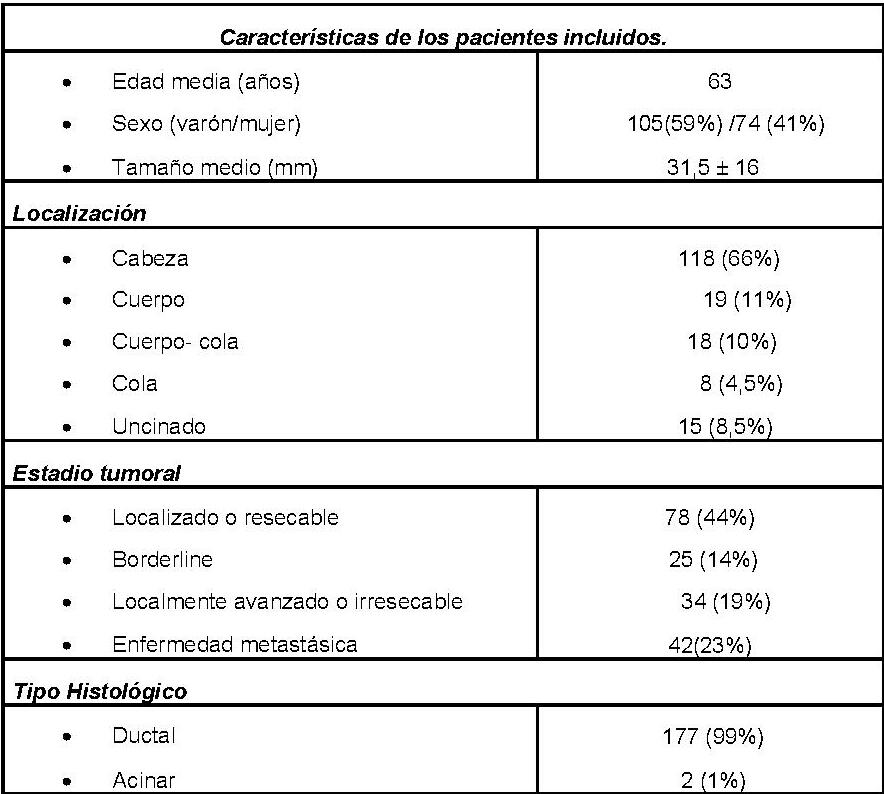
En este periodo se han diagnosticado histológicamente 179 casos de ADP, siendo la incidencia media de 29,7 casos/año (Figura 1). Edad media de 63 años. El 58,3% (n=105) fueron hombres y el 41,3% (n=74) mujeres. No se han identificado pacientes portadores de mutaciones susceptible de cáncer de páncreas hereditario ni pacientes que cumplan criterios de cáncer pancreático familiar. El 15,6% (28) fueron diagnosticados de diabetes mellitus los 6 meses previos al diagnóstico o sufrieron descompensación glucémica. El síntoma más frecuente al diagnóstico fue el dolor abdominal (39%) seguido de ictericia (30%) y síndrome constitucional (15%). La localización más frecuente fue cabeza de páncreas (66%) y el tamaño medio del tumor fue de 31,5 ± 16,45 (DE) mm.
El 43,6% de los pacientes se diagnosticaron en estadio localizado o resecable mientras que enfermedad metastásica se presentó en el 23,5% de los pacientes (Tabla 1).
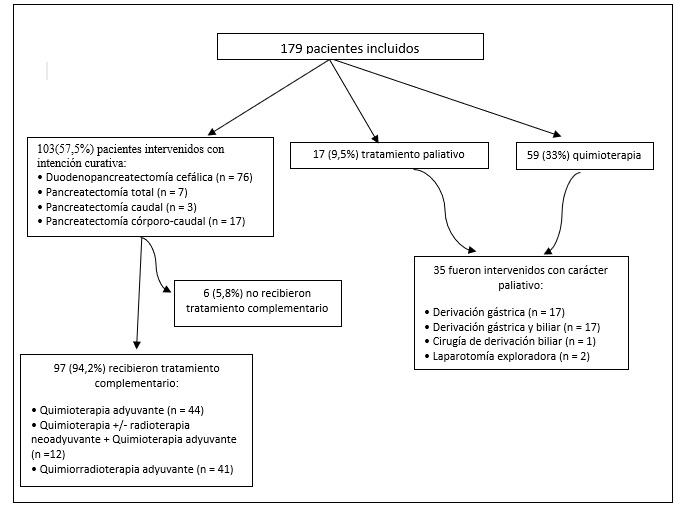
Se realizó cirugía con intención curativa en el 57,5% (n=103) de los pacientes, mientras que el 33% (n=59) se trató con quimioterapia y el 9,5% (n=17) restante solo fue candidato a tratamiento paliativo (Figura 2). En el 52,5% (n=94) de los pacientes se realizó drenaje biliar, realizándosemediante CPRE en el 66%.
La mediana de supervivencia desde el diagnóstico fue de 16 meses (IQR 7-29) (Figura 3). La supervivencia global observada al año, tres y cinco años fue del 56,2%, 18,5% y 10,7% respectivamente.
Conclusiones
El análisis de nuestros datos revela una supervivencia global mayor a la descrita en la literatura, en probable relación al mayor número de pacientes que son diagnosticados en estadio resecable, lo que pone de manifestó la importancia de buscar estrategias para la detección precoz y prevención de este tumor.
CP-174. EXTRAÑA COMPLICACIÓN EN EL ADENOCARCINOMA DE PÁNCREAS
García García MD, Gálvez Criado JM, Rodríguez Delgado C, Grande Santamaria L, Caunedo Álvarez A
Unidad Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: adenocarcinoma, necrosis, hepática.
Introducción
El adenocarcinoma de páncreas es una entidad maligna y agresiva. Normalmente, el diagnóstico se lleva a cabo en estadios avanzados por la ausencia de síntomas característicos, siendo la afectación vascular uno de los puntos clave que limitan el tratamiento y pronóstico de nuestros pacientes.
Caso clínico
En relación a esto, presentamos el caso de una mujer de 63 años, diagnosticada de adenocarcinoma de cabeza-cuerpo de páncreas estadio III (T4N0M0) borderline resecable desestimada posteriormente para intervención quirúrgica por progresión tumoral, encontrándose en tratamiento quimioterápico activo. El tumor englobaba la arteria hepática y ocasionaba trombosis de la vena porta con dilatación secundaria de vena esplénica. Además, requirió la colocación de prótesis plástica biliar por infiltración neoplásica del colédoco.
Acude a urgencias por melenas con caída de dos puntos de hemoglobina, realizándose gastroscopia urgente en la que se visualizaban dos cordones varicosos en esófago distal sin estigmas de sangrado reciente que aplanaban con la máxima insuflación, dos aftas fibrinadas prepilóricas (LAMG) y lo que impresionaba de lesiones varicosas en 2ª porción duodenal, encontrándose una de ellas erosionada con vaso visible en su cúspide, friable al roce, que se trató mediante la colocación de un hemoclip (Figura 1). En gasometría de control presentó Hb 4,8g/dl, necesitando la transfusión de 3 concentrados de hematíes. Tras esto, comienza con dolor en zona lumbar, mal estado general e inestabilidad hemodinámica. En la exploración presentaba un abdomen poco depresible, muy doloroso y con peritonismo, por lo que se solicitó un TAC abdominal (Figuras 2 y 3) en el que se describía gran cantidad de gas intrahepático lo que sugería isquemia/necrosis hepática, la arteria hepática no logró identificarse y presentaba infartos esplénicos, gas extraperitoneal perihepático y un intestino de shock, todo ello en relación a fallo multiorgánico. Se decide sedación paliativa y la paciente fallece a las 4 horas.
Figura 1.
Imagen endoscópica en la que se visualiza una lesión varicosa en 2ª porción duodenal con vaso visible en su cúspide.
Discusión
La necrosis hepática masiva es una entidad clínica poco frecuente y generalmente descrita en la bibliografía por afectación del eje vascular abdominal tras procedimientos quirúrgicos hepatobiliopancreáticos. De igual forma, existen casos publicados en relación a tratamientos locales del hepatocarcinoma (embolización o ablación con etanol), así como secundario a la trombosis completa de la arteria hepática tras la realización de trasplante hepático. Lo que destacamos de este caso es la infrecuente presentación de la trombosis aguda completa del eje vascular hepático en relación con la progresión neoplásica pancreática, no estando relacionada con la iatrogenia como encontramos habitualmente descrita esta entidad en la bibliografía.
CP-175. HEMORRAGIA DIGESTIVA ALTA DE ORIGEN INESPERADO
MORENO BARRUECO M, BAILÓN GAONA MC, OLVERA MUÑOZ R, BERDUGO HURTADO F
Servicio Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: hemorragia digestiva alta, cáncer de páncreas, síndrome constitucional..
Introducción
El cáncer de páncreas es un tumor localmente agresivo y con poco potencial de curabilidad por la frecuente infiltración vascular del mismo, lo cual supone un criterio de irresecabilidad. Suele ser un tumor sintomatológicamente silencioso, que cuando debuta supone un estado avanzado del mismo.
Caso clínico
Paciente de 85 años sin antecedentes de interés que consulta por dolor en epigastrio, hiporexia y episodios aislados de deposiciones melénicas de un mes de evolución. En análisis realizado destacar anemia ferropénica de 3 meses de evolución, con hemoglobina de 9.3 g/dl a nuestra valoración (Hemoglobina basal 14-15g/dl). Ante la sospecha de hemorragia digestiva alta, se realiza gastroscopia con hallazgo en cara posterior de cuerpo alto de lesión de posible origen subepitelial con ulceración central y restos hemáticos, que se biopsia (Figura 1). Se completa estudio con TC toracoabdominopélvico con datos sugerentes de neoplasia de cuerpo-cola de páncreas con metástasis hepáticas, que infiltra arteria esplénica, vena esplénica y vena mesentérica superior; y contacta ampliamente realizando efecto masa sobre curvadura mayor/cara posterior de cuerpo gástrico (Figura 2). Histológicamente se confirma que la lesión subepitelial gástrica concuerda con infiltración por adenocarcinoma pancreático. Finalmente, dado lo avanzado de la enfermedad, se consensua con la paciente y familiares seguimiento y tratamiento sintomático por parte de la Unidad de Cuidados Paliativos.
Discusión
La hemorragia digestiva alta es una forma de debut infrecuente del cáncer de páncreas. De los pocos casos descritos, la forma más frecuente son las melenas o hematoquecia, siendo aún más infrecuente en forma de hematemesis. Lee et al describe hasta ocho pacientes en los que una hemorragia digestiva mayor fue el primer signo de una neoplasia maligna de páncreas comprobada posteriormente. En siete de ellos, hubo invasión tumoral directa en una porción contigua del tracto gastrointestinal, en forma de masa ulcerativa similar a la descrita en nuestro caso.
Los pacientes con este grado de infiltración asocian tumores de gran tamaño que con frecuencia asocian infiltración vascular y extensión metastásica, cumpliendo criterios de irresecabilidad, que desechan cualquier tipo de opción terapéutica curativa, quedando únicamente disponible el tratamiento paliativo, situación en la que se encontraba nuestro paciente en el momento del diagnóstico.
CP-176. HEMOSUCCUS PANCREATICUS: UNA CAUSA DE HEMORRAGIA DIGESTIVA E ICTERICIA
Rosa Sánchez C, López Vico M, Tendero Peinado C, Redondo Cerezo E, López Tobaruela JM
Departamento Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: hemosuccus pancreaticus.
Introducción
La hemorragia digestiva es un problema al que nos enfrentamos a diario y que puede deberse a muy diversas causas. Sin embargo, hay ciertas etiologías que no suelen tenerse en cuenta a priori por su escasa frecuencia en la práctica clínica diaria. Este es el caso de una paciente que ingresó por un cuadro de ictericia y hemorragia digestiva en relación a un hemosuccus pancreaticus secundario a pancreatitis aguda grave.
Caso clínico
Mujer de 40 años, con importante hábito enólico previo, que acude por emisión de heces hematoquécicas con moderada anemización, sin repercusión hemodinámica y sin dolor abdominal u otra clínica asociada. Al ingreso analíticamente destaca ictericia (con bilirrubina de hasta 22) de perfil analítico obstructivo, sin alteración de las enzimas de citolisis ni pancreáticas. Se realiza colonoscopia, en la que se aprecian restos hemáticos en todo el trayecto explorado, sin visualizarse ninguna lesión, tras lo cual se realiza gastroscopia, visualizándose un coágulo fresco sobre el orificio papilar, estable y que no se desprende con el lavado (Figura 1). Ante la sospecha de hemobilia se realiza angioTC, en el que se aprecian datos de pancreatitis aguda necrotizante sobre páncreas atrófico y con datos de pancreatitis crónica, con presencia de dos colecciones peripancreáticas de hasta 53 mm (Figura 2), sin encontrarse punto de sangrado activo. Desde entonces la paciente se mantiene hematimétrica y hemodinámicamente estable, sin nuevas exteriorizaciones de hemorragia digestiva, y con una resolución progresiva de la ictericia. Posteriormente, ante la aparición de fiebre persistente y la ausencia de mejoría de una de las colecciones, se realiza drenaje de la misma guiado por ecoendoscopia mediante colocación de una prótesis de aposición luminal, drenándose material necrohemorrágico con cultivo positivo para Candida parapsilosis. Tras esto la paciente presentó gran mejoría clínica, con retirada de la prótesis dos semanas después y pudiendo ser derivada al alta sin complicaciones posteriores.
Figura 1
EDA en la que se aprecia papila con un coágulo en su superficie sin datos de sangrado activo y que no se desprende con el lavado.
Figura 2
Angio-TC abdominal en que se aprecia un páncreas desestructurado con un conducto de Wirsung dilatado y con áreas de hipocaptación de contraste compatible con pancreatitis aguda necrotizante sobre páncreas atrófico (flecha verde). En cuerpo pancreático se aprecian dos colecciones (flecha azul).
Discusión
En casos como este, en los que apreciamos simultáneamente datos de hemorragia digestiva y una alteración del perfil biliopancreático, debemos plantearnos el diagnóstico de Hemosuccus pancreaticus. Afortunadamente, en este caso la hemorragia fue autolimitada y no requirió intervención, si bien suele ser necesaria la realización de una embolización arterial y a veces incluso de medidas quirúrgicas para el control del sangrado, dado que en ocasiones puede resultar grave y potencialmente mortal (hasta en el 90% sin tratamiento). Por tanto, un diagnóstico y tratamiento precoces resultan fundamentales para el pronóstico en este tipo de situación clínica.
CP-177. ICTERICIA INDOLORA DE ORIGEN HEMATOLÓGICO.
Lecuona Muñoz M, López Vico M, Lancho Muñoz A, Redondo Cerezo E, Rodríguez Sicilia MJ
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: ictericia, sarcoma mieloide.
Introducción
La ictericia obstructiva de causa tumoral se asocia habitualmente con neoplasias de origen biliar o pancreático. Sin embargo, existen otras neoplasias menos frecuentes que pueden tener esta forma de presentación.
Caso clínico
Varón de 63 años diabético e hipertenso que consulta por ictericia y coluria de una semana de evolución. Asocia pérdida de peso de 10 Kg en el último mes. Analíticamente destacan bilirrubina total de 13.3 mg/dl (directa 11.2 mg/dl), GGT 2627 UI/ml y FA 625 UI/ml. Se solicita ecografía abdominal (Figura 1) identificando una lesión hipoecogénica mal delimitada en cabeza pancreática que condiciona dilatación de la vía biliar intra y extrahepática, en probable relación con colangiocarcinoma distal. Se realiza estudio de extensión mediante TC (Figura 2) donde se evidencia un probable implante a nivel hepático. Con el objetivo de confirmar afectación a distancia se solicitan PET-TC (Figuras 3-4) y RMN hepática (Figura 5) donde se visualiza una lesión en segmento VI hepático de probable naturaleza neoplásica. En Comité Multidisciplinar se decide realización de duodenopancreatectomía cefálica, linfadenectomía radical y metastasectomía hepática.
El estudio anatomopatológico de la pieza quirúrgica evidenció infiltración tumoral por progenitores hematopoyéticos en el contexto de sarcoma mieloide diferenciado, con expresión inmunohistoquímica de mieloperoxidasa y CD68. Posteriormente, un aspirado de médula ósea confirmó la presencia de manera sincrónica de una Leucemia Aguda Mielomonocítica M4 de la FAB. El paciente fue derivado a Hematología encontrándose en la actualidad en tratamiento de consolidación con Idarrubicina y Citarabina.
Figura 1
Ecografía abdominal. Masa hipoecogénica irregular en cabeza de páncreas de hasta 5.6 cm de diámetro antero-posterior, sugerente de Colangiocarcinoma distal.
Discusión
Se denomina sarcoma mieloide a la proliferación extramedular de blastos mieloides que ocurre en cualquier lugar diferente a la médula ósea, y que puede estar o no asociado a una neoplasia medular mieloide concomitante. Se trata de una entidad infrecuente, que afecta a menos del 1% de pacientes con Leucemia Mieloide Aguda, y que cuando aparece se localiza preferentemente a nivel óseo, cutáneo o linfático, resultando excepcional su presencia en la vía biliar. Cuando esto sucede, el diagnóstico diferencial con el colangiocarcinoma puede ser extremadamente complejo, siendo el estudio histológico e inmunohistoquímico fundamentales.
CP-178. ICTERICIA OBSTRUCTIVA COMO DEBUT DE UN SCHWANNOMA DE LA VÍA BILIAR.
Ortiz Chimbo DS1, Valdivia Krag C1, Castro Rodriguez J1, Leiva-Cepas F2, Ruiz Rodríguez AJ1, Guerrero Misas M1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba. 2UGC Anatomía Patológica. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: ictericia, schwannoma, obstrucción biliar.
Introducción
Los Schwannomas de la vía biliar son tumores neurogénicos benignos que se originan de la red de fibras nerviosas simpáticas y parasimpáticas existentes en la pared de la vía biliar. Son infrecuentes, incidentales, generalmente asintomáticos y en muy raras ocasiones son una causa de ictericia obstructiva. Por su excepcionalidad y relevancia clínica presentamos el siguiente caso clínico.
Caso clínico
Varón de 31 años, sin antecedentes de interés que acude por ictericia indolora de 72 horas de evolución y pérdida de 14 kilogramos de peso en 6 meses. Analíticamente, destacaba hiperbilirrubinemia mixta de 10.20 mg/dL a expensas de directa y elevación marcada de enzimas de colestasis y citolisis. En ecografía y tomografía abdominal (TC) se evidenció una marcada dilatación de la vía biliar intrahepática y extrahepática en relación con una masa hipodensa intraductal de unos 4,2 x 3.5 cm que se extendía desde la confluencia de los conductos hepáticos y ocupaba el conducto hepático común. Los marcadores tumorales fueron negativos. Se realizó angio-TC hepático y TC de tórax, sin objetivarse afectación vascular, ni a distancia, así como una colangiorresonancia (colangio-RM) que demostró la dilatación de la vía biliar por la masa hiliar conocida, situada a unos 9 milímetros de la confluencia de los conductos hepáticos (tipo I de la clasificación de Bismuth). Ante el cuadro de ictericia obstructiva y la localización de la lesión, se decidió drenaje por vía percutánea, realizándose una colangiopancreatografía transhepática (CTH) que objetivó una dilatación de la vía biliar secundaria a una estenosis significativa debido a una masa hiliar con caracteristicas de crecimiento intracanalicular y extracanalicular con posible origen en la pared biliar. Dada la sospecha de colangiocarcinoma como primera posibilidad diagnóstica, se intervino quirúrgicamente observándose una tumoración de aspecto cerebroide que englobaba la vía biliar principal y comprimía la arteria hepática, sin presentar signos de infiltración local. Se realizó resección de la vía biliar y linfadenectomía del pedículo hepático, con reconstrucción mediante hepaticoyeyunostomía terminolateral en Y de Roux. Durante la intervención, el margen distal fue informado como libre de infiltración tumoral, siendo el resultado anatomopatológico de schwannoma. Posteriormente la evolución postoperatoria fue favorable y al alta hospitaloria el paciente se encontraba asintomático.
Figura 1.
TC abdominal. Corte Coronal. Marcada dilatación de la vía biliar intrahepática en relación con una masa hipodensa intraductal de unos 4.2 x 3.5cm de diámetro que se extiende desde la confluencia de los conductos hepáticos derecho e izquierdo ocupando el conducto hepático común.
Figura 2.
AngioTC. Corte Coronal. Arteria hepática con origen del tronco celiaco, contacta con la masa, pero <180º, sin signos de infiltración. Porta troncular permeable de 17 mm contacta con la masa pero sin signos de infiltración.
Figura 3.
ColangioRM. Dilatación de la vía biliar intrahepática condicionada por masa hiliar conocida que afecta al conducto hepático común, situado a unos 9 mm de la confluencia de los conductos hepáticos (tipo I de la clasificación de Bismuth).
Discusión
Los schwannomas de la vía biliar son raros e infrecuentes, similares radiológicamente al colangiocarcinoma, por lo que este es su principal diagnóstico diferencial. Sin embargo, a diferencia de estos, la resección quirúrgica de los schwannomas biliares presenta un excelente pronóstico, siendo el riesgo de recidiva excepcional.
CP-179. ICTERICIA OBSTRUCTIVA SECUNDARIA A SÍNDROME DE LEMMEL: A PROPÓSITO DE UN CASO.
Ternero Fonseca J, Naranjo Pérez A, Calderón Chamizo M, Quirós Rivero P, Maraver Zamora M
Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Juan Ramón Jiménez, Huelva.
Palabras clave: divertículo duodenal, ictericia obstructiva. .
Introducción
El síndrome de Lemmel es una causa muy infrecuente de ictericia obstructiva secundaria a un divertículo duodenal (DD), frecuentemente yuxtapapilar, en ausencia de coledocolitiasis, tumores o cualquier otra causa.
Caso clínico
Mujer de 84 años que 4 semanas antes había ingresado por coledocolitiasis resuelta por CPRE y esfinterotomía, ingresa de nuevo por cuadro de dolor abdominal en hipocondrio derecho, astenia y anorexia de semanas de evolución asociado a náuseas y vómitos postprandiales. Afebril. Presenta colestasis y citólisis, elevación de reactantes de fase aguda y leucocitosis.
En TAC abdominal, marcada dilatación de la vía biliar intra y extrahepática, alcanzando el colédoco un diámetro máximo de 16mm e identificándose en su porción distal intrapancrática una imagen de densidad intermedia. Se solicita CPRE ante la sospecha de coledocolitiasis residual que se descarta. Se objetiva papila en el interior de divertículo ya conocido, en la porción más distal de su tabique medio. En la colangiografía la vía biliar está dilatada 18mms, con aerobilia y estenosis en pico de loro retropapilar secundaria a compresión diverticular. Se somete a esfinteroplastia con cepillado biliar que descarta malignidad, y se deja alojada prótesis plástica (7Frx7cm) que se retira semanas después quedando la paciente asintomática.
Discusión
Los DD tienen una incidencia aproximada del 5-27% (Kang HS et al. JKoreanMedSci.2014,29:874-878) aumentando su prevalencia con la edad. La mayoría son extraluminales y adquiridos. Cuando son sintomáticos normalmente es por disfunción del esfínter de Oddi secundaria, por fibrosis papilar asociada a diverticulitis de repetición, o por compresión del divertículo dificultando el drenaje biliar (Ono M, et al. JOP.2005,6:277-278). Sin embargo, sólo el 5% son sintomáticos, siendo normalmente un hallazgo incidental. El riesgo de complicaciones graves como la colangitis, la ictericia obstructiva y la pancreatitis, es muy bajo (1%). Su transformación maligna es excepcional. Otras técnicas como la TAC, la ultrasonografía endoscópica o la colangioresonancia magnética, pueden ser de utilidad. Cuando se utilizan estas técnicas, debido a su frecuente contenido líquido, el diagnóstico diferencial deberá hacerse con colecciones necróticas, neoplasias quísticas de cabeza del páncreas o pseudoquistes, entre otros.
La CPRE es el método de referencia para el diagnóstico y el tratamiento, permitiendo excluir otras causas como coledocolitiasis o neoplasias. La esfinterotomía endoscópica es el tratamiento de elección en los casos sintomáticos (Tobin R et al. JSurgCaseRep.2018,10:263), reservándose la cirugía para el fracaso endoscópico o para pacientes jóvenes con clínica recidivante y sin comorbilidades. En los casos asintomáticos se recomienda actitud conservadora.
CP-180. ÍLEO BILIAR COLÓNICO COMO PRESENTACIÓN CLÍNICA INFRECUENTE DE LA FÍSTULA COLECISTOCOLÓNICA.
Sánchez Arenas R, Vías Parrado C, Aparcero López R, Caunedo Álvarez A
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen Macarena, Sevilla.
Palabras clave: fístula colecistocolónica, ileo biliar colónico, colonoscopia. .
Introducción
La fístula colecistocolónica (FCC) constituye, generalmente, una complicación tardía de la litiasis biliar crónica. Es la segunda fístula colecistoentérica más común después de la fístula colecistoduodenal, documentándose en aproximadamente el 0,1% de las colecistectomías.
La mayoría de los pacientes están asintomáticos, diagnosticándose en el acto quirúrgico indicado por una complicación biliar. Los síntomas más frecuentes son diarrea, dolor abdominal, ictericia, fiebre y pérdida de peso. Puede presentarse en el contexto de un síndrome de Mirrizi tipo V cuando asocia obstrucción del conducto hepático común por compresión extrínseca de la litiasis en la vesícula. La presentación clínica como obstrucción colónica por el paso de una litiasis de gran tamaño a través de la fístula es extremadamente rara.
Caso clínico
Mujer de 77 años con carcinoma ductal infiltrante de mama estadio IV en tratamiento paliativo con inmunoterapia y en situación basal de dependencia para todas las actividades básicas.
Acude a urgencias por cuadro de dolor, distensión abdominal y estreñimiento de diez días de evolución. Se realiza tomografía computerizada (TC) de abdomen observándose litiasis de 43x31 mm en colon sigmoides que condiciona dilatación retrógrada del marco cólico (Figuras 1-3) y aerobilia en relación con fístula colecistocolónica (Figura 4).
Figura 1
TC abdomen y pelvis corte transversal: cálculo de 3.4 x 3,8 mm en sigma con cambios inflamatorios en su pared.
Figura 2
TC abdomen y pelvis corte coronal: distensión retrógrada del marco cólico con asas de intestino delgado colapsadas.
Figura 4
TC abdomen y pelvis corte transversal: aerobilia por fístula colecistocolónica en la flexura hepática del colon.
Dadas las características de la paciente y la falta de mejoría clínica con tratamiento conservador, se realiza colonoscopia con la intención de resolver el cuadro obstructivo y evitar el acto quirúrgico. Durante el procedimiento, se visualiza cálculo de gran tamaño en sigma distal que ocupa la totalidad de la luz colónica (Figuras 5-6). A pesar de abordarla con diferentes asas de polipectomía y cesta de Roth, resulta imposible su extracción por adherencia a la pared colónica y falta de agarre del material a la superficie lisa del cálculo. Finalmente, la paciente es sometida a intervención quirúrgica realizándose sigmoidectomía y colostomía terminal por vía laparoscópica con buena evolución clínica posterior.
Discusión
Aunque existen algunos casos publicados de resolución de íleo biliar colónico mediante colonoscopia, el tamaño del cálculo y la formación de adherencias, por el tiempo de evolución, pueden suponer una limitación técnica requiriéndose, en la mayoría de los casos, de tratamiento quirúrgico.
En nuestro caso, la paciente precisó de intervención quirúrgica, no procediéndose a la colecistectomía y reparación de la fístula dada su situación basal y la ausencia de síntomas biliares y de datos bioquímicos de colestasis.
CP-181. LO QUE LA PIEL NOS CUENTA: ICTERICIA Y LETÁLIDES SECUNDARIAS A TUMOR VESICAL
Pérez Campos E, Navarro Moreno E, Lázaro Sáez M
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: ictericia, letalides, tumor uroterial.
Introducción
La ictericia como debut de tumores vesicales resultan un hallazgo altamente infrecuente, con muy pocos casos descritos. Presentamos un paciente que debuta con clínica digestiva y cutánea secundaria a la progresión tumoral a distancia antes de manifestar sintomatología urinaria, aportando imágenes inusuales y de gran interés docente.
Caso clínico
Paciente de 71 años exfumador desde la juventud. Comienza a presentar ictericia indolora progresiva, además de lesiones dérmicas coincidentes en el tiempo, inicialmente aisladas en hombro izquierdo y extendiéndose posteriormente en contigüidad.
En la analítica presenta hiperbilirrubinemia a expensas de directa (6,14 mg/dl), además de deterioro de su función renal y leve elevación de reactantes inflamatorios. Tras ingresar para estudio de ictericia obstructiva, sospechando origen tumoral y síndrome paraneoplásico (por el aspecto de las lesiones dérmicas, que se biopsian), comienza con hematuria franca con coágulos, precisando nefrostomía bilateral.
Se realiza TC que describe engrosamiento irregular de pared vesical, además de carcinomatosis peritoneal y adenopatías axilares, en tronco celiaco y alrededor de la cabeza pancreática, que dilatan la vía biliar (descartando con colangio-RMN la presencia de tumor sincrónico hepatobiliar). Poco después, el paciente se deteriora de forma brusca, entrando en fallo multiorgánico y falleciendo aún en espera de los resultados de las biopsias, que finalmente confirman su la naturaleza metastásica y el origen uroterial del tumor primario.
Discusión
Los órganos diana más comunes de la enfermedad metastásica de origen uroterial son el hueso, los pulmones, el hígado, el peritoneo, la pleura y el tejido celular subcutáneo. También existen algunos casos descritos de infiltración intestinal. Las letálides procedentes de tumores vesicales son altamente infrecuentes, representando alrededor del 0.84% de las metástasis cutáneas. Su diseminación linfática comienza por el alcance de los ganglios obturadores y las cadenas iliacas externas, drenando a través de las cadenas para-aórticas en el conducto torácico y pasando así a la circulación sistémica; la siembra se vierte entonces hacia vena cava, alcanzando la circulación periverterbal e intercostal, territorio afecto en este caso.
Estas lesiones pueden simular otras dermatopatías, siendo clave la filiación histológica e inmunohistoquímica. Como curiosidad, cabe destacar que nuestro paciente debuta con sintomatología secundaria a la progresión tumoral a distancia (compresión duodenal extrínseca por adenopatías, ictericia y lesiones dérmicas) antes de manifestar semiología urinaria. También por ello, el informe final anatomopatológico resultó un dato especialmente esclarecedor, reafirmando la ausencia de sincronicidad de tumor digestivo, de cara a poder plantear tratamiento quimioterápico dirigido.
CP-182. MELANOMA COROIDEO COMO CAUSA INFRECUENTE DE METÁSTASIS EN CABEZA DE PÁNCREAS
CASTRO RODRÍGUEZ J1, OSUNA SOTO J2, RODRÍGUEZ TIRADO MI1, ALEJANDRE ALTAMIRANO RM1, EL FALLOUS EL MRAGHID M1, PERDICES LÓPEZ EV1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Reina Sofía, Córdoba. 2Servicio Anatomía Patológica. Complejo Hospitalario Regional Reina Sofía, Córdoba.
Palabras clave: melanoma, coroides, metástasis pancreática.
Introducción
Las metástasis suponen solo el 2-5% de los tumores malignos de páncreas, pudiendo simular una neoplasia primaria. Se estima que < 1% de melanomas metastatizan en páncreas.
Caso clínico
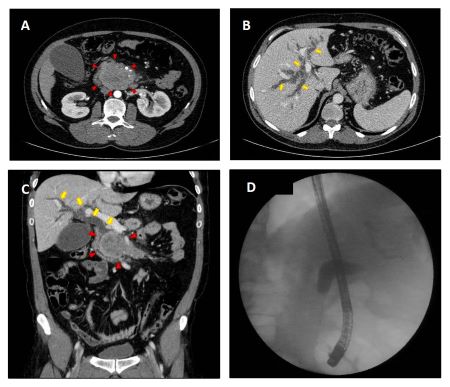
Varón de 45 años con ceguera en ojo derecho por glaucoma neovascular que ingresa en julio de 2020 por ictericia, coluria y epigastralgia con elevación del perfil hepatobiliar en analítica (bilirrubina 10 con directa 8, FA 920, GGT 1295, AST 718, ALT 1063). En pruebas de imagen se identifica una lesión sólida en cabeza pancreática de 7,5cm con dilatación de vías biliares y Wirsung (Figura 1), infiltración vascular, presencia de adenopatías locorregionales y metástasis hepáticas.
Figura 1
TC abdominal con contraste (A, B, C): lesión en cabeza de páncreas (puntas rojas) que ocasiona dilatación de la vía biliar intra y extrahepática (flechas amarillas). CPRE (D) donde se visualiza un stop brusco del contraste en la fluoroscopia por la presencia del tumor.
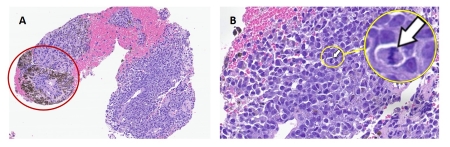
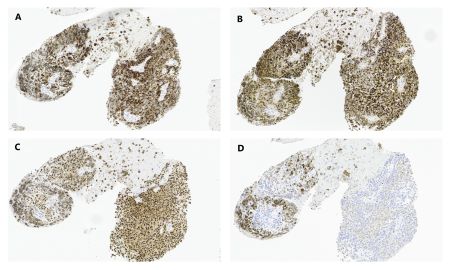
Mediante CPRE y colocación de prótesis plástica se realiza drenaje biliar, y por ecoendoscopia se toman biopsias, con histología de tumor maligno indiferenciado sugestivo de melanoma por la inmunohistoquímica: HMB45, MelanA, S100 y MITF positivos, y citoqueratina AE1/3 negativa (Figuras 2 y 3). Se contacta con dermatología, que descarta origen mucocutáneo, y Oftalmología, que determina un fondo de ojo izquierdo normal, siendo el derecho invalorable. Se completa estudio con RM observando una lesión en globo ocular derecho sugestiva de melanoma coroideo extendido a tejidos blandos y nervio óptico (Figura 4).
Figura 2
PAAF de páncreas. Pieza histológica con tinción de Hematoxilina-Eosina a 15x (A) y 40x (B). Células malignas con citoplasma basófilo granular y núcleos pleomórficos. Se aprecian mitosis atípicas (flecha blanca) y pigmento melánico (círculo rojo).
Figura 3
Técnicas de tinción por inmunohistoquímica (15x). (A): Melan A positivo. (B): HMB-45 positivo. (C): MITF positivo. (D): CK AE1/AE3 negativo en las células tumorales. Todo ello sugestivo de melanoma.
Figura 4
RM craneal en T1, corte axial (A, B): lesión en región coroidea con extensión a órbita y nervio óptico derechos, hiperintensa en T1 y con captación de contraste (puntas verdes). RM craneal en T2, corte axial (C) y coronal (D): la lesión coroidea hacía imposible la valoración de dicho fondo de ojo.
El paciente inicia tratamiento oncológico con inmunoterapia en septiembre de 2020 con nivolumab, precisando hasta tres CPREs por obstrucción biliar secundaria a crecimiento neoplásico endoprotésico (Fig.5), insertándose finalmente una prótesis metálica recubierta. Se realiza radioterapia paliativa sobre la metástasis pancreática debido a la progresión tumoral y se asocia ipilimumab, a pesar de lo cual el paciente fallece finalmente en mayo de 2021.
Discusión
La incidencia anual del melanoma es <10-25/100000 en Europa, siendo el origen cutáneo el más frecuente. El melanoma uveal es infrecuente, pues solo representa el 3-5% de los melanomas, constituyendo no obstante la neoplasia primaria intraocular más común; el 85-90% de ellos asientan en la coroides. El desarrollo de metástasis en este tipo de tumores se asocia a mal pronóstico, con una mediana de supervivencia de 8 a 18 meses. En el melanoma en estadio avanzado la inmunoterapia se ha establecido como uno de los tratamientos sistémicos de elección, siendo preferibles los inhibidores de PD-1 (nivolumab y pembrolizumab), solos o en combinación con los anticuerpos anti CTLA-4 (ipilimumab), con aceptables tasas de respuesta e incremento de la supervivencia.
El diagnóstico etiológico de las metástasis pancreáticas pueden suponer un auténtico reto diagnóstico, siendo para ello fundamental la histología y el estudio inmunohistoquímico que permitieron en nuestro caso identificar el melanoma coroideo.
CP-183. METASTASIS INTRABILIAR: UNA CAUSA INFRECUENTE DE ICTERICIA OBSTRUCTIVA.
OROZCO BERNARDEZ-ZERPA N1, OLVERA MUÑOZ R2, MOLINO RUIZ L1, OTERO LOPEZ-CUBERO S1
1Servicio Aparato Digestivo. Hospital de Especialidades de Puerto Real, Puerto Real. 2Servicio Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: cancer colorrectal, metástasis, intrabiliar.
Introducción
La ictericia obstructiva es una entidad común en nuestra práctica clínica, implicando en ocasiones un diagnóstico diferencial complejo especialmente en el caso de pacientes oncológicos.
Caso clínico
Presentamos el caso de un paciente de 76 años que se diagnostica en 2012 de adenocarcinoma de colon izquierdo, sin aparente afectación ganglionar ni metastásica, que se interviene mediante hemicolectomía izquierda y no recibe coadyudancia. Durante el seguimiento por parte de oncología se detectan metástasis hepáticas con buena respuesta a tratamiento neoadyudante y hepatectomía parcial, en la cual también se realiza colecistectomía profiláctica.
En 2020 acude a urgencias por cuadro clínico y analítico compatible con colangitis aguda. Al ingreso se realizan de modo urgente ecografía y TC donde no se observan dilataciónón de la vía biliar ni otros hallazgos patológicos relevantes. Durante su ingreso se programa colangioRM en donde nuevamente se visualiza vía biliar normal pero se identifica un defecto de repleción inespecífico en la desembocadura del muñón cístico a nivel del conducto hepático (Figura 1). Se realiza CPRE en cuya colangiografía el defecto de repleción adquiere aspecto polipoide (Figura 2); se toma citología de la vía biliar a este nivel y se asegura el drenaje biliar mediante colocación de prótesis biliar plástica. El estudio anatomo-patológico fue compatible con metástasis intrabiliar del adenocarcinoma de colon. Posteriormente el paciente evoluciona favorablemente, si bien meses más tarde se produce el éxitus del paciente meses en relación con progresión de su enfermedad.
Discusión
La vía biliar es una localización infrecuente en la metástasis del cáncer de colon. Al presentarse puede producir ictericia obstructiva y colangitis. Establecer su diagnóstico puede ser difícil debido a que los signos radiológicos son poco específicos y puede confundirse con otras entidades como el colangiocarcinoma. El antecedente oncológico de cáncer de colon y finalmente el estudio anatomo-patológico mediante la toma de muestras por CPRE o colangioscopia permite su confirmación tras realizar técnicas inmunohistoquimicas que muestran positividad para CK-20 y negatividad para citoqueratina CK-7.
CP-184. METÁSTASIS PANCREÁTICAS DE TUMOR NEUROENDOCRINO DE ORIGEN PULMONAR
Fernández Carrasco M, Sánchez García O
Servicio Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: tumor neuroendocrino, carcinoma microcítico, metástasis pancreáticas.
Introducción
Las metástasis pancreáticas son excepcionales con difícil diagnóstico diferencial de tumores primarios.
Los tumores neuroendocrinos (TNE) son un grupo heterogéneo de neoplasias originadas en las células secretoras del sistema neuroendocrino difuso. Existen distintos tipos de TNE, entre ellos vamos a hablar de los que afectan al tracto gastrointestinal y páncreas y los de origen pulmonar. Si bien es cierto no todos los TNE de páncreas son primarios.
Presentamos el caso de una ictericia indolora secundaria a metástasis pancreáticas de origen neuroendocrino con naturaleza primaria pulmonar.
Caso clínico
Mujer de 61 años fumadora de un paquete diario, con antecedentes de broncopatía. Ingresa por ictericia indolora. En analítica muestra hiperbilirrubinemia 30 mg/dl a expensas de directa, y niveles de CEA 7,24 ng/ml y CA 19.9 67,5 U/ml.
Se realiza TAC de abdomen que objetiva dilatación de vía biliar con lesión tumoral en cabeza pancreática. Se completa el estudio de extensión con TAC torácico que objetiva masa sólida hiliar derecha compatible con carcinoma pulmonar, extendida a región mediastínica, con adenopatías regionales.
Se toman biopsias de la tumoración pulmonar y de la lesión pancreática por con hallazgos histológicos e inmunohistoquímicos concordantes con carcinoma neuroendocrino de célula pequeña, en probable relación con metástasis de pancreática de probable naturaleza primaria pulmonar.
Se realizó PET-TC que objetiva una gran masa neoplásica hiliar pulmonar derecha, con afectación ganglionar mediastínica y subcarinal, lesiones hipercaptantes en páncreas, suprarrenal y renal izquierda.
Se realiza drenaje de vía biliar colocando stent metálico por CPRE y finalmente es valorada por oncología para tratamiento quimioterápico.
Discusión
Los TNE gastroenteropancreáticos suponen el 2% de tumores malignos del tracto gastrointestinal, desde el punto de vista biológico una parte deriva de las células de Langerhans de los islotes pancreáticos, y otros que derivan de las células enterocromafines (TNE del tracto gastrointestinal o tumores carcinoides).
Los TNE de pulmón comprenden un 20% dentro de los tumores pulmonares, abarcando un subgrupo heterogéneo con diversos comportamientos. El carcinoma neuroendocrino de células pequeñas o carcinoma pulmonar microcítico, es el subtipo más frecuente, ocupando un 15%, de naturaleza altamente agresiva.
Están descritos los carcinomas de células pequeñas extrapulmonares pero son extremadamente inusuales,presentándose ocasionalmente como enfermedad metastásica sin llegar a identificar un lugar primario.
En este caso, se llega al diagnóstico de probable naturaleza primaria pulmonar con metástasis a distintos niveles, dando la cara como ictericia por compresión extrínseca de las metástasis pancreáticas.
CP-185. PÁNCREAS EN EL SACO HERNIARIO, UN HALLAZGO INFRECUENTE EN LA HERNIA DE HIATO.
Díaz Alcázar MDM
UGC Aparato Digestivo. Hospital San Cecilio, Granada.
Palabras clave: hernia hiatal, saco herniario, páncreas.
Introducción
La hernia hiatal es un trastorno común que se caracteriza por el desplazamiento de estructuras de la cavidad abdominal al tórax a través de un orificio en el diafragma.
Caso clínico
Mujer de 73 años con antecedente de obesidad que consulta por intolerancia oral progresiva de 2 semanas de evolución. Se realiza endoscopia digestiva alta con hallazgo de hernia de hiato de 10 cm. Se completa estudio con tomografía computarizada abdominal que confirma hernia de hiato por deslizamiento con herniación de casi la totalidad de la cámara gástrica, parte del cuerpo pancreático y ramas del tronco celíaco. En la exploración de esófago, estómago y duodeno con doble contraste hay datos de volvulación gástrica parcial y retraso del vaciamiento esofágico y gástrico. Dados los hallazgos se decide tratamiento quirúrgico, realizándose extracción de saco herniario y funduplicatura Floppy-Nissen laparoscópica, con buena evolución clínica posteriormente.
Discusión
La hernia hiatal está presente en hasta el 20% de los pacientes que se realizan una endoscopia digestiva alta. Se divide en cuatro categorías según la extensión de la herniación y la localización de la unión gastroesofágica: hernia por deslizamiento (tipo I, más del 95% de los casos), hernia paraesofágica (tipo II), hernia mixta (tipo III) y herniación de elementos adicionales (tipo IV).
El prolapso del estómago, el colon transverso, el intestino delgado y el bazo es relativamente frecuente. Sin embargo, la herniación del páncreas es extremadamente rara porque la cabeza del páncreas está ubicada en el retroperitoneo y está fijada por el ligamento de Treitz.
Cuando ocurre, la herniación del páncreas es habitualmente asintomática y se diagnostica incidentalmente en pruebas de imagen, aunque se ha descrito raramente pancreatitis aguda y alteración de la función hepática por traumatismo de las ramas vasculares y los conductos biliopancreáticos.
El tratamiento es quirúrgico en los casos sintomáticos, aunque también se puede plantear en pacientes asintomáticos para prevenir potenciales complicaciones.
CP-186. PANCREATITIS AGUDA SECUNDARIA A PUNCIÓN-ASPIRACIÓN CON AGUJA FINA GUIADA POR ECOENDOSCOPIA. UNA COMPLICACIÓN A TENER EN CUENTA.
Lancho Muñoz A, Fernández García R, Tendero Peinado C, Redondo Cerezo E, Rodríguez Sicilia MJ
Servicio Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: pancreatitis, use-paaf, complicaciones..
Introducción
La punción- aspiración con aguja fina guiada por ecoendoscopia (USE-PAAF) presenta un elevado rendimiento diagnóstico tanto de lesiones intraluminales como extraluminales próximas al tracto digestivo. Por ello, se está convirtiendo en una prueba diagnóstica rutinaria en los servicios de aparato digestivo y con ello sus complicaciones.
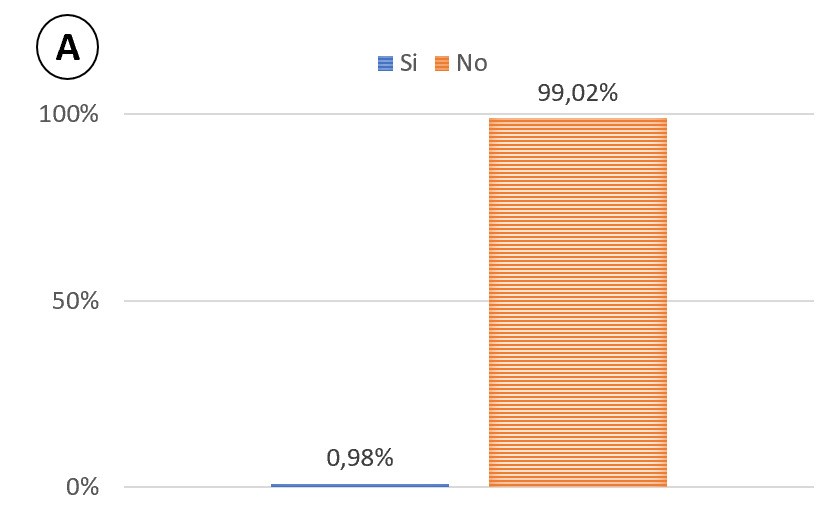
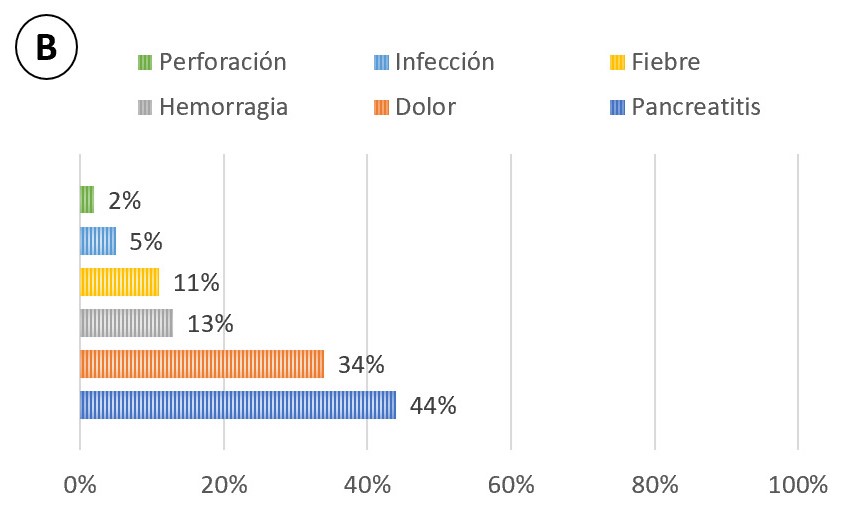
La tasa de complicaciones tras USE-PAAF es baja, en torno al 2,5%, y entre ellas la más frecuente es la pancreatitis aguda (Gráficos A y B). Algunos factores de riesgos de pancreatitis por USE- PAAF propuestos son: 1) lesiones pancreáticas quísticas; 2) lesiones <2cm; 3) lesiones en cabeza pancreática o proceso uncinado, ya que, se atraviesa mayor cantidad de parénquima pancreático hasta llegar al sitio de punción; 4) lesiones benignas respecto a lesiones malignas con cambios escleróticos que atenúan la respuesta inflamatoria local y 5) antecedentes de pancreatitis aguda.
Caso clínico
Hombre de 46 años afectado por mutación MEN tipo 1 manifestada mediante hiperparatiroidismo primario, en seguimiento por endocrinología. Se detecta en controles analíticos hipergastrinemia en ascenso asintomática, con octreoscan negativo. Se solicita EDA donde se detecta en biopsias endoscópicas de cuerpo y antro datos histológicos de gastritis crónica y metaplasia intestinal. Ante hipergastrinemia persistente y valores elevados de cromogranina A se decide realizar USE para descartar tumor neuroendocrino. Se identifica una lesión isoecoica e irregular de 5mm en cabeza de páncreas y se realiza PAAF cuyos resultados corresponden con células acinares pancreáticas sin atipias.
Trascurrido cuatro días, el paciente acude a urgencias por dolor abdominal intenso en flanco y fosa iliaca izquierda y febrícula de hasta 37,8ºC sin cortejo bacteriémico. Analíticamente, amilasa de 67 mg/dl y lipasa de 58 mg/dl junto con PCR de 111,2 mg/dl. Se realiza TC de abdomen que mostró alteraciones compatibles con pancreatitis aguda edematosa leve (Figura 1). Finalmente, se diagnosticó al paciente de pancreatitis leve tras USE-PAAF. El paciente evolucionó favorablemente, siendo dado de alta pocos días tras el ingreso.
Gráfico B
Complicaciones asociadas a la USE-PAAF y su proporción aproximada. Un paciente puede presentar más de una complicación.
Figura 1
Corte transversal de TC de abdomen y pelvis con contraste IV. Se observa un engrosamiento leve de la glándula pancreática junto con infiltrados peripancreáticos y realce completo de la glándula con el contraste. Estos hallazgos son compatibles con pancreatitis aguda edematosa intersticial leve.
Discusión
Este caso sirve para mostrar la existencia, aunque infrecuente, de pancreatitis aguda secundarias a USE-PAAF. Mayoritariamente se trata de cuadros leves que debutan de forma insidiosa pudiendo ser fácilmente infradiagnosticados si no tenemos en cuenta esta relación causal.
En conclusión, la USE-PAAF constituye una prueba fundamental para el diagnóstico histológico de diversas lesiones y altamente segura. No obstante, las complicaciones graves son posibles y por ello, los gastroenterólogos debemos conocerlas y saber manejarlas, especialmente, ante la previsión de un incremento del número de pacientes que se someterán a esta intervención en un futuro cercano.
CP-187. PANCREATITIS DEL SURCO SIMULANDO ADENOCARCINOMA DE DUODENO
Griio Bensusan I
Unidad Aparato Digestivo. Hospital de Alta Resolución de Écija, Écija.
Palabras clave: pancreatitis del surco, groove pancreatitis, pancreatitis crónica.
Introducción
La pancreatitis del surco es una forma poco frecuente de pancreatitis crónica. Al afectar a la pared duodenal puede provocar engrosamiento de la misma y dar lugar a imágenes sugestivas de tumores de dicha región.
Caso clínico
Una mujer de 50 años, acude a consulta por dolor a nivel de epigastrio, irradiado a hipocondrio izquierdo y a la espalda, a lo largo de todo el día. Dicho dolor se ha acentuado en las últimas 2 semanas, con pérdida de apetito, unos 5 kg de peso y síntomas nocturnos. El dolor comenzó 2 años antes. Se acompaña además de síntomas de distrés postprandial, toma frecuente de AINEs y una historia de más de 20 años de tabaquismo de 20 cigarrillos al día. Se realizó una endoscopia oral en la que se describía un engrosamiento mural de la segunda porción duodenal de aspecto infiltrativo o inflamatorio y se tomaron biopsias (Figura 1). Se solicitó una TAC abdominal con contraste en la que describe un engrosamiento y realce de la segunda porción duondenal y región proximal de la tercera, borrosidad de sus contornos y aumento de la densidad grasa y lesiones redondeadasmilimétricas y en el proceso uncinado una lesión de 13 mm sugiriendo un proceso neoformativo duodeno-pancreático (Figura 2). Las biopsias del duodeno son descritas como mucosa duodenal con erosión superficial. Dada la sospecha se completa el estudio con una RM abdomnal que inicialmente describe hallazgos superponibles al TAC, pero una segunda RM con estudio dinámico del páncreas describe un menor engrosamiento de la región del surco y una desaparición de la lesión de la región pancreática. Con el diagnóstico de pancreatitis del surco, la paciente redujo el consumo de tabaco y tras un año de seguimiento ha ganado algo de peso y ha reducido la necesidad de analgesia.
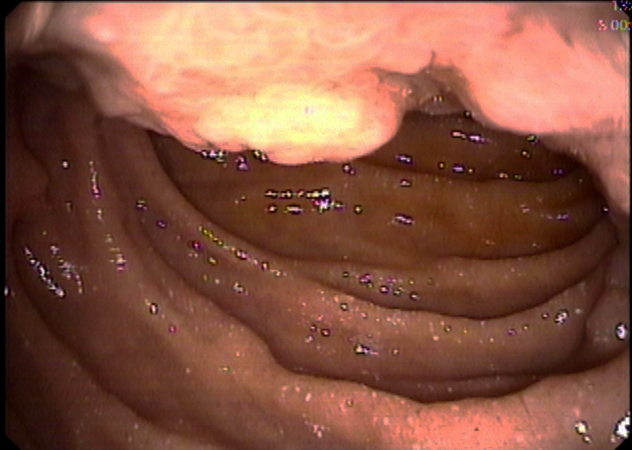
Figura 1
Imagen la segunda porción duodenal en la que se aprecia un engrosamiento irregular de la pared. Datos extraídos de: Mizuide M, Ryozawa S, Fujita A, Ogawa T, Katsuda H, Suzuki M, et al. Complications of endoscopic ultrasound-guided fine needle aspiration: A narrative review. Diagnostics (Basel) [Internet]. 2020;10(11):964. Disponible en: http://dx.doi.org/10.3390/diagnostics10110964
Figura 2
TAC abdominal con contraste en la que se observa el engrosamiento de la pared duodenal, junto con un nódulo de unos 13 mm , hipodenso, con un halo de realce en su periferia.Datos extraídos de: Mizuide M, Ryozawa S, Fujita A, Ogawa T, Katsuda H, Suzuki M, et al. Complications of endoscopic ultrasound-guided fine needle aspiration: A narrative review. Diagnostics (Basel) [Internet]. 2020;10(11):964. Disponible en: http://dx.doi.org/10.3390/diagnostics10110964
Discusión
La pancreatitis del surco exige el diagnóstico diferencial con el carcinoma de cabeza de páncreas fundamentalmente. Sin embargo, también hay que incluir entre los procesos a descartar el carcinoma duodenal. En este caso, la primera exploración realizada fue la endoscopia oral y en ella se observó un engrosamiento de la pared duodenal que hizo sospechar dicho proceso, descartado por las biopsias. La TC abdominal y la RM abdominal con contraste pueden ser útiles para el diagnóstico pero en otras ocasiones el diagnóstico es histológico tras cirugía. El tratamiento habitualmente es conservador mediante tratamiento sintomático, ocasionalmente endoscópico y rara vez quirúrgico.
CP-188. PANICULITIS PANCREÁTICA: UNA MANIFESTACIÓN POCO HABITUAL DE LA ENFERMEDAD PANCREÁTICA
Calvo Bernal MDM, Hallouch Toutouh S, Pérez Campos E
UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: pancreatitis aguda, paniculitis, manifestaciones dermatológicas.
Introducción
La paniculitis pancreática (PP) es una manifestación cutánea poco frecuente de enfermedad pancreática. Su evolución es paralela al proceso desencadenante, pudiendo en ocasiones preceder a la clínica propia del mismo.
Caso clínico
Mujer de 74 años con antecedentes de hipertensión arterial, diabetes y leucemia linfática crónica en tratamiento con ibrutinib, que ingresa en planta de hospitalización bajo el diagnóstico de pancreatitis aguda (PA) tras presentar clínica de epigastralgia asociada a vómitos de 4 días de evolución y una analítica con hiperamilasemia de de 3040 U/L.
Al tercer día de ingreso, presenta mal control del dolor y dificultad respiratoria con derrame pleural bilateral. En analítica, deterioro de la función renal y elevación de reactantes de fase aguda (PCR 46 mg/dl) requiriendo traslado a UCI. Se realiza una primera TC abdominal con datos de PA y necrosis <30% y una segunda TC con necrosis peripancreática y una colección de 12 cm (Figura 1).
Figura 1.
TC abdominal. Se aprecia un aumento de densidad de la grasa peripancreática con realce periférico, en relación con colección con tejido necrótico, de hasta 12 cm de eje mayor.
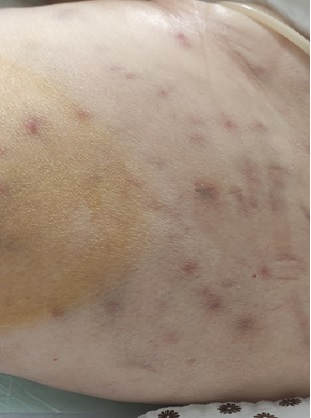
Durante el ingreso, presenta lesiones nodulares violáceas en ambos miembros inferiores, dolorosas a la palpación (Figura 2), valoradas por Dermatología que realiza biopsia subcutánea (Figura 3).
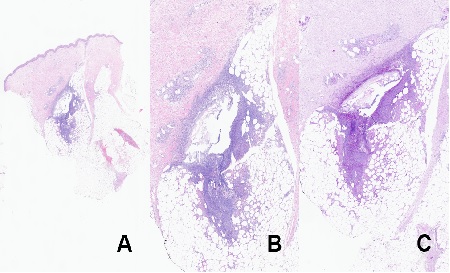
Figura 3.
Anatomía patológica. Tinción con hematoxilina-eosina. Se aprecia área de necrosis tisular con abcesificación de predominio lobulillar en unión de dermis profunda con panículo adiposo, con destrucción de adipocitos y predominio de neutrófilos.
La evolución de la paciente es tórpida, con empeoramiento progresivo presentando fallo multiorgánico lo que conlleva finalmente a su fallecimiento.
Discusión
La PP es una complicación rara de los procesos pancreáticos, su prevalencia es del 3% (1) y suele aparecer entre la cuarta y la sexta década de la vida, con mayor prevalencia varones (5:1).
Se manifiesta con nódulos eritematosos o violáceos, dolorosos a la palpación, que pueden sufrir ulceración espontánea y emitir un material oleoso. Suelen afectar a las extremidades inferiores, aunque también pueden extenderse a glúteos, tronco, brazos y cuero cabelludo. Puede estar asociada a manifestaciones sistémicas como fiebre, dolor abdominal, poliartrosis y con menos frecuencia, ascitis o derrame pleural.
El diagnóstico se confirma mediante una biopsia subcutánea. El cuadro histopatológico consiste en una paniculitis lobulillar, con presencia de las típicas células fantasma que corresponden a adipocitos necróticos.
El tratamiento de la PP se dirige a la enfermedad pancreática subyacente. Los signos subcutáneos suelen remitir entre 15 y 30 días después de su aparición. El pronóstico es malo en los casos asociados a carcinoma de páncreas.
En hasta un 50% de los casos, las manifestaciones cutáneas pueden preceder a los síntomas abdominales de la enfermedad pancreática por lo que la aparición esta entidad nos obliga a descartar una enfermedad pancreática, incluso en aquellos pacientes asintomáticos.
CP-189. QUISTE DE CÓLEDOCO TIPO 1
Grilo Bensusan I
Unidad Aparato Digestivo. Hospital de Alta Resolución de Écija, Écija.
Palabras clave: quiste de colédoco, patología congénita biliar.
Introducción
Los quistes biliares o malformaciones del colédoco son alteraciones poco frecuentes y que generalmente se detectan en la infancia. Presentamos el caso de un quiste biliar tipo I en la edad adulta.
Caso clínico
Una mujer de 24 años acude a la consulta con síntomas compatibles con una dispepsia funcional tipo mixto. Un año antes se había realizado una endoscopia oral sin alteraciones, con infección por H. pylori tratada y confirmada la erradicación. Se solicita una ecografía abdominal en la que se observa la presencia de colelitiasis y una aparente dilatación del colédoco sin observar causa obstructiva, ni dilatación de la vía biliar intrahepática. Para completar el estudio se solicita una ColangioRM ( figura 1 y 2) en la que se describe la presencia de un colédoco dilatado en forma fusiforme hasta los 14 mm sin otras alteraciones. Dado los hallazgos de deriva a la paciente a cirugía hepatobiliar donde se interviene mediante una colecistectomía y una hepatico yeyunostomía. La pieza quirúgica fue examinada por Anatomía Patológica sin observar lesiones malignas.
Discusión
Los quistes de colédocos son raros y más aún que se diagnostiquen en la edad adulta. Suelen debutar en la infancia por dolor abdominal, ictericia y la presencia de una masa abdominal. En los adultos, puede ser asintomático y ser un hallazgo de una prueba de imagen. Generalmente el diagnóstico se basa en la sospecha realizada mediante una ecografía abdominal y confirmada mediante una RM abdominal con conangioRM. En ocasiones puede ser necesaria una CPRE o una ecoendoscopia. Los quistes de colédoco tipo I se caracterizan por no afectar a las vías intrahepáticas y por constituir dilataciones fusiformes del colédoco. Uno de los aspectos fundamentales de este tipo de quiste, es que aumentan el riesgo de colangiocarcinoma y este riesgo aumenta con la edad. Por ello se recomienda el tratamiento quirúrgico de la lesión.
CP-190. RECIDIVA DE TUMOR NEUROENDOCRINO DE VÍA BILIAR Y PÁNCREAS
Pérez Ramírez A1, Ruz Zafra P1, Mohigefer Barrera J2, Herrera Justiniano JM1
1UGC Aparato Digestivo. Complejo Hospitalario Regional Virgen del Rocío, Sevilla. 2UGC Anatomía Patológica. Complejo Hospitalario Regional Virgen del Rocío, Sevilla.
Palabras clave: tumor neuroendocrino, páncreas, vía biliar.
Introducción
Los tumores neuroendocrinos (TNE) son un grupo heterogéneo de neoplasias que afectan, entre otros, al tracto gastrointestinal y biliopancreático. Se originan a partir de las células enterocromafines, encargadas de la producción de diferentes hormonas y aminas. Pueden dar síntomas en función de su tamaño y localización (dolor, obstrucción, ictericia), así como derivados de la producción hormonal excesiva.
Caso clínico
Mujer de 74 años, con colitis ulcerosa diagnosticada en 1970 en tratamiento con mesalazina oral. Intervenida en 1994 de tumor carcinoide del conducto colédoco mediante resección y hepaticoyeyunostomía.
En analítica de control presentaba patrón colestásico, por lo que solicitamos ecografía de abdomen evidenciando dilatación de vía biliar. La resonancia magnética (RM) abdominal corroboró dilatación a nivel intrahepático y conducto hepático común debido a masa intraluminal, sospechosa de recidiva tumoral.
Una tomografía computerizada (TC) toracoabdominal confirmó los hallazgos y objetivó lesión neoplásica en cabeza pancreática, sin lesiones metastásicas.
Se realizó ecoendoscopia (USE) y toma de biopsias con hallazgos sugestivos de recidiva tumoral en cabeza pancreática. El ácido 5-hidroxiindolacetico (5-HIAA) en orina y la cromogranina A sérica se encontraban elevados. La histología confirmó el diagnóstico de TNE grado 1.
Descartada resecabilidad en comité de tumores, se solicitó gammagrafía con análogos de somatostatina (ASS), que mostró un foco hipercaptante coincidente con la masa pancreática descrita y tres focos hepáticos compatibles con metástasis.
Finalmente se decidió iniciar tratamiento con ASS.
Discusión
Los TNE pancreáticos suponen un 10% de los TNE digestivos, mientras que los TNE de vía biliar, representan menos del 1%.
Los tumores carcinoides son un subtipo de TNE productor de serotonina, entre otras sustancias, cuyo metabolismo a nivel hepático impide que alcancen la circulación sistémica y produzcan síntomas. Cuando estas sustancias escapan del metabolismo hepático (p.ej. en caso de metástasis) producen un síndrome carcinoide, derivado de la acción periférica de estas aminas.
La TC y RM, son pruebas ampliamente utilizadas en el diagnóstico por su elevada disponibilidad. Sin embargo, su sensibilidad empobrece en lesiones de pequeño tamaño. Para el estadiaje debemos utilizar pruebas más sensibles como la gammagrafía y tomografía por emisión de positrones con ASS. En caso de lesiones pancreáticas la USE es un método óptimo para el diagnóstico que además ofrece la posibilidad de tomar biopsias.
La cirugía es el único tratamiento curativo. En los TNE metastásicos, la resección quirúrgica puede ser una opción, sin embargo, el uso de ASS es el tratamiento más frecuentemente empleado en TNE metastásicos de grado 1 y 2.
CP-191. RITUXIMAB COMO TRATAMIENTO DE MANTENIMIENTO EN PANCREATITIS AUTOINMUNE CORTICODEPENDIENTE
Morales Bermúdez AI, Bracho González M, Gómez Rodríguez P, Durán Campos A, Jiménez Pérez M
UGC Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: pancreatitis, corticodependencia, rituximab.
Introducción
La pancreatitis autoinmune es una enfermedad fibroinflamatoria benigna del páncreas de probable origen autoinmune que puede presentarse como ictericia obstructiva secundaria a masa pancreática o como pancreatitis recurrente. El tratamiento de primera línea son los corticoides, pero las recaídas son frecuentes y algunos pacientes necesitan otros tratamientos para mantener la remisión.
Caso clínico
Paciente de 45 años. Hija con enfermedad de Crohn. Sin antecedentes personales de interés. No hábitos tóxicos. Presenta primer episodio de pancreatitis aguda necrotizante tras CPRE realizada por coledocolitiasis; necesidad de drenaje percutáneo de colección necrótica infectada, con buena evolución. Posteriormente presenta otros dos episodios de pancreatitis leve, tras los cuales se realiza colecistectomía por colelitiasis.
Durante su ingreso por cuarto episodio de pancreatitis se actualizan pruebas complementarias: perfil lipídico, iones y marcadores tumorales normales, IgG4 elevada, RMN de páncreas con amputación de conducto pancreático en cabeza de páncreas. Se realiza ecoendoscopia, visualizando páncreas globuloso con bandas hiperecogénicas y dilatación leve del conducto de Wirsung con estrechamiento del mismo a nivel de papila, sin lesiones sugestivas de malignidad. Se toman biopsias de papila y en espera de resultados, se inicia tratamiento con corticoides ante la sospecha de pancreatitis autoinmune. Posteriormente se reciben resultados histológicos: cambios inflamatorios inespecíficos con aisladas células IgG4 (<10 células/CGA).
El paciente presenta evolución tórpida, con episodios recurrentes de pancreatitis coincidiendo con la bajada de dosis de corticoides <10mg. Se inicia tratamiento concomitante con azatioprina, pese a lo cual presenta varios episodios más de pancreatitis al intentar bajada de corticoides. Se decide iniciar tratamiento con rituximab ante pancreatitis autoinmune corticodependiente: 2 dosis de 1000mg iv. Actualmente el paciente se encuentra en disminución progresiva de corticoides y azatioprina, sin nuevos episodios de dolor abdominal hasta el momento.
Discusión
El tratamiento de primera línea de la pancreatitis autoinmune son los corticoides. El fármaco de elección es la prednisolona oral a dosis de 0,6mg/kg/día durante 2-3 semanas con descenso gradual durante 2-3 meses. La suspensión de corticoides conlleva una alta frecuencia de recurrencia, por lo que se recomienda tratamiento de mantenimiento con prednisolona 2,5-5mg/día o inmunomoduladores como azatioprina 2mg/kg/día por un período de 1 a 3 años. En caso de recurrencias se puede realizar tratamiento concomitante, como fue el caso de nuestro paciente, en nuestro caso sin éxito. Rituximab es un anticuerpo anti-CD 20 descrito como tratamiento de mantenimiento, aunque en la actualidad se necesitan más estudios que definan mejor su papel en términos de frecuencia y duración como tratamiento en esta patología.
CP-192. SÍNDROME DE BOUVERET, UNA CAUSA DE OBSTRUCCIÓN INTESTINAL INFRECUENTE
Alonso Belmonte C1, Bracho González M2, Parra López B1, Bravo Aranda A1, Jiménez Pérez M1
1Servicio Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga. 2Sección Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: síndrome de bouveret, fístula colecistoduodenal, colelitiasis..
Introducción
La colelitiasis es una patología frecuente con una prevalencia entre 10-20%, siendo en un 80% de las ocasiones asintomática, aunque también puede conllevar complicaciones frecuentes como colecistitis, cólicos biliares o pancreatitis. Existen otras complicaciones menos habituales en la práctica clínica, como el síndrome de Bouveret.
Caso clínico
Mujer de 90 años. Antecedentes de hipertensión arterial, fibrilación auricular y enfermedad renal crónica.
Acude hasta en tres ocasiones en la misma semana a urgencias por cuadro de dolor en hipocondrio derecho irradiado a flanco, con vómitos de 7 días de evolución, sin alteraciones del hábito intestinal, orina maloliente, puño percusión renal negativa, y sin signos de abdomen agudo. Se diagnostica de infección del tracto urinario no complicada y se maneja con ciprofloxacino ambulatorio.
Acude en una cuarta ocasión a urgencias por persistencia del dolor e intolerancia oral. Se evidencia en nueva analítica con perfil hepatopancreático una lipasa en límite bajo de diagnóstico de pancreatitis aguda (1225 U/L) por lo que se realiza ecografía abdominal, en la que se aprecia abundante líquido en cámara gástrica y primera-segunda porción duodenal, así como contenido hiperecogénico en 2ª porción duodenal con gran sombra acústica posterior y aerobilia. Se completa estudio con tomografía computarizada de abdomen que confirma la presencia de fístula colecistoduodenal con migración de litiasis biliar a duodeno y dilatación retrógrada, correspondiendo a un síndrome de Bouveret. Ingresa a cargo de cirugía por el cuadro de obstrucción intestinal secundario a íleo biliar, realizándose cirugía con apertura duodenal para extracción de la litiasis con posterior duodenorrafia con colocación de drenaje y sonda nasogástrica, con evolución favorable.
Foto 1
Corte coronal de TC abdomen donde se visualiza gran litiasis en área teórica de 2º porción duodenal, condicionando dilatación duodenal retrógrada y estómago de retención
Discusión
El síndrome de Bouveret es la forma más infrecuente de íleo biliar. Se produce por impactación en el bulbo duodenal de una litiasis migrada a través de una fistula colecistoduodenal.
Clínicamente produce vómitos y dolor en hipocondrio derecho. Alteraciones analíticas y la triada de Rigle (aerobilia, dilatación de intestino delgado con niveles hidroaéreos y visualización del cálculo) se dan en menos de un 30% de las ocasiones. Para el diagnóstico se emplea ecografía, colangiopancreato resonancia magnética, técnicas endoscópicas, pero lo más frecuente es confirmarlo con una tomografía computarizada. El tratamiento puede ser endoscópico, haciendo progresar la litiasis, aunque lo habitual es el tratamiento quirúrgico con extracción manual de la litiasis, y en un segundo acto colecistectomía y cierre de la fistula.
Dada la morbimortalidad que puede ocasionar este cuadro es importante tenerlo en cuenta a pesar de su poca frecuencia.
CP-193. SINDROME DE BOUVERET: UNA COMPLICACIÓN INFRECUENTE DE LA COLELITIASIS.
Hermida Pérez B1, Soto Dopazo M2, López González J3, De Jorge Turrión M1
1Servicio Aparato Digestivo. Hospital de Cabueñes, Gijón. 2Servicio Cirugía General y Digestiva. Hospital de Cabueñes, Gijón. 3UGC Aparato Digestivo. Complejo Hospitalario de Especialidades Torrecárdenas, Almería.
Palabras clave: sindrome bouveret, colelitiasis, obstrucción duodenal.
Introducción
El Síndrome de Bouveret es una entidad clínica infrecuente consistente en la obstrucción duodenal o gástrica secundaria a un cálculo biliar, generalmente de gran tamaño; que supone un reto diagnóstico y terapéutico.
Caso clínico
Presentamos el caso de una mujer de 77 años con antecedentes de HTA, hernia de hiato y colelitiasis con episodios previos de cólico biliar. La paciente acude a urgencias con clínica de 10 días de evolución de molestias epigástricas, pirosis y emesis de contenido alimenticio que no presentó mejoría con procinéticos. Se realizan radiografía de tórax y abdomen, objetivando nivel hidroaéreo gástrico y analítica general sin hallazgos relevantes salvo PCR: 44mg/L. Se decide colocación de sonda nasogástrica con aspiración e ingreso hospitalario.
A las 20 horas del ingreso se realiza TC abdominal en el que se describe la presencia de una imagen redondeada a nivel duodenal de unos 3cm en probable relación con cálculo biliar que condiciona obstrucción a dicho nivel y la presencia de una fístula colecistoduodenal. Se solicita gastroscopia urgente en la que se constata presencia de cálculo biliar que condiciona obstrucción, con imposibilidad para su extracción, por lo que se reevalúa a la paciente junto con el Servicio de Cirugía General, decidiéndose la realización de intervención quirúrgica urgente. Se realizó migración manual proximal de cálculo a cavidad gástrica, gastrotomía, extracción del cálculo y sutura. Se extrajo un cálculo biliar de 4,5x3x1,5cm.
La paciente evolucionó favorablemente, siendo dada posteriormente de alta sin complicaciones reseñables.
Figura 1.
Endoscopia digestiva alta. Visión frontal de litiasis causando obstrucción a nivel de bulbo duodenal.
Discusión
El Síndrome de Bouveret es una complicación clínica infrecuente de la colelitiasis que generalmente se presenta en pacientes de edad avanzada o con comorbilidades. Su diagnóstico requiere una elevada sospecha clínica y su tratamiento puede ser endoscópico o, en caso de imposibilidad para el mismo, quirúrgico. La introducción y generalización de nuevas técnicas endoscópicas podría en un futuro disminuir el número de intervenciones quirúrgicas realizadas y con ello la morbimortalidad asociada a las mismas
CP-194. SINDROME DE COLA PANCREATICA DESCONECTADA: CAUSA PANCREATITIS RECIDIVANTE
OROZCO BERNARDEZ-ZERPA N, OSORIO MARRUECOS M, BOCANGERA VINIEGRA M
Servicio Aparato Digestivo. Hospital de Especialidades de Puerto Real, Puerto Real.
Palabras clave: wirsung, disrupción, pancreatitis recidivante.
Introducción
La desconexión del ducto pancreático, o síndrome del ducto pancreático desconectado (SDPD), es una entidad clínica que consiste en la existencia de una situación anatómica en la que hay ausencia de la continuidad del conducto pancreático entre el tejido pancreático viable y el tracto gastrointestinal, por necrosis ductal siendo la pancreatitis aguda grave o el traumatismo las principales causas.
Caso clínico
Mujer de 77 años con antecedentes personales de HTA, DM, DLP y ERC que presentó ingreso por cuadro de pancreatitis aguda biliar grave con colecciones necróticas no infectadas y con hasta dos reingresos posteriores por reagudización del cuadro y aparición de nuevas colecciones. Se realiza TC de abdomen donde se visualiza colección en contacto con Wirsung sin poder descartar disrupción del mismo (Figura 1). Posteriormente se realizó RMN de páncreas sin secretina al no disponer en nuestro centro, no objetivándose dicha anomalía. Debido a la alta sospecha de Síndrome de Cola Pancreática Desconectada (SCPD) se realiza pancreatografía por CPRE objetivándose paso de contraste a colección adyacente y ausencia del mismo en la cola del páncreas, confirmándose dicho diagnóstico (Figura 2). Se posiciona prótesis pancreática realizando drenaje transpapilar. Tras dicho procedimiento presentó mejoría progresiva de colecciones sin presentar nuevas reagudizaciones de la clínica. Se realizó nueva CPRE con retirada de prótesis a los dos meses y realizando pancreatografía donde se visualizaba la integridad del Wirsung.
Discusión
El síndrome del ducto pancreático desconectado (SDPD) consiste en la pérdida de continuidad entre una parte viable del páncreas y el tubo digestivo, continuando la función exocrina pancreática a través del extremo disruptivo y originando colecciones intra o peripancreaticas, incluso fistulas externas.
Debe sospecharse ante una pancreatitis aguda grave necrótica, con afectación en la región central del páncreas, reagudizaciones o colección pancreáticas sin resolución. Su confirmación se basa en demostrar la extravasación del material de contraste inyectado en el ducto principal mediante CPRE, ecoendoscopia o mediante cirugía. No se recomienda la realización de drenaje percutáneo por el riesgo de aparición de fistula pancreática.
El tratamiento previamente conocido del SCPD era quirúrgico, mediante pancreatectomía distal o derivación a un asa en y de roux pero con este caso tras revisión bibliográfica describimos la resolución del mismo mediante tratamiento endoscópico.
CP-195. SÍNDROME LPAC, CUANDO LA COLECISTECTOMÍA NO ES LA SOLUCIÓN.
Alonso Belmonte C, Morales Bermúdez AI, Bracho Gónzalez M, López Ortega S, Jiménez Pérez M
Servicio Aparato Digestivo. Complejo Hospitalario Regional de Málaga, Málaga.
Palabras clave: síndrome lpac, ácido ursodesoxicólico, cólico biliar.
Introducción
El síndrome LPAC (low-phospholipid-associated cholelithiasis) es una entidad rara asociada a mutaciones del gen ABCB4, que codifica la proteína MDR3, lo que conlleva una producción de bilis con un bajo contenido en fosfolípidos y una mayor producción de cálculos de colesterol intrahepáticos y colelitiasis, con repercusión clínica en forma de síntomas biliares, incluso a pesar de colecistectomía.
Caso clínico
Varón de 29 años, con antecedentes familiares de tía con colangitis autoinmune y hermana con cólicos biliares desde los 30 años, en seguimiento por digestivo desde los 20 años debido a cólicos biliares de repetición.
Comienza con episodios de dolor a nivel epigástrico, acompañado de vómitos, fiebre, ictericia y alteración de perfil hepático con colestasis y citólisis. Se descartan causas de hepatitis aguda y se realiza ecografía que pone de manifiesto la presencia de colelitiasis y coledocolitiasis. Se realiza colangiopancreatografía retrógrada endoscópica (CPRE) con extracción de coledocolitiasis y posteriormente colecistectomía con tratamiento de mantenimiento con ácido ursodesoxicólico (AUDC) 150mg/8h permaneciendo asintomático 3 años. Se continúa seguimiento por hipertransaminasemia mantenida, con estudio de hepatopatía, autoinmunidad y biopsia hepática negativos.
Dada la estabilidad clínica se abandona tratamiento con AUDC, comenzando desde entonces con cólicos de repetición y alteración del perfil hepático (hipertransaminasemia y colestasis disociada). Se realiza colangio-resonancia magnética sin alteraciones, así como ecografía abdominal donde el único hallazgo fue la presencia de vía biliar intrahepática ligeramente dilatada con aerobilia. Se valora entonces el diagnóstico de Síndrome LPAC por cumplir criterios. Se comienza tratamiento con AUDC 600mg permaneciendo asintomático. Se realizó estudio genético, resultando positivo la mutación del gen ABCB4.
Discusión
El síndrome LPAC debe sospecharse en un paciente joven con síntomas biliares (colangitis, ictericia colestásica, cólico biliar). El diagnóstico se basa principalmente en criterios clínicos y ecográficos. Deben existir al menos dos de los siguientes: edad ≤ 40 años, reaparición de síntomas biliares tras colecistectomía, focos hiperecogénicos intrahepáticos, barro biliar o microlitiasis. Otras características clínicas asociadas son: predominio en mujeres, colestasis intrahepática en el embarazo, colelitiasis en parientes de primer grado, y mejoría franca con AUDC. El análisis genético de ABCB4 sirve para apoyar el diagnóstico, aunque no es necesario ya que solo se identifica en un 60% de los pacientes. El tratamiento se realiza con AUDC, que potencia el efecto MDMR3 y solubiliza el colesterol, a dosis 7-10 mg/kg.
CP-196. TUMOR QUISTICO MUCINOSO PANCREÁTICO
Grilo Bensusan I, Herrera Martín P
Unidad Aparato Digestivo. Hospital de Alta Resolución de Écija, Écija.
Palabras clave: tumor quístico pancreático, tumor mucinoso, cáncer de páncreas.
Introducción
Los tumores quísticos del páncreas son lesiones relativamente poco frecuentes, algunos de los cuales tienen riesgo de malignización. Presentamos el caso de un tumor quístico mucinoso de gran tamaño.
Caso clínico
Una mujer de 46 años acude a la consulta por estreñimiento, de unos meses de evolución, acompañado de distensión abdominal y molestias abdominales inespecíficas. También refiere plenitud precoz. En este contexto, se realiza una ecografía abdominal en la que se observa una lesión de 10 cm a nivel del hipocondrio izquierdo, aparentemente dependiente de la cola del páncreas, anecogénica, con refuerzo acústico y con aparentes tabiques y contenido hiperecogénico en su interior (figura 1 y 2). Ante este hallazgo se solicita una RM abdominal con contraste en la que se observa una lesión quistica de 10 x9 x 8,6 cm, con septos finos en su interior . No se observan nódulos sólidos ni detritus, ni dilatación de los conductos pancreáticos ni comunicación con los mismos. Se describe la lesión como probable cistoadenoma/cistoadenocarcinoma mucinoso (figura 3,4 y 5). Se deriva a la paciente a cirugía que realiza una esplenectomía con pancreatectomía distal. En el análisis histológico de la pieza se confirma la neoplasia mucinosa quística multilocular con tapizamiento de epitelio mucinoso e intestinal, sin atipia, con estroma de tipo ovárico y sin afectación ganglionar.
Figura 1
Imagen de ecografía abdominal en la que se observa una lesión quística anecogénica con presencia de tabiques hiperecogénicos.
Figura 2
Imagen de ecografía abdominal de lesión quística de la cola del páncreas, con tabiques y aparente contenido hiperecogénico en su interior.
Figura 3
Imagen de RM en T1 con lesión quística, de la cola del páncreas, bien delimitada y encapsulada.
Discusión
Los tumores quísticos mucinosos del páncreas suponen el 25 % de las lesiones quísticas del páncreas. Se producen más frecuentemente en la cola del páncreas y suelen ser asintomáticos. Son diagnósticados incidentalmente mediante una prueba de imageno. La sospecha requiere la confirmación mediante resonancia magnética y /o ecoendoscopia con estudio del líquido quístico. Generalmente son únicos y sin tabiques, a diferencia de nuestro caso. A diferencia del tumor mucinoso papilar intraductal no se comunica con los conductos pancreáticos. En su composición están formados por estroma ovárico lo que explica que se diagnostiquen casi exclusivamente en mujeres. Hasta en un 15 % de los casos existe degeneración maligna, especialmente si el tamaño es mayor de 6 cm, existen calcificaciones o nódulos en las paredes o una pared gruesa o irregular. En nuestro caso ante la sospecha radiológica y el tamaño de la lesión se optó por la cirugía descartándose la degeneración maligna. En algunos casos, con tumores de pequeño tamaño y sin signos sospechosos de malignización y dependiendo del riesgo quirúrgico, se puede plantear el seguimiento mediante pruebas de imagen, existiendo variaciones de las recomendaciones según las guías clínicas vigentes.
CP-197. UNA ETIOLOGÍA POCO FRECUENTE DE PANCREATITIS CRÓNICA: PANCREATITIS TROPICAL
Rosa Sánchez C, Librero Jiménez M, Lecuona Muñoz M, Redondo Cerezo E, Valverde López F
Departamento Aparato Digestivo. Complejo Hospitalario Regional Virgen de Las Nieves, Granada.
Palabras clave: pancreatitis tropical.
Introducción
La pancreatitis crónica tropical es una patología característica de zonas endémicas como África subsahariana y se ve con poca frecuencia en nuestro medio. Su etiología es desconocida, si bien se postula que podría ser de origen genético. Dicha enfermedad se caracteriza por la aparición de dolor recurrente en la juventud con calcificaciones pancreáticas características en personas sin antecedentes de consumo de alcohol, en ocasiones asociada a la aparición de diabetes temprana. Este es el caso de un paciente con pancreatitis tropical.
Caso clínico
Paciente de 24 años natural de Nigeria y residente en España desde los 15 años, sin antecedentes de interés, que ingresa en múltiples ocasiones por episodios de epigastralgia intensa, siendo necesario valoración por la Unidad del Dolor para control del dolor. En las pruebas de imagen realizadas se aprecian abundantes calcificaciones (hasta 17 mm) en todo el parénquima pancreático y en el conducto pancreático principal, condicionando su dilatación (Figuras 1 y 2). Debido a la intensidad y refractariedad de estos cuadros de dolor abdominal, se realizó CPRE para el drenaje de las litiasis intrapancreáticas, consiguiendo una permeabilización completa del conducto de Wirsung, con resolución del dolor abdominal. Sin embargo, poco después el paciente vuelve a presentar nuevas crisis de dolor secundario a la reaparición de nuevas litiasis (e incluso presentó un episodio de pancreatitis aguda moderada-grave), siendo necesaria en el último año la realización de 5 CPREs. Debido a esto, el paciente se encuentra actualmente en lista de espera para manejo quirúrgico de la pancreatitis crónica.
Discusión
Presentamos el caso de un paciente joven con un cuadro clínico, radiológico y un contexto epidemiológico compatible con pancreatitis crónica tropical. En pacientes con un cuadro como este, con una pancreatitis crónica con calcificaciones de gran tamaño (a diferencia de la pancreatitis alcohólica) en pacientes sin hábitos tóxicos, especialmente si proceden de regiones endémicas, la pancreatitis tropical debe ser una patología a tener en cuenta, si bien deben descartarse las causas más frecuentes de pancreatitis crónica. A día de hoy no hay un tratamiento específico para esta enfermedad; sin embargo, es necesario tener en cuenta su alta tendencia a la diabetes mellitus (hasta el 90%) y el alto riesgo de cáncer de páncreas (hasta el 22%), las dos causas fundamentales de mortalidad en estos pacientes, que sin seguimiento médico alcanzan una supervivencia media de 35 años tras el primer episodio de dolor, por lo que es fundamental realizar un seguimiento estrecho y un buen control de la diabetes.

 Descargar número completo
Descargar número completo Download full issue
Download full issue