CITA ESTE TRABAJO
Selfa Muñoz A, Candel Erenas JM, Moreno Barrueco M, Bailón Gaona MC. Malformaciones vasculares intestinales: un desafío terapéutico. RAPD 2026;49(1):13-23. DOI: 10.37352/2026491.2
Listado de abreviaturas
AD: angiodisplasia.
TAVI: implantación de válvula aórtica transcatéter.
THH: telangiectasia hemorrágica hereditaria.
VEGF: factor de crecimiento endotelial vascular.
APC: coagulación con plasma argón.
GAVE: ectasia vascular gástrica antral.
ECA: ensayo controlado aleatorizado.
HDOO: hemorragia digestiva de origen oscuro.
Definición de angiodisplasias
La angiodisplasia (AD), también llamada angiectasia o ectasia vascular, es la malformación vascular más común del tubo digestivo. Se trata de vasos sanguíneos tortuosos y dilatados, generalmente menores de 5 mm de diámetro, que asientan en las capas mucosa y submucosa. Aunque se describió inicialmente en 1839, el término angiodisplasia (AD) fue introducido por primera vez en 1974 por Galdabini al describir agrupaciones anormales de vasos mucosos en el colon[1].
Las AD se pueden encontrar en cualquier segmento del tubo digestivo. Son más frecuentes en intestino delgado (57-80%, especialmente en yeyuno), seguido del colon (44%, sobre todo en ciego) y estómago (32%). Entre el 40% y el 60% de los casos las AD son múltiples. Y, aunque suelen presentarse en la misma porción del tracto gastrointestinal, en aproximadamente el 20% de los casos afectan a más de un segmento del tubo digestivo[2].
Prevalencia y manifestaciones clínicas
La prevalencia de las AD es difícil de determinar, ya que la mayoría son asintomáticas. En un análisis combinado de tres estudios prospectivos sobre el cribado colonoscópico de neoplasia en adultos sanos asintomáticos, mayores de 50 años, sólo 8 de 964 participantes (0.8%) presentaron AD[3].
En 2025 se publica un estudio observacional, retrospectivo y de base poblacional que incluye a 4327 adultos con AD gastrointestinales (basados en los códigos de diagnóstico) que concluye que la prevalencia general de AD es del 0.092%, alcanzando una prevalencia máxima del 0.37 % entre los 71-80 años[1].
Las AD causan el 10% de las hemorragias gastrointestinales y el 50% de los casos de hemorragia del intestino delgado. El 77% de los pacientes con AD gastrointestinales experimenta al menos un episodio de sangrado visible (hematemesis o melena) con o sin inestabilidad hemodinámica, mientras que los restantes presentan anemia crónica dependiente de transfusión o de infusión intravenosa de hierro[2].
Factores de riesgo
Se ha encontrado una asociación significativa entre las AD y la edad mayor de 60 años, así como con otras enfermedades como enfermedad pulmonar obstructiva crónica, cirrosis hepática, estenosis aórtica (síndrome de Heyde) e insuficiencia renal crónica (las AD se relacionan con la duración y gravedad de la enfermedad renal)[2],[4].
La asociación entre AD sangrantes y estenosis aórtica se conoce como Síndrome de Heyde. La explicación más aceptada es que la estenosis aórtica podría causar la destrucción de multímeros del factor de Von Willebrand. Los multímeros del factor de Von Willebrand son grandes complejos de proteínas formados por la unión de subunidades más pequeñas (monómeros) y son fundamentales para la adhesión y agregación plaquetaria y para proteger al factor VIII de la degradación. Se postula una patogenia similar como etiología de hemorragia digestiva secundaria a AD en pacientes con dispositivos de asistencia ventricular izquierda.
Antes del siglo XXI, el reemplazo valvular aórtico quirúrgico era la única técnica disponible, pero la implantación de válvula aórtica transcatéter (TAVI) cada vez se utiliza más. Goltstein et al[5] realizaron un metanaálisis que incluyó a 300 pacientes con síndrome de Heyde procedentes de 10 estudios de cohorte, el cual determinó una tasa combinada de cese del sangrado después de la reparación valvular del 73 % (62–81%, IC 95%). Los análisis de subgrupos revelaron tasas de cese de sangrado significativamente más bajas después de TAVI en comparación con el recambio valvular quirúrgico (64% vs 82%), lo cual es atribuido a que la fuga paravalvular es más frecuente tras la TAVI. Los avances en válvulas TAVI de última generación han disminuido la tasa de fuga paravalvular, lo cual acerca los resultados del TAVI al recambio valvular quirúrgico. También cabe destacar que las tasas de cese del sangrado son más elevadas entre uno y cinco años después de la TAVI, en comparación con el primer año (85% vs 53%)[6].
Dentro de las causas hereditarias de AD destaca el Síndrome Rendu-Osler-Weber o Telangiectasia Hemorrágica Hereditaria (THH). Es una enfermedad rara de herencia autosómica dominante con diversas manifestaciones clínicas, incluyendo malformaciones arteriovenosas que pueden presentarse en piel, mucosas y en cualquier órgano, hasta el 80-90% de los pacientes tienen AD en intestino delgado. En estos pacientes la afectación gastrointestinal es la segunda causa más frecuente de hemorragia (25-30%), siendo la primera la epixtasis. En 2020 se publica en la revista Annals of Internal Medicine una guía clínica para el diagnóstico y manejo terapéutico de los pacientes con THH[4],[7].
Patogénesis
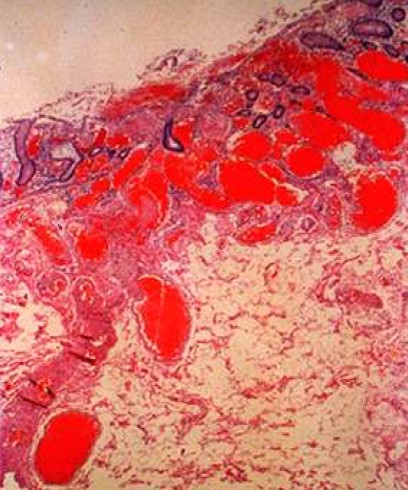
Se postula que contracciones musculares a nivel de la muscular propia producen obstrucciones vasculares crónicas, intermitentes y recurrentes de bajo grado en la submucosa. Esto desencadena una hipoxia local que conduce a la angiogénesis mediada por agentes químicos, de los cuales el más importante es el factor de crecimiento endotelial vascular (VEGF). El VEGF estimula la neovascularización con formación de AD que son vasos aberrantes, ya que están revestidos únicamente por endotelio con músculo liso mínimo o nulo (Figura 1)[2],[8].
Figura 1
Biopsia colónica de una angiodisplasia, se muestra dilatación vascular mucosa y submucosa y congestión (imagen tomada de Saltzman JR, angiodysplasia of the gastrointestinal tract, UpToDate: 2025).
En la angiogénesis participan múltiples mediadores químicos. Se ha observado una mayor expresión tisular y niveles séricos elevados de VEGF en pacientes con AD gastrointestinales en comparación con sujetos sanos[9]. Se ha encontrado una asociación significativa entre las AD y la vía metabólica de las angiopoyetinas (Ang-1y Ang-2), que son un grupo de proteínas involucradas en la formación de nuevos vasos sanguíneos. Se han demostrado niveles elevados de Ang-2 y una baja tendencia en los niveles de Ang-1 y TNF-α en pacientes con AD, en comparación con individuos con hemorragia por otras causas[10]. El factor de von Willebrand se almacena en las células endoteliales y regula la liberación de Ang-2 e integrina mediante una interacción compleja con el receptor VEGF[11].
La monitorización de los marcadores bioquímicos de angiogénesis podría servir como herramienta de diagnóstico o para evaluar la respuesta al tratamiento y distinguir a los respondedores de los no respondedores. A pesar de los avances logrados, el uso clínico de biomarcadores de angiogénesis aún se encuentra en fase de investigación[2].
Tratamiento endoscópico
El tratamiento de las AD gastrointestinales (en particular las localizadas en el intestino delgado) representan un gran desafío debido al comportamiento insidioso de la enfermedad, la inaccesibilidad a los sitios afectados y la elevada tasa de recidiva.
Tras la terapia endoscópica la tasa de resangrado es del 36% durante un seguimiento promedio de 22 meses. Este riesgo aumenta al 45% en AD localizadas exclusivamente en intestino delgado[12].
La alta recurrencia del sangrado en pacientes con AD tras el tratamiento endoscópico podría deberse a la presencia de AD no tratadas, no detectadas endoscópicamente o a la neoformación de lesiones. Por todo ello es necesario disponer de otras opciones como sería el tratamiento farmacológico como veremos más adelante.
Hay disponibles múltiples métodos endoscópicos para tratar las AD, la elección entre estos abordajes dependerá de la localización de la lesión, la experiencia del endoscopista y la disponibilidad de equipos[2],[4],[8],[13]:
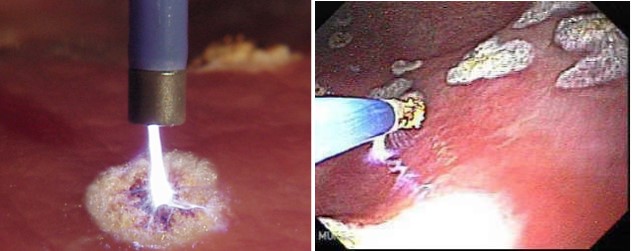
- Coagulación con plasma argón (APC): el gas argón inerte se convierte en gas argón ionizado (plasma) mediante un electrodo monopolar en la punta de la sonda que se coloca entre 2 y 8 mm de la lesión sangrante, lo que produce la coagulación del tejido con una baja penetración en profundidad (2-3 mm), reduciendo por ello el riesgo de perforación (Figura 2). La inyección de solución salina submucosa (con o sin adrenalina) en AD localizadas en colon protege contra lesiones profundas y reduce aún más el riesgo de perforación. Por su disponibilidad, bajo coste y buen perfil de seguridad, la APC se posiciona como tratamiento endoscópico de primera línea para las AD gastrointestinales sangrantes. Se han descrito casos de perforación intestinal por explosión de gas colónico debido a una preparación intestinal deficiente[14],[15]. Por lo tanto, se recomienda una adecuada limpieza del colon antes de realizar APC.
Figura 2
Aplicación de coagulación con plasma argón (APC) sobre angiodisplasia en estómago. Imagen tomada de la web del Centro De Endoscopia Terapéutica Anvanzada®.
- Electroagulación bipolar y fotocoagulación con Nd:YAG (Neodimio: Itrio-Aluminio-Granate) y láser Argón. Los métodos endoscópicos de sonda de contacto tienen una eficacia hemostática similar a la APC para las AD sangrantes. Pero presentan una mayor incidencia de perforación, especialmente cuando se utilizan en colon.
- Escleroterapia: la lesión se oblitera mediante la inyección de un esclerosante que conduce a inflamación y trombosis local, y posteriormente, hemostasia. No se ha asociado con complicaciones graves pero la literatura es limitada.
- Mecánicos: colocación endoscópica de hemoclips o ligadura con bandas elásticas, lo que conduce a la isquemia y la posterior necrosis de los vasos diana. Al evitar la lesión tisular pueden ser particularmente útiles en pacientes que toman anticoagulantes y/o antiagregantes. La ligadura con bandas elásticas es el método de elección para tratar la ectasia vascular gástrica antral (GAVE) con excelentes resultados clínicos y mínimos eventos adversos[16].
- Ablación por radiofrecuencia: se ha utilizado para el tratamiento de la GAVE y para AD de intestino delgado. En una serie de casos de 20 pacientes con sangrado por AD de intestino delgado, se hizo pasar un catéter de ablación por radiofrecuencia a través del canal del enteroscopio. La mediana del tiempo de seguimiento fue de 195 días (30-240 días) y se observó recidiva del sangrado en 4 pacientes (20%), 3 de los cuales tenían un dispositivo de asistencia ventricular izquierda[17]. Se necesitan más trabajos que evaluen esta técnica.
Hay en marcha un trabajo de la Cochrane[13] para realizar un protocolo de tratamiento endoscópico de las AD. Incluirán ensayos controlados aleatorizados (ECA) y ensayos cuasialeatorizados sobre adultos con AD a cualquier nivel del tracto gastrointestinal, con sangrado gastrointestinal oculto o manifiesto, o anemia por déficit de hierro. En los que se compare cualquier tratamiento, ya sea endoscópico o no, incluyendo uno o más de los siguientes: médico (cualquier fármaco y dosis), tratamiento quirúrgico, radiología intervencionista, transfusión sanguínea o abstención terapéutica. Se excluirá GAVE y gastropatía portal hipertensiva, así como la combinación de tratamientos (por ejemplo, endoscopia y terapia médica, combinación de abordajes endoscópicos…). Valorarán la respuesta y también los eventos adversos.
¿Cuándo realizar tratamiento endoscópico?
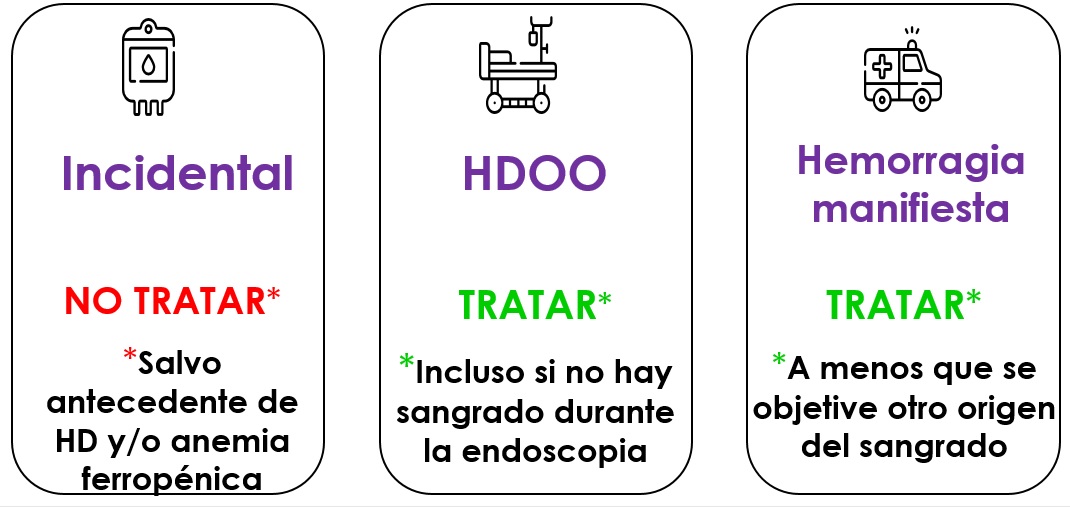
Durante la endoscopia digestiva podemos objetivar la presencia de AD, según los diferentes escenarios clínicos posibles será necesario o no realizar tratamiento endoscópico (Figura 3)[8],[18]:
Figura 3
Escenarios posibles sobre el hallazgo de angiodisplasias durante la endoscopia digestiva y necesidad o no de realizar tratamiento endoscópico (de la autora del manuscrito). HD: Hemorragia digestiva; HDOO: Hemorragia digestiva de origen oscuro.
-Hallazgo incidental: en caso de AD encontradas de forma incidental durante la endoscopia digestiva no es necesario hacer tratamiento endoscópico. Siempre y cuando el paciente no tenga antecedente de hemorragia digestiva y/o de anemia ferropénica.
-Hemorragia digestiva de origen oscuro (HDOO): en pacientes con HDOO se recomienda tratar las AD, incluso si éstas no están sangrando en el momento de la endoscopia. La terminología actual ha cambiado de "HDOO" a "hemorragia del intestino delgado", reservándose el término HDOO para los casos en los que no se detecta el origen de la hemorragia a pesar de una evaluación exhaustiva de todo el tracto gastrointestinal, incluido el intestino delgado[4].
-Hemorragia digestiva manifiesta: en caso de sangrado activo se debe tratar las AD, salvo si se identifica durante la endoscopia otro origen del sangrado digestivo.
Embolización mediante angiografía
Se realiza mediante la cateterización selectiva del vaso que nutre la lesión sangrante y la posterior inyección de agentes embolizantes (los más utilizados son las esponjas biodegradables y los microcoils). Tiene una alta eficacia hemostática, del 80-90%. Y se asocia a complicaciones en el 5-9% de los casos, de las cuales el 2% son graves e incluyen hematomas, infarto intestinal, disección arterial, trombosis y pseudoaneurismas[2],[19].
Es un procedimiento complejo que requiere equipo técnico especial, operadores altamente capacitados en radiología endovascular y que presenta más complicaciones que la terapia endoscópica[2],[19].
Tratamiento farmacológico
Somatostatina
La somastostatina es un polipéptido cíclico secretado por las células D en la mucosa gastrointestinal e inhibe la secreción de ácido gástrico, bilis y secreciones pancreáticas.
La somatostatina nativa no es útil en la práctica clínica debido a su vida media extremadamente corta, de 1 a 3 minutos. Es por ello que de forma sintética se desarrollan los análogos de la somatostatina con una vida media más larga. Hasta la fecha, 3 han sido aprobados para su uso clínico: lanreotida y octeotrida de primera generación, y pasireotida de segunda generación. Se pautan en dosis diarias por vía subcutánea, y ya hay disponible una forma de acción prolongada de octreotida (octreotida LAR) que se puede administrar por vía intramuscular una vez al mes.
Los análogos de la somatostatina han demostrado su utilidad en el tratamiento de las AD gastrointestinales mediante varios mecanismos de acción[20],[21]:
- Inhiben el VEGF, reduciendo así la angiogénesis.
- Disminuyen el flujo sanguíneo esplácnico y portal por inhibición de péptidos vasodilatadores (óxido nítrico, glucagón) y por efecto vasoconstrictor directo.
- Mejoran la agregación plaquetaria.
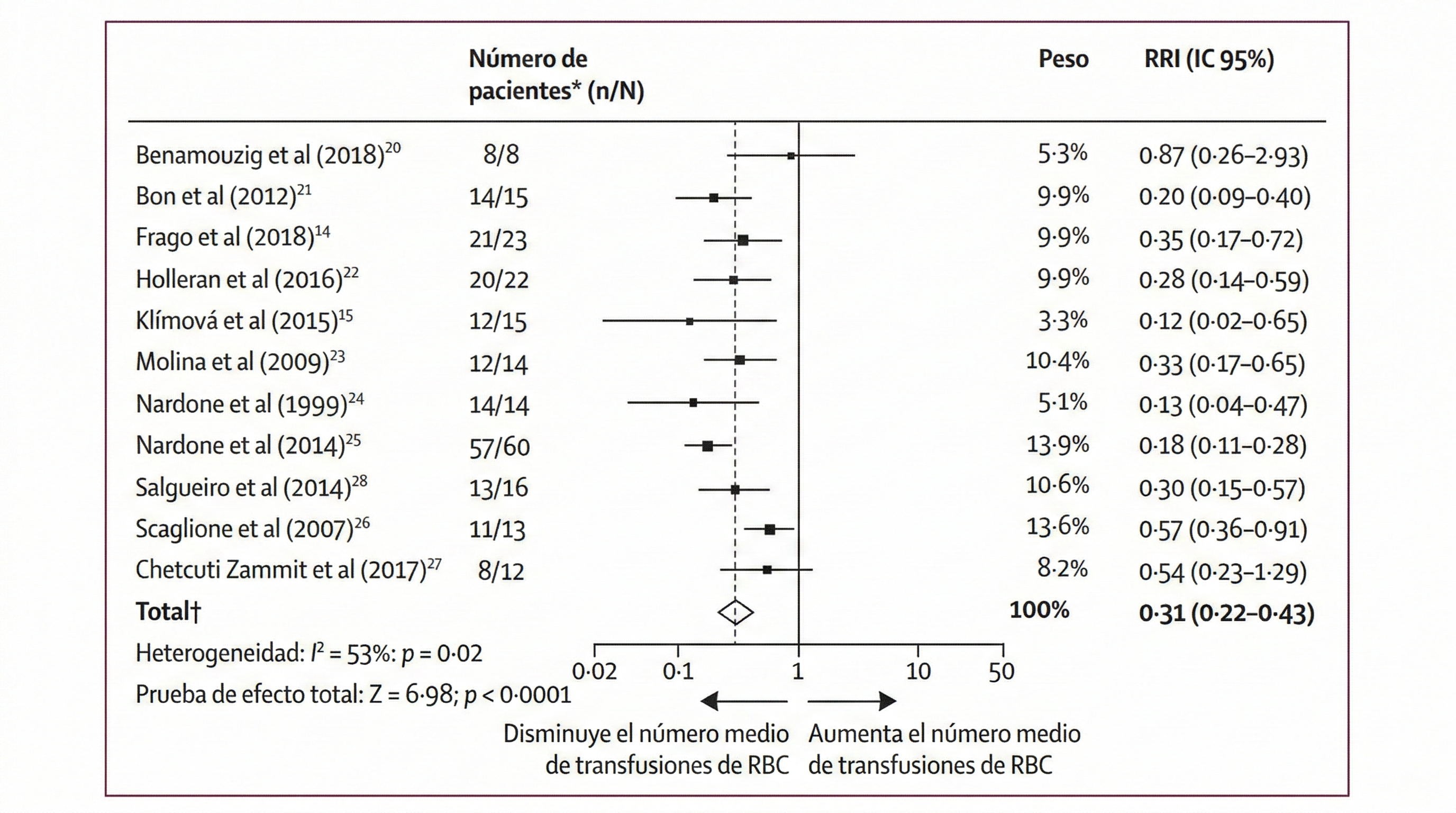
Se han realizado varios estudios desde la década de los 90 que han investigado el uso de análogos de SSA en el contexto de AD gastrointestinales (Figura 4). Se trata de muestras pequeñas, grupos de pacientes heterogéneos, con criterios de inclusión y diseño de estudio variables.
Figura 4
Estudios sobre el efecto de los análogos de somatostatina en el número medio de transfusiones de glóbulos rojos. RBC: transfusiones de glóbulos rojos. Imagen tomada de Goltstein et al., The Lancet Gastroenterology & Hepatology 2021.
En el 2021 Goltstein et al[22] publican un metaanálisis de datos individuales de 212 pacientes de 11 estudios (1 ensayo controlado aleatorizado y 10 estudios de cohortes), con AD gastrointestinales y sangrado refractario, tratados con análogos de somatostatina. Demostraron una reducción significativa de la necesidad de transfusión sanguínea de una media de 12.8 a 2.3 unidades con los análogos de somatostatina durante un periodo de seguimiento de 12 meses. El subanálisis mostró que la localización de las AD en estómago, en comparación con las AD en intestino delgado y colon, se asoció con una peor respuesta al tratamiento. Y que la octreotida tuvo una mejor respuesta al tratamiento que la lanreotida (Figura 5). Este hallazgo podría explicarse por la afinidad de unión un 30 % mayor de la octreotida al SSTR2, que se expresa principalmente en el intestino delgado y el colon. Asimismo, la octreotida de acción prolongada mantiene mejor las concentraciones séricas que la lanreotida de liberación prolongada[22].
Figura 5
La angiodisplasia en estómago tuvo peor respuesta al tratamiento con análogos de somatostatina, en comparación con las del intestino delgado y colon. La octreotida fue más efectiva que la lanreotida. Imagen tomada de Goltstein et al., The Lancet Gastroenterology & Hepatology 2021.
Evidencia adicional que respalda la eficacia de los análogos de somatostatina proviene de un amplio ECA multicéntrico y abierto publicado en 2024[23]. En pacientes con sangrado por AD en los que se requería haber tenido transfusión de al menos 4 concentrados de hematíes, infusiones intravenosas de hierro o ambas, en el año previo a la aleatorización; se compara la administración intramuscular de 40 mg de octreotida LAR cada 28 días con el tratamiento estándar (hierro intravenoso +/- transfusión de glóbulos rojos). A los pacientes de ambos grupos se les permitió recibir atención concomitante, incluyendo la aplicación endoscópica de APC, la suspensión de antitrombóticos y el uso de ácido tranexámico.
Los pacientes que recibieron octreotida presentaron una necesidad de transfusión significativamente menor (11.0 unidades frente a 21.2 unidades), y el 61 % logró una reducción de al menos el 50 % en las transfusiones en comparación con el valor inicial, frente a sólo 19 % en el grupo de tratamiento estándar. La octreotida también redujo el volumen anual de procedimientos endoscópicos en 0.9[23]. El efecto beneficioso se hizo evidente durante el primer mes y se mantuvo de forma constante durante el año del estudio.
Se utilizó una dosis relativamente alta de octreotida, lo que posiblemente resultó en más eventos adversos. Los cuales se informan en el 25-65% de los pacientes y fueron en su mayoría leves: intolerancia a la glucosa, colelitiasis, gastrointestinales (dolor abdominal, diarrea), reacciones en el lugar de la inyección. Sólo en el 5-6% de los pacientes se produjeron eventos adversos graves que requirieron la interrupción del tratamiento, como trombocitopenia, insuficiencia renal, insuficiencia cardíaca y control deficiente de la glucemia[23],[24].
Los análogos de somatostatina tienen un elevado coste (Figura 6). Pocos estudios han examinado el coste-beneficio. Un estudio retrospectivo de veteranos que presentan sangrado por AD concluyó que su uso no es rentable en EEUU[25]. Tai et al.[26] mostró que el uso de análogos de somatostatina como complemento de la endoscopia es coste-neutral frente al manejo conservador.
Figura 6
Orden SND/1118/2025, de 6 de octubre, por la que se procede a la actualización en 2025 del sistema de precios de referencia de medicamentos en el Sistema Nacional de Salud. Publicado en: «BOE» núm. 246, de 13 de octubre de 2025, páginas 131294 a 132480 (1187 págs).
A pesar del precio y de los eventos adversos, quedarían posicionados como tratamiento farmacológico de primera línea en las AD[27].
Talidomida
La talidomida es conocida por causar graves defectos congénitos. Es inhibidor de la angiogénesis a través del VEGF y del factor de crecimiento de β-fibroblastos e inmunomodulador (suprime el factor de necrosis tumoral). En el tratamiento de las AD se administra vía oral en dosis diarias (50 a 300 mg), durante un período de 4 a 6 meses, más frecuentemente 4 meses, ya que se ha demostrado que tiene un efecto duradero después de la interrupción[24].
Un ECA doble ciego multicéntrico[28] evaluó la eficacia de la talidomida para reducir la hemorragia en una cohorte de 150 pacientes con AD gastrointestinales (y al menos 4 episodios de sangrado el año anterior). Los pacientes fueron asignados aleatoriamente en tres grupos que recibieron 100 mg o 50 mg diarios de talidomida o placebo durante 4 meses. Al año de seguimiento, el 68.6%, el 52% y el 16% de los pacientes tuvieron una reducción en el número de episodios hemorrágicos de al menos el 50% cuando recibieron 100 mg de talidomida, 50 mg de talidomida y placebo, respectivamente.
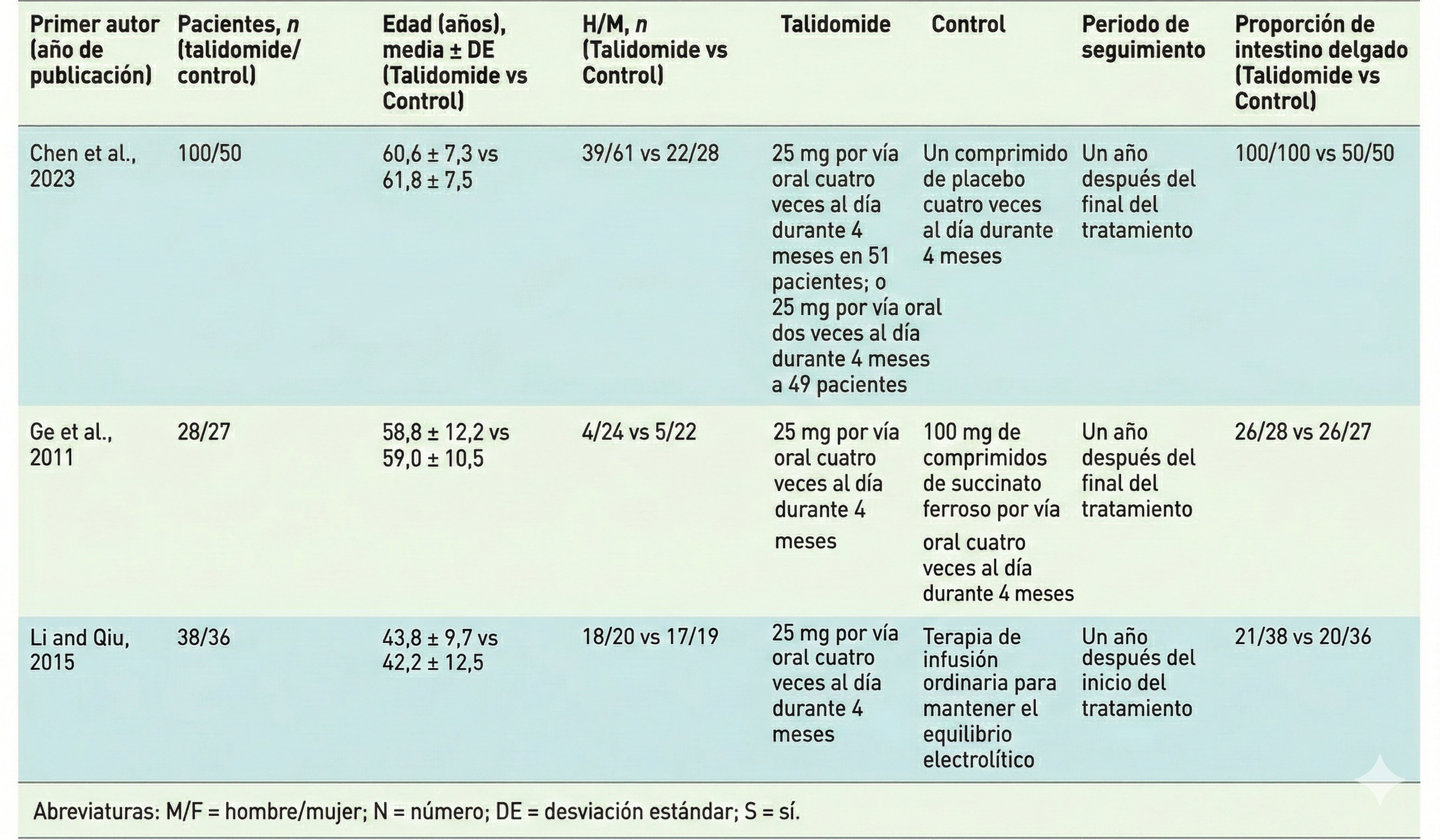
En 2024 Song et al[29] realizan un metaanálisis de ECA sobre la talidomida en AD gastrointestinales (279 pacientes: 166 talidomida y 113 controles) (Figura 7). La talidomida produjo una mejoría en los niveles de hemoglobina, redujo el número de episodios de hemorragia y mejoró la tasa de hospitalización en comparación con el grupo control.
Figura 7
Características de los estudios incluidos en el metaanálisis de ensayos clínicos aleatorizados sobre el efecto beneficioso de la talidomida en las angiodisplasias gastrointestinales. Imagen tomada de Song et al., Therapeutic Advances in Gastroenterology 2024.
La talidomida tiene efectos secundarios leves-moderados muy frecuentes (≥1/10) como son: somnolencia, fatiga, estreñimiento, mareos, edema periférico. Y efectos secundarios graves muy frecuentes (≥1/10): neuropatía periférica (dosis dependiente, ocurre en el 80% de los pacientes después de 6 meses de tratamiento), leucopenia, anemia y trombocitopenia.
En ficha técnica[30] se recomienda:
- Valorar la tromboprofilaxis en pacientes con factores de riesgo trombóticos adicionales.
- Estudiar el virus de la hepatitis B para prevenir una reactivación.
- Usar métodos anticonceptivos en mujeres 4 semanas antes, durante y 4 después del tratamiento, y en hombres hasta al menos 7 días después de la interrupción del tratamiento.
- Someter a los pacientes a reconocimientos clínicos y neurológicos antes de iniciar el tratamiento con talidomida. Y monitorizarlos por si presentan síntomas de neuropatía (parestesia, disestesia, molestias, coordinación anormal o debilidad).
Los eventos adversos y la menor adherencia que a los análogos somatostatina (inyección mensual) lo situan como tratamiento farmacológico de segunda línea, en caso de intolerancia o fracaso a los análogos de somatostatina[24],[27].
Bevacizumab
Es un anticuerpo monoclonal humanizado, antagonista del VEGF. Se utiliza en oncología para inhibir el crecimiento tumoral y la metástasis, por ejemplo en el cáncer colorrectal metastásico y el cáncer de pulmón de células no pequeñas.
Existe cada vez más evidencia de la eficacia del bevacizumab en el tratamiento de la hemorragia gastrointestinal en el contexto de la THH. Se utiliza vía intravenosa y a dosis más baja que para fines oncológicos, en la fase de inducción 5 mg/kg cada 2 semanas, de 4 a 6 dosis, y en el mantenimiento 5 mg/kg al mes[31],[32].
Al revisar la literatura hay algunos informes de casos que describen el uso de bevacizumab en AD. Y sólo un estudio de cohorte retrospectivo[32] de 21 pacientes tratados con bevacizumab iv para la hemorragia digestiva refractaria secundaria a GAVE y AD de intestino delgado. Al año de tratamiento el 86%[18] lograron una reducción del 50 % en las necesidades de transfusión de glóbulos rojos. Y la concentración media de hemoglobina aumentó de 8.3 g/dl a 9.8 g/dl. Además la necesidad de procedimientos endoscópicos disminuyó al año (mediana de 5 a 0).
Entre los efectos secundarios destacan el tromboembolismo venoso (2.8-17.3%) y la perforación gastrointestial (1-2.7%, con desenlace mortal en aproximadamente un tercio de los casos graves de perforaciones gastrointestinales). Está contraindicado en el embarazo y no debe iniciarse durante los 28 días siguientes a una intervención de cirugía mayor o hasta que la herida quirúrgica haya cicatrizado completamente[33].
Pacientes que tengan antecedentes de diabetes o sean mayores de 65 años tienen un riesgo aumentado de sufrir reacciones tromboembólicas arteriales (infarto agudo de miocardio, accidente cerebrovascular) durante el tratamiento. En mayores de 65 años hay más riesgo de leucopenia, trombocitopenia grave y de hipertensión severa[33].
El bajo nivel de evidencia, elevado coste y los eventos adversos lo posicionan como una opción alternativa de último recurso.
Otros tratamientos:
Sirolimus
Sirolimus es un inhibidor de mTOR (mammalian target of rapamycin ó diana de la rapamicina en mamíferos) y su mecanismo de acción consiste en bloquear esta proteína para suprimir la respuesta inmune y el crecimiento celular.
Sirolimus ha demostrado eficacia terapéutica en la inhibición de la formación anormal de vasos sanguíneos en la piel, la córnea y los tumores, lo que respalda indirectamente su posible uso para las AD gastrointestinales.
Sólo hay un estudio autocontrolado[34] que evalúa la eficacia y seguridad de sirolimus en 11 pacientes con hemorragia recurrente por AD. Los pacientes recibieron cápsulas orales, 0.8 mg/m² de superficie corporal una vez al día. Se midió la concentración plasmática a los 1, 3 y 6 meses con el objetivo de mantener una concentración de 5-10 ng/mL. El tratamiento con sirolimus logró una reducción significativa en el número de episodios de sangrado, mejoró los niveles de hemoglobina y redujo la necesidad de transfusiones hemáticas.
En cuanto a los efectos adversos se describen como muy frecuentes (≥1/10): infecciones, anemia, leucopenia y trombocitopenia[35].
Estos resultados sugieren que sirolimus puede ser una opción terapéutica eficaz en pacientes con AD gastrointestinales refractarias, aunque la evidencia actual es limitada por el tamaño muestral y la ausencia de grupo control. Se requieren ECA y mayor número de pacientes para establecer recomendaciones clínicas sobre sirolimus.
Estrógenos +/- progesterona
Se ha propuesto que la terapia hormonal (estrógenos con o sin progesterona) reduce la tasa de sangrado gastrointestinal por AD al contribuir a la hemostasia y disminuir la fibrinólisis. Pero un ECA multicéntrico y doble ciego, que incluyó a 72 pacientes con sangrado por AD, no mostró ningún beneficio terapéutico en comparación con el placebo. En base a estos hallazgos, parece haber poco papel para la terapia hormonal en pacientes con AD[24],[36].
Ácido tranexámico
Ha habido poca investigación sobre el uso de ácido tranexámico en el tratamiento de las AD gastrointestinales. El ECA internacional HALT-IT[37] mostró que el ácido tranexámico no redujo significativamente el riesgo de resangrado o muerte por hemorragia gastrointestinal.
Algoritmo de manejo
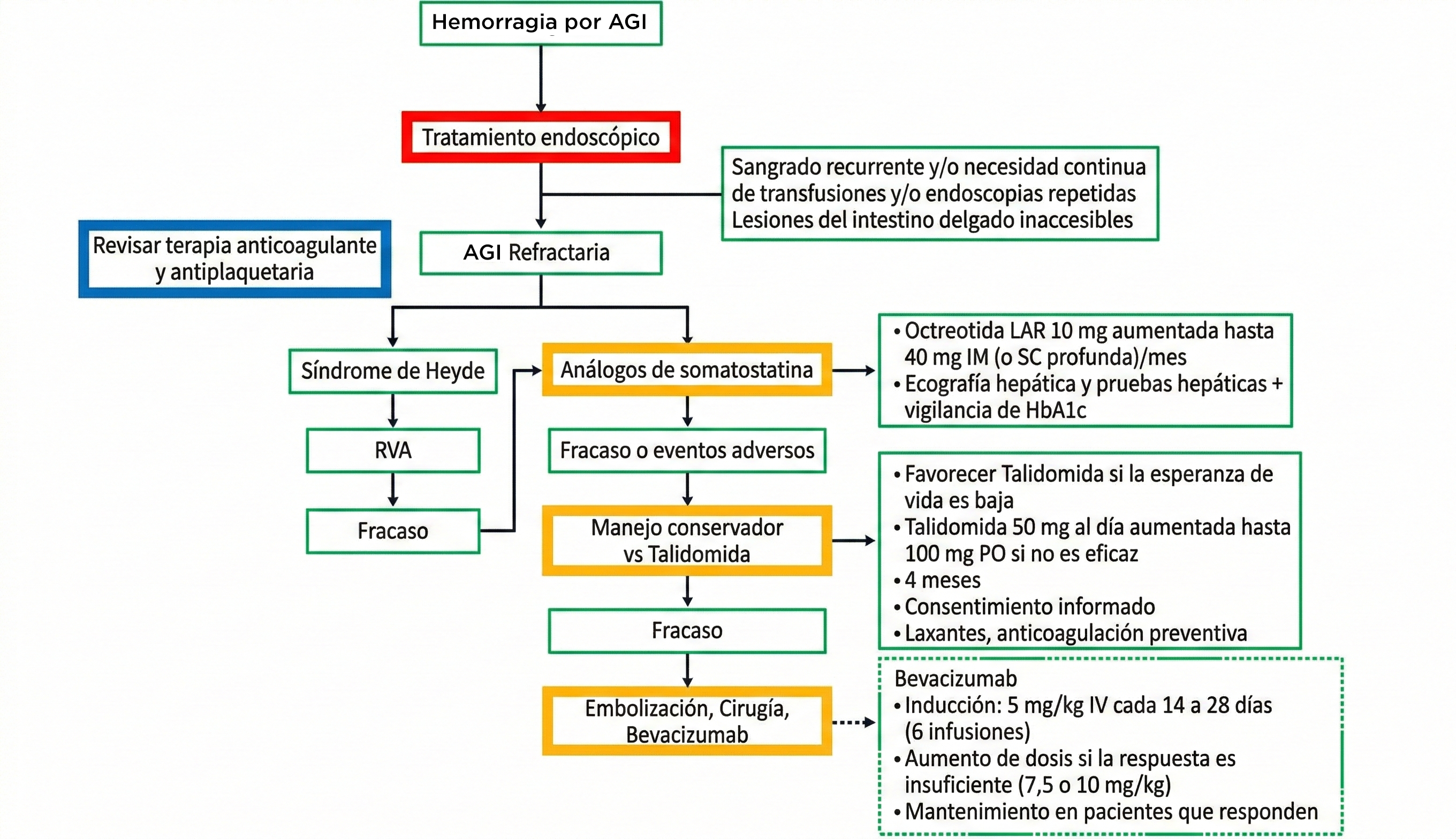
Publicaciones recientes proponen valorar un cambio en el manejo de los pacientes con AD[24],[27]. En el artículo de Becq et al[27] proponen un algoritmo de manejo (Figura 8).
Figura 8
Algoritmo de manejo de la angiodisplasia gastrointestinal refractaria (imagen tomada de Becq A et al., United European Gastroenterology Journal 2024). AVR, reemplazo valvular aórtico; SB, intestino delgado; GIA angiodisplasia gastrointestinal.
En caso de hemorragia por AD valorar tratamiento endoscópico. Una buena opción por perfil de seguridad, coste y disponibilidad sería APC.
Aunque no existe una definición consensuada de tratamiento endoscópico fallido, los criterios de AD refractarias generalmente incluyen sangrado recurrente, seguir precisando transfusiones y/o endoscopias repetidas. En este momento valorar el riesgo/beneficio de suspender anticoagulantes y/o antiagregantes si el paciente los tomase.
En caso de estenosis aórtica valorar el reemplazo valvular aórtico. Y en el resto de casos de AD refractaria, valorar como primera opción terapéutica los análogos de somatostatina por su buen perfil de tolerancia: octreotida LAR 10 mg, intramuscular, mensualmente, amentando hasta 40 mg si no hay respuesta. Se recomienda realizar un cribado de colelitiasis mediante ecografía abdominal antes y después de 6 meses de tratamiento, así como un seguimiento de las pruebas de función hepática y los niveles de hemoglobina glicosilada.
En caso de fracaso o interrupción debido a eventos adversos, valorar manejo conservador o talidomida. Especialmente en pacientes que no es probable que sufran polineuropatía (dosis dependiente, ocurre en el 80% de los pacientes después de 6 meses de tratamiento) debido a su corta esperanza de vida. Talidomida a dosis de 50 mg, vía oral y por la noche (da somnolencia), con aumento a 100 mg si no es eficaz, durante un total de 4 meses. Es fundamental informar sobre los efectos adversos y obtener el consentimiento informado. Según ficha técnica, valorar tromboprofilaxis en pacientes con factores de riesgo trombóticos adicionales[30].
La siguiente opción terapéutica, según el algoritmo propuesto, sería embolización, cirugía ó bevacizumab. El bevacizumab sería de uso compasivo, se administra vía intravenosa, en la fase de inducción 5 mg/kg cada 2 semanas, de 4 a 6 dosis, y en el mantenimiento 5 mg/kg al mes. El tratamiento debe suspenderse en caso de trombosis venosa profunda reciente, enfermedad infecciosa grave o arteriopatía grave.

 Descargar número completo
Descargar número completo Download full issue
Download full issue